人核心蛋白聚糖基因靶向肺癌細胞特異性表達載體的構建及鑒定
呂俊鋒 杜珍武 張玉成 張桂珍 (吉林大學中日聯誼醫院中心實驗室,吉林 長春 30033)
肺癌的分子靶向藥物治療是近年新興的一種治療手段,具有高度選擇性地殺死腫瘤細胞而不殺傷或僅很少損傷正常細胞的特點,然而,恰恰由于靶向治療是為攻擊特異性靶分子而設計,所以須找到合適靶點才能發揮其療效。研究發現核心蛋白聚糖 (decorin,DCN)在腫瘤細胞的生長轉移過程中發揮重要作用,具有較好的抑制腫瘤細胞生長的作用〔1〕。因此,運用特定的基因表達調控元件,使 DCN基因特異地在腫瘤細胞中表達,從而提高DCN基因治療安全性。人分泌型白細胞蛋白酶抑制劑 (human secretory-leukop rotease inhibitor,hSLPI)是由呼吸道及生殖道黏膜上皮分泌的蛋白質,在非小細胞肺癌 (NSCLC)中高表達,hSLPI作為基因啟動子具有相對更好的特異性,該基因啟動子控制的特異表達及殺傷作用已在動物實驗中得到證實〔2〕。本實驗采用基因克隆技術從人外周血白細胞的基因組中釣取 SLPI啟動子片段構建并鑒定 pcDNA3.1-hSLPI-decorin的真核表達體系,為進一步研究 decorin靶向基因治療肺癌奠定基礎。
1 材料與方法
1.1 材料 人肺腺癌 A549細胞、質粒 pcDNA-decorin、細菌克隆宿主大腸桿菌 JM109和質粒 pcDNA3.1來自本實驗室。各種限制性內切酶、TaqDNA聚合酶、T4DNA連接酶購于大連寶生物工程有限公司。質粒小提試劑盒、DNA marker購自天根生化科技有限公司。DNA凝膠回收試劑盒購自維特潔生化技術有限公司。抗人DCN單克隆抗體購于 R&D公司;Lipofectamine 2000購于 Invitrogen公司;G418購于寶泰克生物工程公司。
1.2 引物設計 根據 GenBank中 SLPI基因的 cDNA序列,上游 5′末端轉錄調控區的序列設計一對引物,上游引物:5′-TTCGACGCGTCTCACTGCAGCCTCAAAC-3′并在 5′端引入 MluⅠ酶切位點;下游引物:5′-TTCTAGCTAGCGGTGAAGGCAGGAGTGAC-3′并在 5′端引入 NheⅠ酶切位點。由上海生工公司合成。
1.3 SLPI基因啟動子的克隆與鑒定 取新鮮的人外周血2 m l,按試劑盒說明提取細胞基因組 DNA,并以此為模板,應用TaqDNA聚合酶和上述引物進行 PCR擴增 SLPI基因啟動子序列。PCR反應條件為:95℃預變性 5 m in,94℃變性1 min,58℃退火 45 s,72℃延伸 1 m in 40 s,共 35個循環,最后 72℃延伸10 m in。PCR產物通過 1%瓊脂糖凝膠電泳進行初步鑒定。DNA凝膠回收試劑盒回收全部 PCR產物,得到的目的片段克隆到 pcDNA3.1載體中,并轉化大腸桿菌 JM109,經藍白篩選,隨機挑取白色菌落,搖菌后提取質粒,以 MluⅠ和 NheⅠ雙酶切,1%瓊脂糖凝膠電泳,進行酶切鑒定,鑒定正確后得到 pcDNA3.1-SLPI菌株,再送交上海生工測序中心鑒定 。
1.4 雙酶切 pcDNA3.1-decorin和 pcDNA3.1-hSLP I連接并轉化 用 EcoR I、Xba I雙酶切質粒 pcDNA3.1-decorin,凝膠回收DCN基因片段,通過 T4連接酶定向克隆入Mlu I和 Nhe I雙酶切測序正確的載體 pcDNA3.1-hSLPI基因啟動子 SLPI的下游,連接產物轉化到已置備好的感受態 JM109菌中,并且涂布在含有氨卞青霉素的LB平板上,過夜后挑取單克隆菌,搖床過夜,質粒小提試劑盒提取重組質粒 pcDNA3.1-hSPL I-decorin。
1.5 質粒 pcDNA3.1-hSLPI-decorin的酶切鑒定 pcDNA3.1-hSPL I-decorin陽性重組克隆通過 Mlu I和 Nhe I、EcoR I和 Xba I酶切,酶切產物經 1%瓊脂糖凝膠電泳,進行初步鑒定。

圖 1 SLPI啟動子 PCR擴增產物的瓊脂糖凝膠電泳圖譜

圖 2 pcDNA3.1-SLPI酶切鑒定瓊脂糖凝膠電泳圖譜
2 結 果
2.1 SLPI基因啟動子的克隆與鑒定
2.1.1 PCR產物的瓊脂糖凝膠電泳 見圖 1,在約 1 250 bp處獲得 SLPI基因啟動子單一目的條帶。
2.1.2 酶切鑒定 pcDNA3.1-SLPI陽性重組克隆通過 Mlu I和 Nhe I雙酶切,酶切產物經 1%瓊脂糖凝膠電泳,結果見圖 2,在約 1 250 bp處切出目的片段。
2.1.3 序列測定 經酶切、PCR鑒定正確的質粒進行測序。將測序結果與 GenBank中的 SLPI基因上游 5′末端轉錄調控區序列比對,序列完全一致,測序結果為:

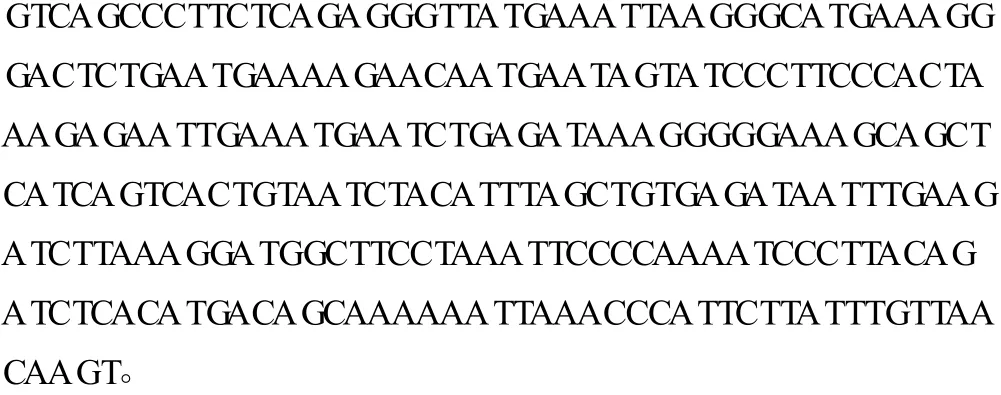
2.2 重組質粒 pcDNA3.1-hSLPI-deco rin的酶切鑒定 重組質粒 pcDNA3.1-hSLPI-decorin經MluⅠ和 NheⅠ、EcoR Ⅰ和 XbaⅠ酶切后 1%瓊脂糖凝膠電泳,結果可見酶切下 1 000 bp的DCN基因片段及 1 250 bp處獲得 SLPI基因啟動子的條帶,見圖3。

圖 3 pcDNA3.1-hSLPI-decorin酶切鑒定瓊脂糖凝膠電泳圖譜
3 討 論
DCN是在細胞外基質中存在的小分子蛋白聚糖,1978年首次由美國國立衛生研究院骨科研究所的 Fisher教授分離、純化。1986年 Krusius等〔4〕通過提取人胚胎成纖維細胞系IMR290RNA、構建 DNA文庫,成功克隆 DCN基因并測序鑒定。研究發現,DCN在體外可抑制各種組織來源的腫瘤細胞增殖,尤其是 hNSCLC細胞,國外學者先給裸鼠接種 A431肺鱗狀細胞癌細胞株,出現接種的瘤體后,多次瘤體內注射 DCN基因的腺病毒載體。結果移植瘤體生長減緩,瘤體與正常組織分界變清楚,并且在鱗狀細胞癌的移植瘤體內出現了數個角化珠〔5〕。也就是 DCN基因在抑制腫瘤細胞生長的同時,還有促進細胞分化的作用。Araki等〔6〕進一步報道,巨細胞病毒介導的 DCN cDNA轉染轉移性乳腺癌細胞株MDA-MB-231,能表達 DCN,可以抑制腫瘤細胞的生長、運動和轉移,骨轉移下降了 90%,這些結果表明DCN對腫瘤轉移有預防作用,并可能最終導致對轉移性乳腺癌的更好的治療。
文獻〔4〕顯示 SLPI基因在各種 NSCLC患者的癌組織中呈過量表達,在肝中表達極弱,相比于其他肺癌特異性啟動子,SLP I基因啟動子調控的肺癌組織類型更廣。Maemondo等〔7〕應用該啟動子調控腫瘤選擇性完全復制型腺病毒治療NSCLC取得較好的特異抗瘤效果,該研究為尋求針對肺癌的更有效的腫瘤基因治療、最大限度地避免對正常組織的損傷打下基礎。
為尋求針對肺癌的更有效的腫瘤基因治療,最大限度地避免對正常組織的損傷,本研究選用 SLPI基因啟動子作為NSCLC基因治療的靶開關。通過 PCR方法從人外周血基因組中釣取 1.2 kb的 SLPI啟動子,測序結果證實與 GenBank上 SLPI基因上游 5′末端轉錄調控區的序列完全一致。實驗成功構建 SLP I啟動子調控下的DCN報告基因表達載體,最終成功構建了真核表達載體 pcDNA3.1-hSLPI-decorin,這為進一步研究DCN靶向治療肺癌作用及其抑癌機制奠定了基礎。
1 Reed CC,Gauldie J,Iozzo RV.Supp ression of tumorigenicity by adenovirus-mediated gene transfer of decorin〔J〕.Oncogene,2002;21(23):3688-95.
2 Nukiwa T,Suzuki T,Fukuhara T,et a l.Secretory leukocyte pep tidase inhibitor and lung cancer〔J〕.Cancer Sci,2008;99(5):849-55.
3 Kr usius T,Ruoslahti E.Primary structure of an extracellular matrix p roteoglycan core p riein deduced from clone cDNA〔J〕.Proc Natl Acad Sci USA,1986;83(20):7683-7.
4 Ameshima S,Ishizaki T,Demura Y,et a l.Increased secretory leukop rotease inhibitor in patientswith nons mall cell lung carcinoma〔J〕.Cancer,2000;89(7):1448.
5 Reed CC,Gauldie J,Iozzo RV.Supp ression of tumorigenicity by adenovirus mediated gene transfer of decorin〔J〕.Oncogene,2002;21(23):3688-95.
6 Araki K,Wakabayashi H,Shintani K,et a l.Decorin supp resses bone metastasis in a breast cancer cell line〔J〕.Oncology,2009;77(2):92-9.
7 Maemondo M,Saijo Y,Narumi K,et a l.Gene therapy with secretory leukop rotease inhibitor p romoter-controlled rep lication-competent adenovirus for non-small cell lung cancer〔J〕.Cancer Res,2004;64(13):4611.

