含乙型肝炎病毒S-PreS1基因的DNA疫苗與蛋白顆粒疫苗聯合免疫可增強免疫應答
陳紅,鄧瑤,譚文杰,王文,管潔,文波,殷霄,阮力
中國疾病預防控制中心病毒病預防控制所 病毒病應急技術中心,北京 100052
含乙型肝炎病毒S-PreS1基因的DNA疫苗與蛋白顆粒疫苗聯合免疫可增強免疫應答
陳紅*,鄧瑤*,譚文杰,王文,管潔,文波,殷霄,阮力
中國疾病預防控制中心病毒病預防控制所 病毒病應急技術中心,北京 100052
為研制新型有效的HBV治療性疫苗,構建了含PreS1與S融合基因的HBV DNA疫苗,即pVRC-HBSS1 (PreS1 21–47 aa融合在S抗原1–223 aa的羧基端),并制備了CHO表達相同結構的蛋白顆粒亞單位疫苗HBSS1。在Balb/C小鼠中采用不同的DNA免疫方式 (即肌肉注射、皮內注射加電轉) 初免3次,蛋白顆粒亞單位疫苗 (不同佐劑) 肌肉注射加強免疫 1次,然后我們分析比較了各組疫苗所引起的免疫應答特點。抗體檢測結果表明:皮內注射結合電轉初免組產生的PreS1與S特異性抗體水平皆高于肌肉直接注射組。進一步還發現DNA疫苗與蛋白顆粒亞單位疫苗兩種疫苗聯合應用后S抗原特異的細胞免疫應答 (IFN-γ ELISpot分析) 明顯高于DNA疫苗或蛋白顆粒亞單位單獨應用,其中皮內注射+電轉結合蛋白顆粒亞單位疫苗聯合免疫組可產生最強的細胞免疫應答。這些研究為新型HBV治療性疫苗的優化設計與合理應用提供了依據。
乙型肝炎病毒 (HBV),DNA疫苗,顆粒亞單位疫苗,電轉,聯合免疫
Abstract:To develop novel and effective HBV therapeutic vaccine, we constructed an expression vector, pVRC-HBSS1, in which PreS1 (21?47aa) coding gene fused to the C-terminal of the S (1?223 aa) coding gene of HBV, and prepared the protein particle vaccine HBSS1 that consist of S and PreS1 fusion antigen derived from CHO system. We immunized mice by priming three times with DNA vaccine via different methods (i.e., intramuscular injection, intradermal injection with electroporation), then boosting oncewith protein particle vaccine. We analyzed the immune response among various vaccination groups. The higher level of S or PreS1 specific antibodies was detected in the group via intradermal injection with electroporation, compared with that of direct intramuscular injection. We further found that the specific cellular immune responses (IFN-γ ELISpot analysis) in the group priming with DNA vaccines and boosting with protein subunit vaccine particles, was significantly higher than that of the DNA or protein particle subunit alone. Moreover, combination vaccination priming with intradermal injection DNA via electroporation and boosting with protein particle induced the strongest cellular immune response. These results provide a basis for rational design and application of the novel HBV therapeutic vaccine.
Keywords:Hepatitis B virus (HBV), DNA vaccine, subunit particle vaccine, electroporation, prime boost vaccination
乙型肝炎病毒 (HBV) 不僅可引起急慢性肝炎,而且與肝硬化、肝癌的發生密切相關,盡管乙肝疫苗的使用已逾20年,目前HBV仍是傳播最為廣泛的病原之一[1]。HBV疫苗在中國已納入計劃免疫,使用最為廣泛的為酵母或CHO表達含S全長的顆粒亞單位疫苗[2]。盡管 HBV疫苗的應用已達 20余年并取得極大成功,但仍有5%~10%的人群不能產生保護性anti-HBS抗體,且近年來,S變異流行株呈增長趨勢[2]。目前全球絕大多數慢性HBV感染者得不到有效治療,而長期持續性感染將可能最終導致肝硬化、肝衰竭或者肝癌,當前臨床上乙肝主要藥物的治療效果有限,且長期應用中存在不良反應,仍需開發新的治療策略,因而HBV治療性疫苗的研發與應用成為近年來研究的熱點。
HBV的治療性疫苗主要包括重組蛋白疫苗、多肽疫苗、DNA疫苗等[2],DNA疫苗與蛋白疫苗相比,除了可激發特異性抗體應答外,還可產生較強的、持久的T輔助 (Th) 細胞應答與抗原特異的CTL反應。此外,DNA疫苗還具備制備簡單、低廉并易于多價使用等優點[3],多種DNA疫苗應用的結果表明其主要的問題是其免疫原性相對較弱 (尤其是在大動物與人中),故近年來科學家們探索了采用多種途徑增強其免疫原性[3],如抗原改造、與蛋白疫苗或載體疫苗聯合應用、采用基因槍及體內電轉等方式免疫等。
本研究在前期工作基礎上[4-5]首先構建了含PreS1與S融合抗原的HBV DNA疫苗[6],即pVRCHBSS1 (PreS1與S融合),分別采用肌肉注射、皮內注射+電轉兩種方式初免后,用蛋白顆粒亞單位疫苗(不同佐劑) 肌肉注射加強免疫1次,在小鼠中比較分析了體液與細胞免疫應答特點。
1 材料與方法
1.1 HBV顆粒蛋白疫苗與佐劑
CHO表達的含 S+PreS1融合抗原的顆粒疫苗(HBSS1) 的制備及表達鑒定 (SDS聚丙烯胺凝膠電泳及電鏡觀察) 參見文獻[4]。Al(OH)3佐劑為北京華爾盾科技服務公司提供,濃度為2 mg/mL;CpG-ODN 1826[4-6]由NEB 公司合成,由上述抗原與佐劑分別配伍成2種免疫制劑,即HBSS1+Al(OH)3、HBSS1+CpG,其中每劑中抗原含量皆為 2 μg,Al(OH)3含量為 1 mg/mL,CpG 含量為 10 μg。
1.2 HBV DNA疫苗的構建與表達鑒定
包含 HBV S抗原 (S:1–223 aa) 與前 S1抗原(PreS1:21–47 aa) 融合基因的pcHBSS表達質粒為本室保存[9],可用于在 CHO細胞中表達制備 HBV顆粒樣蛋白疫苗。乙肝病毒顆粒樣 DNA疫苗質粒pVRC-HBSS1的構建參見文獻[6],即將HBV S抗原 (S:1–223 aa) 與前 S1 抗原 (PreS1:21–47 aa) 融合基因的目的片段,連接到pVRC8301載體上,限制酶分析和測序篩選獲得HBV DNA疫苗陽性質粒pVRC-HBSS1。DNA疫苗質粒用 Endofree試劑盒(德國 Qiagen) 純化。純化的 pVRC-HBSS1質粒DNA瞬時轉染293T細胞,轉染48 h后裂解293T細胞,取樣進行SDS-PAGE電泳,轉膜進行Western blotting分析,用抗PreS1小鼠單抗作為一抗檢測靶抗原表達 (圖1)。
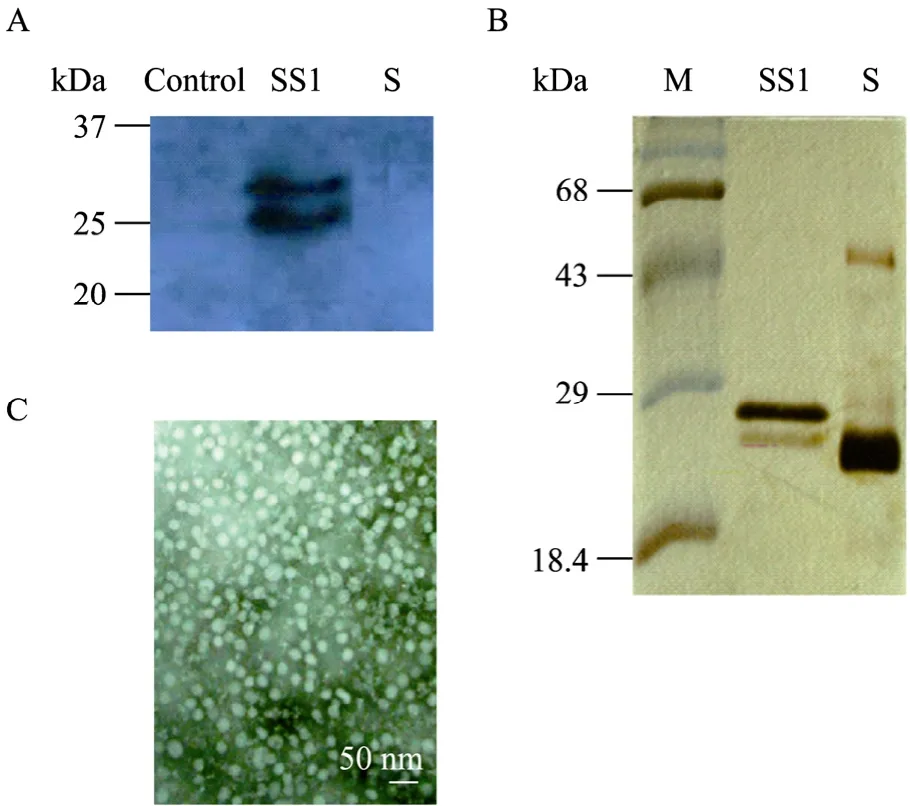
圖1 乙肝病毒新型DNA疫苗的表達檢測及顆粒亞單位蛋白疫苗的鑒定Fig. 1 Expression detection of HBV DNA vaccine containing PreS1 and S fusion gene. (A) Western blotting analysis of expression of SS1 antigen in the HBV DNA vaccine. (B)Characterization of HBV particle subunit vaccine which consist of SS1 antigen by SDS-PAGE staining. (C) Electronmicrograph of HBV particle subunit vaccine which consist of SS1 antigen. M: protein marker; SS1: S+PreS1 fusion antigen;S: S antigen.
1.3 動物分組與免疫方案
Balb/C小鼠,雌性,6~8周齡,購自中國醫學科學院動物實驗繁殖中心,按照免疫方式隨機分為4組 (表1),A、B與C每組12只,另設生理鹽水對照組 (6只),注射方式和免疫劑量見表1。DNA 疫苗初免 (0、3、6周),A組和 B組為肌肉注射,C組為皮內注射,結合卡鉗式電轉免疫 (表1)[7-8],采用BTX ECM830電穿孔儀,卡鉗式電極皮內免疫 (C組) 的電轉參數為:100 V,10 ms間隔,3次脈沖;然后電極反向,75 V,15 ms,3次脈沖,間隔1 s/次。蛋白加強 (第 10周) 為肌肉注射免疫。A、B與 C每組分別于第10周與第14周各取6只采血與脾細胞進行抗體檢測與細胞免疫應答分析。
1.4 體液免疫應答檢測
眼眶采血檢測抗體,倍比稀釋后,參照試劑盒說明進行[5-6]。每組血清混合后皆從1∶10起倍比稀釋。
1.5 IFN-γ ELISpot檢測
HBV S抗原合成肽庫參見文獻[5],分別與小鼠脾細胞 (5×105) 孵育,具體操作按試劑盒說明書進行[5-6]。反應終止后在ELISpot 讀數儀上計數分析,以106脾細胞中斑點 (減去無關肽孔) 計數求均值。實驗數據采用SPSS14.0軟件處理,統計學分析采用One-way ANOVA 檢驗法。
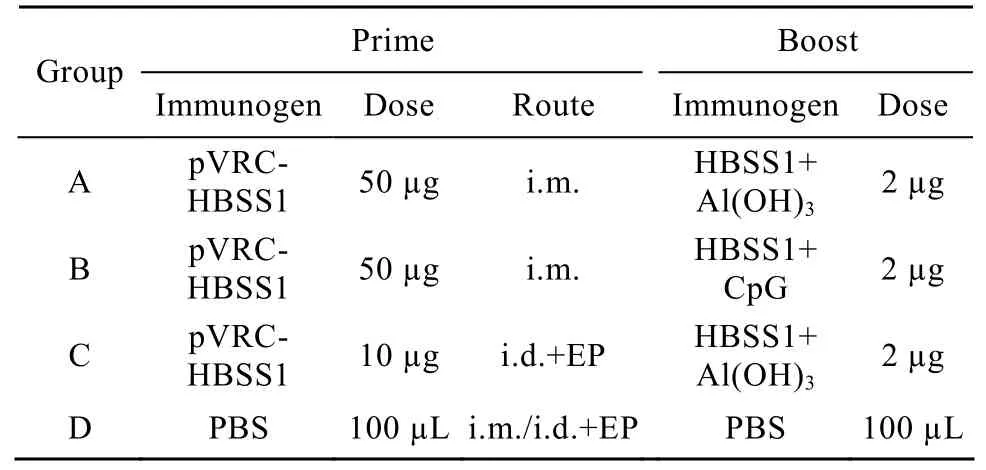
表1 動物分組及免疫方案Table 1 Group and immunization of mice used in this study
2 結果
2.1 DNA疫苗的表達及顆粒亞單位蛋白疫苗的檢定
本實驗以前的研究表明[4],將 HBV PreS1區21-47位氨基酸融合到截短型S抗原 (1?223 aa) 的羧基端,可在CHO系統中表達形成穩定的VLP結構抗原,為此本研究中將上述含 PreS1的融合抗原克隆到DNA疫苗載體pVRC上形成DNA侯選疫苗,即 pVRC-HBSS1,體外瞬時轉染 293T細胞后進行Western blotting分析證實融合抗原的有效表達 (圖1A)。因糖基化不同,SS1出現大小約為24、27 kDa兩條帶。顆粒亞單位蛋白疫苗的SDS-PAGE電泳及顆粒的電鏡鑒定參見文獻[4] (圖1B,1C)。Western blotting與SDS-PAGE染色實驗中采用僅含S主蛋白的DNA疫苗或顆粒亞單位蛋白作對照。這些結果均與前述文獻報道相符。
2.2 DNA疫苗初免顆粒樣蛋白疫苗加強后小鼠的抗體應答及IgG亞型
DNA疫苗初免后4周,肌肉注射組抗PreS1及抗S抗體平均滴度分別為60與10,而皮內注射結合電轉組則分別為200與1 000;蛋白疫苗加強免疫后4周采血進行特異性抗體滴度的測定,結果表明(表2):與初免后4周測定結果相比,抗體平均滴度各組皆有所提高,其中抗PreS1抗體以A組 (肌肉注射 DNA疫苗初免,蛋白疫苗結合 Al(OH)3佐劑加強免疫) 抗體平均滴度最高,而抗S抗體以C組(DNA疫苗皮內注射+電轉初免,蛋白疫苗結合Al(OH)3佐劑加強免疫) 平均滴度較高,蛋白疫苗結合CpG 佐劑加強免疫組 (B組) S與PreS1抗體平均滴度皆低于蛋白疫苗結合Al(OH)3佐劑加強免疫組 (A和C組)。除了對抗體滴度進行分析外,我們也在末次免疫后第4周采血以1∶100稀釋后對各組誘導的IgG亞型進行分析 (表2),結果表明:DNA疫苗肌肉注射或皮內注射結合電轉初免,含鋁佐劑的蛋白制劑加強后 (A和 C組) 產生的針對 S與PreS1的抗體 IgG亞型各組 IgG2a /IgG1>1;而含CpG佐劑的蛋白制劑加強后 (B 組) 抗 PreS1抗體以IgG2a為主,而針對S的抗體IgG亞型,則IgG1略高于IgG2a。
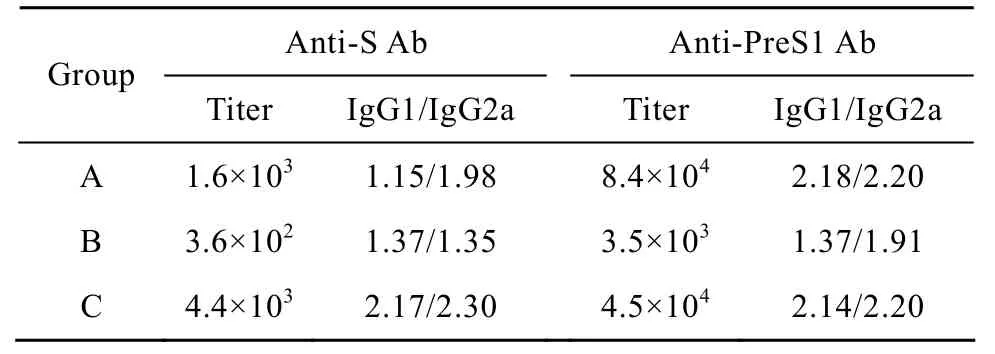
表2 聯合免疫后抗原特異的總抗體平均滴度與亞型Table 2 Total antibody titers and subtype class in sera of mice after prime-boost vaccination
2.3 DNA疫苗初免顆粒樣蛋白疫苗加強后小鼠的抗原特異性細胞免疫應答明顯增強
作為治療性DNA疫苗,細胞免疫應答是評定有效性最關鍵的評價指標,為此我們采用 IFN-γ ELISpot方法檢測了DNA疫苗初免后4周及 DNA疫苗與蛋白疫苗聯合免疫后 4周各組小鼠脾細胞中抗原特異的IFN-γ分泌細胞數,結果如圖2所示。DNA疫苗初免蛋白疫苗加強應用后 S特異的 SFC讀數明顯提高,SFC讀數均值>400 SFC/106脾細胞,顯著高于DNA疫苗肌肉注射初免各組。而且以DNA疫苗皮內電轉初免 (10 μg),結合蛋白制劑加強應用后增強效果最明顯 (SFC讀數均值>800 SFC/106脾細胞)。
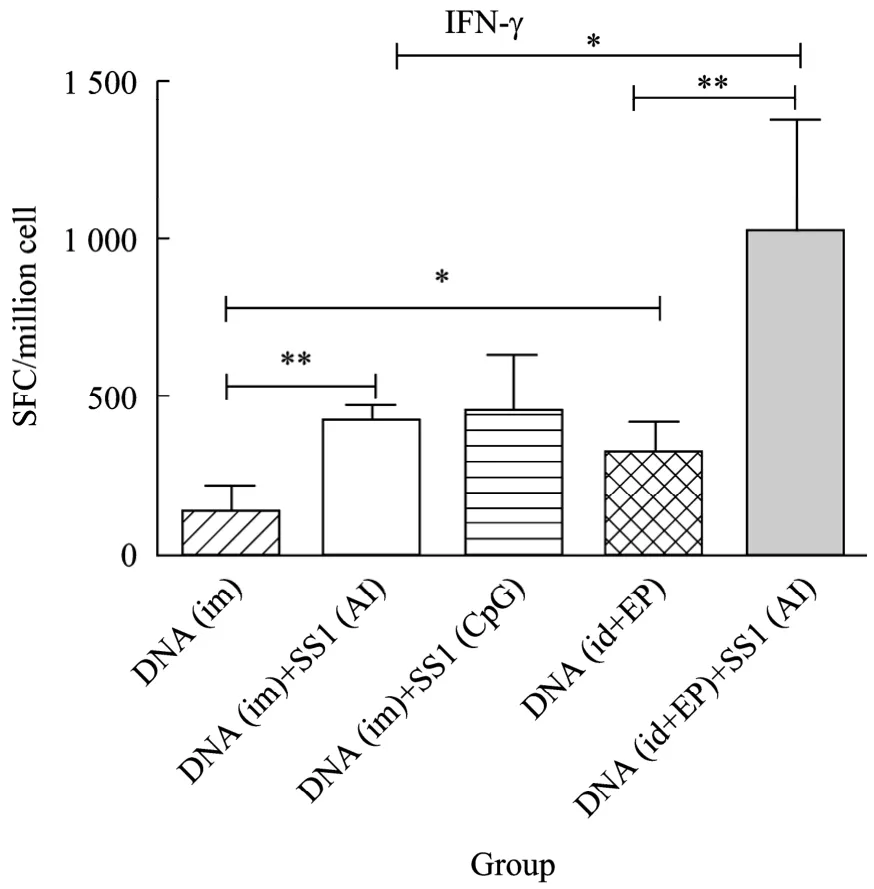
圖2 ELISPOT分析不同HBV疫苗免疫后小鼠脾細胞中IFN-γ分泌斑點形成細胞數 (SFCs)Fig. 2 ELISPOT analysis for IFN-γ secretion in mouse splenocytes immunized with different HBV vaccines as indicated. Data represent the average of spot forming cells(SFCs) per million of splenocytes from 6 mice/group. * P<0.05;** P<0.01.
3 討論
誘導針對多個抗原的較強的體液與細胞免疫應答是研制新型 HBV治療性疫苗的目標[2,11-12]。HBV 表面抗原 (HBS) 在 CHO細胞或酵母中表達可自我裝配成22 nm球形VLP,是市售HBV疫苗的有效保護性抗原[2]。PreS1含多個比S蛋白免疫原性更強的 T細胞和 B細胞表位[9-10],并含肝細胞結合位點 (21?47 aa),對于病毒的附著與進入等有重要作用[13],故對PreS1抗原的免疫反應在中和和阻斷HBV感染及清除HBV感染上起著重要作用[9-12]。
前期的實驗結果表明[4]:在 CHO細胞中表達HBSS1 即 S (1?223 aa)+PreS1 (21?47 aa) 亦可形成穩定分泌的病毒樣顆粒,PreS1與S抗原的摩爾比率為1∶1。這種病毒顆粒樣蛋白抗原皆可在動物模型中快速激發有效的體液免疫應答[4-5]。而 DNA疫苗制備快速、低廉,而且較蛋白疫苗更易激發較強的細胞免疫應答,但目前DNA疫苗面臨的主要挑戰是免疫強度有待增強[3,11]。最近大量文獻報道[3,7-8,11]通過體內電轉可明顯增強細胞對外源 DNA的攝取與表達水平,外源蛋白引起局部的炎性因子聚集從而可同時提高DNA疫苗所誘導的體液與細胞免疫應答水平,而DNA疫苗與蛋白疫苗或載體疫苗聯合應用則是增強 DNA疫苗免疫應答最有效的策略之一[3]。
本研究旨在研制可誘導多抗原特異細胞免疫應答的HBV治療性疫苗,故首先采用DNA疫苗載體構建了包含上述顆粒樣結構的 DNA疫苗,即pVRC-HBSS1,為增強免疫原性,結合應用電轉方式進行初免;同時為進一步增強免疫應答水平,采用了與蛋白顆粒亞單位疫苗聯合應用的免疫策略,在小鼠中分析比較其免疫應答特點。
我們的前期研究采用 2次蛋白疫苗 (含不同佐劑) 肌肉注射初免,1次DNA疫苗皮內電轉免疫加強的聯合免疫方式,在小鼠中分析比較了各疫苗所引起的體液與細胞免疫應答。結果表明[6]:HBSS1 DNA疫苗結合皮內注射+電轉方式可明顯加強含S-PreS1顆粒的蛋白疫苗在小鼠中免疫效果,其特異性抗體滴度皆高于104,高于本研究中采用的聯合免疫所誘導的抗體水平,但細胞免疫強度卻明顯低于本研究中采用的聯合免疫,前者小鼠中 IFN-γ分泌斑點形成細胞數均值皆低于250 SFC/106脾細胞,而本研究中聯合免疫后SFCs讀值均高于400 SFC/106脾細胞,最高均值達800 SFC/106脾細胞。故本研究中所采用的聯合免疫方案更適合 HBV治療性疫苗的要求。
總之,本研究中HBSS1 DNA疫苗初免蛋白疫苗加強的聯合免疫策略,結合皮內電轉方式可產生最強的抗原特異的細胞免疫應答,是研發新型有效HBV治療性疫苗的侯選制劑與免疫方案,值得進一步在大動物或人群中評價與應用。
REFERENCES
[1] Lavanchy D. Worldwide epidemiology of HBV infection,disease burden, and vaccine prevention. J Clin Virol,2005, 34(Suppl1): S1?S3.
[2] Tan WJ, Ruan L. Progress on combination strategies of therapeutic vaccine approaches for the treatment of chronic HBV infection. Chin J Virol, 2006, 22(5):407?411.
譚文杰, 阮力. HBV 病毒慢性感染疫苗治療的組合策略及研究進展. 病毒學報, 2006, 22(5): 407?411.
[3] Lu S, Wang SX, Grimes-Serrano JM. Current progress of DNA vaccine studies in humans. Expert Rev Vaccines,2008, 7(2): 175?191.
[4] Tian SF, Zong F, Chen H, et al. The physicochemical and biological properties of SS1 fusion antigen of HBsAg secreted by mammalian cells. Chin J Virol, 2002, 18(4):312?316.
田淑芳, 宗芳, 陳紅, 等. 哺乳動物細胞分泌的乙型肝炎病毒表面S+PreS1融合抗原的理化和生物學性狀. 病毒學報, 2002, 18(4): 312?316.
[5] Chen H, Deng Y, Tan WJ, et al. Impact of different adjuvant on immunogenicity of the HBV particle vaccine containing the S+PreS1 fusion antigen in Balb/C mice.Chin J Biotech, 2010, 26(1): 74?78.
陳紅, 鄧瑤, 譚文杰, 等. 不同佐劑對含 S+PreS1融合抗原的乙型肝炎病毒顆粒疫苗免疫原性的影響. 生物工程學報, 2010, 26(1): 74?78.
[6] Chen H,Zhang LL, Tan WJ, et al. HBV DNA vaccination with electroporation enhances significantly the specific cell-mediated immune response in mice against HBV protein vaccine consisting of S-PreS1 fusion particles.Chin J Exp Clin Virol, 2010, 24(2): 94?97.
陳紅, 張陵林, 譚文杰, 等. 乙型肝炎病毒 DNA 疫苗電轉加強含 S-PreS1顆粒的蛋白疫苗在小鼠中免疫效果. 中華實驗和臨床病毒學雜志, 2010, 24(2): 94?97.
[7] Zhang L, Nolan E, Kreitschitz S, et al. Enhanced delivery of naked DNA to the skin by non-invasive in vivoelectroporation. BBA, 2002, 1527(1): 1?9.
[8] Yin X, Lu J, Tan WJ, et al. Enhancement of the immune response of a novel DNA vaccine encoding conserved NS3 and core fusion gene of HCV injected by intradermal electrotransfer in mice. Chin J Microbio Immunol, 2010,30(1): 41?45.
殷霄, 魯健, 譚文杰, 等. 表達丙型肝炎病毒 NS3和Core融合蛋白基因的DNA疫苗免疫方案優化. 中華微生物學和免疫學雜志, 2010, 30(1): 41?45.
[9] Neurath AR, Seto B, Strick N. Antibodies to synthetic peptides from PreS1 region of hepatitis B virus (HBV)envelop (env) protein are virus-neutralizing and protective. Vaccine, 1989, 7(3): 234?236.
[10] Milich DR, Melachlan A,Thornton GB. T-cell recognition of pre-S regions of HbsAg can bypass nonresponse to the S region. Adv Exp Med Biol, 1987, 225: 233?239.
[11] Bertoletti A, Gehring A. Therapeutic vaccination and novel strategies to treat chronic HBV infection. Expert Rev Gastroenterol Hepatol, 2009, 3(5): 561?569.
[12] Depla E, Van der Aa A, Livingston BD, et al. Rational design of a multiepitope vaccine encoding T-lymphocyte epitopes for treatment of chronic hepatitis B virus infections. J Virol, 2008, 82(1): 435?450.
[13] Dash S, Rao KVS, Panda SK. Receptor for pre-S1 (21-47)component of hepatitis B virus on the liver cell: role in virus cell interaction. J Med Virol, 1992, 37(2): 116?121.
Boosting with HBV subunit particle vaccine enhance immune response of novel DNA vaccine consisting of S-PreS1 fusion gene in mice
Hong Chen*, Yao Deng*, Wenjie Tan, Wen Wang, Jie Guan, Bo Wen, Xiao Yin, and Li Ruan
Biotech Center for Viral Diseases Emergency, National Institute for Viral Disease Control and Prevention, Chinese Center for Disease Control and Prevention, Beijing 100052, China
Received: April 7, 2010; Accepted: June 7, 2010
Supported by: National Natural Science Foundation of China (Nos. 30770146, 30770149), National Basic Research Program of China (973 Program)(No. 2009CB119104).
Corresponding author: Qingyin Zeng. Tel: +86-10-62836440; E-mail: qingyin.zeng@ibcas.ac.cn
國家自然科學基金 (Nos. 30770146, 30770149),國家重點基礎研究發展計劃 (973計劃) (No. 2009CB119104) 資助。

