去乙酰毛花苷注射液的雜質研究
李舸遠,陳東亞,蔡美明,陳民輝,王 玉
江蘇省食品藥品檢驗所,南京 210008
去乙酰毛花苷(Deslanoside)是由毛花洋地黃葉中提取的毛花洋地黃苷丙,經去乙酰化得到的化合物,又名去乙酰西地蘭、去乙酰毛花洋地黃苷丙。該原料藥制成的注射液主要用于治療心力衰竭。由于其作用較快,適用于急性心功能不全或慢性心功能不全急性加重的患者[1-2]。隨著該注射液的廣泛使用,其不良反應的報道也逐漸增多。該注射液常見的不良反應有心律失常[3]、胃納不佳或惡心、嘔吐(刺激延髓中樞)、下腹痛,異常的無力、軟弱,其中心律失常最為重要,為此,有必要對該注射液的安全性進行研究。然而,目前對該注射液的有關物質研究報道較少,在各國藥典中,對該品種有關物質的規定都限量較寬且不夠具體[4-5]。本文主要對去乙酰毛花苷注射液的雜質進行研究,為進一步監測去乙酰毛花苷注射液的不良反應,對其安全性進行再評價,以及提高去乙酰毛花苷注射液的質量標準提供科學依據。
1 儀器與試藥
1.1 儀器
Agilent 1100 series LC/MSD Trap高效液相色譜離子阱質譜聯用儀;Bruker AV-500型核磁共振儀;Thermo Nicolet 6700型傅立葉變換紅外分光光度計;島津UV-3600型紫外分光光度計;YM-3型熔點儀;旋轉蒸發儀;電熱手提高壓蒸汽消毒器。
1.2 試藥與試劑
去乙酰毛花苷注射液及同批原料(國內某藥業有限公司,注射液批號:100401,規格0.2 mg·mL-1,原料批號:091201);去乙酰毛花苷對照品(中國藥品生物制品檢定所);地高辛苷元對照品(USP);甲醇、乙腈為色譜純;水為超純水;氯仿、乙醇、甘油均為分析純。
2 方法與結果
2.1 溶液的制備
原料、雜質A、去乙酰毛花苷對照品、地高辛苷元對照品分別用甲醇配制成約0.2 mg·mL-1。
輔料溶液:按處方量取甘油50g、95%乙醇100 mL,加水至1000 mL,搖勻。
酸破壞:取去乙酰毛花苷原料兩份,各加1 mol· L-1鹽酸5 mL,放置2 h,用1 mol·L-1氫氧化鈉溶液調節pH至中性。
堿破壞:取去乙酰毛花苷原料兩份,各加1 mol· L-1氫氧化鈉溶液5 mL,放置2 h,用1 mol·L-1鹽酸溶液調節pH至中性。
氧化破壞:取去乙酰毛花苷原料加30%雙氧水2 mL,放置4 h。
光照破壞:取去乙酰毛花苷原料在3000Lx光照條件下分別放置5d、10d。
上述破壞均用輔料溶液配制成約0.2 mg·mL-1。
高溫破壞:取去乙酰毛花苷原料,用輔料溶液配制成約0.2 mg·mL-1,分別于121℃高壓滅菌20、40、60、120、240、720 min。
2.2 色譜與質譜條件
色譜柱:Agilent ZORBAX-SB C18色譜柱(4.6 mm×250 mm,5 μm);流動相A:乙腈-甲醇 (232∶148);流動相B:水;流速:1.0 mL·min-1;梯度洗脫:0~20 min流動相A 38%、20~22 min流動相A由38%升至52%、45~47 min流動相A又降至38%繼續平衡5min;檢測波長:220nm;柱溫:30℃;進樣量:20μL。
電噴霧離子源(ESI),源電壓4.5 kV,毛細管溫度:270℃,毛細管電壓20V,載氣流速70 mL·min-1,正負離子檢測,掃描方式:全掃描一級質譜,相對碰撞能量100%,質量數范圍100~2000。進樣方式:分流進樣,分流比為1∶4。
2.3 專屬性試驗
取“2.1”項下各溶液,分別按“2.2”項下色譜條件進行試驗,考察色譜條件專屬性及樣品雜質情況。結果酸、堿、氧化、光照及高溫破壞供試品溶液中的各雜質均能良好分離,輔料對雜質檢測無干擾。去乙酰毛花苷注射液中以歸一化法測含量大于0.1%的主要雜質有7個,分別依次命名為雜質A、B、C、D、E、F、G,其中最大的雜質為雜質A。結果表明,去乙酰毛花苷在高溫、酸、光照的條件下均可產生雜質A,以高溫條件下產生的較多。見圖1~4。
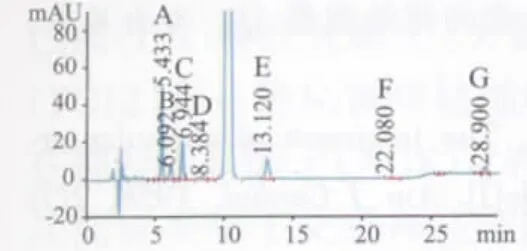
圖1 供試品溶液中主要雜質典型色譜圖
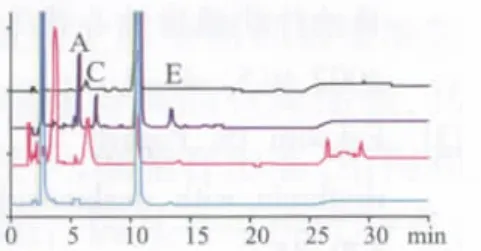
圖2 去乙酰毛花苷原料破壞試驗匯總圖
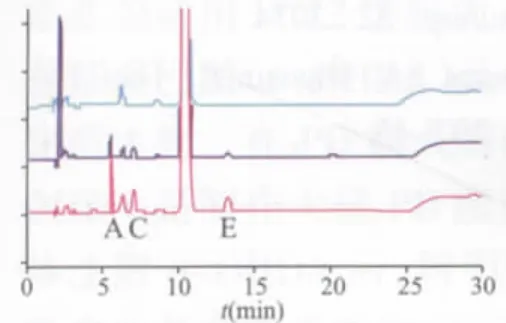
圖3 去乙酰毛花苷原料破壞試驗匯總圖從上至下依次為原液、光照破壞5天、10天
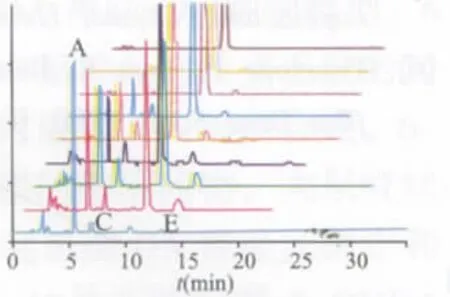
圖4 去乙酰毛花苷原料破壞試驗匯總圖從上至下依次為原液、高溫破壞20、40、60、120、240、720 min
2.4 雜質A的制備、分離與純化
取去乙酰毛花苷原料3 g,用輔料溶液配制成約0.2 mg·mL-1,121℃ 120 min后,注入預先制備好的大孔樹脂(Amberlite XAD-6)柱中進行吸附,先以水、20%乙醇水溶液各洗脫一個柱體積,再以100%乙醇洗脫,收集100%乙醇洗脫液,旋轉蒸發濃縮,得到固體A。再進行硅膠柱層析,以氯仿-甲醇(10∶1.2)為洗脫液洗脫,收集雜質A的濃集部分洗脫液,旋轉蒸發濃縮,得雜質A的粗品,反復進行硅膠柱層析,得到雜質A的精制品,再經甲醇重結晶,裝于西林瓶中,置盛有五氧化二磷的減壓干燥器中,40℃減壓干燥24 h,即得。
2.5 雜質A的紫外光譜解析
取雜質A與去乙酰毛花苷對照品用甲醇配制成約10 μg·mL-1,在200~400 nm波長范圍掃描測定UV光譜圖。雜質A與去乙酰毛花苷的紫外光譜圖完全一致,最大吸收波長均為220 nm。去乙酰毛花苷分子結構中具有C=C和C=O的共軛結構,其中C=O是強吸收,吸收系數ε>104。雜質A與去乙酰毛花苷均符合甲型強心苷元的吸收特征,以此推斷:雜質A與去乙酰毛花苷具有相同的苷元母核共軛結構。
2.6 雜質A的紅外光譜解析
取雜質A、地高辛苷元對照品與KBr粉末混勻、研細、壓片,在4000~400 cm-1波數范圍測定。結果雜質A與地高辛苷元對照品的紅外光譜一致。
2.7 主要雜質的質譜解析
取注射液和“2.1”項下的雜質A溶液、去乙酰毛花苷對照品溶液、地高辛苷元對照品溶液,分別按“2.2”項下色譜與質譜條件進行試驗,結果雜質A溶液與注射液中雜質A及地高辛苷元對照品溶液的一級質譜顯示出相同的m/z 413.5、m/z 803.5、m/z 389.5,推測分別為 [M+Na]+峰、[2M+Na]+峰、[M-H]+峰,可以推測雜質A的分子量為390.5,分子式為C23H34O5,初步確定為地高辛苷元。雜質C的一級質譜顯示出m/z 521.6、m/z 519.6,推測分別為[M+H]+峰、[M-H]+峰,推測雜質C分子量為520.6,分子式為C29H44O8,初步確定為Digoxigenin Monodigitoxoside。雜質 E的一級質譜顯示出 m/z 651.7、m/z 649.7,推測分別為[M+H]+峰、[M-H]+峰,推測雜質E分子量為650.7,分子式為C35H54O11,初步確定為Digoxigenin Bisdigitoxoside。
2.8 雜質A的核磁共振及綜合解析
取雜質A以CD3OD溶解并繪制1H-NMR、13CNMR。雜質A:白色粉末,熔點210℃,熔融同時分解。Legal反應顯陽性,噴以10%硫酸乙醇試劑顯橙色,提示該化合物可能為甲型強心苷類化合物。1HNMR結果顯示:δ 5.90(1H,s)和δ 4.92(2H,dd)兩個質子信號分別為五元不飽和內酯環上22位及21位H信號,δ 0.97(3H,s)和δ 0.79(3H,s)分別為18、19位甲基氫信號。13C-NMR化學位移結果與文獻[6]報道的Digoxigenin的13C-NMR數據一致,故鑒定該化合物為地高辛苷元,Digoxigenin,化學名:3β,12β,14-三羥基-5β-強心甾-20(22)-烯內酯。
3 討 論
3.1 本次實驗的色譜條件,對2010版《中國藥典》收載的去乙酰毛花苷有關物質檢查項下色譜條件進行了優化,通過對梯度的調整,使得色譜圖的基線更加平穩,有利于雜質F的檢測。
3.2 曾經按“2.2”項下色譜與質譜條件同時對去乙酰毛花苷注射液及其生產時使用的對應批號原料進行有關物質分析測定,結果原料中未檢出雜質A,可見注射液中雜質A產生主要來源于制劑工藝。
3.3 由破壞性試驗結果顯示,去乙酰毛花苷原料在酸破壞、光照破壞條件下降解產生雜質A、C、E(見圖1、2),在121℃高溫破壞下也同樣均可產生雜質A、C、E,其中雜質C、E的量在120 min時達到最大,720 min時幾乎完全轉化為雜質A。根據上述破壞試驗以及對雜質A的質譜分析結果,推測降解產生雜質A的可能途徑如下:去乙酰毛花苷在酸、光照、高溫等條件下,三處洋地黃毒糖基的氧苷鍵發生斷裂產生雜質A(雜質C、E的制備、分離及結構鑒定由另文發表),其可能的降解途徑見圖5。
3.4 按“2.2”項下色譜條件在200~400 nm波長范圍內對雜質A進行掃描檢測,結果顯示其純度為99.9%。曾測得雜質A熔點為210℃,熔融時同時分解,與地高辛苷元對照品(來源:USP)說明書提供的熔點(210℃)相同。
3.5 取雜質A、去乙酰毛花苷原料用甲醇配制成0.1 mg·mL-1的溶液,在200~400 nm波長范圍進行掃描,結果雜質A、去乙酰毛花苷原料均在220 nm波長處有最大吸收,且紫外光譜圖完全一致。去乙酰毛花苷分子結構中具有紫外吸收的化學鍵為苷元結構中的C=C和C=O的共軛結構,其中C=O是強吸收,吸收系數ε>104,根據紫外光譜圖判斷雜質A與去乙酰毛花苷具有相同的苷元母核共軛結構。
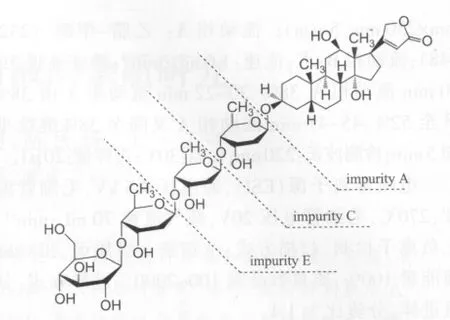
圖5 去乙酰毛花苷降解產生雜質A的途徑示意圖
[1] 賈俊彬,王愛明.普羅帕酮與去乙酰毛花苷在轉復心房顫動中的臨床觀察 [J].山西醫藥雜志,2010,39(10):964-5.
[2] 秦佳和.舌下含化倍他樂克聯合靜脈注射去乙酰毛花苷治療快速房性心律失常的療效觀察 [J].西南軍醫,2007,9(5):43-4.
[3] Eskwith IS,Fogarty TF.The treatment of auricular arrhythmia with deslanoside[J].Am J Cardiol,1958,2(5): 579-85.
[4] 國家藥典委員會.中華人民共和國藥典:二部[S].北京:中國醫藥科技出版社,2010:81.
[5] Deslanoside,Deslanoside Injection[S].U.S.Pharmacopeia and National Formulary,32:2074.
[6] Penelope R,Foss B,Benezra SA.Digoxin[J].Anal Profiles Drug Subt,1980,9:207-43.