兩例凝血因子Ⅴ缺陷癥患者的基因分析
謝海嘯,王明山,牛真珍,謝耀盛
(溫州醫學院附屬第一醫院 實驗診斷中心,浙江 溫州 325000)
凝血因子V(coagulationg factor V,FV)是凝血過程中一種重要的輔因子,其活化形式FVa與Ca2+、磷脂和FXa形成的復合物是體內凝血酶原最主要的激活物。除了凝血功能,FV也通過輔助活化蛋白C下調活化因子VI I I間接參與生理性抗凝旁路途徑。FV的這一雙重作用,使得FV基因缺陷的臨床表現差異較大,可表現為出血、血栓形成,也可無明顯臨床癥狀[1]。我們發現了2例凝血因子V缺陷患者,現報告如下。
1 資料和方法
1.1 一般資料 患者1:女,62歲。白內障術前凝血常規篩查發現血漿凝血酶原時間(PT)、活化部分凝血活酶(APTT)顯著延長,分別為31.5和104.1 s。進一步做凝血因子活性檢測,發現FV:C為4%。患者無肝腎功能障礙,無出血病史,父母非近親結婚。
患者2:女,41歲。眼部翼狀胬肉切除術前凝血常規檢查發現PT 23.6 s、APTT 75.9 s,FV:C為5%。患者無出血病史,肝腎功能正常,父母亦非近親婚配。
正常對照組:50例,其中男27例,女23例,平均年齡34(18~60)歲,均為我院健康體檢者,經查均無肝腎功能疾病,無血栓或出血史,采樣前已征得本人同意。
1.2 方法
1.2.1 標本的采集和處理:在征得患者知情同意后,采集外周靜脈血,0.109 mol/L枸櫞酸鈉1:9抗凝,立即于3 000 r/min離心10 min后收集上層血漿用于凝血指標檢測,2 h內檢測完畢。剩余的血細胞-40 ℃凍存,用于DNA提取。
1.2.2 凝血相關指標檢測:法國STAGO全自動血凝儀檢測APTT、PT、纖維蛋白原(FIB)、FI I:C、 FV:C、FX:C。試劑由STAGO公司配套提供。所有操作步驟均嚴格按照試劑說明書進行。
1.2.3 血漿凝血因子V抗原(FV:Ag)檢測:采用雙抗體夾心酶聯免疫吸附試驗(ELISA)法。綿羊抗人FV抗體為Cedarlane Laboratories Limited公司產品,辣根過氧化物酶標記的FV抗體的制備使用EZ-Link Plus Activated Peroxidase Kit(Pierce Biotechnology,Inc.公司產品)。血漿樣本1:200稀釋,酶標記抗體濃度為2μ g/mL,492 nm比色。以50人份正常對照混合血漿為100%,計算患者及家系成員FV:Ag含量。
1.2.4 FV基因測序:按常規酚-氯仿法抽提患者外周血基因組DNA。引物序列參照文獻[2]設計并由上海桑尼生物科技有限公司合成。PCR擴增FV的25個外顯子序列。PCR反應總體積為50μL,包括10×PCR Bufer,MgCl2(終濃度為 1.5 mmol/L),dNTP(終濃度為200μmol/L),2 U Taq DNA聚合酶,引物(終濃度為0.5μmol/L)。擴增條件:94 ℃,5 min,94 ℃變性30 s,50~60 ℃退火30 s,72 ℃延伸30~60 s,30~35個循環后,72 ℃,10 min。PCR產物在全自動測序儀上進行測序(美國Applera公司,ABI3730XL型)。
2 結果
2.1 凝血指標檢測 患者1 APTT 104.1 s、PT 31.5 s,均明顯延長,FV:C為4%,FV:Ag為2.6%。患者2 APTT 75.9 s、PT 23.6 s,亦明顯延長,FV:C為5%,FV:Ag為18.9%。見表1。
2.2 FV基因分析 通過Chromas軟件將2例患者FV基因測序結果與NCBI基因文庫AY364535序列進行比對(Blast)后,再與NCBI中的單核甘酸多態性數據庫(http://www.ncbi.nlm.nih.gov/SNP/snp.ref.cgi?locusId=2153)比對。2例患者共發現了8個基因多態性位點,其中有4個共同的多態性位點均在B區,分別為Lys858Arg、His865Arg、Lys925Glu和Pro1404Ser。具體見表2。
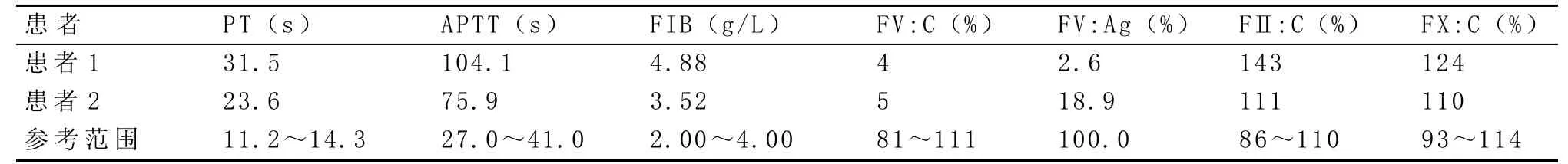
表1 2例FV缺陷患者凝血指標項目檢測結果

表2 2例FV缺陷癥患者基因分析結果
3 討論
遺傳性凝血因子V缺乏是一種罕見的常染色體隱性遺傳性疾病,發病率為百萬分之一[3]。FV基因位于人類1q21~25上,由25個外顯子和24個內含子組成,長度約80 kb,成熟FV蛋白結構為A1-A2-B-A3-C1-C2,FV在凝血酶或FXa的作用下,在第709、1018和1545位精氨酸處發生裂解,切去其B結構域,活化成為FVa,形成由A1、A2區組成的重鏈和A3、C1、C2區組成的輕鏈所構成的異二聚體。FV缺陷癥主要分為兩型:I型為CRM-,交叉反應物質陰性,即FV抗原(FV:Ag)和活性(FV:C)同步減少;I I型為CRM+,FV:C極低而FV:Ag正常,其產生了無功能或是功能異常的FV蛋白。本研究結果,患者1,FV:C為4%,FV:Ag為2.6%,CRM-。患者2,FV:C為5%,FV:Ag為18.9%,抗原水平稍高,為非典型的CRM-。有趣的是,兩人FV:C與FV:Ag水平都很低,診斷為FV缺陷,但皆無明顯的臨床癥狀,且除了較多的多態性位點外,目前尚未發現其他突變。
曹麗娟等[4]曾報道兩病例具有相同的FV活性和抗原含量,皆為2%,但臨床表現卻有很大的不同,患者1自出生起出現周期性自發性鼻出血,患者2卻一直無癥狀。FV抗原和活性的含量與臨床表現之間沒有很好的一致性,目前還沒有合理的理論來解釋這一點。FV的下降并不是決定FV缺陷患者臨床癥狀輕重的唯一因素。有學者推測可能存在一種未知的調節因子或機制[5]。
本研究2例FV缺陷患者,基因分析未發現其他突變,而只有8個基因多態性位點,國內外文獻未報道過類似病例。2例患者同時擁有Lys858Arg、His865Arg、Lys925Glu和Pro1404Ser這4個多態性位點,且均位于B結構域。長期以來,人們對B區的功能不夠重視,因為FV活化為FVa時,B區是被切除而游離出來。但凝血酶激活FV的3個位點都位于B區,B區對于FV活化是必要的。Yamazaki等[6]曾報道Met385Thr、His1299Arg、Met1736Val和Asp2194Gly這4種多態性,并對其作了體外表達研究,發現這4種多態性同時存在時,FV的表達水平比野生型顯著降低,細胞培養液中FV表達水平僅約為野生型的20%,其原因是變異的蛋白質合成率明顯降低且伴分泌障礙,其中Asp2194Gly是造成分泌障礙的關鍵因素。故推測本研究2例患者B區多態性位點的疊加可能與FV缺陷有關或是某一兩個位點起主要作用,具體機制有待進一步研究。
另外患者2 FV:C為5%,FV:Ag為18.9%,抗原水平稍高,為非典型的CRM-,推測其多態性除了導致FV分泌障礙外,還可能有蛋白正常功能的缺失。由于FV基因龐大,基因結構比較復雜,其龐大的內含子區序列突變也可能對其功能產生影響。僅僅通過對外顯子區的測序分析,一些FV缺陷癥的基因缺陷還是不能被完全確認。因此,對患者的FV基因外顯子側翼含拼接點的內含子進行測序分析是必要的,以期發現新的有意義的突變。
[1] Mannnucci PM,Duga S,Peyvandi F.Recessively inherited coagulation disorders[J].Blood,2004,104(5):1243-1252.
[2] Fu QH,Zhou RF,Liu LG,et al.Identification of three F5 gene mutations associated with inherited coagulation factor V deficiency in two Chinese pedigree[J].Haemophilia,2004,10(3):264-270.
[3] Kalafatis M.Coagulation factor V:a plethora of anticoagulant molecules[J].Curr Opin Hematol,2005,12(2):141-148.
[4] 曹麗娟,王兆鉞,蘇雁華,等.兩例先天性凝血因子V缺乏癥基因突變的鑒定[J].血栓與止血學,2007,13(1):17-19.
[5] Wilk R,Nieuwenhuis K,Berq M, et al.Five novel mutations in the gene for human blood coagulation factor V associated with type I factor V deficiency[J].Blood,2001,98(2):358-367.
[6] Yamazaki T, Nicolaes GA, Sorensen KW, et al. Molecular basis of quantitative factor V de?ciency associated with factor V R2 haplotype[J]. Blood,2002,100(7):2515-2521.

