毛細管電泳電化學法檢測過氧化氫
董冉冉 張 燕 時克林 馬艷芳 李玲君 王曉蕾
(1.山東師范大學化學化工與材料科學學院,濟南 250014; 2.淄博六中,淄博 252300)
毛細管電泳電化學法檢測過氧化氫
董冉冉1張 燕1時克林2馬艷芳1李玲君1王曉蕾1
(1.山東師范大學化學化工與材料科學學院,濟南 250014; 2.淄博六中,淄博 252300)
以金微盤電極和離子液體修飾單壁碳納米管糊微盤電極分別作為毛細管電泳電化學檢測器,試驗了兩種電極對過氧化氫的響應情況,將金微盤電極與毛細管電泳聯用,對過氧化氫進行了定性和定量檢測。探討了分離電壓、緩沖溶液pH值和工作電位等條件對H2O2檢測的影響。實驗結果表明,峰電流與H2O2濃度在1.0×10-6~1.0×10-5mol/L和3.0×10-5~1.0×10-3mol/L呈良好的線性,線性回歸方程分別為y(nA)=0.041 78+0.015 5x (μmol/L),y(A)=-3.304 5×10-4+0.024 29x (mmol/L),相關系數分別為0.997 5和0.999 0,當信噪比S/N=3時,濃度檢出限為5×10-7mol/L。實驗中發現,樣品中的多巴胺、抗壞血酸等對H2O2的測定無干擾。
金微盤電極 碳納米管糊微盤電極 毛細管電泳 電化學檢測 過氧化氫
自由基是近年來基礎醫學和生命科學領域的研究熱點,在生命活動的代謝過程中不斷產生各種活性氧自由基(ROS)。過氧化氫(H2O2)作為活性氧家族中的一員也是體內氧化代謝的產物,氧化作用很強,可由超氧陰離子自發岐化生成,并能進一步生成羥自由基;可直接作用于膜脂質,形成脂質過氧化物,導致細胞膜的損傷、DNA損傷及其它的生物疾病[1];還可通過脂質過氧化物分解代謝產物丙二醛(MDA),促使蛋白質交聯聚合反應引起細胞損傷[2]。H2O2不僅能直接氧化細胞膜上的脂質及蛋白,而且能自由穿過細胞膜和細胞內的鐵離子反應生成·OH等活性更強的自由基,引起一系列的損傷[3]。由于H2O2在生命體中發揮著重要的作用,設計一種有效、準確地檢測H2O2的方法,可以提前診斷和預防某些氧化脅迫和損傷誘導的重要疾病[4]。
H2O2的檢測方法主要有電化學檢測法[5]、分光光度法[6]、化學發光法[7]、熒光法[8]。在這些方法中紫外檢測法的樣品用量大且檢測靈敏度不高;熒光法靈敏度雖高但因儀器昂貴而不能得到廣泛推廣;電化學檢測法因其靈敏度較高、儀器設備較廉價等優點而常見報道[9]。A lpat[10]用石墨粉、礦物油、H2O2酶、沸石混合制成碳糊電極,利用脈沖和循環伏安法檢測了 H2O2,H2O2濃度在5×10-6~1×10-3mol/L范圍內與循環伏安信號具有良好的線性關系,檢出限為8×10-7mol/L,該方法成功地用于檢測牛奶中的H2O2。毛細管電泳電化學檢測法因樣品用量小、靈敏度高、選擇性好、分析時間短、儀器設備價格低而被廣泛應用。
筆者自制了金微盤電極和離子液體修飾碳納米管糊微盤電極作為毛細管電泳電化學檢測器,通過實驗比較了兩種電極對H2O2的響應情況,選擇了金微盤電極與毛細管電泳聯用在正電位區檢測H2O2,探討了分離電壓、緩沖溶液pH值和工作電位等條件對H2O2檢測的影響,實現了H2O2的定性和定量分析。
1 實驗部分
1.1 主要儀器與試劑
電化學工作站:CHI802b 型,上海辰華儀器公司;
高壓電源:山東師范大學儀器廠;
毛細管:?25 μm×35 cm,河北永年瑞灃色譜器件有限公司;
H2O2:30%,國藥集團化學試劑有限公司;
抗壞血酸(AA):純度99%,美國Sigma公司;
多巴胺(DA):純度98%,美國Sigma公司;
N-辛基吡啶六氟磷酸鹽:上海成捷有限公司;
磷酸氫二鈉、氫氧化鈉等:分析純,國藥集團化學試劑有限公司;
實驗中所用水均為石英亞沸高純水,所用溶液使用前均用0.22 μm尼龍濾膜過濾。
1.2 離子液體修飾碳納米管糊微盤電極和金微盤
電極的制備
(1)離子液體修飾碳納米管糊微盤電極的制備
將單壁碳納米管和離子液體以不同的質量比混合均勻,加熱后裝入內徑200μm、外徑375 μm、長約4 cm的石英毛細管中,用一銅絲在加熱的情況下將單壁碳納米管和離子液體壓緊以保持良好導電性,將銅絲另一端纏繞到一直徑0.4 mm,長5 cm的銅絲上,兩銅絲接觸部分涂上銀導電膠,放在80℃ 烘箱中烘干。將石英毛細管和銅絲插入一長約3.0cm、外徑約1 mm、內徑約為0.3 mm的玻璃管,用GJ-301型環氧樹脂膠將銀導電膠所覆蓋的部分封在玻璃管內,將電極晾干,在硫酸紙上打磨光滑待用。
(2)金微盤電極的制備
將一直徑為200μm、長約4 cm金絲插入一段長約3 cm、內徑250μm、外徑375 μm的石英毛細管中,一端露出金絲,一端與石英毛細管末端對齊,用GJ-301型環氧樹脂膠填滿整個毛細管,將露在外面的金絲纏繞到一長約5 cm的銅絲(?0.4 mm×5 cm)上,并用銀導電膠將纏繞部分覆蓋,使其導電良好,將其放在80℃烘箱中烘1 h后,插入一段長約3.0cm、外徑約1 mm、內徑約為0.5 mm的玻璃管,用GJ-301型環氧樹脂膠封住玻璃管的兩端,將毛細管和銅絲接口處封在玻璃管內,用金相砂紙打磨使電極表面光滑,依次用二次水、乙醇、二次水各超聲5 min,晾干待用。
1.3 H2O2的分析
毛細管電泳分離系統建立在自組裝的電泳儀上,毛細管進樣端與高壓電源正極一起插入電泳緩沖液池中。毛細管出口端用固定在檢測電解池上,高壓電源負極與此檢測池連通。充滿電泳緩沖液的毛細管與高壓電源形成回路,構成毛細管區帶電泳的分離系統。工作前,利用三維顯微操縱器調節工作電極的位置與毛細管的出口端緊密對接。調節高壓電源電壓為18 kV,當基線電流平穩后,電壓調到5 kV電遷移進樣10.0s,并開始記錄電泳圖。檢測系統在CHI802b上利用三電極體系,以柱端安培檢測法對H2O2進行檢測。毛細管在使用前依次用0.1 mol/L NaOH、二次水、電泳緩沖液各清洗5 m in,工作電極電勢均相對于飽和甘汞電極(SCE)。
2 結果與討論
2.1 工作電極的篩選
根據文獻[11]報道的以N-辛基吡啶六氟磷酸鹽為粘合劑的CNTs電極對H2O2的電化學反應有明顯的催化作用,筆者認為該類電極可以用作毛細管電泳檢測器。實驗中筆者以不同比例制備了離子液體修飾碳納米管糊微盤電極和金微盤電極,分別試驗了單壁碳納米管和離子液體質量比為1∶9、2∶8、3∶7、4∶6、1∶1 時制成的離子液體修飾單壁碳納米管糊微盤電極和金微盤電極對H2O2的響應情況。圖1為H2O2在單壁碳納米管與離子液體的質量比為3∶7的糊微盤電極和金微盤電極上的電泳圖。分離電壓:圖1A為14 kV,圖1B為18 kV;H2O2濃度:圖1A為1 mmol/L,圖1B為0.1 mmol/L;緩沖溶液:0.025 mol/L pH 7.4 PBS;5.0kV電遷移進樣10.0s;檢測電勢:0.80V;毛細管:內徑25 μm,外徑 375 μm, 長 35 cm。
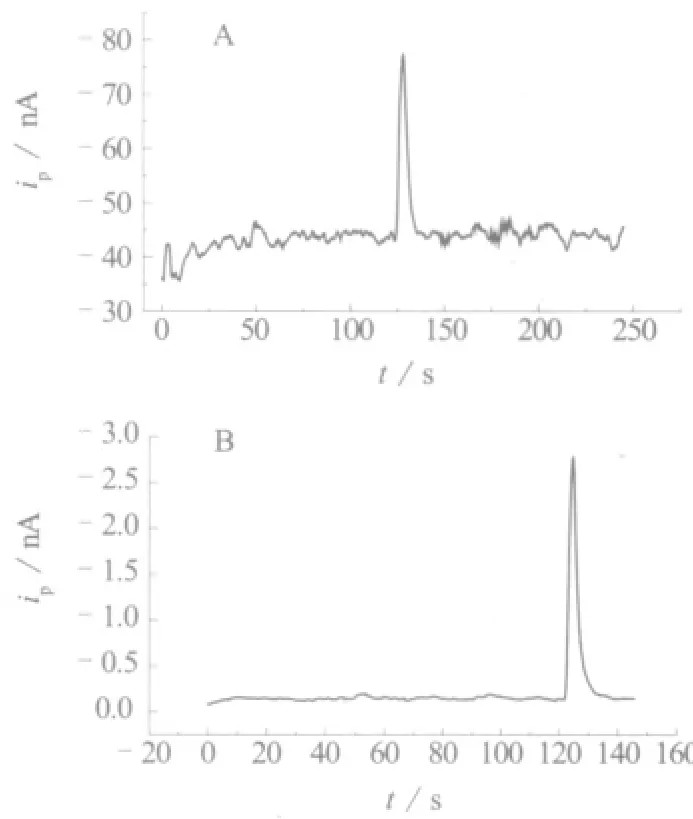
圖1 H2O2在離子液體修飾碳納米管糊微盤電極(A)和金微盤電極(B)上的電泳圖
實驗發現,單壁碳納米管含量越大,基線則越高,噪音也越大,當質量比為3∶7時所制得的糊微盤電極信噪比較好,但這種離子液體修飾碳納米管糊微盤電極檢測H2O2時基線仍太高、噪音太大,信噪比很小,不適合用于毛細管電泳檢測。因此實驗選擇了金微盤電極作為工作電極。
2.2 檢測電勢
在0.025 mol/L Na2HPO4-NaH2PO4緩沖液中,固定進樣條件和分離條件,改變檢測電勢Ed,對H2O2進行檢測。實驗中發現,當檢測電位在負電位區時,電流基線過高,且空白液出現峰電流(檢測條件同圖1),這是由于在負電位區時水中的溶解氧會在電極表面反應所致[5]。當檢測電勢在正電位區時,峰電流隨著檢測電位的增大而增大,信噪比增大,當高于0.9 V后,隨檢測電勢增大,基線電流也顯著增大,基線噪音也增大,信噪比明顯減小,所以選擇檢測電勢為0.8 V。
2.3 分離電壓
分離電壓對分離速度、分離度、半峰寬等均產生影響。實驗在0.025 mol/L Na2HPO4-NaH2PO4緩沖液中,固定進樣條件及檢測條件,在10~20kV電壓范圍內選擇不同的分離電壓Vs進行H2O2檢測(實驗條件同圖1)。表1列出了遷移時間tm、峰半寬W1/2、分離電壓Vs與峰電流ip值。
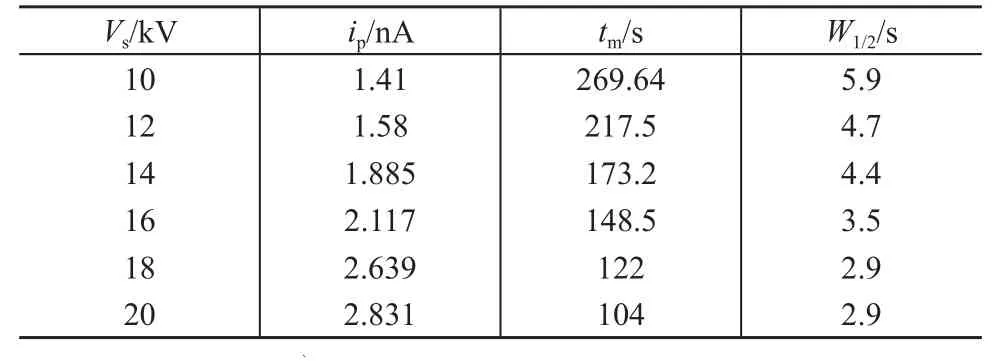
表1 分離電壓與i p、t m、W1/2的關系
由表1可以看出,遷移時間隨分離電壓的增大而減少,峰電流隨分離電壓增大而增大,但是高電壓也同時造成了基線噪音增大,從而降低了信噪比。因此實驗中選擇18 kV為分離電壓。
2.4 緩沖溶液的pH值
試驗了不同pH值的NaH2PO4-Na2HPO4緩沖液對H2O2測定的影響。實驗發現,當pH值在6.8~9.0時,峰電流隨著pH值的增大而增加,但變化幅度不大。由于H2O2在pH 3.5~4.5時最穩定,在堿性溶液中極易分解,本實驗將用于檢測生物樣品,因此選擇了緩沖溶液的pH值為7.4。
綜合上述結果,毛細管電泳檢測H2O2的最佳實驗條件:緩沖液為0.025 mol/L Na2HPO4-NaH2PO4(pH 7.4),分離電壓為18 kV,檢測電勢為0.8 V,進樣時間為5 kV下進樣10.0s。
2.5 工作曲線、精密度、檢出限
在上述最佳實驗條件下,對不同濃度的H2O2進行電泳分離,H2O2濃度在1.0×10-6~1.0×10-5mol/L和 3.0×10-5~1.0×10-3mol/L范圍內與峰電流呈較好的線性關系,線性回歸方程分別為y(nA)=0.041 78+0.015 5x (μmol/L),y(A)=-3.304 5×10-4+0.024 29x (mmol/L),相 關 系 數 分 別 為 0.997 5,0.999 0。當信噪比S/N=3時,H2O2的檢出限為5×10-7mol/L。對1×10-4mol/L的H2O2進行7次平行測定,統計結果顯示,tm與ip的相對標準偏差分別為2.2%、2.7%,表明這種測定H2O2的方法具有良好的重現性。
實驗中,對其它常見的電活性物質進行了檢測,結果如圖2所示(分離電壓:18 kV,其它檢測條件同圖1)。

圖2 H2O2、多巴胺、抗壞血酸混合液的電泳譜圖
從圖2中可以看出,抗壞血酸(AA)和多巴胺(DA)在毛細管電泳譜圖上能夠得到很好的分離,說明這些電活性物質不會干擾H2O2的測定。
2.6 樣品檢測
酶催化反應在生命的新陳代謝過程中具有重要的作用。酶作為具有高度專一性和高效性的特殊生物源催化劑, 在藥物化學、食品檢驗、分析化學、生物化學等領域有著廣泛的應用[12]。葡萄糖氧化酶(GOD)是一種需氧脫氫酶,對人體無毒、無副作用,廣泛存在于動植物和微生物體內,是一種高效高度專一的生物催化劑,葡萄糖氧化酶的每個酶分子中含有兩單位FAD(黃素腺嘌呤二核苷酸),在有氧條件下能專一性地催化β-D-葡萄糖生成葡萄糖酸,并產生H2O2。利用有氧催化葡萄糖生成葡萄糖酸這一性質可以有效除氧,例如果汁、啤酒、油脂罐頭中除氧,金屬器械防腐,并且廣泛用于抗氧化劑、葡萄糖酸的生產[13]。
在最佳的實驗條件下,向葡萄糖溶液中加入葡萄糖氧化酶,檢測不同時間下催化反應生成的H2O2的量,每5 m in取樣檢測一次,得到催化反應中電流大小與催化時間的關系圖(見圖3,其中葡萄糖:1 mmol/L, GOD:43.6 U/L;其它檢測條件同圖1)。
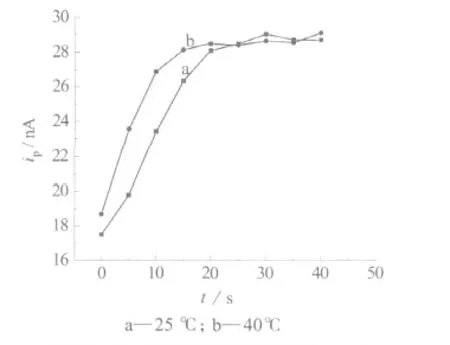
圖3 催化反應中H2O2的峰電流與催化時間的關系
由圖3可見,加入GOD后,立即有H2O2生成,由此說明,酶催化反應基本沒有滯后期。在反應開始時,電流明顯增大,電流與催化時間成正比,隨酶催化反應的進行,反應速率逐漸變小,曲線彎曲;當催化時間繼續延長,底物葡萄糖基本耗盡,反應達到終點,不再有H2O2生成,酶催化反應達到平衡,電流達到穩定。
研究了溫度對酶活性的影響,當催化反應控制在25℃時,催化反應進行25 m in達到平衡,之后電流沒有明顯的變化,而當催化反應控制在40℃時,催化反應只需進行15 m in,反應很快達到平衡,并且電流增大的幅度比在25℃時明顯大,說明隨著溫度的升高,葡萄糖氧化酶的活性提高,酶催化反應能更快地達到平衡。
3 結語
通過對金微盤電極與離子液體修飾碳納米管糊微盤電極測定H2O2的響應情況的比較,選擇了金微盤電極在正電位區不用除氧即可實現過H2O2的檢測,在優化的實驗條件下,H2O2的檢出限為5×10-7mol/L。該法可用于葡萄糖氧化酶催化反應的研究。
[1]Inoue S, Kawanishi S. Hydroxyl radical production and human DNA damage induced by ferric nitrilotracetate and hydrogen peroxide [J]. Cancer Res, 1987, 47: 6 522-6 527.
[2]趙保路. 氧自由基和天然抗氧化劑[M].北京:科學出版社,1999: 9.
[3]葉錦霞,王嵐,楊濱,等.紅花水提物對乳鼠心肌細胞H2O2所致損傷的保護作用及ESR譜研究[J].中國實驗方劑學雜志,2010,16(2): 56-59.
[4]Gong X C, Li Q L, Xu K H, et al. A new route for simple and rapid determ ination of hydrogen peroxide in RAW 264.7 macrophages by m icrochip electrophoresis[J]. Electrophoresis, 2009,30(11):1 983-1 990.
[5]Radschuw eit A, Rüttinger H H, Nuhn P. Capillary zone electrophoresis w ith electrochem ical detection-a sim ple and effective method to analyze oxygen-consum ing and peroxideforming processes[J]. J Chromatogr A, 2001, 937: 127-134.
[6]Schm itz O, Gab S. Separation of isomeric hydroperoxides of unsaturated fatty acids by CE [J]. J Chromatogr A, 1997, 767:249-253.
[7]Hu Y, Zhang Z, Yang C. The determ ination of peroxides generated from cigarette smoke w ith an ultrasensitive and highly selective chem ilum inescence method [J]. Anal Chim, 2007, 601(1): 95-100.
[8]Srikum D, M iller E W, Domaille D W, et al. An ICT-Based Approach to Ratiometric Fluorescence Imaging of hydrogen peroxide in Living Cells [J]. J Am Chem Soc, 2008, 130: 4 596-4 597.
[9]Toniolo R, Geatti P, Bontempelli G, et al. Amperometric monitoring of hydrogen peroxide in workplace atmospheres by electrodes supported on ion-exchange membranes [J]. Electroanal Chem,2001, 514: 123-128.
[10]A lpat S, A lpat S K, Dursun Z, et al. Development of a new biosensor for m ediatorless vo ltamm etric determ ination of hydrogen peroxide and its application in m ilk samples [J]. J Appl Electrochem, 2009, 39: 971-977.
[11]Kachoosangi R T, Musameh M M, Yousef I A, et al. Carbon Nanotube-Ionic Liquid Composite Sensors and Biosensors[J].Anal Chem, 2009, 81: 435-442.
[12]Liu C, Yuan J G , Wang Y X, et al. Progress on Glucose Oxidase[J].Food and Drug, 2010(7): 285-289.
[13]陳剛, 葉建農, 張劍霞, 等.新型葡萄糖氧化酶電極與毛細管電泳的聯用[J].復旦學報,2002(4): 382-387.
DETERM INATION OF HYDROGEN PEROXIDE BY CAPILLARY ELECTROPHORESIS W ITH AMPEROMETRIC DETECTION
Dong Ranran1, Zhang Yan1, Shi Kelin2,Ma Yanfang1, Li Lingjun1, Wang Xiaolei1
(1.College of Chemistry Chemical Engineering and Materials Science, Shandong Normal University, Jinan 250014, China;2.Zibo No.6 High School of Shandong, Zibo 252300, China)
Gold m icroelectrode and ionic liquid modified-SWNTs paste m icroelectrode made by ourselves were used in capillary zone electrophoresis w ith electrochem ical end-column amperometric detection to determ ine hydrogen peroxide. Gold m icroelectrode showed higher sensitivity to H2O2was used as the detector of capillary electrophoresis. Factors influencing the performance, including separation voltage, detection potential and pH value of the buffer were studied. Under optim ized detection conditions, hydrogen peroxide responded linearly from 1.0×10-5-1×10-3mol/L and 3.0×10-5-1.0×10-3w ith a correlation coefficient of 0.997 5 and 0.999 0respectively. The concentration limit of detection of the method was 5×10-7mol/L(S/N=3). The experiment also showed that there was no electroactive interferences such as dopam ine and ascorbic acid.
gold m icroelectrode, SWNTs paste m icroelectrode, capillary electrophoresis, electrochemical detection,hydrogen peroxide
2011-09-19

