蜈蚣敗毒飲對小鼠尾部鱗片表皮顆粒層形成及血清IL-2影響的實驗研究
楊素清,閆景東,周妍妍
(1.黑龍江中醫藥大學附屬第一醫院,黑龍江 哈爾濱 150040;2.黑龍江中醫藥大學,黑龍江 哈爾濱 150040)
銀屑病,中醫學將其歸屬于“干癬”、“白疕”、“松皮癬”等病證范疇,是一種常見的慢性復發性、炎癥性皮膚病,本病發病率高,病程長,易反復發作,嚴重影響了患者的身心健康,是國內外皮膚科領域重點研究和防治的疾病之一。迄今為止,銀屑病的確切病因和發病機制尚未完全闡明。多認為是多基因遺傳背景下T細胞介導的免疫異常性疾病,其發病主要涉及遺傳、感染、免疫、神經、內分泌、環境等多方面的因素。目前,臨床中治療該病尚未有突破性進展。中醫藥治療銀屑病強調整體觀念和辨證論治,用藥靈活、治法豐富、療效肯定,且副作用小、不易復發,顯示出了明顯的優勢。
1 實驗材料
1.1 動物
健康昆明種小鼠50只,雄性,體重(18~22)g,由黑龍江中醫藥大學實驗動物中心提供。
1.2 藥物與試劑
蜈蚣敗毒飲(由黑龍江中醫藥大學附屬第一醫院中藥局提供);復方青黛丸(陜西天寧制藥有限責任公司,批號:060505);0.9%生理鹽水(哈爾濱三精艾富西藥業有限公司,批號:20023690)。
1.3 主要儀器
普通切片機(YD-1508,中國金華市醫療儀器廠);光學顯微鏡(OLYMPUS BX60,日本);病理圖像分析系統(cimas Med 6.0,麥克奧迪圖像技術有限公司)。
2 實驗方法
2.1 蜈蚣敗毒飲制備
蜈蚣敗毒飲由蜈蚣3條,烏蛇30g,紫草30g,鬼箭羽30g,土茯苓30g,甘草10g組成,加8倍量水浸泡4h,加熱煎煮1h,藥渣再加6倍水,煎煮1h,過濾,兩次濾液合并,最后濃縮成生藥濃度分別為0.59g·mL-1(低濃度)、1.17g·mL-1(中濃度)、2.34g·mL-1(高濃度)。
2.2 復方青黛丸懸濁液的制備
當沒有勇氣接納不幸,沒有力量擁抱內心深處的痛苦或恐懼,在封閉地承受支離的心靈面前,除了尊重與等待,可選擇的援助之一,是讓當事人有機緣親臨一種彼此分享“教導自己認識自我”體驗的場中,意識到要重獲力量,必須復歸自身認同與完整。而自身認同與完整的真諦,是尊重直面生命經歷的一切,有定力讓所有力量匯聚不分離。抽身靜觀自己的思想、情緒和身體,悅納悲喜寵辱,不以物喜,不以己悲,是重新匯聚力量獲得勇氣更新的密鑰。
復方青黛丸溶于生理鹽水中,配成藥物濃度為0.052g·mL-1的混懸液備用。
2.3 分組方法
將50只昆明種小鼠隨機分成五組,即蜈蚣敗毒飲低劑量組(簡稱中低組)、蜈蚣敗毒飲中劑量組(簡稱中中組)、蜈蚣敗毒飲高劑量組(簡稱中高組)、復方青黛丸組(簡稱陽性對照組)和生理鹽水組。
2.4 給藥方法
中低組、中中組、中高組、陽性對照組和生理鹽水組,分別給予低濃度蜈蚣敗毒飲[8.78g·(kg·d)-1]、中濃度蜈蚣敗毒飲[17.55g·(kg·d)-1]、高濃度蜈蚣敗毒飲[35.10g·(kg·d)-1]、復方青黛丸懸濁液[0.78g·(kg·d)-1]和生理鹽水[15mL·(kg·d)-1]灌胃 15d。
2.5 取材
連續給藥15d后,脫頸椎處死小鼠,摘眼球取血處死小鼠,并取距鼠尾根部約1.5cm處的背面皮膚,立即投入4%多聚甲醛溶液中固定,常規脫水,石蠟包埋,切片。
2.6 HE染色和IL測定
HE染色流程如下:二甲苯脫蠟→梯度酒精脫二甲苯→水洗→蘇木素染色→鹽酸乙醇分化→氨水返藍→伊紅染色→梯度酒精脫水→二甲苯透明→光學樹膠封片→烘片。
IL-2的測定嚴格按照試劑盒說明書操作。根據預實驗確定樣本稀釋倍數及標準曲線所使用的濃度,每個樣本做雙復孔。除空白孔外,分別將標本或不同濃度的標準品(100mL/孔)加入相應孔中,用封板膠紙封住反應孔,37℃孵箱孵育90min,洗板5次。除空白孔外,加入生物素化抗體工作液(100mL/孔),37℃孵箱孵育 60min,洗板 5次。加入酶結合物工作液(100mL/孔),37℃孵箱孵育 30min,洗板 5次。加入顯色劑(100mL/孔),避光37℃孵育10~15min,加入終止液,混勻后即刻測量OD450值。
2.7 統計學處理
3 實驗結果
3.1 HE染色結果
在光學顯微鏡下觀察,凡鱗片表皮有連續成行的顆粒細胞者,稱為有顆粒層形成之鱗片,計數100個鱗片中有顆粒層形成的鱗片數。結果見圖1~5及表1。
表1 蜈蚣敗毒飲對小鼠尾部鱗片表皮顆粒層形成的影響(±s)

表1 蜈蚣敗毒飲對小鼠尾部鱗片表皮顆粒層形成的影響(±s)
注:與生理鹽水組比較,**P<0.01;與陽性對照組比較,△P<0.05;與陽性對照組比較,△△P<0.01。
組別 n 顆粒層鱗片數/100鱗片生理鹽水組10 9.10±2.13陽性對照組 10 19.6±3.41**中低組 10 19.4±3.20**中中組 10 22.8±4.29**△中高組 10 27.4±3.17**△△
如圖所示,生理鹽水組顆粒層細胞少,有缺失。陽性對照組與中藥各劑量組顆粒層細胞較多,比較完整。中中組、中高組表現更為明顯,能夠顯著促進小鼠尾部鱗片中顆粒層的形成,出現數層顆粒細胞,細胞肥大,呈菱形,胞漿內顆粒粗大、深染,細胞界限清楚,細胞核及核仁明顯,細胞體積增大。
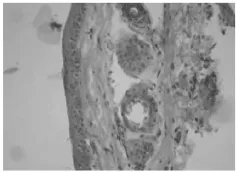
圖1 生理鹽水組40×

圖2 陽性對照組40×

圖3 中低組40×

圖4 中中組40×

圖5 中高組40×
3.2 對小鼠血清IL-2的影響 結果見表2。
表2 蜈蚣敗毒飲對小鼠血清IL-2的影響(±s)

表2 蜈蚣敗毒飲對小鼠血清IL-2的影響(±s)
注:與生理鹽水組相比,**P<0.01;與陽性對照組相比,△P<0.05。
組別 n 血清IL-2(pg·mL-1)10 4.20±0.68陽性對照組 10 2.94±0.44**中低組 10 2.95±0.61**中中組 10 2.62±0.40**中高組 10 2.45±0.47生理鹽水組**△
4 討論
銀屑病發病急,反復發作,不易根治,與中醫“毒、邪”致病特點相符。所謂“毒邪”,不僅是指從外感受的特殊致病因素,如有毒食物、藥物、化學制劑等所致的毒性反應,也是人體受某種致病因素作用后在疾病過程中所形成的病理產物,如熱毒、濕毒、風毒、火毒等。毒邪致病特點是發病急驟,發展迅速,易于傳變,病情重,病程久,頑固難愈。毒邪侵入人體,致氣血凝滯,經脈不暢,毒邪久積不化又生瘀毒,瘀滯肌膚。現代醫學研究亦表明,銀屑病患者常有全血粘度增高,真皮乳頭毛細血管擴張,臨床可見薄膜現象和點狀出血,這些均符合中醫“血瘀”理論。筆者總結多年臨床經驗,認為“毒”、“瘀”二邪是銀屑病發病的主要病理基礎。基于這一理論,創制了解毒清熱、活血化瘀的蜈蚣敗毒飲并將其用于臨床銀屑病患者的治療,取得了很好的療效。方中蜈蚣為君藥,以毒攻毒,取其解毒、化瘀、祛風之功,一藥而三用,且其善行之性入絡剔毒,直搗病所。紫草尤善清血分熱毒,本方取其涼血、活血、解毒之功;鬼箭羽破血、通經、殺蟲,其寒能堅陰清熱,又能入血,是常用的活血化瘀藥,具有破血、通經、解毒之功;土茯苓解毒除濕,通利關節。上三藥祛熱毒、瘀毒、濕毒,共為臣藥。烏梢蛇搜風邪,通經絡,蛇類善行,祛風而能止癢,其性走竄,能搜風邪,透關節,通經絡;配蜈蚣,剔除經絡之風,為佐藥。生甘草既調和諸藥,又保護胃氣,且兼解毒,為使藥。縱觀全方,共奏解毒祛瘀、搜風通絡之功。本方特點為重用蟲類藥物,利用其毒性之偏,以毒攻毒,并取其善行之性入絡剔毒,直搗病所。
迄今為止,銀屑病的發病機制尚不清楚,但是諸多因素導致的角質形成細胞過度增殖或分化障礙是其發病的基礎。銀屑病表皮的主要病理生理特點包括增生過快和角化不全兩個方面,基底細胞增殖加快,表皮通過時間由正常的28~56d縮短為3~4d,使角質形成細胞來不及成熟,故出現角化不全、顆粒層減少或消失的銀屑病典型病理特點[1]。小鼠尾部鱗狀上皮顆粒層細胞天然缺失,僅在毛囊處有少量的顆粒細胞,故可模擬銀屑病角化不全的病理特點。因此,鼠尾表皮模型屬天然模型,是目前公認的實驗性銀屑病病理模型之一[2]。此模型簡便易行,重復性好,在銀屑病藥物研究中較為常用。實驗結果表明,蜈蚣敗毒飲可顯著促進小鼠尾部鱗片中顆粒層細胞的形成,并隨劑量的增大而作用增強。且中、高濃度組的蜈蚣敗毒飲療效優于復方青黛丸組。由此推斷,蜈蚣敗毒飲是治療銀屑病的有效復方中藥制劑,其作用機制可能與改善銀屑病表皮細胞角化不全有關。
IL-2可促進B細胞分化,增加其分泌抗體的能力及促進NK細胞活性,是免疫調節中最關鍵的細胞因子,作為T細胞活化所必需的第3種信號,IL-2與IL-2受體(IL-2R)的結合對于T細胞的活化與增殖起著至關重要的作用;另外IL-2還可誘導c-myc及IL-2R表達,誘導細胞分泌IFN-γ、TNF、CSF等細胞因子,引起細胞因子網絡的失衡。銀屑病患者皮損處的IL-2異常增高是銀屑病發病組織損傷的病理基礎,是導致疾病發生的重要環節。目前已有學者提出,可通過阻止IL-2的產生或抑制其活性來特異性防止T細胞激活從而達到治療銀屑病的目的[3]。本研究采用ELISA方法測定各組小鼠血清IL-2水平,結果表明,各劑量蜈蚣敗毒飲均可降低小鼠血清IL-2的水平,與生理鹽水組比較,有顯著性差異(P<0.01);且中高組的效果優于陽性對照組,有顯著性差異(P<0.05)。提示蜈蚣敗毒飲抗銀屑病的作用可能與降低血清IL-2水平有關,通過降低血清IL-2水平,從而改善免疫功能狀態而發揮治療作用。
[1] 陳洪鐸.皮膚性病學[M].第4版.北京:人民衛生出版社,1999:110-115.
[2] 林熙然,黃敏.喜樹酊治療銀屑病的臨床觀察及實驗研究[J].中華皮膚科雜志,1982,15(4):210.
[3] Salim A,Emerson R.Targeting interleukin-2 as a treatment for psoriasis[J].Curr Opin Investig Drugs,2001,2(11):1546 -1548.

