進展期胃癌術前介入治療療效的觀察
印春濤 徐高峰
胃癌是我國高發的常見病之一,而且檢查出來后常常為進展期胃癌,少數患者已不能手術,即使能進行根治性手術的患者,手術后的復發率及轉移率也很高,常規放化療的緩解率也很低[1]。國內外報道經腫瘤供血動脈介入化療后,腫瘤組織病理學有效率達65%~80%。我科2001年3月至2005年5月,對50例進展期胃癌經影像學檢查能行外科手術切除的患者,進行術前動脈介入化療栓塞,取得了一定的療效,現報告如下。
1 資料與方法
1.1 一般資料
2001年3月至2005年5月,我們對50例經影像、胃鏡及病理檢查確診的進展期胃癌患者,行術前動脈化療栓塞,其中男性32例,女性18例,年齡41~73歲,中位年齡54歲。腫瘤部位:賁門和胃底部16例,胃體部12例,胃竇部22例。病理學分化:低分化腺癌31例,未分化腺癌2例,中、高分化腺癌6例,印戒細胞癌3例,管狀腺癌5例,黏液腺癌3例。腫瘤按大體形態分為腫塊型和浸潤潰瘍型:腫塊型26例,浸潤潰瘍型24例;前者進行化療及栓塞治療,后者僅行化療。根據1985年國際抗癌聯盟頒布的國際TNM分期:Ⅱ期21例,Ⅲ期27例,其中Ⅲa期15例,Ⅲb期12例,Ⅳ期2例。
1.2 治療方法
常規消毒局麻下采用改良Seldinger法,行股動脈穿刺,引入4F血管鞘,經鞘引入4FRH導管至腹腔干動脈造影,根據腫瘤所在部位和血供分布情況,進行超選擇性插管至相應的腫瘤供血動脈,一般賁門和胃底部腫瘤選擇胃左動脈,胃體部腫瘤選擇胃左動脈及胃右動脈,胃竇部腫瘤選擇胃右動脈及胃十二指腸動脈,經導管注入化療藥物,采用FDM方案:5-Fu 750 mg/m2,MMC 10 mg/m2,DDP 60 mg/m2。根據腫瘤供血情況,其中26例腫塊型胃癌先經導管化療后,再將10 mg MMC與5~10 ml超液化碘油制成的乳劑,經供血動脈栓塞,至供血動脈血流緩慢時停止注入。術后常規補液及抗炎治療3天,并給予抗酸及保護胃黏膜治療,栓塞治療患者術后禁食48~72 h,并予靜脈營養,從流質逐步到正常飲食。根據患者介入治療術后恢復情況,7~14 d后行胃癌根治術。
1.3 觀察項目
經介入化療(栓塞)術后及胃癌根治術后觀察下列情況:①介入術后不良反應情況,手術中腫瘤剝離切除情況及外科術后恢復情況。② 切除標本組織病理學改變情況。按照日本胃癌規約12版中關于胃癌內科治療的記載要求,0級(無效)為癌前緣細胞無變性、壞死;1級(輕度有效)為1/3~2/3的癌細胞變性、壞死;2級(中度有效)為2/3以上的癌細胞變性、壞死;3級(顯著有效)為全部癌細胞壞死消失,以肉芽組織或纖維組織代替。1~3級為有效。③ 外科術后,患者每6個月行影像學檢查一次,記錄術后復發及轉移情況。
2 結果
2.1 介入治療術后不良反應
50例術前行介入治療患者中,26例腫塊型胃癌行化療加栓塞治療,未行栓塞治療的患者僅出現一過性惡心、嘔吐,經補液、對癥治療后迅速好轉。26例栓塞患者均有不同程度的惡心、嘔吐,其中有2例出現黑便,分別給予補液、抗酸以及保護胃黏膜治療后癥狀消失。血常規檢查19例出現白細胞不同程度下降,分別給予升白細胞藥物治療后,恢復正常。所有病例均未出現嚴重的不良反應,都在預定時間內完成手術。
2.2 外科手術術中及術后情況
50例患者均進行了外科手術治療,其中全胃切除16例,胃部分切除34例,術中見腫瘤周圍組織出現不同程度的纖維化,腫塊易于剝離切除,出血少。術后均未出現吻合口瘺、出血及感染等嚴重并發癥。
2.3 組織病理學檢查結果
所有切除標本均行組織病理學檢查,總有效率為74.0%,其中輕度有效為52.0%,中度有效為22.0%。大體類型與療效的關系見表1,病理分化程度與病理療效的關系見表2。

表1 胃癌大體類型與病理療效的關系(例)
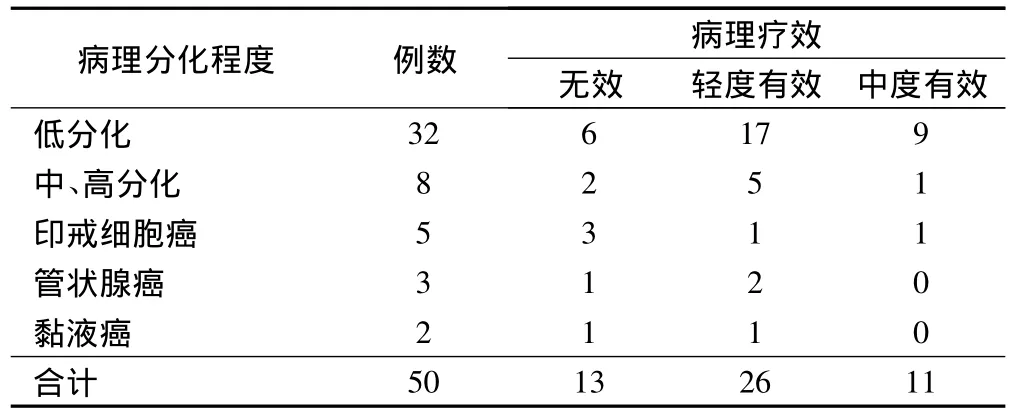
表2 胃癌病理分化程度與病理療效的關系(例)
2.4 術后復發及轉移情況
胃癌患者介入治療及外科根治術后,每6個月行1次影像學檢查,50例患者均獲得隨訪,患者術后6、12、18、24 個月的復發轉移率分別為 0、2.6%、12.0%、23.6%。
3 討論
術前動脈介入治療是近年來采用的新輔助化療的重要方法之一,進展期胃癌行外科根治術前經動脈灌注化療及栓塞治療能提高腫瘤部位的藥物濃度,增強對腫瘤細胞的殺傷能力,縮小病灶,使病變與周圍正常組織的界限變得清晰,提高手術切除率[2,3]。本組50例中大多數患者病灶周圍出現不同程度的纖維化,病變周圍組織浸潤黏連程度減輕,腫瘤易于剝離切除。
介入化療的重要作用之一就是促使腫瘤細胞的組織壞死。通過介入化療可使腫瘤細胞核濃縮,細胞間質呈嗜酸性改變,癌腺管結構破壞,使癌細胞變性壞死,癌細胞核可見核固縮、核碎裂,癌組織間質炎性細胞浸潤,可見泡沫細胞及多核巨細胞,腫瘤組織可見鈣化及纖維化,腫瘤細胞的壞死消失以肉芽組織或纖維組織代替。本組病例當中,所有病例均進行組織病理學檢查,組織病理學有效率達74.0%。腫塊型胃癌組織病理學改變較浸潤潰瘍型有效率高,可能是因為進行栓塞的原因。
腫瘤的生長依賴于腫瘤血管的生成,抑制腫瘤血管的生成或控制腫瘤血供可以阻斷原發腫瘤和轉移瘤的侵襲和生長[4]。胃癌術前經動脈灌注及栓塞治療,一方面可使微小轉移灶和亞臨床病灶的腫瘤細胞消除,同時,介入灌注及栓塞可使腫瘤缺血,從而減少了術中牽拉和擠壓可能造成的腫瘤醫源性播散,降低了胃癌術后復發及轉移率。另外,胃癌術前選擇性動脈化療栓塞可能通過TNF介導腫瘤血管內皮細胞損傷及內皮細胞合成抗凝血因子TM的能力下降致血管內凝血而發揮抗腫瘤效應,從而減少腫瘤的復發及轉移[5]。本組對26例腫塊型血供豐富的腫瘤,在化療的同時進行栓塞治療,進一步阻斷腫瘤血供,使得腫瘤血管發生炎性水腫,血管黏膜增厚,血栓形成,使腫瘤組織出現大片凝固性壞死,減少腫瘤細胞脫落,控制術后復發和轉移。
介入治療后進行胃癌根治術的手術時間,一般為1~2周,因為化療藥物抑制腫瘤細胞是暫時的,48 h細胞增殖指數下降,7~10天后出現反跳現象,又進入增殖期[6]。所以,患者一般情況良好,最好于介入治療7天后進行根治術,一般情況不好的對癥處理后,手術時間不超過2周,時間太長影響治療效果。
進展期胃癌外科根治術前行動脈灌注化療藥物及栓塞治療,作為1種有效的輔助治療手段,創傷小,不良反應少,術后雖出現一過性惡心、嘔吐等消化道反應,通過補液、消炎、抗酸以及保護胃黏膜治療,癥狀迅速消失,不影響手術的同時,使得腫瘤易于切除,使組織病理學發生有效改變,降低腫瘤的復發轉移率。因此,胃癌外科根治術前進行介入化療或手術,是1種非常有效的方法。
[1] Schipper DL,Wagener DJ.Chemotherapy of gastric cancer〔J〕.Anticancer Drugs,1996,7(2):137.
[2] 李茂全,顏志平,王建華,等.胃癌介入治療的療效探討〔J〕.介入放射學雜志,2000,9(1):28.
[3] Kelsen.Adjuvant and Neoaddjuvant therapy for gastric cncer〔J〕.Semin Oncol,1996,23(3):379.
[4] 張跟山,周勝利,曹建明,等.術前介入治療預防胃癌術后復發的療效評價〔J〕.腫瘤學雜志,2003,9(4):204.
[5] 孫碎康,蒲忠豪,嚴律男,等.胃癌患者術前選擇性動脈栓塞化療對腫瘤血管的影響〔J〕.中國普通外科雜志,2002,11(4):202.
[6] 于學林,崔進國,孫興旺.進展期胃癌規范化介入治療方案〔J〕.介入放射學雜志,2005,14(1):108.

