TET2對非小細胞肺癌細胞活性及運動能力的影響
[摘要]目的觀察甲基雙加氧酶(ten-eleventranslocation,TET2)表達量對非小細胞肺癌細胞增殖能力、凋亡率、細胞周期、遷移和侵襲的影響。方法通過RT-PCR和Westernblot法檢測不同非小細胞肺癌細胞TET2基因和蛋白的表達情況,對高表達TET2的細胞敲低其基因表達(shRNA1),對低表達TET2的細胞過表達其基因(OE-TET2)。通過CCK-8檢測TET2表達量對細胞增殖的影響,通過流式細胞術觀察TET2表達量對細胞凋亡和細胞周期的影響,通過遷移實驗和侵襲實驗觀察TET2表達量對細胞遷移和侵襲能力的影響。結果H1299細胞的TET2基因和蛋白表達量最高,A549的最低(P<0.05)。OE-TET2組細胞增殖能力顯著低于正常A549,shRNA1組細胞增殖能力顯著高于正常H1299細胞(P<0.05)。OE-TET2組細胞凋亡率顯著高于正常A549,shRNA1組細胞凋亡率顯著低于正常H1299細胞,差異有統計學意義(P<0.05)。OE-TET2組細胞遷移和侵襲細胞數量顯著低于正常A549,shRNA1組細胞遷移和侵襲細胞顯著高于正常H1299細胞,差異有統計學意義(P<0.05)。結論TET2可降低非小細胞肺癌增殖能力,提高其凋亡率,減弱其遷移和侵襲能力。
[關鍵詞]甲基雙加氧酶;非小細胞肺癌;增殖;凋亡;遷移
[中圖分類號]R7.342[文獻標識碼]A[DOI]10.3969/j.issn.1673-9701.2024.20.006
EffectofTET2ontheactivityandmotilityofnon-smallcelllungcancercells
YANGBilan1,ZHANGZixian2,OUYangxi1,LIUZhihua1,ZHONGJun1
1.DepartmentofChestTumorRadiotherapy,JiangxiCancerHospital,Nanchang330029,Jiangxi,China;2.DepartmentofBreastOncology,NanchangPeople’sHospital,Nanchang330000,Jiangxi,China
[Abstract]ObjectiveToobservetheeffectsofmethylenedioxygenase(TET2)expressionontheproliferationability,apoptosisrate,cellcycle,migration,andinvasionofnon-smallcelllungcancercells.MethodsDetecttheexpressionofTET2geneandproteinindifferentnon-smallcelllungcancercellsthroughRT-PCRandWesternblot.KnockdownthegeneexpressionofthehighestTET2expressingcells(shRNA1)andoverexpressthegeneinthemostlowTET2expr8q+uG0xaWbea7FnorpHPyw==essingcells(OE-TET2).DetecttheeffectofTET2expressiononcellproliferationthroughCCK-8,observetheeffectofTET2expressiononcellapoptosisandcellcyclethroughflowcytometry,andobservetheeffectofTET2expressiononcellmigrationandinvasionabilitythroughmigrationandinvasionexperiments.ResultsTheexpressionlevelsofTET2geneandproteininH1299cellswerethehighest,whileA549cellshadthelowestexpressionlevels(P<0.05).TheproliferationabilityofOE-TET2groupcellswassignificantlylowerthanthatofnormalA549,whiletheproliferationabilityofshRNA1groupcellswassignificantlyhigherthanthatofnormalH1299cells(P<0.05).TheapoptosisrateofOE-TET2groupwassignificantlyhigherthanthatofnormalA549cells,whiletheapoptosisrateofshRNA1groupwassignificantlylowerthanthatofnormalH1299cells(P<0.05).ThenumberofmigrationandinvasioncellsintheOE-TET2groupwassignificantlylowerthanthatofnormalA549cells,whilethemigrationandinvasioncellsintheshRNA1groupweresignificantlyhigherthanthoseinnormalH1299cells(P<0.05).ConclusionTET2canreducetheproliferationability,increaseitsapoptosisrate,andslowdownitsmigrationandinvasionabilityofnon-smallcelllungcancercells.
[Keywords]Methyldioxygenase;Non-smallcelllungcancer;Proliferation;Apoptosis;Migration
非小細胞肺癌(non?smallcelllungcancer,NSCLC)是肺癌常見的類型,當前NSCLC的早期治療主要是手術切除,但NSCLC的早期癥狀不明顯,經常在中晚期才被發現,錯過最佳手術時機,需采用化療等其他方式治療,不僅療效無法保證且會引起嚴重不良反應,嚴重影響患者生活質量及生命安全[1-4]。因此研發更為有效安全的NSCLC治療手段至關重要。研究顯示,DNA異常甲基化參與多種惡性腫瘤的發生和發展,而甲基雙加氧酶(ten-eleventranslocation,TET2)主要參與DNA甲基化[5-7]。研究顯示,TET2的異常表達與多種腫瘤的發生發展相關[8]。TET2在NSCLC發生發展中的作用研究較少。本研究通過敲低或過表達NSCLC細胞的TET2基因,觀察其對腫瘤細胞的增殖、凋亡、運動能力的影響,以期為NSCLC的治療提供新的思路。
1材料與方法
1.1實驗材料
非小細胞肺癌細胞株A549,H1299,H1975和HCC827均從中國上海中科院細胞庫/干細胞庫購買。RT-PCR試劑盒購自日本TaKaRa公司。Lip2000轉染試劑盒購自美國Thermo公司。DMEM培養基購自美國Corning公司。CCK-8試劑盒購自北京索萊寶公司。TET2抗體購自美國Millipore公司。Transwell小室購自美國Corning公司。Matrigel購自美國BD公司。
1.2培養與檢測方法
1.2.1細胞培養所有細胞分別于DMEM培養基中培養,培養基中加10%雙抗和10%胎牛血清。細胞置于37℃,5%CO2培養箱中培養。細胞轉染:待細胞在培養皿中融合至80%~90%時制備單細胞懸液,調整細胞密度為1×106/ml并接種于6孔板中。嚴格按照轉染試劑盒說明書進行轉染。將全長人TET2cDNA(NM_001127208)插入pLVX-Ires-Puro載體(Clontech)中,構建TET2過表達質粒。siRNA合成序列分別為正向:3’-GUGGUGGUAUUUAGA-5’;反向:3’-UUUAUCUAAAUACCACCAC-5’。對于過表達TET2細胞,A549為正常未處理細胞(A549組),OE-NC為轉染對照(OE-TET2組),OE-TET2為轉染過表達細胞。對于敲低TET2細胞(OENC組),H1299為正常未處理細胞,shRNA-NC為轉染對照,shRNA1、shRNA2、shRNA3為不同程度轉染敲低細胞。
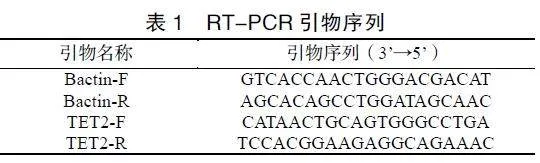
1.2.2RT-PCR法檢測使用Trizol對細胞進行RNA提取,隨后通過反轉錄獲取cDNA。使用熒光定量PCR儀96lightcycler進行RT-PCR法檢測。在96孔光學反應板中進行40個循環進行擴增,1個循環中94℃變性5s,63℃退火30s,72℃延伸60s。Bactin作為內參基因。引物序列見表1。
1.2.3Westernblot法檢測使用RIPA緩沖液裂解所有細胞。將具有等量蛋白質(20μg/孔)的樣品裝載在10%SDS-PAGE凝膠上,并按照說明書進行免疫印跡。抗TET2抗體和β-肌動蛋白的一級抗體購自細胞信號技術公司。用增強化學發光(enhancedchemiluminescence,ECL)觀察免疫反應帶,并使用ImageJ軟件進行分析。
1.2.4流式細胞術取各組對數期生長細胞消化后制備單細胞懸液,使得細胞懸液密度為1×106/ml,隨后在tube管中,分別根據細胞凋亡試劑盒加入RNase5μl(10mg/ml),37℃溫浴1h,加入PI(10mg/ml)染液5μl,室溫避光染色30min,用流式細胞儀測定周期;根據細胞凋亡試劑盒使用AnnexinV-FITC在流式細胞儀上檢測細胞凋亡。
1.2.5細胞遷移與侵襲實驗將各組細胞分別置于Transwell小室中,下室加入600μl含20%血清培養基,上室加入150μl不含血清培養基,培養24h后觀察小室地面細胞數量。使用培養基將Matrigel稀釋至1mg/ml,在Transwell小室的小室上室底部加入100μl稀釋好的Matrigel,待其干成膠狀后加入細胞,方法同細胞遷移實驗。24h后觀察Matrigel中細胞數量。
1.3統計學方法
采用SPSS20.0統計學軟件對數據進行處理分析,計量資料以均數±標準差(![]() )表示,多組間的比較采用單因素方差分析方法(one-wayANOVA),進一步的多重比較則采用LSD方法。組間比較采用兩獨立樣本t檢驗。P<0.05為差異有統計學意義。
)表示,多組間的比較采用單因素方差分析方法(one-wayANOVA),進一步的多重比較則采用LSD方法。組間比較采用兩獨立樣本t檢驗。P<0.05為差異有統計學意義。
2結果
2.1TET2在非小細胞肺癌細胞株中的表達
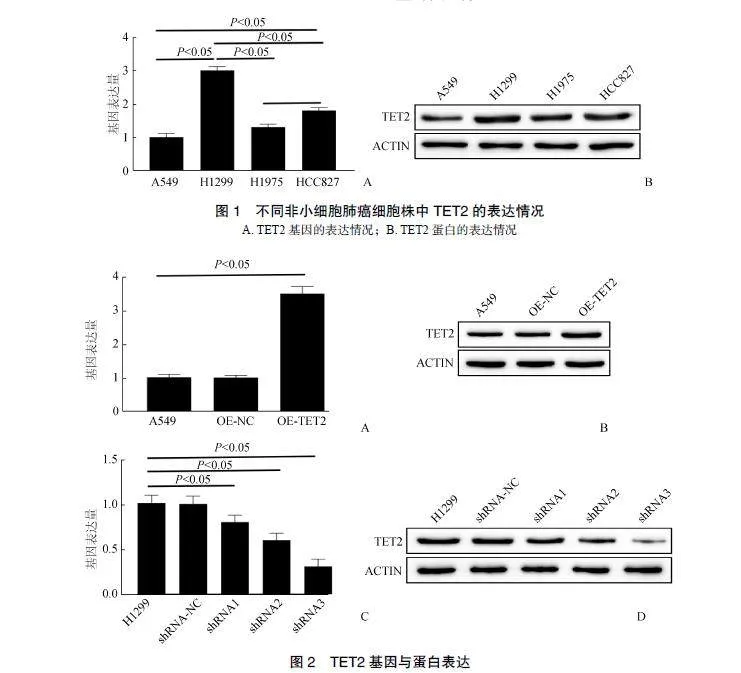
使用RT-PCR和Westernblot法分別檢測4種人非小細胞肺癌細胞株A549、H1299、H1975和HCC827中TET2的基因和蛋白表達情況。H1299的TET2基因表達量最高,其次為HCC827,H1975略高于A549(P<0.05)。H1299的TET2蛋白表達水平顯著高于其他3種細胞,而A549的TET2蛋白表達水平最低(圖1)。
2.2TET2基因干擾及過表達非小細胞肺癌細胞系的建立
H1299的TET2水平表達最高,A549的表達最低,因此分別構建穩定干擾的H1299非小細胞肺癌細胞株和穩定過表達的A549非小細胞肺癌細胞株用于后續研究。穩定過表達的A549(OE-TET2)細胞中TET2的基因(P<0.05)和蛋白水平均出現顯著升高,穩定干擾的H1299(shRNA1、shRNA2、shRNA3)細胞中TET2的基因(P<0.05)和蛋白水平均出現顯著降低(圖2)。干擾的H1299非小細胞肺癌細胞株和穩定過表達的A549非小細胞肺癌細胞株已成功構建。
2.3TET2對細胞增殖的影響
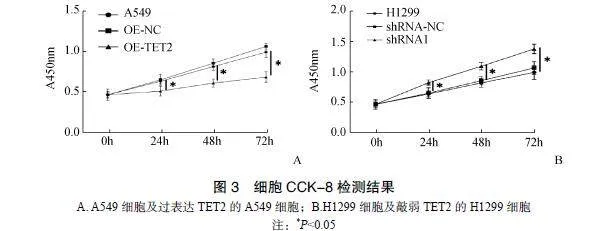
三組A549和H1299細胞的起始濃度相同,隨著培養時間的延長細胞的濃度均出現顯著增加。正常A549細胞以及OE-NC細胞的濃度始終保持一致,然后在培養24h后,OE-TET2組細胞濃度低于A549和OE-NC組,差異有統計學意義(P<0.05),且這種
差異隨著培養時間的延長愈加明顯。正常H1299細胞以及shRNA-NC細胞的濃度始終保持一致,但是在培養24h后,shRNA1組細胞濃度顯著高于H1299和shRNA-NC組,差異有統計學意義(P<0.05),且這種差異隨著培養時間的延長愈加明顯(圖3)。
2.4TET2對細胞凋亡及周期的影響
過表達TET2的細胞凋亡率明顯上升(P<0.05),而敲低TET2表達后,細胞的凋亡率出現明顯下降(P<0.05)。TET2的表達對細胞S期的含量影響較小,過表達TET2后細胞G2期含量顯著上升(P<0.05),G1期含量顯著下降(P<0.05),而敲低TET2的表達則在G2期和G1期表現出相反的趨勢(P<0.05)。
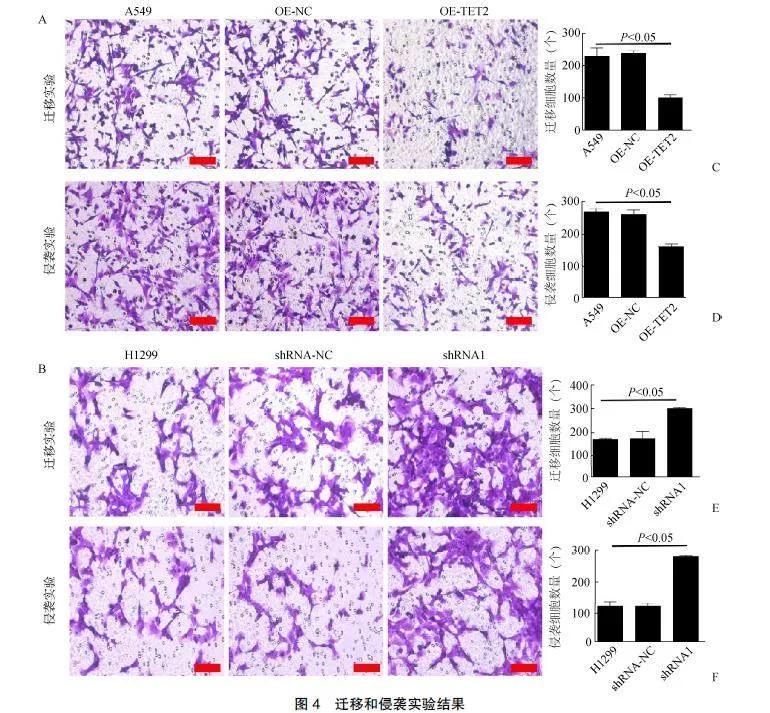
2.5TET2對細胞遷移和侵襲的影響
過表達TET2后,Transwell小室上A549遷移的細胞數量明顯減少(P<0.05),同時侵襲的細胞數量也出現顯著降低(P<0.05)。對于TET2基因敲低的H1299細胞,遷移和侵襲的細胞數量均顯著上升(P<0.05),見圖4。
3討論
肺癌是一種發病率和病死率較高的惡性腫瘤,其中非小細胞肺癌發病率最高,約占肺癌80%~85%,深入研究非小細胞肺癌發生、發展的分子機制可為其治療提供新的思路[9-10]。TET2作為一種去甲基化蛋白,已被證實其表達異常與多種腫瘤發生發展有關,如乳腺癌、白血病、黑色素瘤等[11-13]。同時,已有研究證實,TET2的表達與非小細胞肺癌的發生發展及預后存在一定關系[14]。因此,深入探討TET2在非小細胞肺癌發生發展中的作用或許可成為其有效的治療手段。
A.A549細胞及過表達TET2的A549細胞遷移和侵襲(結晶紫染色,×20);B.H1299細胞及敲弱表達TET2的H1299細胞遷移和侵襲(結晶紫染色,×20);C.過表達組遷移實驗統計結果;D.過表達組遷侵襲實驗統計結果;E.敲弱表達組遷移實驗統計結果;F.敲弱表達組遷侵襲實驗統計結果
TET2是雙加氧酶蛋白家族成員之一,主要參與DNA甲基化。研究發現5-mC能夠在TET蛋白的催化下生成5-羥甲基胞哺唆(5-hydroxvmethylcvtosine,5-hmC),從而導致DNA序列去甲基化。而TET2蛋白可催化氧轉移到5-mC的甲基,產生5-hmC[15-16]。DNA的異常甲基化會抑制抑癌基因的表達,激活原癌基因的表達,促進腫瘤的發生發展[17]。同時,還有研究發現TET2缺失導致5mC的積累,從而促進B細胞發育[18]。TET2缺失還促進CD4+T細胞分化和M1巨噬細胞反應,這可以調節癌癥細胞的活性。相反,攜帶TET2突變的癌癥細胞抵消了包括T細胞和巨噬細胞在內的陽性免疫細胞反應[19]。
本研究體外細胞學實驗,觀察非小細胞肺癌細胞株A549、H1299、H1975和HCC827中TET2的基因和蛋白表達情況。結果顯示A549細胞中TET2的基因和蛋白表達最低,而H1299的基因和蛋白表達最高。因此,分別上調A549細胞中TET2基因表達量和下調H1299細胞中TET2基因表達量,觀察其對腫瘤細胞的影響。
本研究過表達TET2基因的細胞,增殖能力降低,凋亡率增加,遷移和侵襲能力降低,而敲低TET2基因表達后表現出相反的趨勢。通過對細胞周期進行觀察發現,過表達的肺癌細胞G1期細胞數量減少,G2期升高,S期無明顯變化。G1期是DNA合成前期,G2期是DNA合成后期,過表達的肺癌細胞更多的停留在DNA合成后期,這進一步說明TET2具有減弱腫瘤細胞增殖能力、增加細胞凋亡的作用。腫瘤細胞遷移和侵襲是腫瘤發展過程中重要的一環,遷移和侵襲能力越強,腫瘤越有可能長大且轉移。研究顯示,細胞遷移和侵襲能力受多種細胞因子影響[20-21]。如果TET2基因缺失,可能引起腫瘤周圍環境炎性因子表達升高,且部分DNA序列甲基化本身也會引起細胞運動能力增強。這可能是本研究中低表達TET2基因的肺癌細胞出現遷移和侵襲能力增加,高表達TET2基因的肺癌細胞出現遷移和侵襲能力降低的原因。
綜上所述,本研究通過篩選不同非小細胞肺癌細胞株中TET2的表達情況構建TET2的高表達和低表達細胞系,并觀察其對腫瘤細胞的影響。研究結果顯示TET2表達上升后,非小細胞肺癌細胞的增殖能力下降、凋亡率上升,同時其遷移和侵襲能力下降,起到減緩腫瘤發生、發展的作用。本研究并未對TET2與非小細胞肺癌發生發展的更深的機制進行探討,下一步應針對DNA甲基化對其機制進行深入討論。
利益沖突:所有作者均聲明不存在利益沖突。
[參考文獻]
[1] CHENP,LIUY,WENY,etal.Non-smallcelllungcancerinChina[J].CancerCommun(Lond),2022,42(10):937–970.
[2] MITHOOWANIH,FEBBRAROM.Non-small-celllungcancerin2022:Areviewforgeneralpractitionersinoncology[J].CurrOncol,2022,29(3):1828–1839.
[3] YEZ,HUANGY,KEJ,etal.Breakthroughintargetedtherapyfornon-smallcelllungcancer[J].BiomedPharmacother,2021,133:111079.
[4] ALEXANDERM,KIM,SYCHENGH.Update2020:Managementofnon-smallcelllungcancer[J].Lung,2020,198(6):897–907.
[5] DAIX,RENT,ZHANGY,etal.Methylationmultiplicityanditsclinicalvaluesincancer[J].ExpertRevMolMed,2021,23:e2.
[6] PAPANICOLAU-SENGOSA,ALDAPEK.DNAmethylationprofiling:Anemergingparadigmforcancerdiagnosis[J].AnnuRevPathol,2022,17:295–321.
[7] BOYM,BISIOV,ZHAOLP,etal.MyelodysplasticsyndromeassociatedTET2mutationsaffectNKcellfunctionandgenomemethylation[J].NatCommun,2023,14(1):588–602.
[8] JAINN,ZHAOZ,FEUCHTJ,etal.TET2guardsagainstuncheckedBATF3-inducedCARTcellexpansion[J].Nature,2023,15(7951):315–322.
[9] BADEBC,DELACCS.Lungcancer2020:Epidemiology,etiology,andprevention[J].ClinChestMed,2020,41(1):1–24.
[10] SIEGELRL,MILLERKD,JEMALA.Cancerstatistics,2020[J].CACancerJClin,2020,70(1):7-30.
[11] LAURENTA,MADIGOUT,BIZOTM,etal.TET2-mediatedepigeneticreprogrammingofbreastcancercellsimpairslysosomebiogenesis[J].LifeSciAlliance,2022,5(7):e202101283.
[12] LIY,XUEM,DENGX,etal.TET2-mediatedmRNAdemethylationregulatesleukemiastemcellhomingandself-renewal[J].CellStemCell,2023,30(8):1072–1090.
[13] BONVINE,RADAELLIE,BIZETM,etal.TET2-dependenthydroxymethylomeplasticityreducesmelanomainitiationandprogression[J].CancerRes,2019,79(3):482–494.
[14] CHENGG,WUJ,JIM,etal.TET2inhibitstheproliferationandmetastasisoflungadenocarcinomacellsviaactivationofthecGAS-STINGsignallingpathway[J].BMCCancer,2023,23(1):825–837.
(下轉第39頁)

