鐵基納米粒子改性碳布復合材料的制備及其在微生物燃料電池陽極中的應用



關鍵詞 微生物燃料電池;胞外電子轉移;鐵基納米粒子改性碳布陽極;微波輔助合成方法
有機廢水中的潛在能量大約是處理廢水所需能量的9 倍以上[1]。有效地利用廢水中的潛在能量,不僅可顯著降低處理廢水的能源成本,還可開辟一條全新的能源收集途徑。微生物燃料電池(Microbial fuelcells, MFCs)是一種利用微生物代謝將有機污染物轉化為電能的技術。將MFCs 技術用于廢水處理,可降低能源成本,實現廢水的可持續循環利用[2]。MFCs 具有廣泛的底物來源和多樣的電化學活性微生物,在廢水處理領域中具有巨大的應用潛力[3]。
異化金屬還原細菌作為典型的電化學微生物,可通過細胞外電子傳遞(Extracellular electron transfer,EET)機制將氧化有機物的電子傳遞到周圍的電子受體上,從而獲取能量。其中,地桿菌(Geobacter)可采用Fe(Ⅲ)作為電子受體,因此,引入Fe 元素可增加電極上Geobacter 物種的豐度[4]。盡管如此, MFCs 仍受到細菌負載能力和EET 效率均較低的限制,其功率密度有待進一步提高[5]。
陽極作為微生物附著的主要場所,直接影響微生物附著、活性以及細菌與電極之間的EET 效率[6]。傳統的碳布(Carbon cloth, CC)因具有良好的化學穩定性和機械強度,以及易于功能化等優勢被廣泛用作MFCs 陽極材料[7]。然而,碳材料電極在MFCs 中的生物膜/陽極界面反應中表現出較差的生物相容性和有限的電催化活性[8]。過渡金屬碳化物具有類似鉑的性質,如高溫穩定性、耐腐蝕性、導電性和催化性能[9],因此,許多研究采用負載過渡金屬碳化物改性碳基陽極的方法,增強電極與細菌之間的親和力,并降低生物膜與陽極之間的層間電阻,其中, WC[10]、Mo2C[11]和Fe3C[12]等過渡金屬碳化物已被用作MFCs陽極材料,尤其是Fe3C 在氧化還原反應中表現出電容行為,有助于細菌和陽極之間的電荷轉移[13-14]。這些改性碳基陽極可提高MFCs 的功率密度和穩定性。
目前,制備碳基納米復合材料的方法包括層層自組裝[15]、水熱合成法[16]和化學氣相沉積法[17]等。然而,這些方法雖然可改善電池性能,但仍存在成本高和反應時間較長等不足,因此需要開發更高效的制備方法。微波輻射是一種高效的加熱方式,與傳統的加熱方式相比,微波輻射能更均勻地傳遞能量,反應體系升溫快速,克服了傳統加熱方式加熱效率低和不均勻的問題,提高了反應效率[18]。此外,微波輻射還能夠促使反應物更緊密地接觸,有助于制備尺寸均勻的納米材料[19]。因此,微波輔助合成方法被廣泛應用,具有高效、省時、節能且易操作等優勢,而且能夠確保反應的質量[18]。在反應混合物中含有不同微波吸收性質的化合物,微波輻射法表現出高選擇性和產率,減少了副反應的發生,提高了產品的純度[20]。在MFCs 領域,微波輔助方法已被應用于陽極材料的改性和制備,以提高MFCs 的性能[19,21-22]。Zhao 等[22]采用微波輔助溶劑熱法合成了新型G/TiO2 復合材料,以其作為接種希瓦氏菌的MFCs 陽極,在MFC 中的最大功率密度為1060 mW/m2,遠高于水熱處理陽極(409 mW/m2)和炭紙陽極(120 mW/m2)。
本研究采用簡便且高效的微波輔助和高溫退火方法在N 摻雜CC 基底上制備高度分散的鐵基納米粒子(Fe3C/Fe@CC)作為無粘合劑的MFCs 陽極,此MFCs 具有較高的細菌負載能力、電子轉移效率以及輸出功率。
1 實驗部分
1.1 儀器與試劑
Hitachi S-4800 掃描電子顯微鏡(SEM,日本日立公司);Empyrean X 射線粉末衍射儀(XRD)(荷蘭帕納科公司);ESCALAB 250Xi X 射線光電子能譜儀(XPS)(美國賽默飛公司);LabRAM 拉曼光譜儀(日本Hiroba 公司);CHI 860E 電化學工作站(上海辰華公司);數據采集系統(美國吉時利公司)。雙氰胺(DCD)和FeCl3·9H2O(分析純,天津渤化化學試劑有限公司)。CC(上海河森電氣有限公司)。實驗用水為去離子水。
1.2 材料合成方法
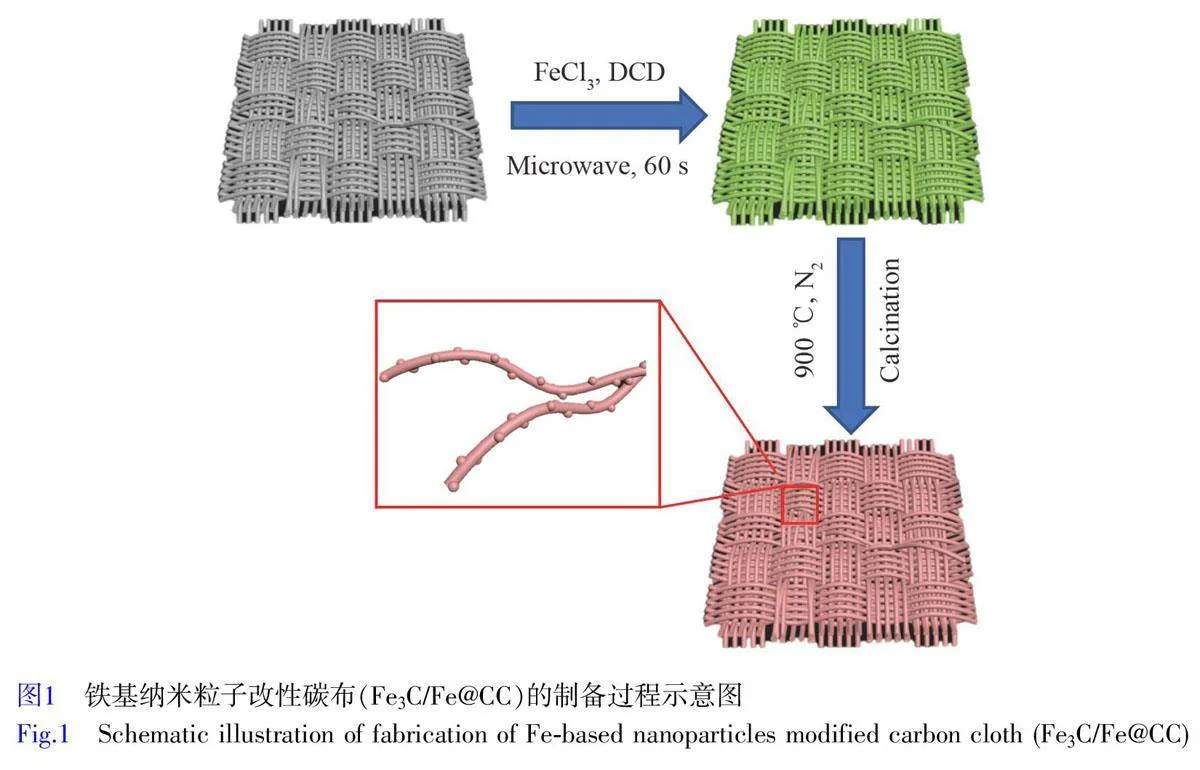
采用微波輔助合成和高溫退火技術制備Fe3C/Fe@CC 電極。首先,將2 g FeCl3 溶解在10 mL 去離子水中,再加入4 g DCD,超聲溶解制備成前驅體。隨后,將CC 浸泡在去離子水中,取出并采用微波處理60 s, 再將CC浸泡在制備的前驅體中,微波處理60 s。將CC在N2 氣氛下以5 ℃/min速度升溫至900 ℃并保溫1 h。Fe3C/Fe@CC的制備過程示意圖見圖1。反應結束后,將改性CC與鈦絲纏繞以形成自支撐電極。
1.3 實驗方法
1.3.1 電化學測試
采用三電極體系對細菌富集前后的陽極進行測試,以鉑片或碳刷作為對電極,參比電極為飽和甘汞電極(SCE)。以電化學交流阻抗法(EIS)測試的電位為開路電壓,振幅為30 mV,頻率范圍為0.1~100 kHz。循環伏安法(CV)測試的電位范圍為?0.8~0.2 V, 掃描速度為2~10 mV/s, 掃描方向為正掃。微分脈沖伏安法(DPV)測試的電位范圍為?0.8~0.6 V, 振幅為0.006 V, 脈沖寬度為0.02 s, 樣品寬度為0.0025 s, 脈沖周期為1s, 靜止時間為8 s。
1.3.2 電池接種與啟動
本研究選用100mL 容積的H 型雙室MFCs,陽極分別為Fe3C/Fe@CC和CC,陰極為商用三維碳刷電極。在陽極室中加入20 mL 實驗室馴化好的出水,混合菌種類采用文獻[23]的方法馴化和接種,并加入80 mL 陽極液。陽極液組成為0.05 mol/L 磷酸鹽緩沖溶液(PBS,11.55 g/L Na2HPO4·12H2O,2.77 g/LNaH2PO4·2H2O,0.31 g/L NH4Cl, 0.13 g/L KCl, pH≈6.5)、2 g/L 乙酸鈉、10 mL/L 維生素溶液和12.5 mL/L礦物質溶液[24]。陰極液為100 mL 含有K3[Fe(CN)6](16.4 g/L)和KCl(3.725 g/L)的混合溶液。組裝好的MFCs 外阻均設置為1000Ω,并在37 ℃下運行,在電壓降至50 mV 以下時更換電解液。數據采集器每10 min 記錄1 次數據。
2 結果與討論
2.1 材料表征
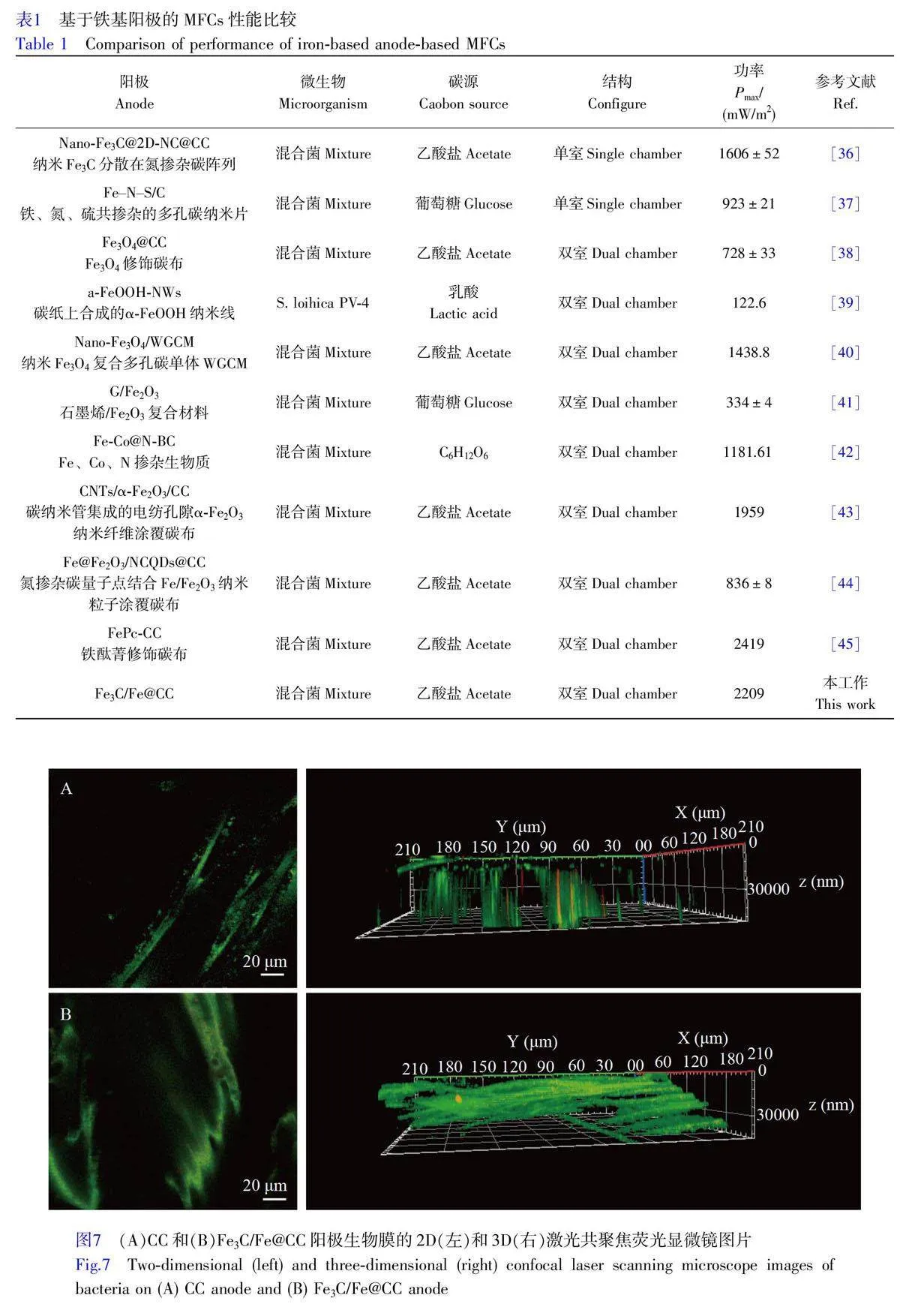
圖2 為材料的SEM 照片。純CC 是由光滑的碳纖維交織而成的開放結構(圖2A);改性后(圖2B),Fe3C/Fe 納米顆粒均勻分散在CC 基底表面上,其平均粒徑約為(439±25) nm(圖2B 插圖)。相比于純CC, Fe3C/Fe@CC 表面的纖維更粗糙,有利于細菌附著[25]。元素分布結果(圖2C)表明, Fe3C/Fe@CC 樣品中的C、Fe、O和N元素分布均勻。EDS 能譜結果(圖2D)進一步表明, Fe3C/Fe@CC 樣品中Fe 元素質量分數達到5.04%。
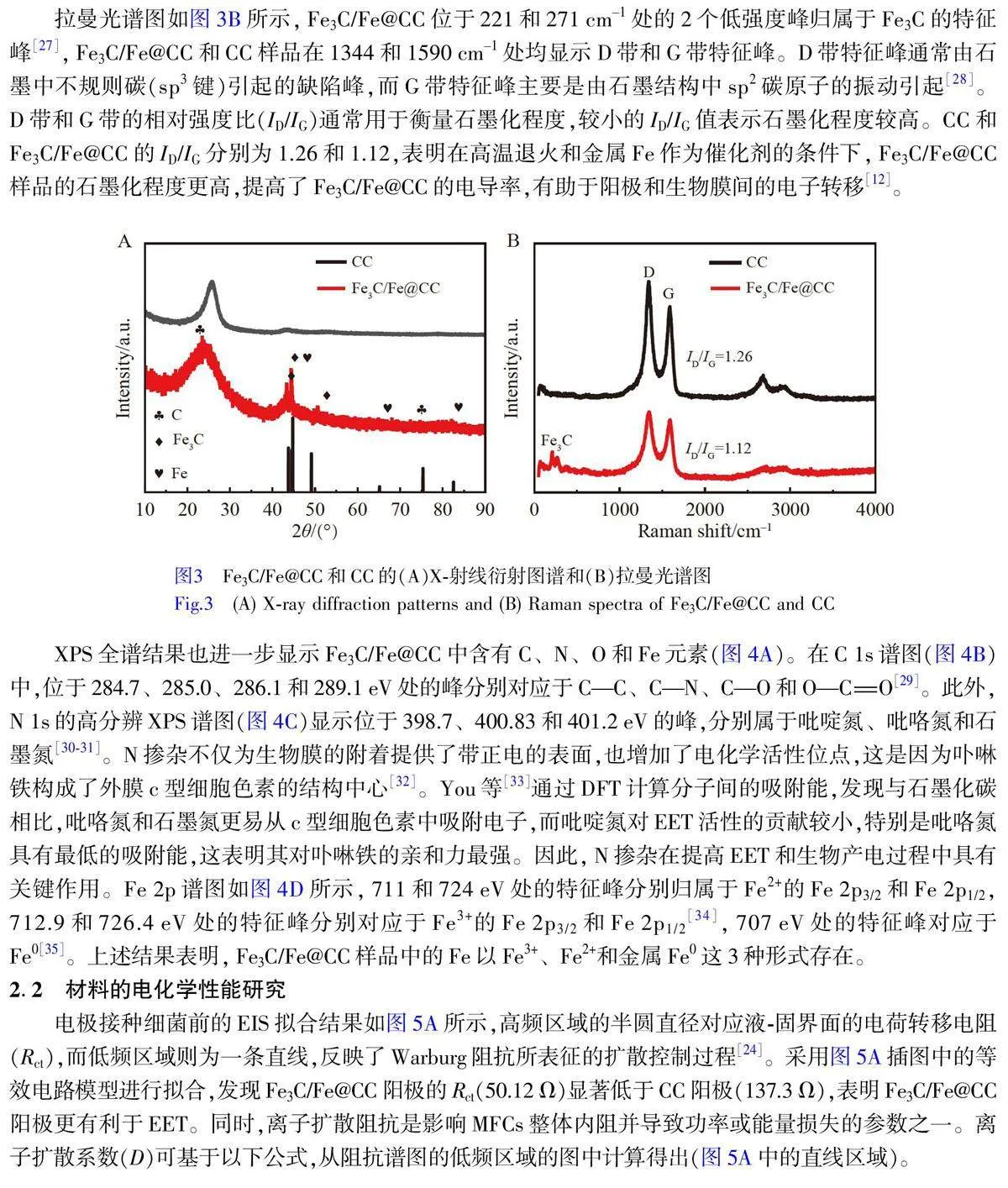
XRD 結果如圖3A 所示, Fe3C/Fe@CC 和CC 分別在2θ=24.0°和25.8°處出現衍射峰,對應于石墨碳(JCPDS#99-0057)層間的(002)晶面。相比于CC 樣品在25.8°處的衍射峰,改性后樣品的相應峰位于較低的角度,這可能是由于氮摻雜到碳晶格中,導致石墨碳在a 或b 方向上微小扭曲,以及C—N 鍵長小于C—C 鍵長[26]。Fe3C/Fe@CC 樣品在2θ=43.58°、44.6°和50.64°處觀察到3 個顯著的特征衍射峰,分別對應于斜方晶系θ-Fe3C(JCPDS#35-0772)的(102)、(220)和(122)晶面。此外,在2θ=44.6°、65°和82.24°處存在3 個尖銳的特征峰,分別對應于體心立方結構α-Fe(JCPDS#06-6069)的(110)、(200)和(211)晶面。XRD 結果表明樣品中存在Fe3C 和Fe 金屬,因此,將此樣品命名為Fe3C/Fe@CC。

