鐵改性污泥生物炭對水中Cr(VI)的吸附性能研究
趙 霞, 羅欣怡, 馮 昊, 劉 慢, 安秋鳳, 馬明華
(1.陜西科技大學(xué) 化學(xué)與化工學(xué)院 陜西省輕化工助劑重點(diǎn)實驗室, 陜西 西安 710021; 2.西安市第五再生水廠, 陜西 西安 710000)
0 引言
隨著制革、印染、化工等行業(yè)的發(fā)展,越來越多的鉻廢水被排放到自然界中[1].鉻在水中主要以Cr(III)和Cr(VI)的形式存在,且在自然界中難以降解,Cr(III)易被氧化成Cr(VI),Cr(VI)具有強(qiáng)毒性,有造成人體器官癌變的風(fēng)險[2].含鉻廢水的處理方法有化學(xué)沉淀法[3]、電化學(xué)法[4]、膜分離法[5]和吸附法等,其中吸附法因價格低廉、環(huán)保等優(yōu)點(diǎn)而作為最常用的處理方法.用于水中鉻去除的吸附劑種類較多,如膨潤土、活性炭、殼聚糖等,但普遍存在吸附性能不理想且吸附質(zhì)不易分離的問題[6].而以工農(nóng)業(yè)廢棄物為原料制備的生物炭,因其吸附能力強(qiáng)、經(jīng)濟(jì)環(huán)保而受到廣泛關(guān)注[7-9].
剩余污泥是城市污水處理廠的副產(chǎn)物[10],含有大量的有機(jī)物和致病菌,會對環(huán)境造成極大危害.污泥含碳量高,可通過高溫?zé)峤鈱ζ溥M(jìn)行無害化處理而制備成具有吸附性能的生物炭[11,12].但污泥生物炭的吸附能力有限,故需要對其進(jìn)行改性.研究表明,鋅改性可使生物炭比表面積顯著增大[13],KHCO3活化可使生物炭的孔隙結(jié)構(gòu)更加豐富[14],過硫酸鈉改性可增加生物炭表面的含氧官能團(tuán),如-C-O、-COOH和-OH,從而使其對重金屬離子具有高的親和力[15],通過鐵改性的生物炭,其比表面積更大、表面官能團(tuán)更加豐富,對金屬離子具有更強(qiáng)的親和力,可通過氧化還原反應(yīng)和絡(luò)合作用促進(jìn)其對金屬離子的吸附能力,且在吸附之后易于固液分離[16-18].
因此,本文以城市剩余污泥為原料,通過高溫?zé)峤狻HCO3活化、鐵改性,制備鐵改性污泥生物炭(Fe-S@HKBC),研究Fe-S@HKBC對水中Cr(VI)的吸附性能,探討吸附機(jī)理,為解決污泥的環(huán)境風(fēng)險和含鉻廢水的污染問題提供依據(jù),以期達(dá)到“以廢治廢”的目的.
1 實驗部分
1.1 實驗方法
1.1.1 生物炭的制備
將取自西安市某城市污水處理廠的剩余污泥進(jìn)行脫水、烘干、粉碎至200目.將污泥粉末放入坩堝,置于馬弗爐中,在限氧條件下,以10 ℃/min加熱至700 ℃,熱解1 h,再經(jīng)氫氟酸酸洗、水洗、烘干得到污泥生物炭(BC).
將10 g BC與KHCO3按1∶2的質(zhì)量比進(jìn)行混合,研磨均勻后放入通N2的馬弗爐中,以10 ℃/min加熱至600 ℃,碳化2 h,待冷卻至室溫取出,放入1.2 mol/L的HCl溶液(W生物炭:VHCl= 1∶10)中攪拌12 h,經(jīng)去離子水洗至中性,烘干、研磨過篩120 目,得到KBC.
將100 mL 2 mol/L H2SO4與22.82 g (NH4)2S2O8混合,配制為1 mol/L (NH4)2S2O8的混合液,取0.5 g的KBC和30 mL的(NH4)2S2O8的混合液,加入圓口燒瓶中,在密封的條件下,攪拌20 min,然后加熱至60 ℃,繼續(xù)攪拌12 h,后用去離子水和無水乙醇洗滌,離心過濾,80 ℃真空干燥,得到HKBC.
將0.86 g HKBC加入到25 mL濃度為0.004 mol/L的Fe(NO3)3·9H2O與25 mL濃度為0.002 mol/L的FeSO4·7H2O的混合液中,磁力攪拌1 h.然后在攪拌條件下往上述混合溶液中滴加15 mL濃度為0.008 mol/L的Na2S·9H2O溶液和10 mL濃度為0.002 mol/L的MnSO4·H2O溶液,繼續(xù)攪拌反應(yīng)2 h.隨后,將10.0 mL濃度為0.003 mol/L的CO(NH2)2溶液逐滴加到混合溶液中繼續(xù)攪拌2 h,最后將混合液體轉(zhuǎn)移到不銹鋼高壓反應(yīng)釜中,將其置于120 ℃的烘箱中恒溫反應(yīng)12 h;實驗過程中用N2吹掃溶液.待其冷卻至室溫后,通過洗滌、離心、過濾和干燥后得到Fe-S@HKBC.
1.1.2 吸附實驗
(1)吸附影響因素實驗:考察接觸時間(10~780 min)、Fe-S@HKBC用量(1~10 g/L)、Cr(VI)初始濃度(10~300 mg/L)、溶液pH(1~12)、Na+和Ca2+(0.01~1.0 mol/L)對Fe-S@HKBC吸附Cr(VI)的影響.將一定量Fe-S@HKBC加入到50 mL Cr(VI)溶液中,置于振蕩培養(yǎng)箱,在25 ℃、220 r/min下振蕩600 min,離心后上清液過0.45 μm濾膜,利用分光光度法測定濾液吸光度,依據(jù)標(biāo)準(zhǔn)曲線計算Cr(VI)的濃度.根據(jù)式(1)和式(2)計算Fe-S@HKBC對Cr(VI)的吸附去除率和平衡吸附量.并對比BC對Cr(VI)的吸附性能,步驟同F(xiàn)e-S@HKBC.所有實驗均一式三份,實驗結(jié)果取平均值并計算偏差.
(1)
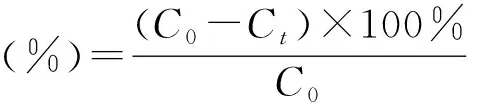
(2)
式(1)、(2)中:qe為平衡吸附量(mg/g),C0、Ce和Ct分別為Cr(VI)的初始濃度、吸附平衡濃度和t時的濃度(mg/L),V為Cr(VI)溶液體積(L),m為Fe-S@HKBC投加量(g).
(2)吸附動力學(xué)實驗:取50 mL 100 mg/L 的Cr(VI)溶液,加入0.2 g Fe-S@HKBC后,在25 ℃的恒溫振蕩培養(yǎng)箱中,以220 r/min振蕩吸附10~780 min,取樣離心,經(jīng)0.45 μm濾膜過濾,測定濾液中Cr(VI)的濃度.根據(jù)偽一級式(3)、偽二級式(4)、粒子內(nèi)擴(kuò)散式(5)和Elovich式(6)等動力學(xué)模型對實驗數(shù)據(jù)進(jìn)行擬合.
(3)
(4)
Q=ks×t0.5+C
(5)
(6)
式(3)~(6)中:qt和qe(mg/g)分別表示t(min)時和吸附平衡時Fe-S@HKBC對Cr(VI)的吸附量;k1(1/min),k2(1/(mg·min))分別是偽一級、偽二級的速率常數(shù);ks(g/mg h0.5)為粒子內(nèi)擴(kuò)散模型的速率常數(shù);C(mg/g)是生物炭邊界層數(shù)量的常數(shù).α(mg/(g·min))為初始吸附系數(shù);β(g/mg)為解吸系數(shù).
(3)吸附等溫線實驗:分別取不同濃度 (20~200 mg/L)的Cr(VI)溶液,加入0.2 g Fe-S@HKBC后,調(diào)節(jié)pH為1,然后在15 ℃、25 ℃和35 ℃的恒溫振蕩培養(yǎng)箱中,以220 r/min振蕩吸附600 min.實驗數(shù)據(jù)用Langmuir式(7)和(8)、Freundlich式(9)、Dubinin-Radushkevich (D-R)式(10)~(12)、Temkin式(13)模型擬合.
(7)
(8)
(9)
qe=qs×exp(-Kdrε2)
(10)
ε=R×T×ln(1+1/Ce)
(11)
(12)
(13)
式(7)~(13)中:qm(mg/g)為最大吸附量;KL(L/mg)、KF(L/g)、ε(kJ/mol)、α(kJ/mol)分別為Langmuir、Freundlic、D-R和Temkin的吸附平衡常數(shù);RL為Langmuir模型中的分離常數(shù),n為Freundlich模型的常數(shù),表示吸附強(qiáng)度;Kdr為吸附平均自由能相關(guān)活度系數(shù)(mol2/J2);E為自由能(kJ/mol);KT(L/mg)是與最大結(jié)合能相關(guān)的平衡結(jié)合常數(shù).
(4)吸附再生實驗:為了評估Fe-S@HKBC的可回收性,進(jìn)行了循環(huán)再生實驗.吸附實驗的Cr(VI) 濃度為100 mg/L,方法同吸附等溫線實驗.將吸附后的Fe-S@HKBC抽濾、烘干,置于0.5 mol/L HCl溶液中,在25 ℃下振蕩解吸1 h.將解吸后的Fe-S@HKBC水洗、烘干、過篩后重復(fù)上述實驗5次.
1.2 分析與表征
采用高分辨場發(fā)射掃描電鏡(SEM,日本電子株式會社)對生物炭的形貌進(jìn)行表征;采用X-射線衍射儀(XRD,德國Bruker公司)分析Fe-S@HKBC的晶體結(jié)構(gòu);采用納米粒度表面電位分析儀(Zeta,英國Malvern公司)對生物炭的表面電位進(jìn)行表征.通過全自動比表面及孔隙度分析儀(BET,美國麥克公司)測定生物炭的比表面積和孔隙度;通過傅里葉紅外光譜儀(FT-IR,德國Bruker公司)分析Fe-S@HKBC吸附Cr(VI)前后的表面官能團(tuán).
2 結(jié)果與討論
2.1 Fe-S@HKBC的表征
2.1.1 SEM分析
BC和Fe-S@HKBC的SEM結(jié)果如圖1所示.由圖1(a)可以看出,BC表面光滑,比較平整,改性后Fe-S@HKBC(圖1(b))的表面變粗糙,形成了許多不規(guī)則的片狀結(jié)晶物,具有良好的多孔結(jié)構(gòu),這為其吸附污染物提供了更多的吸附位點(diǎn).

圖1 BC及Fe-S@HKBC的SEM圖
2.1.2 BET分析
根據(jù)表1和圖2可知,BC和Fe-S@HKBC的比表面積分別為143.16 m2/g和283.96 m2/g,總孔隙體積分別為0.38 cm3/g和0.45 cm3/g,孔徑分別為10.63 nm和8.18 nm.改性后使Fe-S@HKBC比表面積增大了近2倍,總孔體積也有增加,但是孔徑有所減少,這可能是鐵附著在Fe-S@HKBC表面,堵塞了孔道.Fe-S@HKBC的平均孔徑為8.18 nm,表明Fe-S@HKBC中存在微孔結(jié)構(gòu)(2~10 nm).且如圖2 (b)所示,Fe-S@HKBC的N2吸附-脫附等溫線屬于IV型,具有H3型回滯環(huán)[19].這表明Fe-S@HKBC中存在介孔或大孔的層狀結(jié)構(gòu),在P/P0>0.8時,N2吸附急劇上升,也表明存在介孔結(jié)構(gòu)[20].

表1 BC和Fe-S@HKBC孔結(jié)構(gòu)
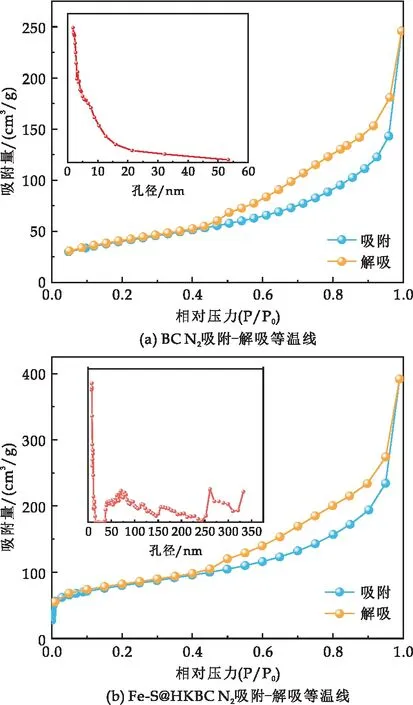
圖2 BC及Fe-S@HKBC N2吸附-解吸等溫線
2.1.3 XRD分析
Fe-S@HKBC的XRD分析如圖3所示,2θ值為18.29 °和30.07 °處的衍射峰為Fe3O4的特征峰.2θ值為35.89 °、41.66 °和60.39 °處的衍射峰為FeO的特征峰.38.99 °、50.45 °和68.10°處的衍射峰為FeS的特征峰,表明Fe成功負(fù)載在Fe-S@HKBC上.
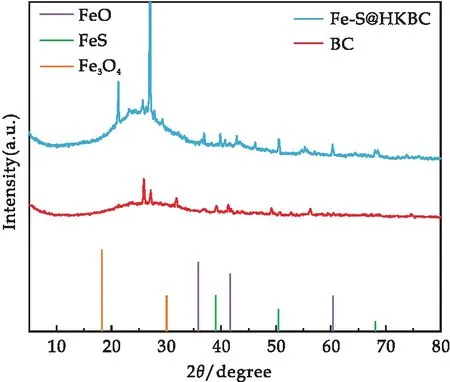
圖3 BC和Fe-S@HKBC的XRD圖
2.1.4 FT-IR分析
FT-IR分析如圖4所示,BC僅在640 cm-1顯示出較強(qiáng)的振動峰,為炔烴類-CH的振動峰.在460 cm-1處為Fe-O振動峰,證明Fe成功負(fù)載在Fe-S@HKBC上.798 cm-1處的振動峰是由Ar-H引起的.1 240 cm-1、1 602 cm-1處分別為C-O、-C=O的振動峰,3 438 cm-1處振動峰為-OH和生物炭表面殘留水的O-H拉伸振動[21].改性后Fe-S@HKBC表面官能團(tuán)更加豐富,如Fe-O、C-O、-C=O、-OH等.
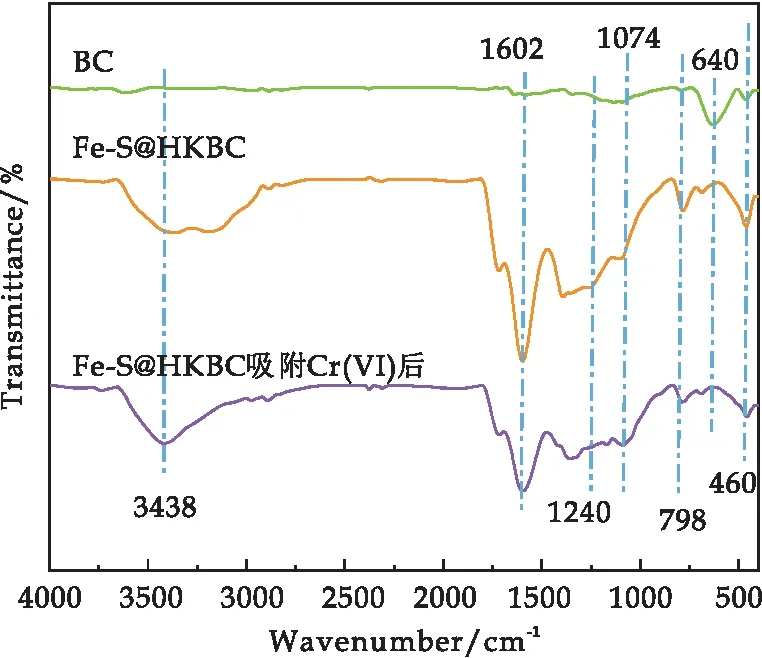
圖4 BC和Fe-S@HKBC吸附Cr(VI)前后的FT-IR譜圖
2.2 吸附影響因素
2.2.1 接觸時間對Cr(VI)去除的影響
在25 ℃,Cr(VI)初始濃度為100 mg/L時,接觸時間對Fe-S@HKBC吸附Cr(VI)的影響結(jié)果如圖5所示.初始階段Cr(VI)的吸附量快速增加,這是由于生物炭表面有大量的結(jié)合位點(diǎn).隨著時間的增加,結(jié)合位點(diǎn)逐漸減少,吸附量穩(wěn)步增加,600 min時Cr(VI)的吸附量達(dá)到22.15 mg/g,此后隨著時間的增加,吸附量變化很小,表明600 min時吸附基本達(dá)到平衡.
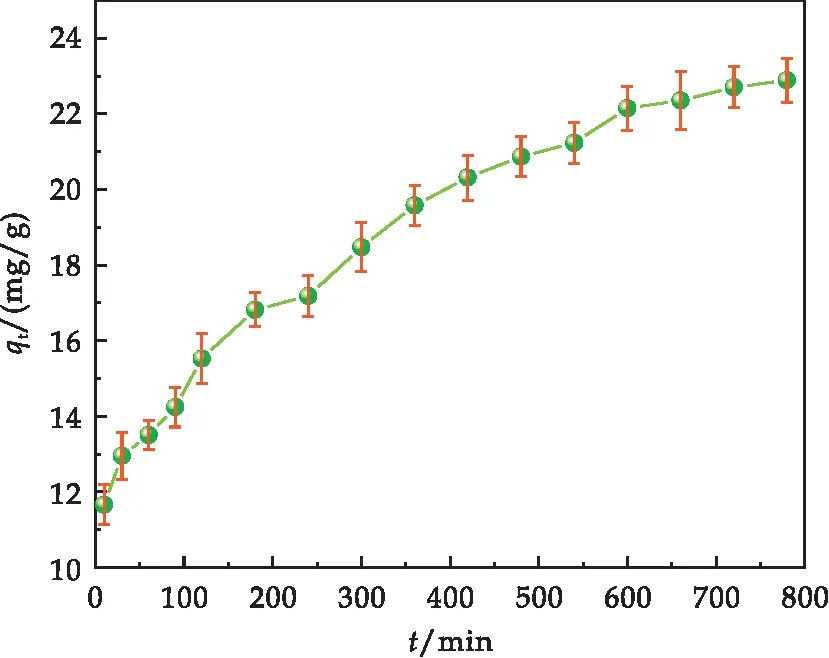
圖5 接觸時間對Cr(VI)去除的影響
2.2.2 生物炭用量對Cr(VI)去除的影響
在25 ℃,Cr(VI)初始濃度為100 mg/L時, 生物炭用量對Cr(VI)去除的影響結(jié)果如圖6所示.隨著生物炭用量從1 g/L增加到4 g/L,Fe-S@HKBC對Cr(VI)的去除率從49.61%增加至90.80%,相應(yīng)的吸附量從49.61 mg/g下降到22.70 mg/g.當(dāng)生物炭用量繼續(xù)增加至10 g/L時,Fe-S@HKBC對Cr(VI)的去除率從90.80%增加至93.01%,相應(yīng)的吸附量從22.70 mg/g下降至9.30 mg/g.當(dāng)生物炭用量大于4 g/L,繼續(xù)增加其用量,Cr(VI)的去除率增加幅度很小,但吸附量下降幅度很大,綜合考慮生物炭成本及吸附去除率因素,適宜的生物炭用量為4 g/L.
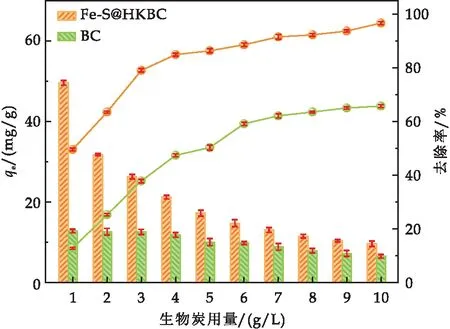
圖6 生物炭用量對Cr(VI)去除的影響
當(dāng)生物炭用量為4 g/L時,BC對 Cr(VI)的吸附量為12.61 mg/g,相應(yīng)的去除率為37.84%.對比可知,改性后Fe-S@HKBC對Cr(VI)的吸附量和去除率顯著增大,表明鐵改性對生物炭的吸附性能有明顯促進(jìn)作用.
2.2.3 Cr(VI)初始濃度對吸附的影響
Cr(VI)初始濃度(10~300 mg/L)對吸附的影響結(jié)果如圖7所示.當(dāng)Cr(VI)初始濃度從10 mg/L增加至100 mg/L時,Fe-S@HKBC對Cr(VI)的吸附量從2.50 mg/g增加至22.70 mg/g,相應(yīng)的去除率由99.82%減少到90.80%,當(dāng)Cr(VI)初始濃度從100 mg/L增加至300 mg/L時,吸附量從22.70 mg/g增加至47.69 mg/g,相應(yīng)的去除率由90.80%下降至58.93%.吸附量隨Cr(VI)初始濃度的增大而增大,這是因為Cr(VI)初始濃度的增大提高了其在固液相體系中的傳質(zhì)推動力[22].但由于Fe-S@HKBC吸附活性位點(diǎn)的有限性,當(dāng)Cr(VI)濃度進(jìn)一步增加時,溶液中存在剩余的Cr(VI)無法與吸附位點(diǎn)結(jié)合,導(dǎo)致吸附去除率逐漸下降[23].
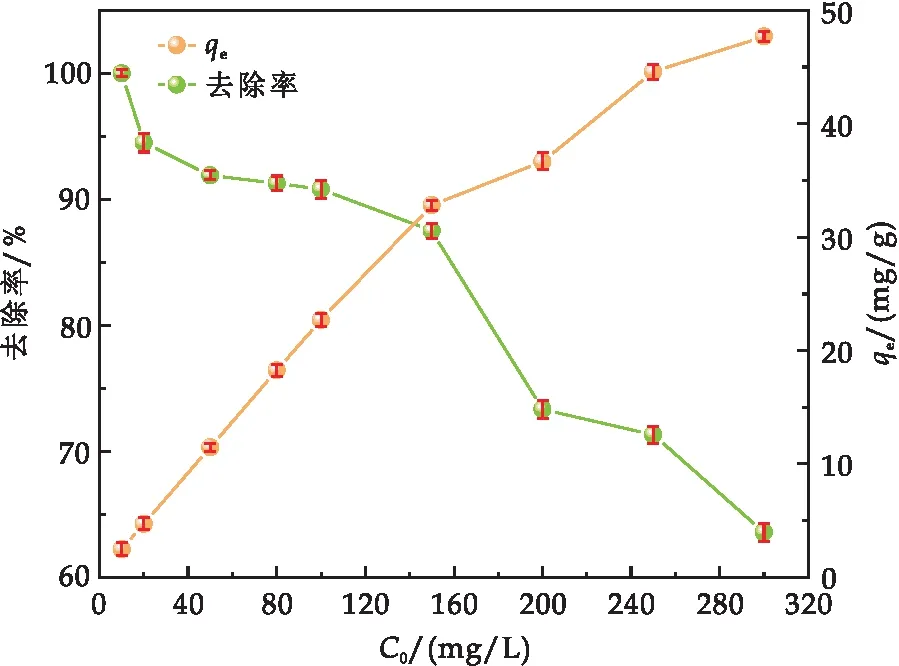
圖7 Cr(VI)初始濃度對吸附的影響
2.2.4 溶液pH對Cr(VI)去除的影響
溶液pH對Cr(VI)去除的影響結(jié)果如圖8所示.當(dāng)pH在1~3時,Fe-S@HKBC對Cr(VI)吸附量由24.36 mg/g緩慢減少至22.70 mg/g,當(dāng)pH在3~6時,吸附量由22.70 mg/g減少至11.58 mg/g,當(dāng)pH在6~12時,吸附量由11.58 mg/g又減少至7.91 mg/g.因此,吸附的最佳pH為1.Fe-S@HKBC對Cr(VI)的吸附量隨著pH的增大而減小,這是因為溶液pH不僅會影響生物炭的表面電荷,還會影響重金屬的化學(xué)形態(tài).由圖8可知,Fe-S@HKBC的Zeta電位隨pH的增大而減小,當(dāng)pH為1~4時,Fe-S@HKBC的Zeta電位為正,當(dāng)pH>4時,Fe-S@HKBC的Zeta電位為負(fù),且隨pH的升高而減小.
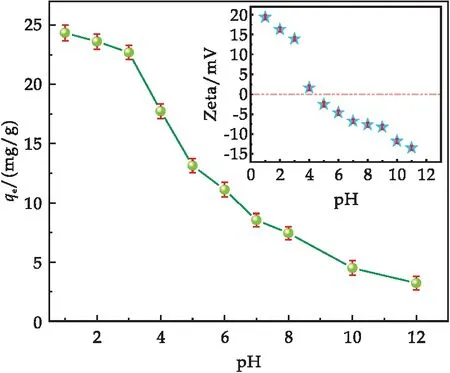
圖8 溶液pH對Cr(VI)去除的影響
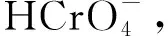
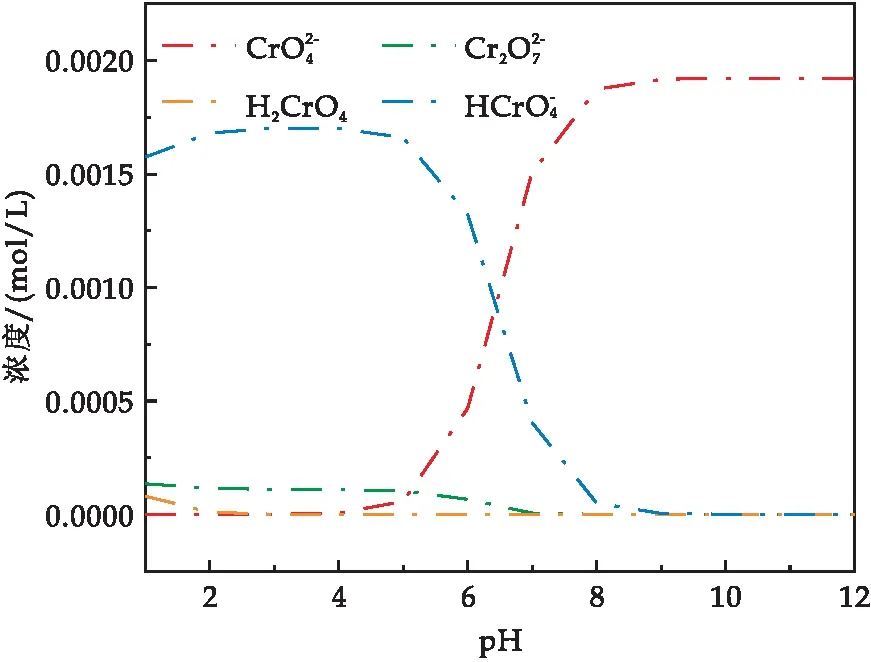
圖9 不同pH下Cr(VI)的存在形態(tài)
2.2.5 Na+和Ca2+對Cr(VI)去除的影響
由于含鉻廢水中常見共存離子有Na+和Ca2+,因此探究了Na+和Ca2+對Cr(VI)去除的影響,結(jié)果如圖10所示.當(dāng)Na+和Ca2+濃度從0變?yōu)? mol/L時,Fe-S@HKBC對Cr(VI)的吸附量從22.70 mg/g分別降至17.18 mg/g和12.40 mg/g.這是由于Na+、Ca2+與Cr(VI)存在競爭吸附[26],Ca2+比Na+的共價性高,離子半徑大,對Cr(VI)的吸附形成空間屏障的影響更大.另外,Ca2+與水結(jié)合形成Ca(OH)2可以覆蓋在生物炭的表面,阻擋生物炭對Cr(VI) 的吸附[27].由此可推斷Fe-S@HKBC對Cr(VI)的去除可能包含離子交換和絡(luò)合作用.
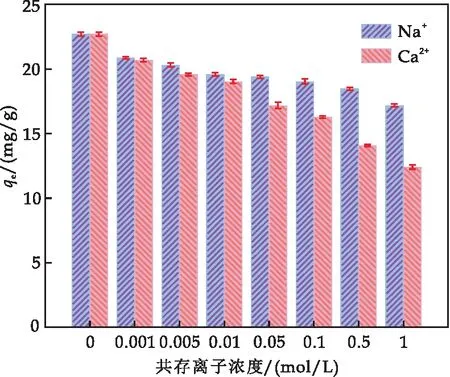
圖10 Na+和Ca2+對Fe-S@HKBC吸附Cr(VI)影響
2.2.6 吸附再生性能
Fe-S@HKBC對Cr(VI)的吸附再生性能實驗結(jié)果如圖11所示.解吸次數(shù)由1次增加至5次時,Fe-S@HKBC對Cr(VI)的吸附去除率由90.8%降低至42.25%.這可能是HCl洗滌對Fe-S@HKBC的孔結(jié)構(gòu)產(chǎn)生不利影響,使其活性位點(diǎn)減少,導(dǎo)致吸附去除率降低.經(jīng)3次循環(huán)后,Fe-S@HKBC對Cr(VI)的吸附去除率仍可達(dá)到69.47%,說明再生的Fe-S@HKBC對Cr(VI)仍具有較好的吸附能力,具備良好的循環(huán)再生性能.
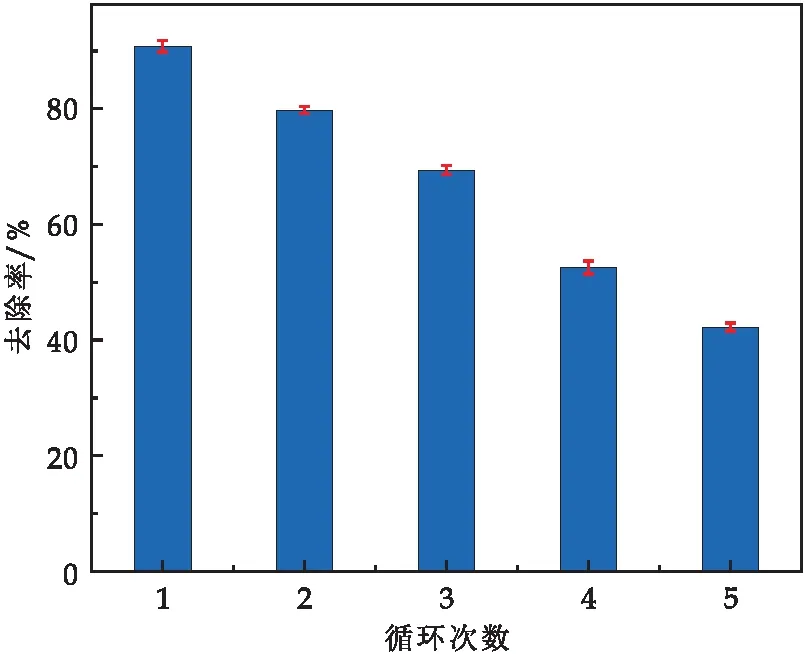
圖11 Fe-S@HKBC對Cr(VI)的吸附再生性能
2.3 吸附動力學(xué)
通過偽一級、偽二級、粒子內(nèi)擴(kuò)散和Elovich模型進(jìn)一步探討Fe-S@HKBC吸附Cr(VI)的動力學(xué)特征,擬合結(jié)果如表2和圖12所示.對比可知,偽一級的R2值高(R2=0.992),其對吸附初始階段的擬合較好(如圖12(a)所示),而偽二級動力學(xué)具有更高的R2值(R2=0.997),其理論計算的平衡吸附量(23.66 mg/g)與實驗值(22.70 mg/g)更接近,說明主要以化學(xué)吸附為主[28].圖12 (c)可知,粒子內(nèi)擴(kuò)散模型將吸附分為三個階段,其速率常數(shù)的順序為k1>k2>k3.常數(shù)較高的第一階段(k1=0.540)表明,Cr(VI)向Fe-S@HKBC表面的轉(zhuǎn)移受邊界層擴(kuò)散的控制[29],常數(shù)較低的后兩個階段(k2=0.499,k3=0.481)表明Cr(VI)逐漸被吸附到生物炭的內(nèi)部孔隙通道上,然后達(dá)到動態(tài)吸附-解吸平衡.粒子內(nèi)擴(kuò)散模型擬合的回歸系數(shù)較高(R2=0.990),表明顆粒內(nèi)擴(kuò)散是限速步驟,但擬合線沒有穿過原點(diǎn),因此表明這并不是唯一的吸附速率控制因素.Elovich模型也很好的擬合了該吸附過程(R2=0.984),表明吸附存在非均相擴(kuò)散過程.
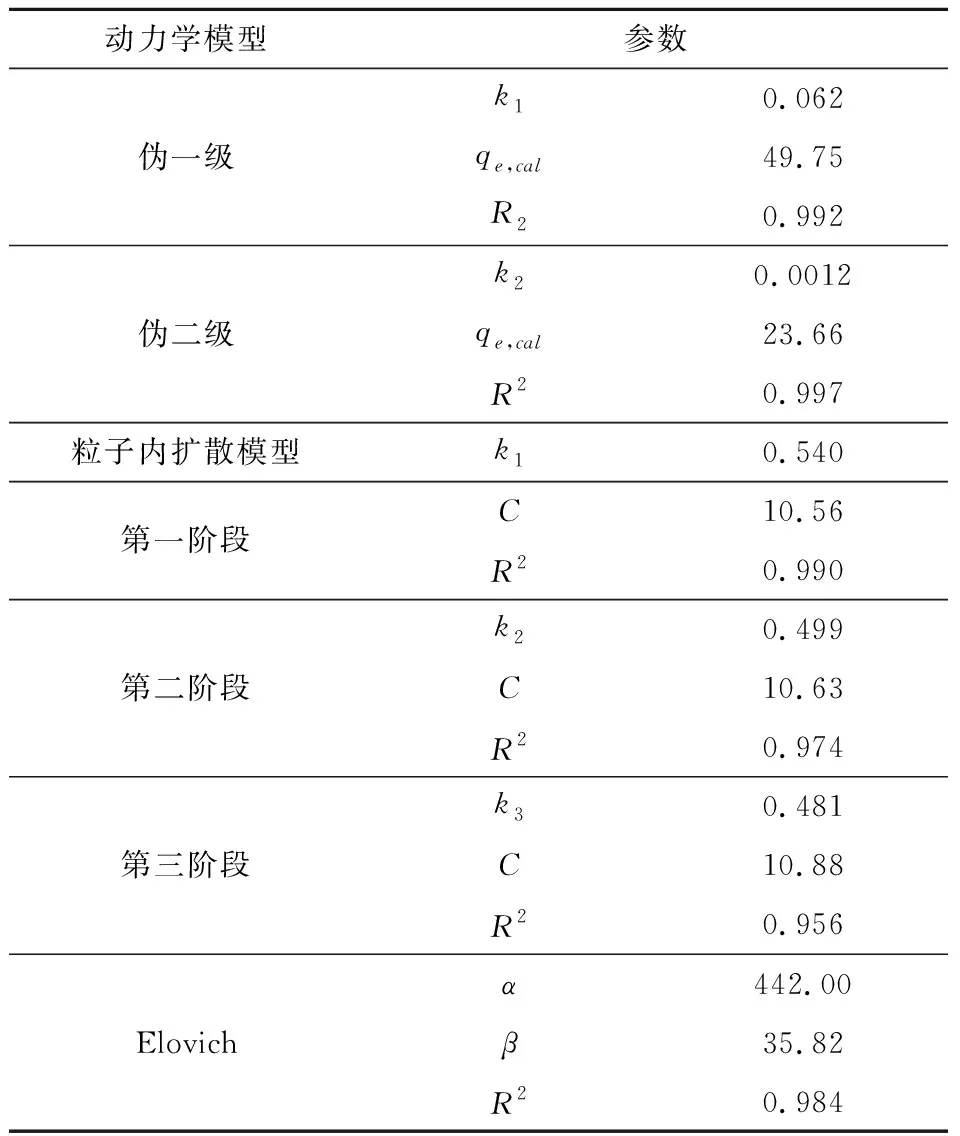
表2 Fe-S@HKBC吸附Cr(VI)動力學(xué)擬合參數(shù)
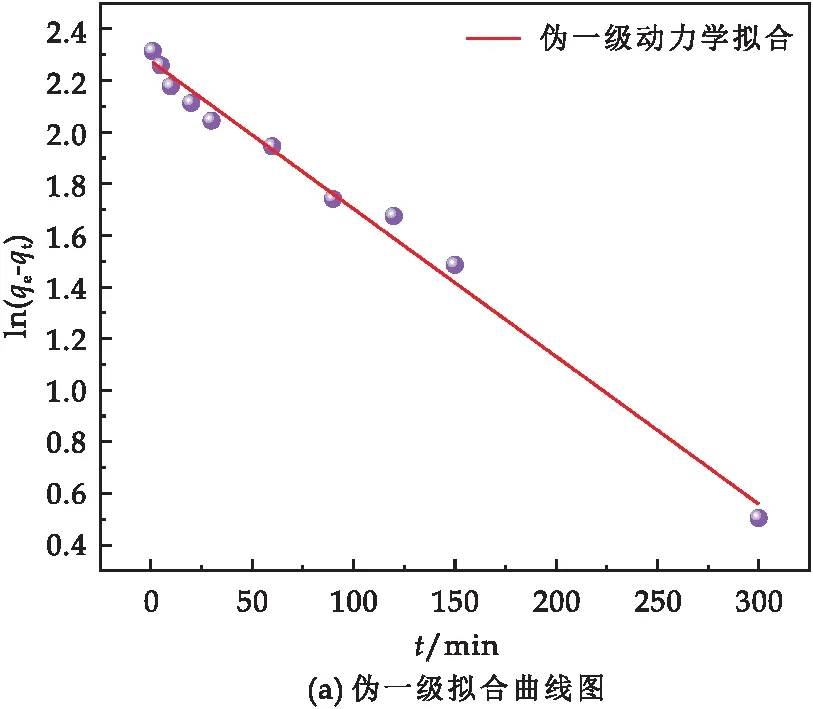
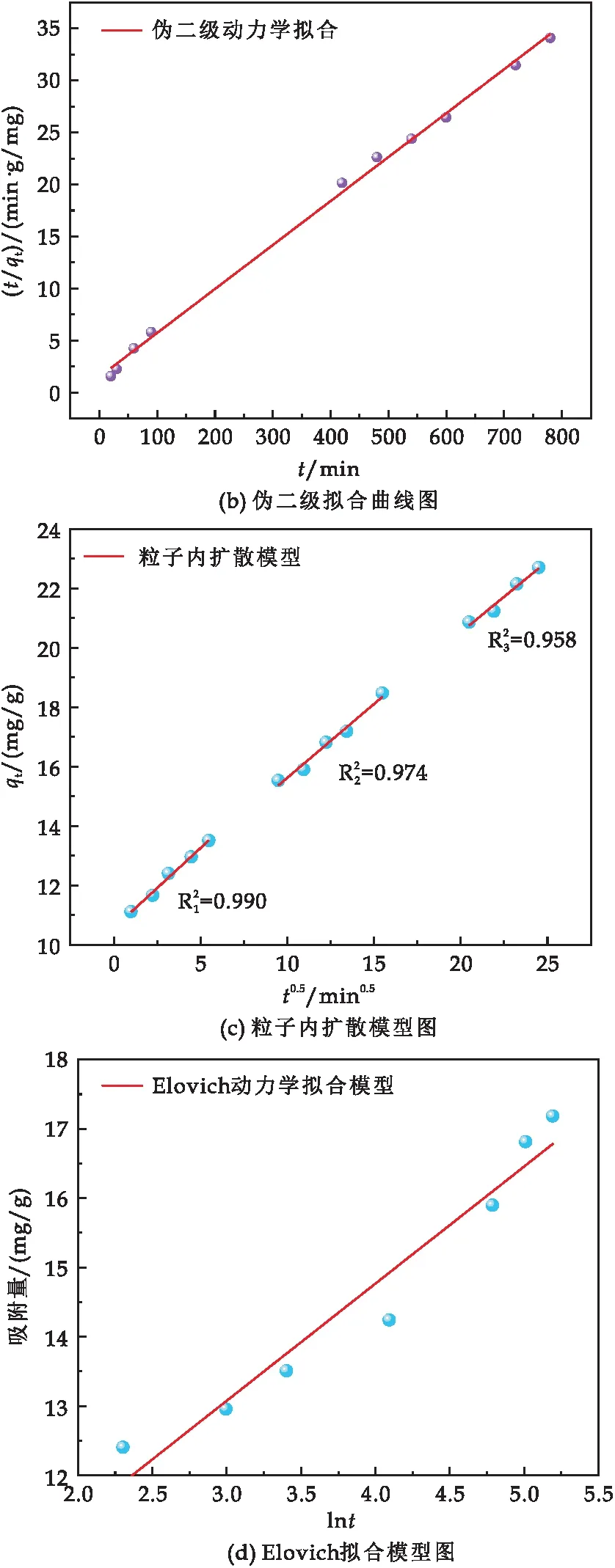
圖12 Fe-S@HKBC吸附Cr(VI)的動力學(xué)擬合曲線
2.4 吸附等溫線
吸附等溫線的擬合結(jié)果如表3和圖13所示.對比表3和圖13可知,Langmuir模型比Freundlich、D-R和Temkin模型擬合得更好,表明Fe-S@HKBC對Cr(VI)的吸附主要是單層吸附,Langmuir模型計算的RL值在0和1之間,表明Fe-S@HKBC對Cr(VI)的吸附是有利的.Freundlich模型也能較好描述Fe-S@HKBC對Cr(VI)的吸附過程(R2值為0.962~0.981),由D-R模型擬合的自由能(E)可知Fe-S@HKBC在不同溫度下吸附Cr(VI)的E<8 kJ/mol,表明物理作用對吸附有利[30].Temkin溫模型也能很好的描述該吸附過程(R2值為0.982~0.992),說明靜電作用在吸附過程中也發(fā)揮了作用.
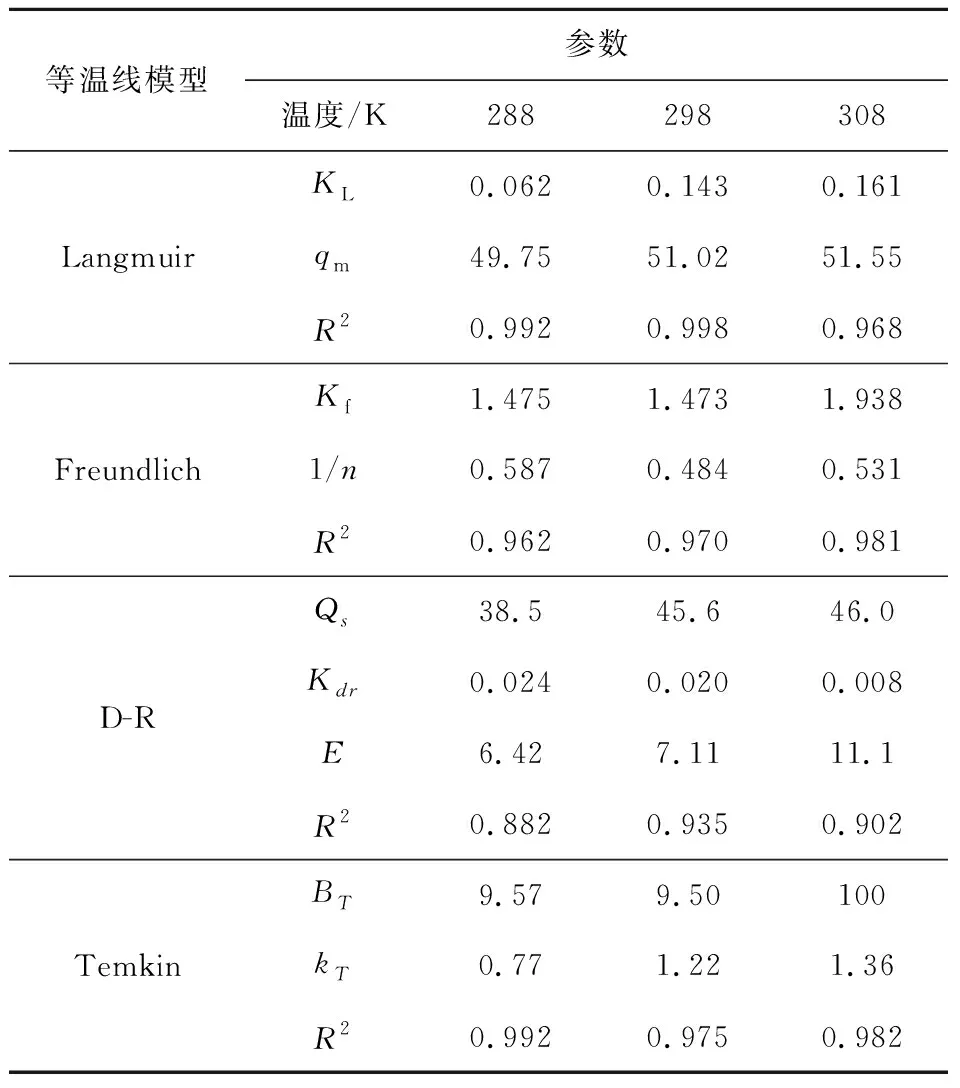
表3 Fe-S@HKBC吸附Cr(VI)等溫參數(shù)
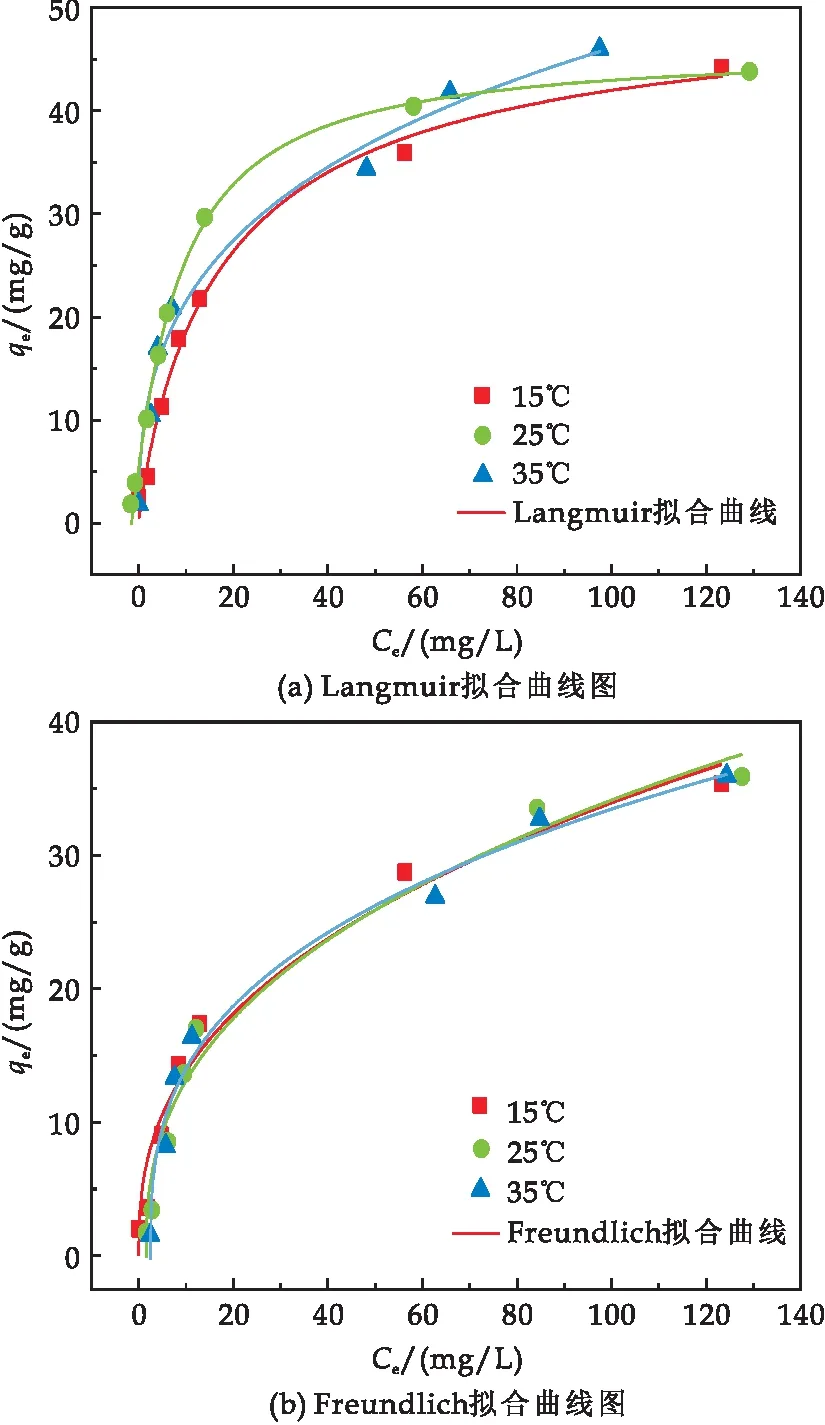
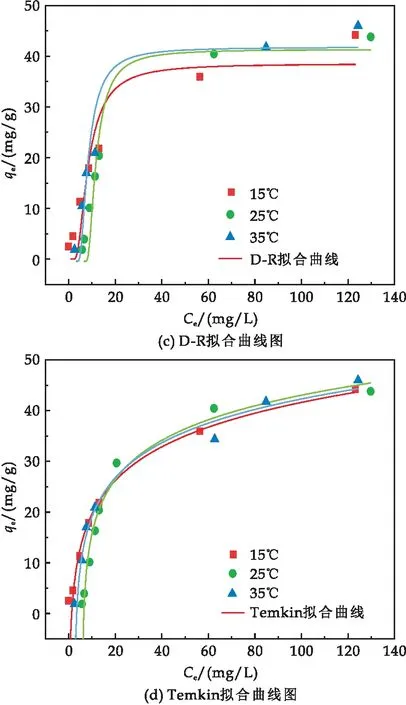
圖13 Fe-S@HKBC去除Cr(VI)的吸附等溫線擬合曲線
綜上可知,Cr(VI)在Fe-S@HKBC表面的吸附過程主要以均相單層物理吸附為主,但也存在非均相表面化學(xué)吸附和靜電相互作用,是一種受多種機(jī)制控制的復(fù)雜過程.
表4對比了幾種不同生物炭對Cr(VI)的最大吸附量.可以看出,Fe-S@HKBC的吸附性能高于表中其他生物炭.此外,Fe-S@HKBC的制備方法簡單,具有原料便宜易得的優(yōu)勢.
2.5 吸附機(jī)理分析
由圖4可知,Fe-S@HKBC吸附Cr(VI)后,在460 cm-1處的Fe-O振動峰強(qiáng)度明顯降低,表明Fe-O參與了對Cr(VI)的吸附.吸附Cr(VI)后C-O和Fe-O基團(tuán)的振動峰強(qiáng)度明顯減小,表明C-O和Fe-O基團(tuán)在Fe-S@HKBC吸附Cr(VI)上發(fā)揮了作用.
SEM、N2吸附-脫附和孔徑分布表明用鐵改性污泥生物炭可以增大生物炭的比表面積;XRD分析可以看出鐵改性后Fe-S@HKBC表面引入了金屬離子;FT-IR分析證明鐵改性在生物炭表面增加了含氧官能團(tuán).總之,改性后的Fe-S@HKBC具有微孔、介孔結(jié)構(gòu),有利于對Cr(VI)的物理吸附;引入了金屬離子,形成金屬氧化物,可以通過靜電引力促進(jìn)Cr(VI)的吸附;表面含有更多的含氧官能團(tuán)(如Fe-O、C-O、-OH),可以與Cr(VI)進(jìn)行絡(luò)合作用.根據(jù)動力學(xué)和等溫線分析,Fe-S@HKBC對于Cr(VI)的吸附是以發(fā)生在非均相表面的化學(xué)吸附為主,物理吸附為輔.具體的吸附作用機(jī)理如式(14)~(18)所示:
FeS+H+→Fe2++HS-
(14)
FeO+2H+→Fe2++H2O
(15)
(16)
(17)
(18)
3 結(jié)論
(1)本文以剩余污泥為原料,制備了鐵改性污泥生物炭Fe-S@HKBC,其比表面積大,具有良好的多孔結(jié)構(gòu),表面官能團(tuán)豐富.
(2)鐵改性可顯著提高污泥生物炭對Cr(VI)的吸附性能.當(dāng)生物炭用量為4 g/L,Cr(VI)初始濃度為10~300 mg/L時,Fe-S@HKBC對Cr(VI)的吸附量可達(dá)47.69 mg/g,去除率高達(dá)99.82%.Langmuir和偽二級動力學(xué)模型能很好描述吸附過程.吸附機(jī)理包括氫鍵、絡(luò)合、還原和靜電引力作用.
(3)Fe-S@HKBC對Cr(VI)具有高效的吸附能力,且再生性能良好,可用于水中Cr(VI)的去除.

