兩種不同品牌谷胱甘肽還原酶檢測試劑盒的性能評價
錢 錦,黃 穎
(南京醫科大學附屬泰州人民醫院 檢驗科,江蘇 泰州 225300)
谷胱甘肽還原酶(GR,Glutathione reductase)是一種利用還原型輔酶II(NADPH)將氧化型谷胱甘肽(GS-SG)催化反應為還原型(GSH)的酶。目前國內主流的全自動生化分析儀均可以完成谷胱甘肽還原酶檢測,這使得大批量快速檢測該項目得到實現。生化檢驗體外診斷試劑品牌多種多樣,選擇一款適合于實驗室及臨床的生化檢測試劑尤為重要。性能驗證實驗無疑是實驗室評價體外診斷試劑的最方便有效的方式。根據行業標準描述[1],驗證是指通過提供客觀證據對規定要求已得到滿足的認定,即醫學實驗室通過具體實驗明確試劑廠商聲明的技術數據有無問題。這是醫學實驗室在新試劑使用前最為重要的一步。
1 資料與方法
1.1 一般資料 新鮮人血清標本1.5ml 左右。驗證參考范圍所需的正常人群來源于我院健康體檢者,共40 名,其中男22 名,女18 名。每種試劑隨機抽取20 名,其中男11 名,女9 名。年齡18~65 歲。要求血常規、肝、腎功能、血糖血脂等實驗室指標正常;B 超、胸透/胸片、心電圖正常;無糖尿病、血液系統、心血管等系統疾病史;排除妊娠人群、排除用藥者及服用保健品者;半年內無手術史及輸血/獻血史。
1.2 儀器、試劑及檢測方法 檢測儀器為Beckman Coulter AU5800全自動生化分析儀。試劑為安徽大千谷胱甘肽還原酶檢測試劑盒,試劑批號20210600101,校準品批號202106001,質控品批號202106001;山東中拓谷胱甘肽還原酶檢測試劑盒,試劑批號21042711,校準品批號2103171L,質控品批號2106031L。兩種品牌的谷胱甘肽還原酶試劑檢測方法均為速率法。
1.3 實驗方法
1.3.1 儀器準備 使用廠家推薦檢測參數進行儀器設置,隨后使用配套校準品進行檢測系統校準,確認校準結果無誤后開始進行性能驗證實驗。
1.3.2 精密度驗證實驗 選取兩個濃度的質控品,關注醫學決定水平,每天檢測1 個分析批,每批檢測2個水平的樣本,每個樣本重復檢測3次,連續檢測5 天,計算實驗室內(總)標準差或CV。判斷標準:實驗室總不精密度CV≤6.67%。
1.3.3 正確度驗證實驗 谷胱甘肽還原酶無可獲取的標準物質,無法使用標準物質進行正確度驗證實驗,因此采用患者樣本比對的方法進行正確度驗證實驗。該方法遵循衛生行業標準的規定要求[1]。我院采用與安徽醫科大學第一附屬醫院(三級甲等)檢驗科(通過CNAS ISO15189 認可)進行人血清標本比對的方案進行正確度驗證。選取患者/受試者樣本20份,被測物濃度、活性等在測量區間內均勻分布,并關注醫學決定水平,用實驗方法和比對方法分別檢測,分成3~4 天,每天5~7個標本檢測完。參比系統:經驗證分析性能符合預期標準,日常室內質控、室間質評/能力驗證合格的檢測系統。優先選用符合以上要求的CNAS認可實驗室的檢測系統。本實驗參比系統為通過ISO15189 認可的實驗室。判斷標準:實驗系統均值與參比系統均值的總體差異≤10%。
1.3.4 線性范圍驗證實驗 選取接近廠家聲明線性上下限濃度樣本,按4H+1L,3H+2L,2H+3L,1H+4L 比例混合,包括原有的高值、低值共6 份樣品,每個濃度水平的樣本重復測定3 次,一次性完成檢測,對測定值與稀釋系數Excel表格計算一次、二次、三次回歸系數;系數標準誤;對應T值及回歸標準誤差。判斷標準:經T檢驗,若二次、三次系數與 “0” 無顯著差異,即線性驗證成功;若當存在非線性時,根據回歸標準誤的大小,將最小者確定為最適擬合模型。對判斷為非線性的數據需進行非線性程度的判斷。首先需進行不精密度和偏離直線平均差異(ADL 值)的計算。將計算出的ADL 值同不精密度與ADL 臨界值表中的數據進行比較,如小于臨界值,則表示數據雖判斷為統計學上的非線性,但不精密度和ADL 為臨床可接受,為臨床可接受的非線性[2]。
1.3.5 參考范圍驗證實驗 選擇20 份無相關疾病的體檢合格的健康人群標本,在檢測系統上進行測定,對結果進行統計并對參考區間進行驗證。判斷標準:若20 份標本的檢測結果經離群值判斷處理后,均在參考區間內或不多于2 個標本超出,則驗證通過。否則需參照行業標準進行參考區間確立實驗。
1.4 統計學方法 結果的統計分析采用Microsoft Excel軟件。
2 結果與結論
2.1 精密度 兩品牌試劑精密度性能均符合要求。精密度驗證結果見表1。
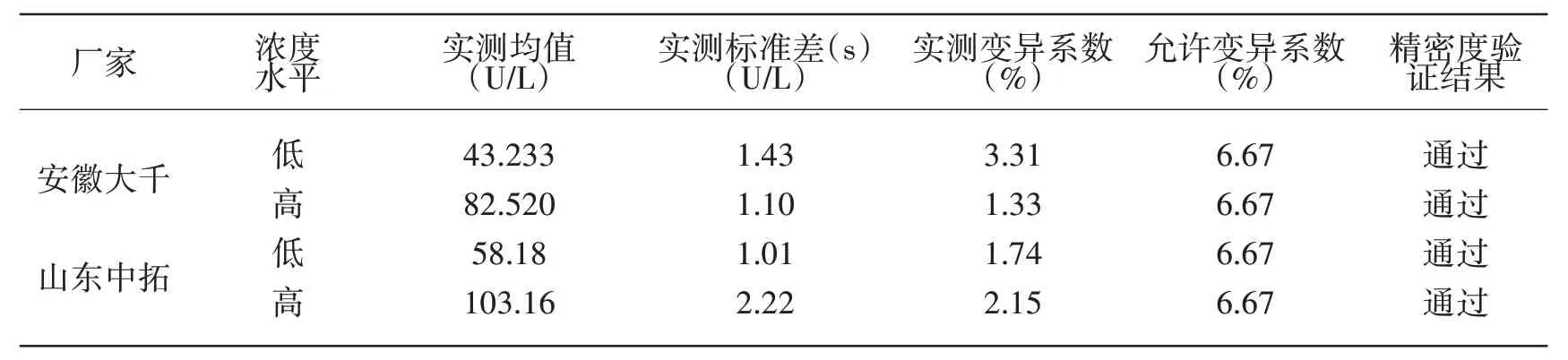
表1 安徽大千和山東中拓精密度驗證實驗結果
2.2 正確度驗證 允許范圍為不超過10.0%。兩品牌試劑正確度性能均符合要求。正確度驗證結果見表2、圖1、圖2。
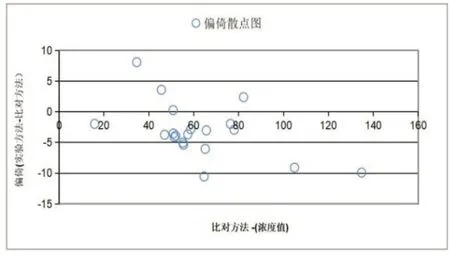
圖1 山東中拓正確度驗證回歸分析圖
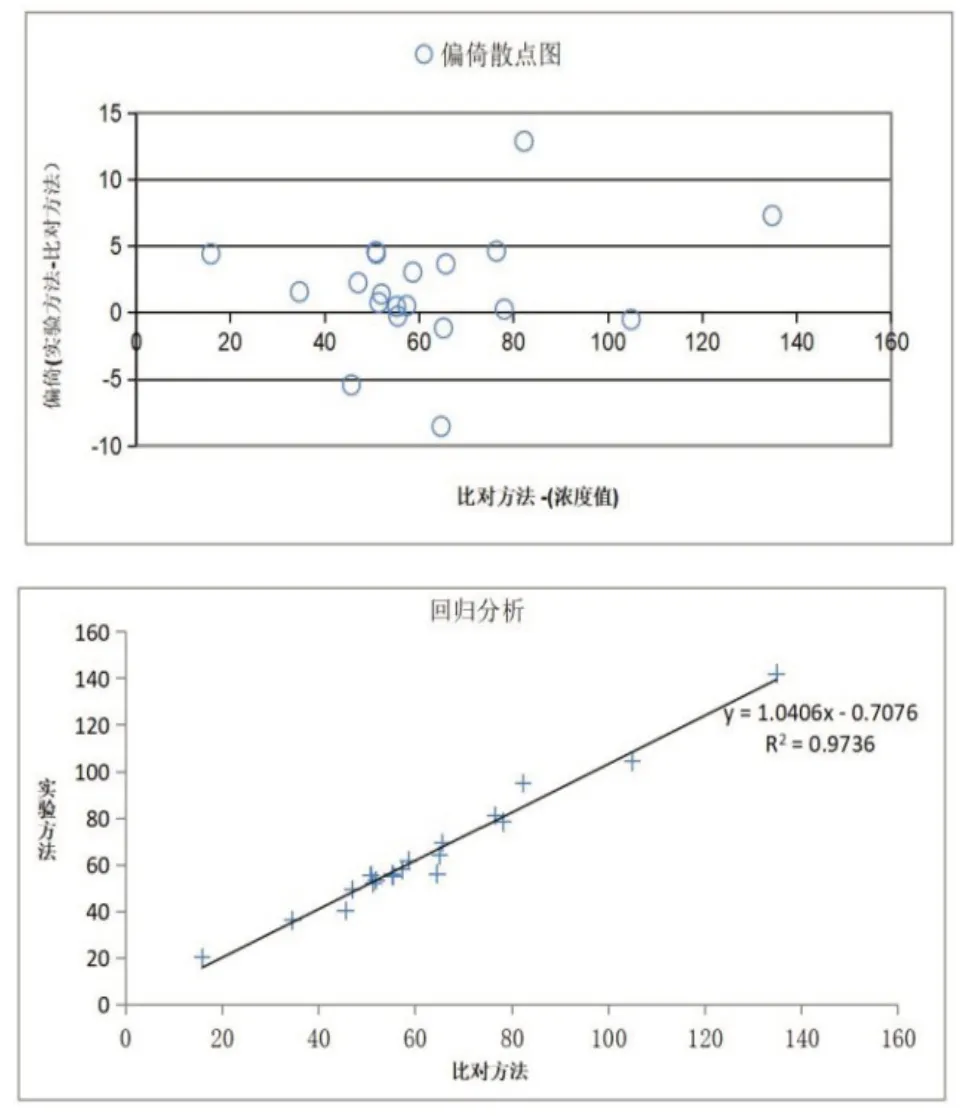
圖2 安徽大千正確度驗證回歸分析圖
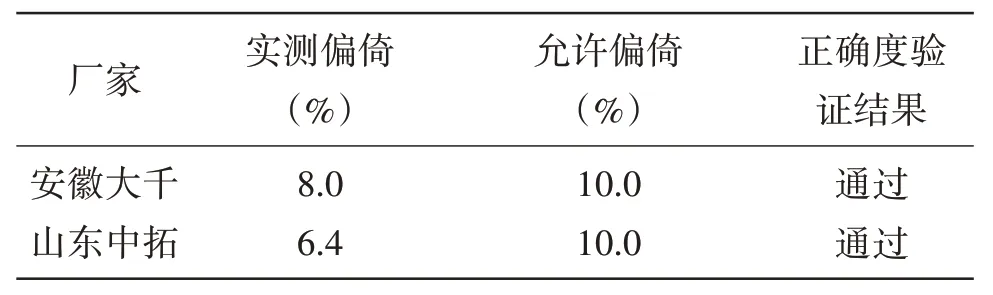
表2 安徽大千和山東中拓正確度驗證實驗結果
2.3 線性范圍驗證 安徽大千的線性范圍為10~200U/L,山東中拓的線性范圍為4~300U/L。通過驗證實驗分析可知,兩品牌試劑線性范圍性能驗證實驗的ADL實測值均低于臨界值(允許值),可判定驗證均通過。其中安徽大千為線性方程,山東中拓為臨床可接受的三階非線性方程。線性范圍驗證結果見表3。
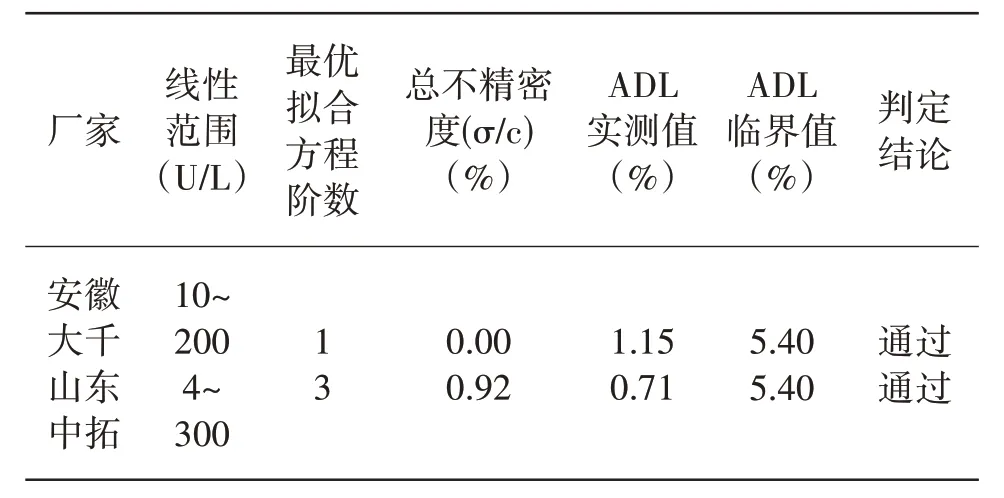
表3 安徽大千和山東中拓線性范圍驗證實驗結果
2.4 參考范圍驗證 通過不同批次正常人的血清檢測和驗證,安徽大千和山東中拓參考范圍均符合要求。參考范圍驗證結果見表4。
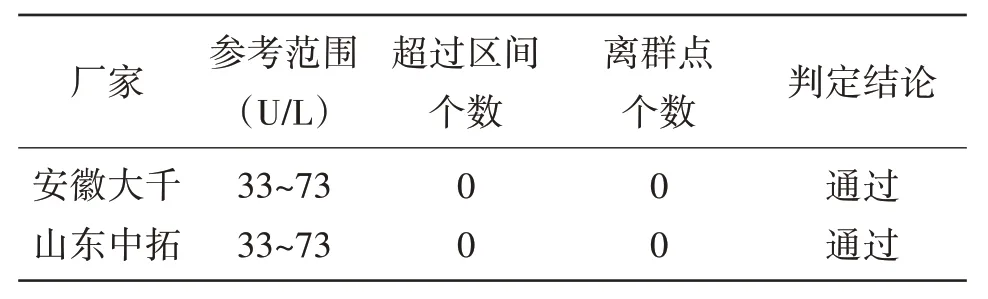
表4 安徽大千和山東中拓參考范圍驗證實驗結果
通過性能驗證實驗發現,安徽大千和山東中拓的檢測性能指標均符合相關要求。其中山東中拓總精密度(取小者)較小、線性范圍(取寬者)較寬,雖正確度方面(取小者)安徽大千略優于山東中拓,但從試劑穩定性(精密度要小)和使用成本(潛在高值復查率要低)方面綜合考慮,山東中拓略優于安徽大千。
3 討論
性能驗證是指由醫學實驗室通過特定實驗,使用客觀證據證明廠家聲明的性能指標是否滿足規定要求的過程,該過程由醫學實驗室獨立完成。
醫學實驗室性能驗證方案離不開標準文件,較為經典的為美國臨床和實驗室標準協會(CLSI)發布的EP(evaluation of permance)文件,用于指導臨床實驗室和制造商進行性能驗證和確認。EP文件多且雜,并帶有復雜的統計學公式。目前中文譯文較少,且最新文件無法免費獲取,因而無法廣泛推廣。近年來我國衛生部門以EP文件為基礎,發布了各種用于醫學實驗室性能驗證的衛生行業標準(WS/T),大大提高了標準文件的閱讀性和普及性。但不同性能驗證內容需要參考不同的衛生行業標準,對于基層醫學實驗室使用時仍不方便。中國合格評定國家認可委員會(CNAS)于2019年開始發布關于不同檢驗領域的性能驗證說明,這些文件將衛生行業標準整合在一起,加入不同專業領域特定要求,對整個性能驗證實驗過程進行系統描述,以期規范不同實驗室操作流程。
相較于室內質控,性能驗證的難主要體現在樣本的選擇和數據的計算。以線性范圍驗證為例,不同于精密度、正確度和參考范圍驗證,線性范圍驗證需要的樣本濃度跨度極大,計算非常繁瑣,以CLSI EP6 方案為甚。雖然CLSI 在臨床實驗室標準的制定上,處于最權威的機構,但對于線性驗證的處理顯得欠妥。2020 年CLSI 發布了最新的EP06 文件(EP06-Ed2),其中對于統計方法做了大幅度改變,不再要求做二項和三項回歸,而是采納加權線性(WLS,Weiguted Least Square)[3]。但原文中專家們仍然認為EP06-A的統計方式更科學。所以猜想這是不是為了在 “數學” 和 “實踐” 之間取得一個平衡,放棄了二項和三項回歸的要求。中國國家衛健委頒布的衛生行業標準中,涉及線性驗證的有兩份文件:(1)WS/T 408-2012《臨床化學設備線性評價指南》;(2)WS/T 420-2013《臨床實驗室對商品定量試劑盒分析性能的驗證》。這兩份文件均未完全遵循CLSI EP06方案。WS/T 420-2013使用相關系數判斷線性,本身在統計方法上值得商榷。WS/T 408-2012 最接近EP06方案,但在臨床可接受的非線性驗證上,確與EP06 方案存在差異。主要體現在計算最優擬合曲線與直線的平均差異值ADL (aveage deviation from linearity)。WS/T 408-2012計算ADL是針對所有濃度的平均值,EP06 是要求對每個濃度的樣本做逐一判斷,即每個濃度包括低值樣本必須通過,往往難以達到臨床可接受的判斷標準。三份文件均存在使用上的難點和不足。2019 年之前CNAS并未明確規定性能驗證的方案,只要求采用相關標準文件即可,實驗室在實施線性范圍驗證時,多數采用WS/T 420-2013 方案,該方案實施簡單,通過率高,但該方案本身存在缺陷,需要淘汰。針對此問題,2019 年CNAS 發布的CNAS GL-037《臨床化學定量檢驗程序性能驗證指南》,建議將WS/T 408-2012作為醫學實驗室線性范圍性能驗證的依據。
綜上所述,CNAS GL-037《臨床化學定量檢驗程序性能驗證指南》文件可進行同一項目不同試劑品牌的性能比較。性能驗證實驗應由醫學實驗室工作人員獨立完成。實驗室選擇試劑品牌時,應根據真實的數據結果,對試劑穩定性、使用成本等多方面進行綜合判斷。總之,CNAS GL-037《臨床化學定量檢驗程序性能驗證指南》通過標準化整合,一定程度上為醫學實驗室尤其是基層實驗室進行試劑品牌的選擇,提供科學的實驗依據和實驗流程。

