高酯柑橘果膠-大豆分離蛋白復合凝膠制備及質構性質研究
張慧敏, 許馨予, 賈 斌, 王 坤,2, 李 丹,2, 左 鋒,3
(黑龍江八一農墾大學食品學院1,大慶 163119) (黑龍江八一農墾大學國家雜糧工程技術研究中心2,大慶 163119) (糧食副產物加工與利用教育部工程研究中心3,大慶 163119)
果膠是一種從天然植物中提取出的陰離子型多糖,具有較高營養價值的功能性成分[1]。CP主要是從柑橘的皮渣中提取制備,具有良好的凝膠性、乳化穩定性,因此常被作為膠凝劑廣泛用在果汁飲料、果醬、乳制品、蜜餞食品中[2]。根據酯化程度,通常可將果膠分為高甲氧基(HM)果膠[酯化度(DE)>50%]和低甲氧基(LM)果膠(DE<50%)[3]。目前,CP膠凝化主要依靠柑橘分子間的氫鍵、范德華力及靜電引力,HM凝膠的形成需要低pH,較高濃度的可溶性固形物,LM凝膠的形成需要Ca2+的參與且少量離子存在。HM相比LM不需要在Ca2+條件下可以通過調節酸糖的濃度比例形成凝膠,且在較高濃度的糖條件下,HM分子與水分子相互作用減弱,而果膠分子之間的相互作用更有利,從而形成了空間網絡結構,使果膠的凝膠穩定性增強。國內外學者對果膠凝膠形成進行了廣泛的研究,Kahlile等[4]研究發現從百香果中制備的HM不需要改變蔗糖的濃度,可以通過調整pH形成穩定的凝膠。李素芬等[5]對佛手瓜復配柚子果醬研究發現柚子皮中提取出來的果膠應用在果醬中可進行膠凝,膠凝效果較好,進一步提高柚子皮的利用價值。但果膠凝膠的制備放一段時間后由于氫鍵、范德華力及靜電引力的作用,易產生凝膠不均勻、脫水收縮現象、形成預凝膠溶液不穩定等問題,這制約了果膠凝膠在食品生產中的應用[6]。
多糖和蛋白質之間可以通過疏水作用、靜電等相互作用形成穩定的復合物,構建形成的復合物不僅具有良好的凝膠均勻穩定性,而且凝膠網絡結構致密,能夠改善食品功能、構建新型功能性食品[7]。Xu等[8]研究結果表明SPI與CP主要通過疏水作用形成復合物,SPI與CP結合,導致氨基酸殘基的微環境及整個蛋白質構象發生改變。汪少蕓等[9]研究表明蛋白質和多糖作為食品原料中重要的生物大分子,經過分子間相互作用形成的復合物比二者單獨使用功能性質更好,兩者復合物比例的不同對復合物凝膠也有著重要作用。Molina等[10]對蛋白與HM進行靜電復合物表征,發現果膠中可電離的羧基可以改變蛋白表面結構,形成致密的復合物。張予心等[11]研究發現乳清蛋白-海藻酸鈉制備的不同比例復合物其凝膠特性存在顯著差異,當海藻酸鈉添加2%時復合物顯示出較好的凝膠特性。
為提高SPI-CP復合凝膠溶液的穩定性,改善復合凝膠質構特性,實驗以SPI和CP為原料,通過制備穩定的SPI-CP復合物,并通過單因素、響應面實驗探究不同pH、蔗糖質量分數、復合物質量濃度對凝膠質構特性的影響,確定最佳凝膠制備工藝參數,構建一種蛋白質-多糖復合凝膠體系,以期為新型凝膠的制備提供思路。
1 材料與方法
1.1 材料與試劑
CP(DE純度為77.99%)、SPI(>90%)、蔗糖(食品級);鹽酸、檸檬酸:分析純。
1.2 儀器與設備
TA-XT2i質構儀, UV-2910紫外分光光度計, Nano-v4電位儀, Nano-v4粒度儀。
1.3 方法
1.3.1 復合物制備
取10 g的SPI溶解在蒸餾水(500 mL)中,攪拌均勻,制備SPI溶液(20 mg/mL)溶液在90 ℃下加熱30 min,在4 ℃保存過夜。
將CP取10 g溶解在500 mL蒸餾水中攪拌均勻,制備果膠溶液(20 mg/mL),在4 ℃保存過夜。
將SPI和CP的體積比分別為3∶1、2∶1、1∶1、1∶2、1∶3,將溶液調pH至4.5后,攪拌均勻備用。
1.3.1.1 復合物濁度測定
采用分光光度法[12],將配制好的復合物溶液在吸光度550 nm處測定吸光度值,濁度值被定義為:
式中:τ為濁度值/cm;L為1 cm;I0;It分別為入、透射光光強,測3次取平均值。
1.3.1.2 復合物粒徑測定
采用Malvern Nano-v4電位儀,將樣品添加到配備有電極的反應杯中,溫度保持在25 ℃下,測定平均粒徑。將待測復合物用磷酸鹽緩沖液稀釋至蛋白質質量濃度為2 mg/mL,所有樣品測定3次。
1.3.1.3 復合物Zeta電位測定
采用Malvern Nano-v4電位儀,將樣品添加到配備有電極的反應杯中,溫度保持在25 ℃下測定Zeta電位。將待測復合物用磷酸鹽緩沖液稀釋至蛋白質質量濃度為2 mg/mL,所有樣品測定3次。
1.3.2 凝膠的制備
參考喻靖[13]的實驗方法,選取SPI-CP體積比1∶1的凍干樣品,將SPI-CP復合物分別配制成0.02、0.03、0.04、0.05 g/mL的溶液,于80 ℃水域條件下加熱1 h,補充水分維持樣品濃度,再用檸檬酸調節pH,加入蔗糖并攪拌均勻后在室溫下靜置10 min。
1.3.2.1 單因素實驗
以硬度、彈性、膠黏性、咀嚼性為測定指標,探究不同pH(2.4、2.6、2.8、3.0、3.2)、蔗糖質量分數(20%、25%、30%、35%、40%)、復合物質量濃度(0.01、0.02、0.03、0.04、0.05 g/mL)對復合物凝膠質構的影響,采用質構儀對凝膠體系進行測定,測定參數AOAC 12.7 mm凝膠專用柱形探頭,測定時探頭速度60 mm/min,形變10%,觸發力5 g,測試3次,取平均值。
1.3.2.2 響應面優化實驗
在單因素實驗結果的基礎上,設計響應面實驗,選擇pH、蔗糖和復合物質量濃度進行響應面實驗,以硬度作為響應值,探究凝膠制備最佳工藝條件,響應面因素水平見表1。
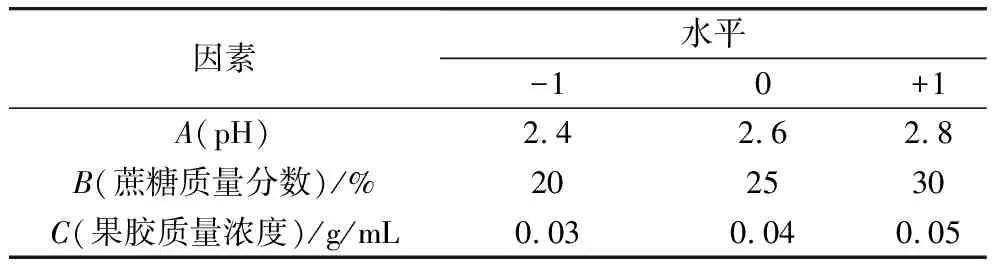
表1 因素水平編碼表
1.4 數據處理
所有數據測定3次,使用SPSS軟件進行顯著性分析。采用Origin 2018軟件和Excel繪圖。
2 結果與分析
2.1 SPI-CP復合物穩定性分析
2.1.1 濁度分析
濁度大小能夠表征復合物中顆粒的分散狀態,也是評價分子間是否相互聚集形成穩定復合物的重要指標,SPI-CP復合物在不同體積比下的濁度變化如圖1所示。隨著復合物中CP濃度的增加,復合物的濁度值呈先下降后上升趨勢,在SPI-CP體積比達到1∶1時濁度值達到最小值(0.26±0.01),這主要是由于當復合物中SPI比例較高時,蛋白分子間相互作用形成大量不溶性復合物,此時溶液濁度值較高。隨著CP比例的增加,SPI與CP之間發生較為強烈的靜電相互作用,較強的靜電排斥力抑制了蛋白分子間相互聚集,此時復合物體系穩定[13]。此時進一步提高SPI-CP復合物中CP比例,濁度值呈上升趨勢,這主要是由于進一步提高復合物中CP比例,復合體系中與單位蛋白結合的CP分子增加,改變了蛋白原有的伸展結構,導致復合物光散射強度的增加[14,15],當達到一定值后復合物濁度值趨于平緩。
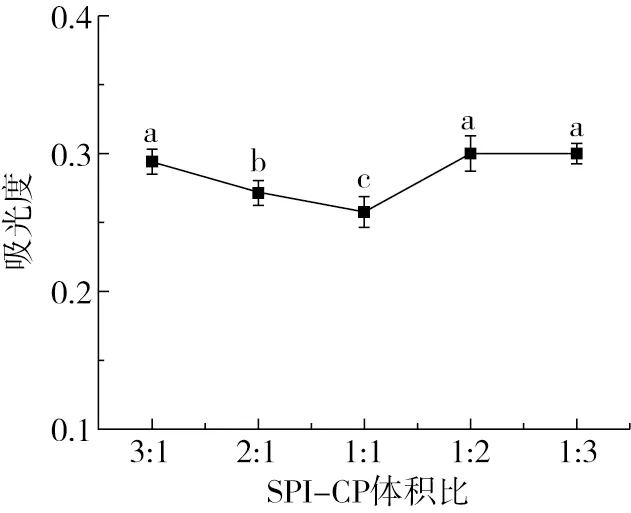
圖1 SPI-CP不同比例復合物濁度曲線
2.1.2 Zeta電位分析
復合物的穩定性是由顆粒間的靜電排斥力決定,顆粒間靜電排斥力越大,形成復合物不容易聚集,電位絕對值越大,溶液越穩定。SPI-CP復合物在不同體積比下的電位變化如圖2所示。在SPI-CP體積比為3∶1和2∶1時,復合物的電位差異不顯著(P>0.05)。隨著復合物中CP濃度的增加,復合物的電位絕對值值呈現先增加后減小的趨勢,在SPI-CP體積比達到1∶1時電位絕對值達到最大值(39.6±0.5)mV,這主要是由于蛋白質是兩性電解質,在復合物中高比例SPI條件下,蛋白質分子間可發生以疏水作用為主體的聚集作用,但隨著帶負電荷果膠增加與蛋白質帶負電荷聚集體結合,靜電排斥作用逐漸增強并阻止蛋白質分子間的相互吸附,致使電位絕對值增大[16]。當SPI-CP體積比達到1∶2和1∶3時電位絕對值逐漸下降,復合物的電位差異顯著(P<0.05)。這可能由于隨著CP比例的添加,蛋白分子與果膠分子由于疏水性作用而發生聚集,靜電排斥作用減弱而使復合物的電位絕對值逐漸減小,體系穩定性會降低[17]。

圖2 不同體積比SPI-CP的電位圖
2.1.3 粒徑分析
SPI-CP復合物在不同比例過程中的平均粒徑變化如圖3所示。在SPI-CP體積比為3∶1和2∶1時,復合物的粒徑差異性不顯著(P>0.05),但隨著復合物中CP濃度的增加,復合物的平均粒徑呈現先下降后上升的趨勢,在SPI-CP體積比達到1∶1時平均粒徑達到最小值(106±4)nm,這主要是由于較高比例的SPI分子聚集形成了大顆粒分子間的復合物,此時平均粒徑較高。但是隨著復合物果膠濃度增加,帶有負電荷的SPI和CP發生靜電排斥,抑制了SPI液滴間的聚集,復合物粒徑減小,與喻靖[13]對復合物粒徑的研究結果一致。在復合物比例達到1∶3時復合物粒徑差異顯著(P<0.05),平均粒徑變大,這主要由于隨著復合體系中CP濃度增多,體系中疏水作用增強導致分子顆粒聚集,并且CP通過疏水作用吸附在SPI顆粒的表面而使顆粒的粒徑進一步變大[18]。
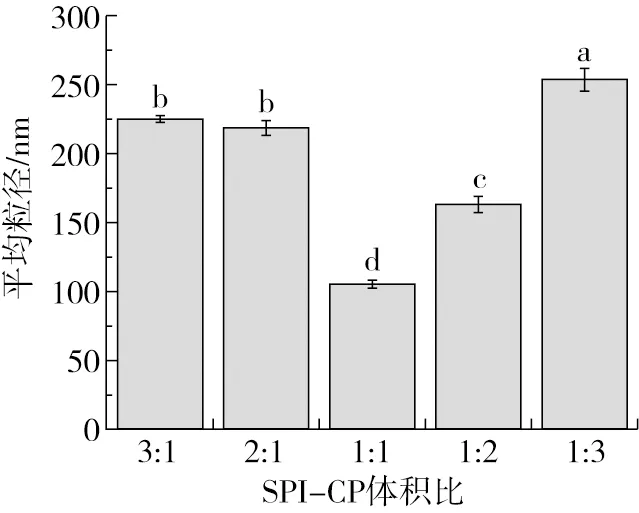
圖3 SPI-CP不同體積比平均的粒徑圖
2.2 復合凝膠的質構特性分析
2.2.1 單因素結果
2.2.1.1 pH對復合凝膠質構的影響
pH對復合凝膠質構影響如表2所示。當pH為3.2時,形成較弱的凝膠體系,凝膠硬度、彈性、膠黏性和咀嚼性均較低,Siew等[19]報道在較弱的酸性介質中,體系缺少氫鍵導致不能形成凝膠,說明此時凝膠網絡結構較弱;隨著pH降低,復合凝膠性能顯著升高(P<0.05),凝膠性能逐漸改善,在pH為2.6時達到最優,產生靜電相互作用,從而使凝膠性能都顯著提高;當pH繼續降低時,pH超出形成凝膠臨界值條件之后,凝膠性質開始降低,因此選擇最優pH為2.6。
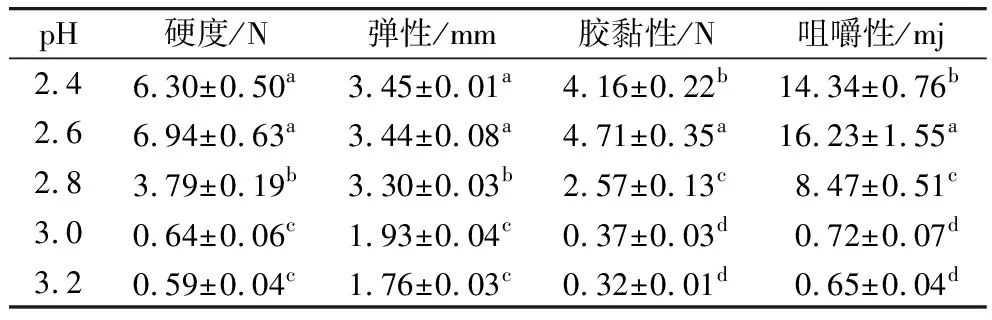
表2 pH對凝膠質構特性的影響
2.2.1.2 蔗糖濃度對復合凝膠質構的影響
由表3可知,當蔗糖質量分數為20%時,凝膠性能較差,隨著蔗糖濃度增加,凝膠性能有所提升,在蔗糖質量分數為25%時,硬度、膠黏性和咀嚼性呈現最大值,此時凝膠性能最好,Mouna等[20]研究蔗糖濃度對凝膠的影響結果表明蔗糖濃度增大,凝膠強度增強;隨著持續增加,體系凝膠性能復降低,過量蔗糖會改變果膠分子間立體的空間結構,最終致使凝膠變軟,因此選擇最優蔗糖質量分數為25%。
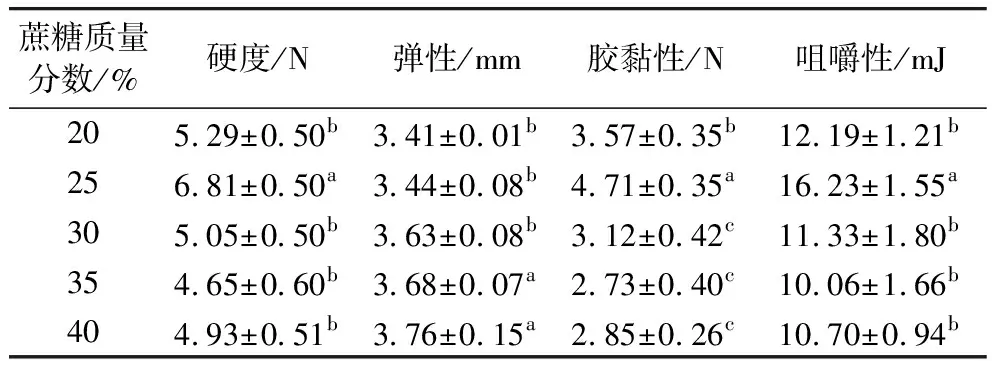
表3 蔗糖濃度對凝膠質構特性的影響
2.2.1.3 復合物質量濃度對復合凝膠質構的影響
復合物質量濃度對復合凝膠質構影響見表4。果膠本身具有黏附性,不易溶于水,通過前期預實驗得出SPI-CP復合物最大溶解質量濃度為0.05 g/mL,因此選擇果膠質量濃度為0.01~0.05 g/mL,隨著SPI-CP復合物質量濃度升高,體系凝膠性能逐漸增強,復合物質量濃度越高,分子間作用力增大,形成的凝膠網絡的結點數變多,結構越緊密,凝膠質構強度變大,因此選擇最優復合物質量濃度為0.05 g/mL。
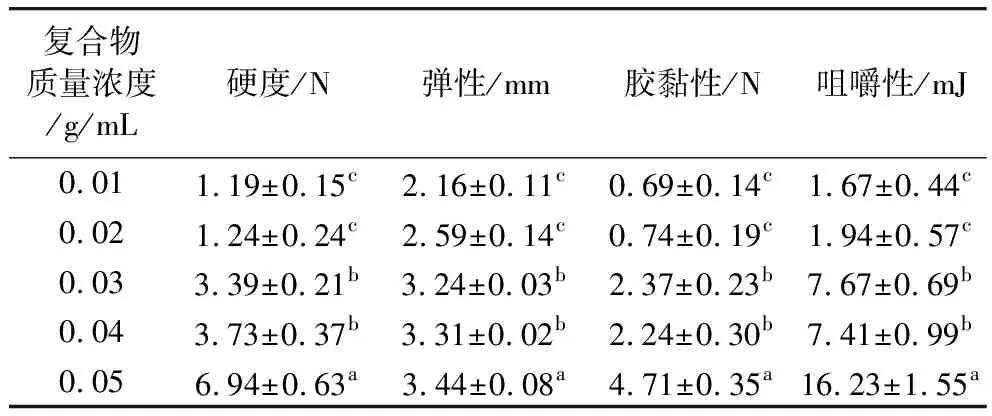
表4 SPI-CP復合物質量濃度對凝膠質構特性的影響
2.2.2 響應面實驗
2.2.2.1 響應面設計結果
從表5中分析可得,模型的回歸方程Y=5.31-0.25A+0.24B+0.99C+0.43AB-0.13AC-0.19BC-0.47A2-0.70B2+0.22C2。
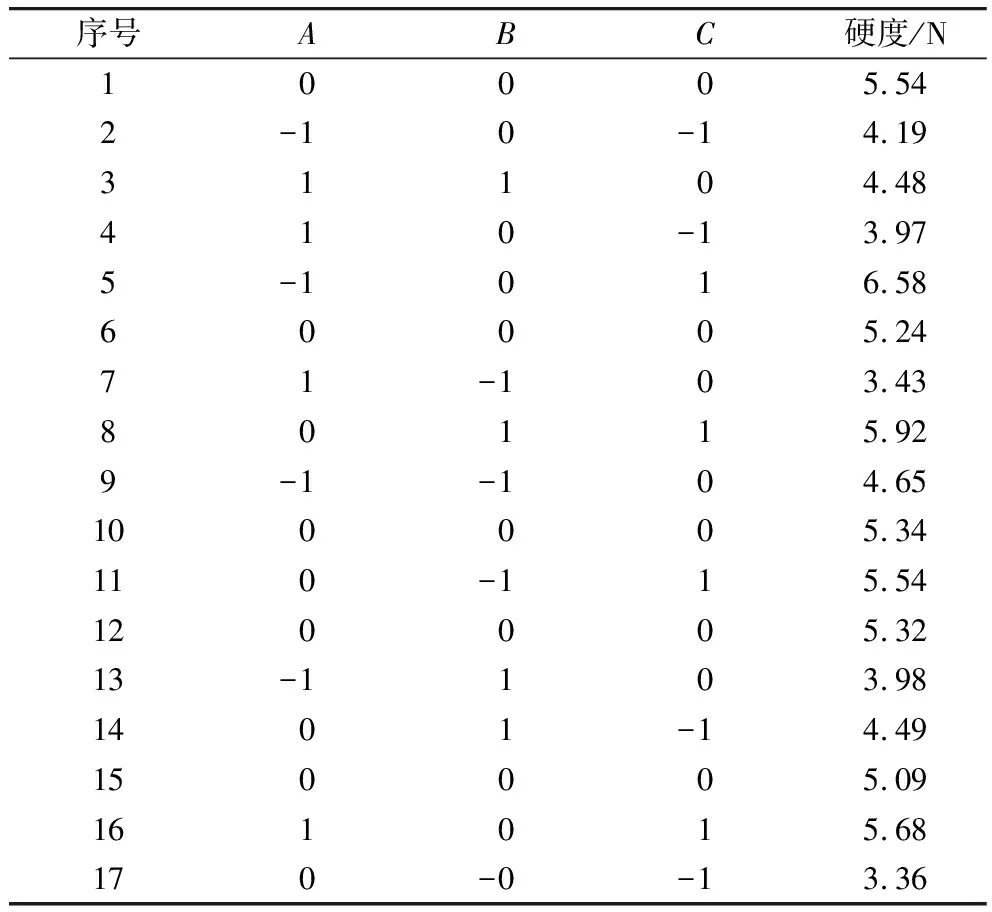
表5 復合凝膠硬度響應面實驗設計與結果
由表6可知,模型極顯著(P<0.01),失擬項不顯著,相關系數R2=0.973 6,表明模型與實際擬合度較高,因素A、B的P值均小于0.05,影響顯著;因素C、AB、A2和B2的P值均小于0.01,影響極顯著。根據F值可知對凝膠硬度的影響的因素順序為復合物質量濃度>pH>蔗糖濃度。
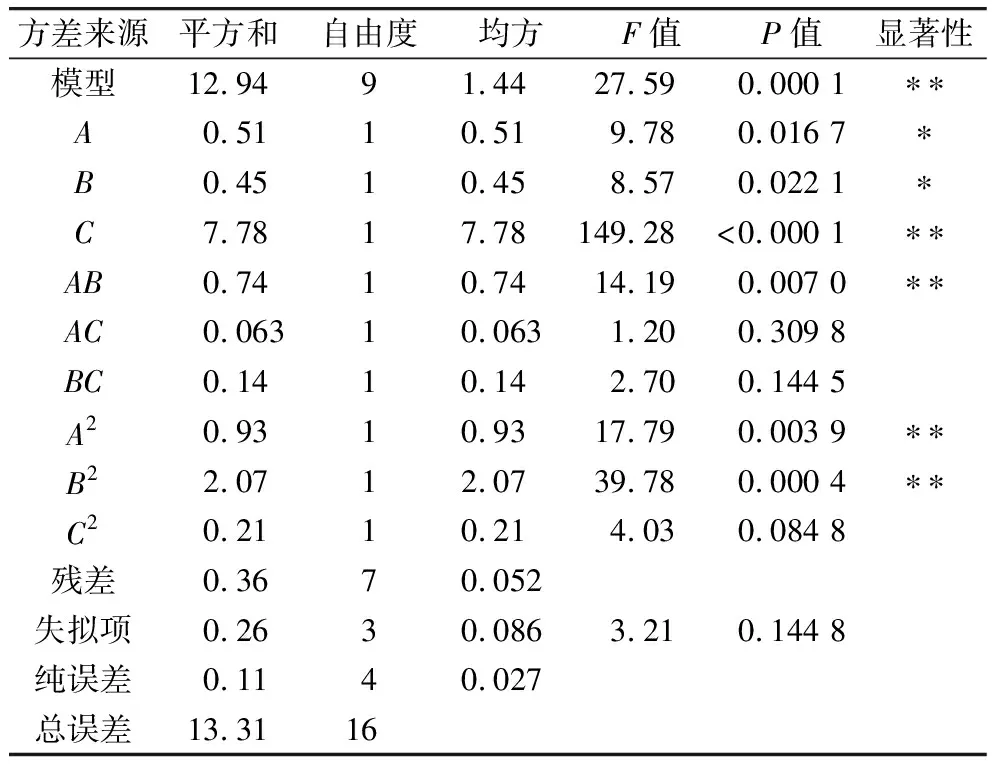
表6 復合凝膠硬度回歸模型的方差分析表
結合實驗,將凝膠硬度作為指標,進行響應面優化實驗,結果見表5、表6。
2.2.2.2 各因素之間的交互作用分析
通過復合凝膠硬度響應面分析得到:復合凝膠硬度隨著各因素的改變呈現先上升后下降,表明復合凝膠的硬度值存在最大值。此外,AB交互的響應面曲圖向下趨勢較大且等高線較接近于橢圓形,表明二者交互作用極顯著;AC和BC間的二維響應面等高線向下曲折較小,表明二者交互作用不顯著。因此,AB間的交互作用對CP凝膠性能影響更大,二者的交互作用使復合凝膠性能網絡結構更加穩定,凝膠性能增強。
2.2.3 驗證實驗
響應面模型優化復合物凝膠最優工藝,在pH為2.51、蔗糖質量分數為23.76%、SPI-CP復合物質量濃度為0.05 g/mL時硬度為6.58 N。為檢驗實驗數據的準確性進行實際實驗驗證,實際值為6.54 N與預測值接近,此時凝膠的彈性、膠黏性、咀嚼性分別是3.95 mm、5.05 N、17.44 mJ,表明在該實驗模型下得到的最佳工藝條件具有較高的可行性,對復合物凝膠質構特性工藝優化具有一定應用價值。
3 結論
通過添加CP來探究不同比例SPI-CP復合物穩定性及復合凝膠的制備質構性質,隨著SPI-CP復合物比例變化,當SPI-CP復合物比例1∶1時,濁度較低,粒徑最小,電位絕對值最大,復合物體系穩定。通過響應面優化分析發現對復合凝膠硬度的影響的因素順序為復合物質量濃度>pH>蔗糖濃度,并且pH和蔗糖濃度間的交互作用對復合物凝膠性質構特性存在顯著影響。SPI-CP復合凝膠可以作為一種新型的凝膠,在食品應用領域具有廣闊的發展前景。

