生物鐘基因調控機制與晝夜節律在近視發展中的研究進展
晏 鑫,邢 凱,亢澤峰,孫宏睿,曹珂兒,王健全
隨著社會的發展,近視的發病率逐年上升,近視人群逐年增加,已經成為一個重大的公共衛生問題,因此對近視的發病機制和防控措施的研究迫在眉睫。近年來對生物鐘在近視發展中起到的作用逐漸引起學者們的興趣,現本文從生物鐘在近視發展中對眼軸、視網膜、脈絡膜的影響,當代社會與生物鐘紊亂角度做一簡單的綜述,以期為近視發病機制以及防控措施的研究提供新的思路。
?KEYWORDS:biological clock; circadian rhythm; myopia; axial length; choroid
0引言
目前,近視是世界范圍內造成視力障礙的主要原因,特別是亞太和北美等地區尤其嚴重[1]。據預測到2050年全世界近視人口將達到47.58億,且高度近視將達到9.38億[2]。近年來近視已成為兒童青少年視力障礙的主要原因,引起了學者們的廣泛關注,但對于其內在機制仍不十分明確。長期以來的觀點認為,近視是一種既有環境因素又有遺傳因素的疾病。隨著人類基因組計劃的逐步完成,人們發現有一類基因可以調控機體的生物節律,這一類基因被稱為生物鐘基因。有研究提出近視的發病機制和臨床表現具有晝夜變化的特點[3],生物鐘基因表達的改變不僅參與近視的病理生理過程,還可能是近視預防和治療的重要靶點。因此,深入探究生物鐘與近視的關系可為近視的防治提供新的思路。
1 生物鐘基因及其調控機制
生物體內存在一種約24h的周期性振蕩,即晝夜節律,而控制這一節律的系統稱為生物鐘[4]。哺乳動物的晝夜節律調節中樞位于下丘腦視交叉上核(suprachiasmatic nucleus,SCN),作為腦時鐘充當主起搏器,同步或夾帶分布在全身的外周時鐘。SCN接收來自視網膜的光并同步神經元的核心時鐘振蕩,然后將其轉化為振蕩性突觸輸出到下丘腦和其他地方的多個核團。SCN的消融導致這些模式的神經元活動喪失,以及多數組織中時鐘基因振蕩連貫的晝夜節律的喪失,最終導致行為和生理性全身節律失常。SCN時鐘還受光亮度周期變化的影響,并在這種環境中調節外周晝夜節律的變化[5]。
生物鐘由基于轉錄翻譯的自動調節反饋回路組成[6]。研究發現幾乎所有的細胞都表達生物鐘基因[7]。哺乳動物晝夜節律時鐘的分子機制是由細胞自主轉錄自動調節反饋環產生的。“核心”時鐘基因包括編碼激活子的Clock和BMAL1,以及編碼抑制子的PER1、PER2、CRY1和CRY2[8]。生物鐘基因在視網膜中同樣廣泛表達,但由于視網膜是一種高度異質的組織,在不同的細胞類型及不同的時間節點中表達不同。有研究發現在大鼠視網膜中,PER1 mRNA在光感受器中的表達水平較低,而在視網膜內部神經元中較高[9]。在BMAL1和Clock mRNA中同樣觀察到類似的模式[10]。Song等[11]發現Clock和BMAL1的表達在亮光環境出現峰值,PER1和PER3在黑暗時達到峰值,并且發現Clock/BMAL1與PERS的同相振蕩和節律性表達不會發生在其他組織中,包括SCN,據此提出光感受器細胞的生物鐘在組織結構和分子組分的節律性都是獨一無二的。
哺乳動物的生物鐘系統公認模型有兩個轉錄-翻譯反饋環,涉及多個“時鐘基因”及其蛋白質產物,最終調節其他被稱為時鐘控制基因的基因轉錄。這些反饋回路由正負分量組成。正性成分包括堿性螺旋-環-螺旋-PAS結構域轉錄因子、時鐘和BMAL1。這些轉錄因子異源二聚并與E-box啟動子元件結合,從而增強編碼負性成分PER1、PER2和CRY1、CRY2基因的轉錄。PER和CRY蛋白質反饋通過阻斷Clock/BMAL1介導的反式激活抑制PER和CRY基因的轉錄。第二個反饋回路通過Clock/BMAL1對Rev-Erbα、Rev-Erbβ和Rora基因的反式激活。這些基因的蛋白產物與BMAL1啟動子中的元件競爭結合,驅動BMAL1轉錄的節律。生物鐘通過BMAL1/Clock復合物直接控制節律性轉錄,該復合物與DNA E-box結合,DNA E-box存在于這些基因的啟動子區域,最終調節生理功能[12]。生物鐘分子機制示意圖見圖1[13]。
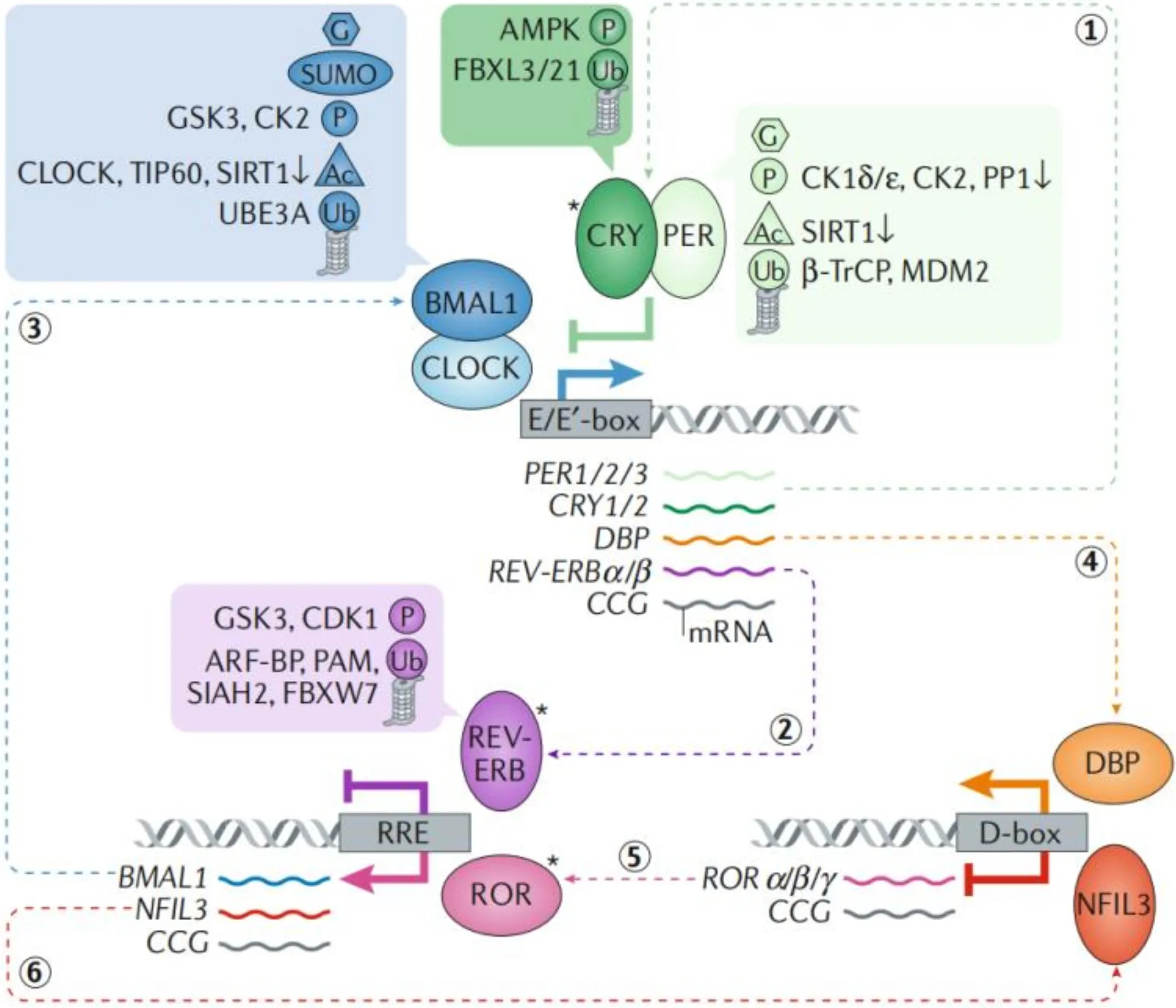
圖1 生物鐘分子機制。
2 視覺環境、多巴胺、生物鐘基因及晝夜節律對眼球發育的影響
2.1視覺環境對眼球發育的影響Weiss等[14]發現剝奪眼睛的視覺形態,可導致眼軸過度延長進一步發生近視,并且改變了眼軸生長的節律,即眼軸并非在夜間變短,而是在夜間和白天同樣生長。然而,盡管形覺剝奪的眼睛的確在夜間生長得更快,但眼軸生長的節律并沒有被廢除,每隔6h進行一次測量,結果顯示節律完整,但具有數小時的移位[15]。眼球生長速度與節律的改變之間存在聯系的更有力證據是,通過使用凸透鏡進行近視離焦減緩生長速度,可導致眼軸生長節律的波動相延遲和脈絡膜節律提前,從而使兩個節律同步,而在配戴凹透鏡的眼睛中,可以觀察到眼軸和脈絡膜節律與形覺剝奪眼的節律相似[16]。來自眼睛以不同速度生長與形覺剝奪或散焦的數據顯示,生長速度與眼軸和脈絡膜節律之間的波動相位差之間存在顯著正相關[17]。
2.2多巴胺對眼球發育的影響多巴胺是一種重要的視網膜神經調節劑,調節晝夜節律、視覺功能的不同方面,以在不同光照條件下獲得最佳視網膜敏感性。多巴胺的合成和釋放發生在多巴胺能無長突細胞的一個亞群中,并受到視網膜ON-OFF通路視覺傳輸的刺激[18]。
在雛雞和哺乳動物模型中,多巴胺是少數與形覺剝奪近視相關的生化信號之一[19]。形覺剝奪導致多巴胺水平下降,可能是由于多巴胺生物合成減少,并非多巴胺能無長突細胞數量減少引起[20]。此外,多巴胺和多巴胺受體激動劑以劑量依賴性減少形覺剝奪實驗性動物模型眼軸延長[21]。通過藥物或基因敲除干預降低小鼠視網膜多巴胺會在正常環境條件下發生近視[22]。然而,多巴胺信號在屈光發育和近視中的作用是復雜的,目前尚無明確研究指出多巴胺與近視發展的具體內在機制,并且不同多巴胺受體所產生的效應也不盡相同,但多巴胺在近視發展中的重要作用已被公認,可將其作為重要靶點進一步深入研究。
2.3生物鐘基因及晝夜節律對眼球發育的影響
2.3.1眼軸的變化近視發生的機制尚不十分明確,但眼軸的進行性延長促進近視的發展是較為公認的機制之一[23]。Weiss等[14]最先報道了24h眼軸長度的變化,發現雛雞的眼軸白天長,夜間逐漸縮短。這一發現得到了后續研究的證實和擴展[24],有研究通過更頻繁的測量表明,眼軸最長的時間段發生在下午,午夜眼軸最短[16]。隨后在靈長類動物也發現了這種生物節律,在幼年絨猴中,眼軸的這種日間周期變化與雛雞相似,眼軸長度在白天達到峰值,而在夜間縮短,并且發現夜間眼軸縮短是由于脈絡膜增厚所致[25]。Stone等[26]研究發現,將小鼠BMAL1基因特異性敲除后可以誘導小鼠發生近視,并延長眼軸長度。Sánchez-Bretao等[27]研究提出E-box介導的Clock/BMAL1復合物可以通過調控1型腺苷環化酶的轉錄,從而調控眼部的晝夜節律,同時1型腺苷環化酶啟動子的活性由晝夜節律通過調控Clock/BMAL1復合物進行調節,從而影響眼軸的24h動態變化。目前的研究僅從實驗動物模型中觀察到眼軸隨著晝夜節律進行變化,那是否人類同樣存在相應的眼軸變化,變化量是多少,這種內在的生物鐘基因表達變化及相應的作用機制也尚不明確,是否可以通過生物節律的外在干預延緩近視發展,以及具體干預的時間節點也都還需要今后進一步深入研究。
2.3.2視網膜及脈絡膜的變化目前對于近視發病機制的研究并不明確,但眼軸延長會給視網膜和脈絡膜施加機械性壓力,導致視網膜和脈絡膜厚度發生變化。Riddell等[28]采用高頻超聲檢查和非接觸式激光干涉測量發現雛雞的脈絡膜厚度也出現晝夜節律,夜間增厚,白天變薄,與眼軸的變化節律同步,即在白天眼軸最長的時間脈絡膜厚度也是最薄,推測夜晚眼軸縮短有一部分原因是由于夜間脈絡膜增厚所致。目前對于人眼脈絡膜厚度的研究很少,Ulaganathan等[29]對現有的非接觸式激光干涉測量數據進行分析同樣發現脈絡膜在夜間最厚,白天最薄,平均晝夜波動幅度約30μm。Blasiak等[30]對雛雞視網膜光感受器細胞進行分析發現,暴露于明暗循環的細胞時鐘基因呈節律性表達。Bmal1和生物節律分子Npas2在白天達到峰值且在夜間最低,但24h暴露于暗環境中的細胞則節律紊亂。Cry1和Per2 mRNA表達水平在明暗循環細胞中同樣在夜間最低,而處于24h暗環境的細胞Per2表達波動幅度降低,褪黑素的表達則在明環境時降低,暗環境上升。Yang等[31]將非洲爪蟾Clock基因敲除后發現褪黑素的分泌節律被破壞,但總體分泌水平沒有較大改變,據此提出褪黑素的分泌節律和分泌水平可以分離,并通過不同的分子機制控制。根據上述零星的研究結果可以得出不同光照條件可能通過影響晝夜節律從而對近視的發生發展產生影響,對于尚處于發育階段的青少年兒童,還需要進一步加強研究現代光線暴露條件和生物鐘節律的相互作用,以評估改變節律是否可以作為控制青少年兒童近視發展的治療靶點。眼軸長度和脈絡膜厚度晝夜變化曲線見圖2[16]。
3 當代生物鐘紊亂的社會因素
對多數生物來說,光環境十分重要,24h的晝夜節律變化幾乎促成了所有生物的生物鐘節律。但隨著現代社會的發展,人造光源已經極大地改變了原有的生態環境。與自然光源相比,人造光源在亮度、時間、光譜等方面具有顯著差異。因此,人類的生物鐘節律會不可避免地受到影響。白天陽光照射不足、夜間光污染、睡眠剝奪等原因均會導致生物鐘紊亂[32]。而目前對于近視影響最大的人造光源就是電子屏幕,而且已經證實夜間觀看電子屏幕會影響青少年兒童的睡眠,從而導致生物鐘紊亂[33]。但夜間觀看電子屏幕加速近視發展是否可以從生物鐘角度來解釋還需進一步研究。眼瞼作為光線過濾器,不能完全隔絕所有光線,因此在夜間處于光污染的環境中,光線仍然可以到達視網膜光感受器,從而引起生物鐘紊亂[34]。所以目前近視防控工作應加強改善光照環境,增加白天室外活動,減少夜間光污染,順應生物鐘節律,促進眼的健康發展。
4 不足與展望
生物鐘可以調控機體隨外界晝夜節律的變化而發生內在相應變化,其不僅參與近視的病理生理過程,還可能是近視預防和治療的重要靶點,但目前的研究還存在以下不足:(1)研究對象多為動物模型,并且多為嚙齒類動物,雖然可以較好地研究病理生理過程,但其活動/休息節律與人類不同,并且相關生物鐘基因的表達是否一致仍然存疑;(2)研究數量很少,且研究大多不夠深入,難以明確生物鐘基因影響近視的真實內在機制。在今后的研究中還需進一步深入探討不同個體之間的內在授時因子和外在生活環境的差異,因其均可導致不同的疾病發展結局,以明確不同個體之間生物節律不同所導致的近視結果差異。另外,我國中醫學早有記載“法于陰陽,和于術數,飲食有節,起居有常”,并且后世的中醫學理論對于生物鐘具有詳細深入的論述,因此將中醫學“治未病”理論與現代醫學生物鐘相結合,可能會在近視防控工作方面取得更大的成就。

