熱浸鍍鋁硅鎂涂層組織與腐蝕性能研究
張敏,王洪金,孫順平,李思林,張卓,李小平,于赟
(江蘇理工學院 材料工程學院,江蘇 常州 213001)
熱浸鍍技術是將被鍍件浸入熔融金屬液體中,以在鍍件表面形成金屬鍍層的過程,其表面形成的金屬鍍層主要有鋅、錫、鋁和鉛等金屬。熱鍍技術廣泛用于鋼鐵材料的防腐,具有加工成本低,保護周期長,操作設備簡單,生產效率高,鍍層耐腐蝕性強等諸多優(yōu)點,且具有一定的裝飾效果[1-3]。熱浸鍍鋁技術將鋼件置于熔融鋁液中,鋁與基體鐵之間互相滲透、擴散并反應形成冶金結合,得到雙層結構涂層,外層是鍍鋁層,內層是鋁與基體鐵之間形成的鐵-鋁化合物層[4-6]。熱浸鍍鋁作為一種簡單有效的保護涂層技術,受到國內外同行的廣泛關注,通過擴散形成的合金層還具有耐高溫氧化性,耐磨性和高硬度的優(yōu)點,已廣泛應用于石油、交通、建筑、化工等各個領域,由于鋁的熔點較高,熱浸鍍溫度通常在700~750 ℃之間,所得鋁鍍層不但具有光潔的表面,還具有良好的耐蝕性,在腐蝕環(huán)境下,鋁自身的鈍化特性使得在鍍層表面形成氧化膜,能夠抵抗大部分的侵蝕作用,可以隔絕外部環(huán)境而保護基體,提高了鋼件的耐蝕性能。但由于涂層中鐵-鋁化合物層的高脆性特點,在加工過程中經常會發(fā)生涂層開裂剝落等現(xiàn)象,將導致涂層界面結合強度降低;同時,純鋁鍍層作為保護鋼材的防護涂層,其耐腐蝕的防護性能有待進一步提高。基于以上局限性,熱浸鍍鋁合金化一直是主要的研究方向,通過合金化的方法[7-10],在鍍液中加入一定量的鋅、鎂、硅和錫等元素來控制合金層的厚度,改善鍍層的腐蝕性能,已成為鋼材防腐的有效途徑之一[11-12]。硅元素是在熱浸鍍過程最常使用的合金元素之一,在熱浸鍍鋁時,硅元素對鍍層的生長有強烈的抑制作用,降低鍍層的厚度[13],而Mg元素能細化鍍層組織,提高鍍層的耐蝕性[14]。熱浸鍍鋁鍍層可以改善鋼材的性能,還具有良好的抗高溫氧化、耐磨及對光和熱的反射性能。為此,本文利用熱浸鍍鋁技術在Fe基體表面制備鋁合金涂層,探討熱浸鍍時間對鋁硅鎂涂層中鐵鋁反應層生長的影響,研究涂層的電化學腐蝕性能。
1 實驗材料與方法
采用高純鋁(99.99%)、高純鎂(99.95%)和鋁硅合金配制不同比例的鋁硅鎂合金鍍液,合金鍍液成分配比:合金粉末質量配比:Al-1Mg2Si(99%Al、0.63%Mg和0.37%Si) Al-2Mg2Si(98%Al、1.27%Mg和0.73%Si)、Al-3Mg2Si(97%Al、1.9%Mg和1.1%Si)、Al-6Mg2Si(94%Al、3.8%Mg和2.2%Si)。設置熱浸鍍實驗溫度為700 ℃,合金熔化后除氣除渣后靜置保溫1 h,實驗基材采用高純鐵片(99.99%),利用線切割機床切割試樣,將切割成25 mm×50 mm×1 mm的鐵片進行熱浸鍍鋁的助鍍處理,然后將鐵片浸入合金鍍液中,改變熱浸鍍保溫時間(15,30,45,60,90,120,300,600,900和1 800 s),制備熱浸鍍鋁硅鎂涂層。采用金相顯微鏡和Sigma 500掃描電子顯微鏡(配套EDS)觀察涂層的顯微組織形貌,采用Reference3000電化學工作站測試涂層的電化學性能,動電位極化曲線的測量采用三電極系統(tǒng),參比電極為飽和甘汞電極(SCE),輔助電極為鉑電極,試樣的工作面積為1 cm2;電化學阻抗譜(EIS)的測量在開路電位下進行,頻率范圍為105Hz到10-2Hz。
2 實驗結果與分析
2.1 熱浸鍍鋁硅鎂涂層制備工藝探討
熱浸鍍120 s時,試樣的橫截面組織如圖1所示。Al-1Mg2Si涂層的橫截面組織有著明顯的變化,由表至里分為3層,最外層是鋁鎂硅的富鋁合金層,中間層為Fe-Al反應化合物層(由Fe2Al5相和FeAl3相構成)[13,15-16],內層為基體純鐵。外層的富鋁合金鍍層厚度在30~50 μm,要薄于Fe-Al反應層,鐵鋁反應層以“舌狀”形態(tài)向基體方向蔓延,與基體鐵呈現(xiàn)冶金結合,其厚度達到50~100 μm,如圖1(a)所示。隨著Mg和Si元素的增加,Fe-Al反應層的厚度不斷減薄,在Al-2Mg2Si和Al-3Mg2Si涂層的橫截面組織中,鐵鋁反應層仍然以Fe2Al5相的“舌狀”形態(tài)生長為主,但Fe-Al反應層厚度不斷降低。當Mg和Si元素含量達到6%時,Fe-Al反應層的生長受到Si元素強烈的抑制作用,具有最薄的反應層厚度,厚度僅為10 μm左右。圖2為熱浸鍍Al-6Mg2Si的橫截面EDS圖,由圖可知,隨著Mg和Si元素添加量的增大,Fe-Al反應層的長舌狀組織厚度逐漸減薄,由表1和圖2(f)可知,Fe-Al反應層中未發(fā)現(xiàn)Mg元素,Mg元素主要分布在熱浸鍍鋁的富鋁鍍層中,與Si元素在鍍層中具有較強的親和力,主要形成Mg2Si相,而Si元素在富鋁層和界面反應層中均有分布,富鋁鍍層中分布一些不規(guī)則的鐵鋁化合物相,這是由于基體的Fe元素不斷向鍍層中擴散,在鍍層中形成鐵鋁化合物,通過EDS分析可知,主要為FeAl3相。在Fe/Al界面反應層中,Si元素對Fe/Al反應起到了抑制作用,促使Fe-Al反應層呈現(xiàn)平坦特征。
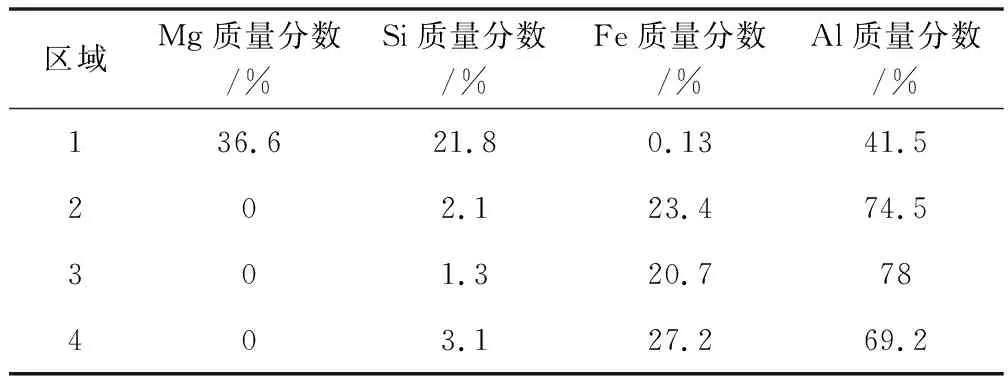
表1 鍍層成分分布

(a) Al-1Mg2Si; (b) Al-2Mg2Si ;(c) Al-3Mg2Si ;(d) Al-6Mg2Si。圖1 熱浸鍍試樣的橫截面組織

(a)顯微組織;(b)元素分布;(c) Al;(d) Fe;(e) Mg;(f) Si。圖2 熱浸鍍Al-6Mg2Si的橫截面顯微組織與元素分布
圖3為不同浸鍍時間下Fe-Al反應層厚度變化曲線,隨著熱浸鍍時間的延長,Fe-Al反應層厚度迅速增加,隨后平緩增長,呈現(xiàn)拋物線式,當熱浸鍍1 800 s時,4種涂層中的Fe-Al反應層厚度均具有最大厚度值,其中Al-1Mg2Si涂層的反應層厚度最厚達300 μm,且由于鐵鋁化合物的高脆性,反應層出現(xiàn)大量裂紋。當Mg和Si元素含量達到3%時,涂層的反應層厚度明顯降低,其中Al-6Mg2Si涂層的反應層厚度最薄,隨著浸鍍時間的延長,Fe-Al反應層的厚度緩慢增加,具有最低的增長速率,浸鍍時間為1 800 s時,反應厚度低于50 μm,隨著Mg和Si元素的增加,鐵鋁反應層的厚度不斷降低,結合EDS可知,Si元素有效抑制了Fe/Al之間的界面反應,降低可熱浸鍍鋁涂層中鐵鋁反應層的厚度,可有效提高鍍層的可加工性能。
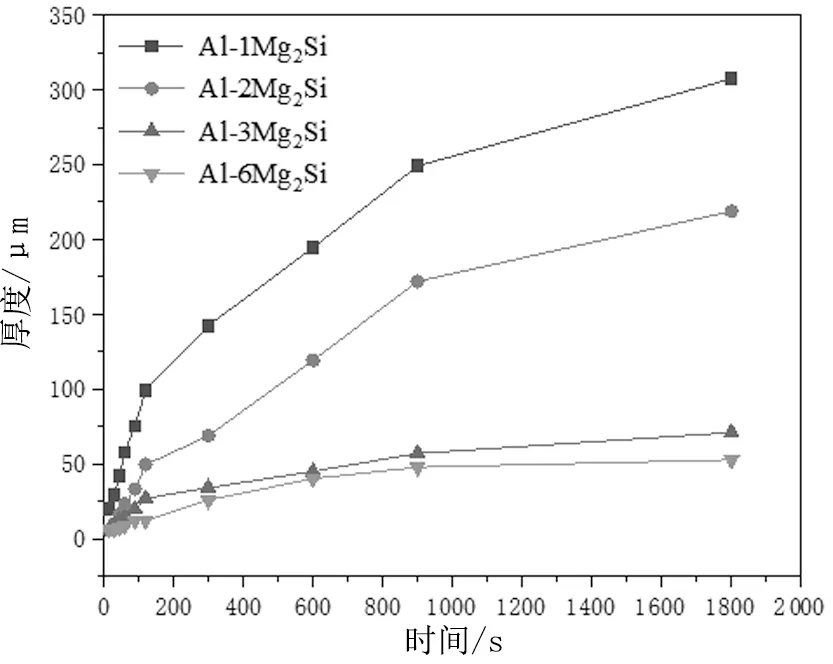
圖3 不同浸鍍時間下Fe-Al反應層厚度變化曲線
2.2 鋁硅鎂涂層電化學腐蝕性能
圖4為熱浸鍍鋁涂層在3.5% NaCl溶液中的動電位極化曲線,由圖可知,隨著Mg和Si元素含量的增加,熱浸鍍鋁鎂硅涂層的自腐蝕電位不斷降低,Al-1Mg2Si涂層的自腐蝕電位為-0.83 V,而Al-6Mg2Si涂層的自腐蝕電位最低達到-1.04 V,降了0.21 V。由動電位極化曲線分析可知,涂層均產生了一定的鈍化現(xiàn)象,腐蝕過程中,鍍層產生了致密的氧化膜,阻礙了離子的擴散,導致腐蝕電流下降。Al-3Mg2Si涂層的自腐蝕電流略高于Al-2Mg2Si涂層的自腐蝕電流,當Mg和Si元素含量低于3%時,隨著Mg和Si元素含量的增加,熱浸鍍鋁鎂硅涂層的自腐蝕電位不斷降低而自腐蝕電流不斷提高,表明Mg和Si元素既可以降低涂層的自腐蝕電位,又可以增大涂層的自腐蝕電流,即增大涂層腐蝕的傾向性,但又增加了涂層的腐蝕速度。由Al-6Mg2Si涂層的Tafel曲線可知,Mg和Si元素含量達到6%時,涂層的自腐蝕電位最低,但相對于其他涂層,Al-6Mg2Si涂層表現(xiàn)出較低的自腐蝕電流密度。可見,具有較負自腐蝕電位和較低自腐蝕電流密度的Al-6Mg2Si涂層,作為Fe基體的保護涂層時,更容易發(fā)生腐蝕,且具有較低的腐蝕速率,對Fe基體具有較好的犧牲保護作用。
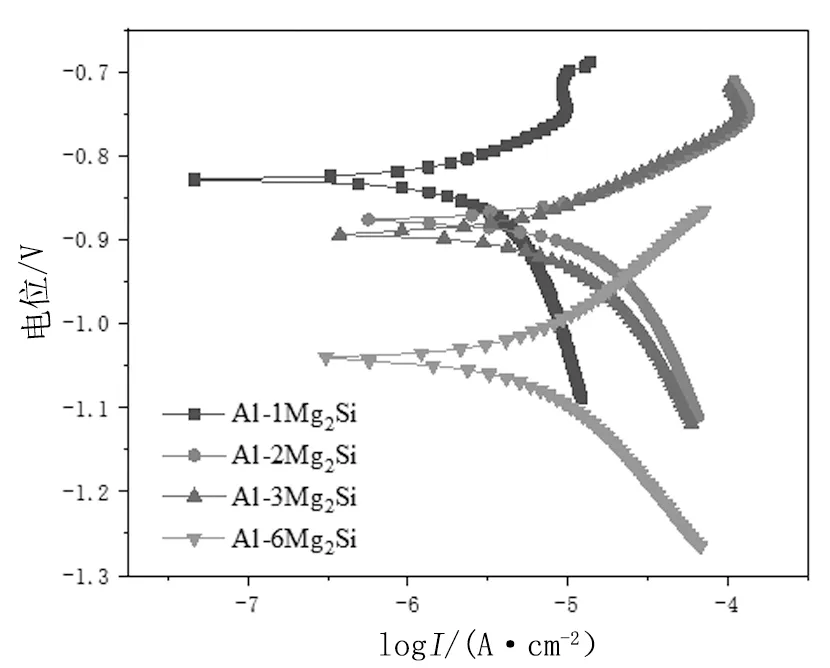
圖4 層在3.5% NaCl溶液中的動電位極化曲線
圖5為熱浸鍍鋁硅鎂涂層在3.5% NaCl溶液中的Nyquist和Bode圖。圖5(a)為涂層在NaCl溶液中的Nyquist曲線,由圖可知,4種成分的涂層均存在鈍化膜,Al-1Mg2Si涂層的容抗弧半徑最大,通過比較曲線圖可知,隨著Mg和Si元素含量的增加,鋁硅鎂涂層的容抗弧逐漸變小,說明腐蝕的阻抗值越小,耐腐蝕性能越差。而Al-6Mg2Si涂層的容抗弧半徑最小,且在低頻區(qū)出現(xiàn)一個感抗弧,這是由涂層表面腐蝕產物吸附造成的,導致阻抗下降。鍍層中Mg和Si元素的增加,降低了鋁硅鎂涂層的阻抗值,高頻區(qū)和低頻區(qū)均為容抗特征。圖5(b)和(c)為涂層在3.5%NaCl溶液中的Bode曲線,由圖可知,4種成分的涂層均產生了鈍化膜,在腐蝕初始階段,產生電荷轉移的電阻都較為接近,但隨著頻率的降低,隨后的腐蝕過程中,鈍化膜的阻抗值出現(xiàn)了差異性,以Al-6Mg2Si涂層的膜電阻最小,鍍層中Mg2Si相促進了涂層阻抗值的降低。

圖5 涂層在3.5% NaCl溶液中的(a)Nyquist和(b)(c)Bode圖
3 結論
(1) 熱浸鍍鋁硅鎂涂層由富鋁層和鐵鋁反應化合物層構成,當Mg和Si元素的含量較低時,鐵鋁反應層向鐵基體生長,呈現(xiàn)舌狀組織。
(2) 熱浸鍍鋁硅鎂涂層中鐵鋁反應層隨著熱浸鍍時間的延長而增厚,呈現(xiàn)拋物線式增長,隨著Mg和Si元素的增加,鐵鋁反應層增厚速率降低,當Mg和Si元素的含量達到3%時,鐵鋁反應受到明顯的抑制作用,反應層增厚的速度較慢。
(3) 隨著Mg和Si元素含量的增加,鋁硅鎂涂層在3.5% NaCl溶液中的自腐蝕電位呈現(xiàn)下降趨勢,元素對涂層的活化作用越強,Al-6Mg2Si涂層具有最負的自腐蝕電位和較小的自腐蝕電流。

