氯酸鉀綜合處置技術
賀平,伍劍兵,寧茂書,王成俊,周逍,凡成萬
(中節能(攀枝花)清潔技術發展有限公司,四川 攀枝花 617000 )
氯酸鉀化學式為KClO3,相對密度2.32,熔點356 ℃。為無色片狀結晶或白色顆粒粉末,味咸而涼,強氧化劑。LD50(大鼠,經口):1 870 mg/kg。常溫下穩定,在400 ℃以上則分解并放出氧氣,與還原劑、有機物、易燃物如硫、磷或金屬粉末等混合可形成爆炸性混合物,急劇加熱時可發生爆炸。因此氯酸鉀是一種敏感度很高的炸響劑,如混有一定雜質,有時候甚至會在日光照射下自爆,與濃硫酸反應生成極易爆炸的氯酸與二氧化氯。
化學領域有許多危險化學品具有難溶、易爆和劇毒的特性,如難溶易爆的氯酸鹽,還有些危險化學品屬于有毒重金屬,如鋇鹽等,這些危險化學品嚴重威脅著環境與人體健康。并且,這些危險化學品的無害化處理還非常困難,如,對于難溶解的化學品常常采取加熱后溶解的方法進行處理,但由于氯酸鹽是易爆類化學品,加熱溶解的方法容易導致爆炸事故的發生,存在較大的安全隱患。目前在生產中對難溶性氯酸鹽采用分開溶解的方法進行處理,將氯酸鹽化學品完全溶解后,再將溶液混合處置,處置效率雖然較高,但后期會產生大量的高鹽廢水,為后期的處置帶來較大的壓力。同樣,單獨處理有毒重金屬鋇鹽和單獨處理劇毒的砒霜或含砷鹽類等危險化學品,也會產生大量的可溶性鹽廢物,造成二次污染,增加二次處置的成本,并且還大大提高了處置周期和人工投入。因此,當前亟需一種處置效率高、處理成本低且處理效果良好的危險化學品處理方法。
1 處置原理
在酸性條件下,將氯酸鹽、七水硫酸亞鐵、濃硫酸按1∶(14~15)∶0.2的質量比混合反應得到反應后溶液;將反應后溶液加到鋇鹽中進行反應,具體處置步驟如下:
第一步:氯酸鉀氧化還原:在酸性條件下,將氯酸鹽、七水硫酸亞鐵、濃硫酸按1∶(14~15)∶0.2的質量比混合反應。首先在反應容器加入足量的硫酸亞鐵,溶解后加入濃硫酸,攪拌均勻后,將氯酸鉀置于帶孔的容器中,并沉于硫酸亞鐵的溶液中,使氯酸鉀固體與硫酸鐵溶液接觸,氯酸鉀不會沉淀在容器底部,不僅避免了氯酸鉀反應不充分的情況,而且還能通過反應促進氯酸鉀的溶解。
6FeSO4+3H2SO4+KClO3=KCl+3H2O+3Fe2(SO4)3
(1)
通過上述反應,易爆的氯酸鉀經處置后生成無毒無害的氯化鉀。并且,使用的原料硫酸亞鐵廉價易得,能夠節約成本,同時反應的產物也能夠無毒無害化。
第二步:在原反應容器中,向反應后的溶液中加入硝酸鋇,進一步發生復分解反應。利用第一步反應后溶液中產生的硫酸根,與硝酸鋇反應生成穩定的硫酸鋇和非易爆的硝酸鐵。反應后過濾,得到非易爆的硝酸鐵溶液和硫酸鋇沉淀。硫酸鋇經洗滌干燥后可以用于醫療上的鋇餐。具體反應如下:
3Ba(NO3)2+Fe2(SO4)3=3BaSO4↓+2Fe(NO3)3
(2)
這樣,通過進一步的反應可以降低第一步反應中的可溶鹽含量,不需要苛刻的條件處置有毒的重金屬鹽硝酸鹽。為了確保重金屬離子鋇離子能夠完全反應,反應物質的質量比控制為m(硫酸亞鐵)∶m(硝酸鋇)≤1.8∶1,同理,按照這種方法不僅可以處理硝酸鋇,也可以處置其他鋇鹽,如氯化鋇、碳酸鋇等。
第三步:若處理劇毒的砒霜,首先在酸性條件下,將高錳酸鉀與砒霜按一定的質量比混合,在不斷攪拌下的情況下完全反應,使砒霜被高錳酸鉀氧化為五價砷,同時高錳酸鉀被還原為二氧化錳或錳離子。具體反應如下:
5As2O3+4MnO4-+9H2O=10AsO43-+4Mn2++18H+
(3)
然后,將該反應后的溶液加到第二步得到的非易爆的硝酸鐵溶液中,使砷酸根與三價鐵反應生成砷酸鐵。為了使砒霜充分反應,砒霜與硫酸亞鐵按一定的質量比,具體反應如下:
Fe3++AsO43-→FeAsO4↓
(4)
第一步和第二步反應體系中的三價鐵可以沉淀砒霜在酸性條件下被氧化產生的砷酸根,生成比較穩定的砷酸鐵沉淀,其中,砷和鐵的質量比不低于15∶1。對反應后的混合物進行過濾,得到砷酸鐵沉淀和濾液。
第四步:將得到的濾液通過消石灰共沉淀,使用消石灰調節濾液的pH值至8.0~9.0之間即可,最后再通過水泥基固化處置不溶物砷酸鐵、砷酸鈣,經7 d養護后,取樣檢測。
2 處置效果檢測
2.1 氯酸鉀處置效果檢測方法選擇
2.1.1 定性檢測方法(鹽酸苯胺法)
當鹽酸苯胺加到含有氯酸鹽的水中,有很美麗的深藍色生成(根據濃度不同有色差),這個反應非常靈敏。有助于現場快速檢測氯酸根。
2.1.2 定量檢測方法
通過檢測溶液中硫酸亞鐵的量的情況,來推斷氯酸鉀是否被反應完全,硫酸亞鐵的檢測方法主要有重鉻酸鉀法、高錳酸鉀法。
2.2 試劑準備
1)稱取27.8 g AR硫酸亞鐵溶于1 000 mL蒸餾水中,定容,配制0.1 mol/L的硫酸亞鐵溶液。
2)鄰啡羅啉指示劑:稱取硫酸亞鐵(分析純)0.695 g和鄰啡羅啉(分析純)1.485 g溶于100 mL水中,搖勻備用。
3)重鉻酸鉀標準溶液:c[1/6(K2Cr2O7)]=0.1 mol/L,稱取經過130 ℃烘3~4 h的重鉻酸鉀(分析純)4.903 1 g,溶解于400 mL水中,必要時可加熱溶解,冷卻后,稀釋定容至1 L,搖勻備用。
4)c[1/6(KMnO4)]=0.1 mol/L:稱取3.22 g高錳酸鉀,溶解于400 mL水中,稀釋定容至1 L,搖勻備用。
2.3 重鉻酸鉀法
取重鉻酸鉀溶液20.00 mL于150 mL三角瓶中,加硫酸3~5 mL和2~3滴鄰菲啰啉指示劑,用硫酸亞鐵溶液滴定,溶液磚紅色為終點。加入指示劑后,硫酸亞鐵溶液顏色較深,呈鮮紅色,隨著滴定的進行,溶液逐漸變為磚紅色,灰綠色,藍色,當溶液呈灰綠色時,終點讀數與硫酸亞鐵滴定重鉻酸鉀溶液的消耗的體積一致。終點顏色變換緩慢,需要靜止30 s后,才能觀察到,對結果造成較大的誤差。兩次平行試驗結果見表1。

表1 重鉻酸鉀法平行試驗結果
2.4 高錳酸鉀法
取上述硫酸亞鐵溶液1 20 mL,用0.1 mol/L的高錳酸鉀溶液滴定至溶液呈粉紅色。平行試驗結果見表2。
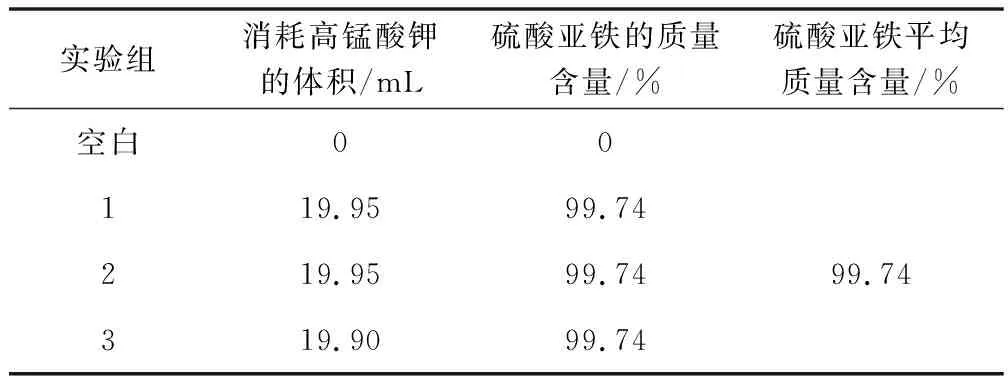
表2 高錳酸鉀法平行試驗結果
總結:1)兩種方法在測定硫酸亞鐵質量含量時,結果相差0.17%,高錳酸鉀法測定更為簡單,終點顏色由無色變為粉紅色,變化明顯,更容易判斷,誤差更小。
2)重鉻酸鉀法在加入指示劑后,硫酸亞鐵溶液顏色較深,呈鮮紅色,隨著滴定的進行,溶液逐漸變為磚紅色,灰綠色,藍色,當溶液呈灰綠色時,終點讀數與硫酸亞鐵滴定重鉻酸鉀溶液的消耗的體積一致,但終點顏色變換緩慢,需要靜止30 s后,才能觀察到,對結果造成較大的誤差。
3 氯酸鉀質量含量的測定-高錳酸鉀法
1)氯酸鉀試樣溶液:稱取AR氯酸鉀1.169 2 g,溶解后定容至250 mL備用。
2)稱量1.280 6 g氯酸鉀待處置樣品溶于水中,定容至250 mL搖勻備用。
分別取上述兩種氯酸鉀溶液各5 mL,加入硫酸亞鐵溶液25 mL,加入10 mL濃硫酸,5 mL磷酸,冷卻10 min,用0.1 mol/L的高錳酸鉀溶液滴定至溶液呈粉紅色。平行檢測結果見表3。

表3 高錳酸鉀法平行試驗結果
通過結果對比,高錳酸鉀法測定氯酸鉀濃度準確,且終點易于判斷,氯酸鉀處置后的棕紅色也能被磷酸/硫酸屏蔽,不影響終點判斷。
4 不同條件對檢測結果的影響論證
稱量1.280 6 g氯酸鉀溶于水中,定容至250 mL搖勻備用,從滴定時間、氯酸鉀與硫酸亞鐵的體積比、溫度等條件進行對比。
(1)取10 mL氯酸鉀溶液于三角瓶中,一次加入25 mL硫酸亞鐵溶液和10 mL硫磷混酸,用高錳酸鉀滴定。結果見表4。

表4 不同反應時間試驗結果
原因分析:反應不完全,從第二個就可以看出,因為第二個結果更高。
方法改進:增加反應時間。
(2)取10 mL氯酸鉀溶液于三角瓶中,一次加入25 mL硫酸亞鐵溶液和10 mL硫磷混酸,反應10 min,用高錳酸鉀滴定,結果見表5。

表5 不同溫度時間試驗結果
原因分析:反應進行的比較完全,但存在反應不徹底,應是反應條件不夠充分,室溫較低。
方法改進:將配好的硫磷混酸改用濃硫酸、濃磷酸,遇水放熱,加速反應的進行。
(3)取10 mL氯酸鉀溶液于三角瓶中,一次加入25 mL硫酸亞鐵溶液和10 mL濃硫酸和5 mL濃磷酸,反應10 min后用高錳酸鉀滴定,結果見表6。
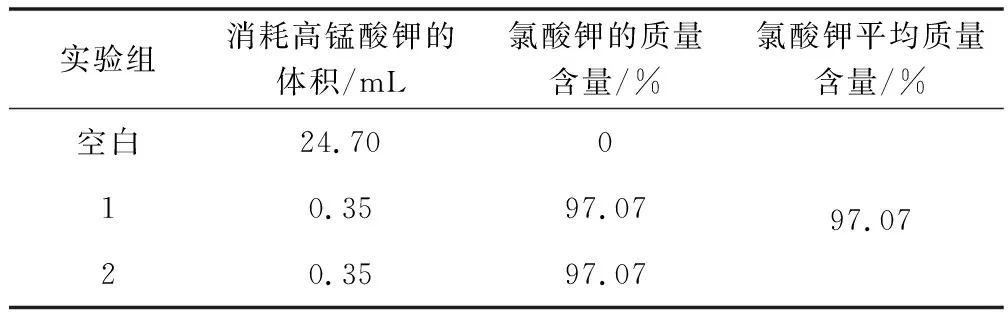
表6 不同體積比時間試驗結果
原因分析:試樣溶液消耗的體積太少,若是硫酸亞鐵量不夠,會造成結果偏低。方法改進:減少氯酸鉀溶液的體積。
(4)取5 mL氯酸鉀溶液于三角瓶中,一次加入25 mL硫酸亞鐵溶液和10 mL濃硫酸和5 mL濃磷酸,反應10 min后用高錳酸鉀滴定,結果同表3。
從以上四個實驗結果可以看出,反應時間、反應條件都直接影響到反應是否充分,最終造成結果的偏差。只加硫酸,溶液呈綠色,會影響終點顏色的判斷,加磷酸后溶液無色,更便于終點的判斷。
5 鋇離子檢測方法
實際處置中,往往通過定性半定量的方式,來確定反應是否完全。本方法通過兩種方法判斷鋇鹽是否反應完全,用氯化鋇溶液加入到反應溶液中,觀察是否有白色沉淀,如有白色沉淀產生則證明溶液中硫酸根未反應完全,同時取底部沉淀溶于水中,取上清液加入硫酸,觀察是否有白色沉淀,如有白色沉淀則表明沉淀中含有鋇離子,如無白色沉淀生產,則表明鋇離子被完全沉淀。
6 砷處置效果論證
6.1 砒霜處置
將得到的濾液通過消石灰共沉淀,使用消石灰調節濾液的pH值至8.0~9.0之間即可,最后再通過水泥基固化處置不溶物砷酸鐵、砷酸鈣,經7 d養護后,取樣檢測。檢測結果如表7所示。

表7 砷化物固化體檢測結果
由表7可以看出,固化體砷指標均滿足GB 18598—2019《危險廢物填埋污染物控制標準》,檢測合格,可以安全填埋處置,可進入柔性填埋場。
6.2 處置含砷廢水
同樣的方法,對于處置高濃度含砷廢水,也能達到較好的效果,按照砷和鐵的質量比的要求,在pH值 6.0~7.0之間,加入含三價鐵的溶液,充分攪拌30 min,控制一定的轉速,攪拌均勻后,加入消石灰調節溶液pH值8.0~9.0,并加入PAC或PAM,絮凝沉淀后取上清液檢測合格后,通過壓濾機處置后,濾液進入污水處置車間,污泥固化處置。對濾液中的砷質量含量進行檢測,檢測結果如表8所示。

表8 高濃度含砷廢水處置效果
通過表8可以看出,經過處理后的廢水中砷質量含量明顯降低,說明本發明提供的危險化學品協同處理的方法取得了明顯的處理效果。在后期的處置中,通過進一步完善砷鐵比、攪拌時間和攪拌速率、沉淀時間、沉淀pH值,砷的去除率能實現穩定去除,達到99.9%以上。
7 結論與討論
7.1 關于氯酸鉀的處置
通過改進處置裝置,達到了反應安全、徹底的目的,優化氧化劑、還原劑的質量比,通過協同處置方式,不僅能有效提高處置效率,降低處置成本,減少了二次處置廢水、廢鹽的量,將可溶性鹽通過協同處置轉化為難溶鹽如硫酸鋇,減少二次處置成本,產物更加穩定、安全,確保了環境安全。對于生產,通過改進氯酸根、鋇離子的檢測方法,大大降低檢測費用和檢測工作量,從檢測方面節約了成本。
對于不具備焚燒處置條件的企業提供了安全有效的處置方式,處置裝置可簡可繁,視處置量而定。
7.2 關于砒霜處置
長期以來,砒霜在常規條件下處置耗時長,僅含砷化合物的處置效率較高,砒霜溶解度小,且對于反應進度、程度無法掌握,通過改變反應條件,在酸性條件下,通過調節高錳酸鉀和砒霜的質量比,控制反應的溫度,能大大提高處置效率,且反應現象直觀可見。
處置中,一是觀察溫度,要控制溫度不能超過60 ℃,避免在反應裝置不滿足控溫的條件下,反應失控;二是要嚴控兩種物質的質量比,進一步達到控制反應速率的目的;三是摸索出了不連續處置的情況下,如何快速提高反應的條件。該處置方法,對于危險廢物處置單位處置氯酸鹽、鋇鹽、砒霜及砷化物、高濃度含砷廢水能提供可靠的參考,尤其自主研發的處置裝置,簡單、實用性強。

