麻黃附子細辛湯治療變應性鼻炎作用機制探究*
陳蘭蘭,陳榮榮,原夢雪,張銘,王安琪,李莉
山西中醫藥大學 山西太原 030024
變應性鼻炎(Allergic rhinitis,AR)是機體接觸過敏原后由IgE介導的鼻黏膜非感染性慢性炎癥,通常以鼻癢、打噴嚏、流清水涕、鼻塞等為主要就診表現,在耳鼻喉科較為常見且多發[1]。在中國,約有1.9億成人和2.2億兒童患有變應性鼻炎,占中國總人口的13.26%和15.79%,而全球患病率也高達10%~40%[2-3]。受環境因素和生活習慣的影響,變應性鼻炎的發病數量也逐年增多,給患者的工作效率、生活質量等產生了很大的負面影響,此外,變應性鼻炎治療不當還可引起哮喘的發作和影響其控制[4],為此變應性鼻炎在全球公共衛生隱患中受到極大關注。
麻黃附子細辛湯出自張仲景的《傷寒論》,可達到溫經解表、宣肺散寒、扶正祛邪的作用,方中麻黃可發汗解表;附子可有溫經通脈、助陽散寒之效;細辛能夠散寒解表、宣通鼻竅[5]。據相關文獻表明[6],麻黃附子細辛湯能夠升高AR大鼠血漿中IFN-γ含量,降低IL-13含量,以達到恢復Th1/Th2免疫失衡狀態的效果,提示了麻黃附子細辛湯可以對變應性鼻炎起到良好的免疫調節作用。
網絡藥理學這一名詞由英國研究者Hopkins AL初次提出,它是基于系統生物信息學,通過綜合運用各類組學、網絡可視化等技術[7],建立“中藥復方成分-疾病-靶點”網絡,多成分、多靶點、系統性地對中藥復方治療疾病的分子機制進行研究分析,對中藥復方配伍及中醫整體觀念的研究具有獨特的優勢[8]。本研究采用網絡藥理學技術推測麻黃附子細辛湯醫治變應性鼻炎的潛在分子機制,為后期相關研究提供理論依據和新的研究思路。
資料與方法
1 麻黃附子細辛湯活性成分的篩選
借助TCMSP數據庫,分別以“麻黃(Mahuang)”、“附子(Fuzi)”、“細辛(Xixin)”為關鍵詞,搜索出各中藥的所有活性成分以及各成分的口服生物利用度(OB)和藥物相似性(DL)。根據相關文獻[9],設定兩個閾值進行篩選,即:OB≥30%、DL≥0.18,對搜索到的化合物進行過濾。
2 中藥活性成分作用靶標的預測
利用TCMSP平臺,挑選得到候選活性化合物所對應的潛在靶標,并將其輸入UniProt平臺(http://www.uniprot.org/)中的UniProt知識庫(UniProt KB),設定物種為人,最后將查詢到的所有化合物活性成分靶點統一進行標準化。
3 AR疾病相關靶蛋白的收集
以“allergic rhinitis”作為檢索詞,分別在Dis-GeNET平臺(https://www.disgenet.org/)、OMIM數據庫(https://www.omim.org/)以及GeneCards數據庫(http://www.genecards.org/)進行檢索,以獲得目前已知的與變應性鼻炎相關的疾病靶點。根據相關文獻[10],score值越高則表示該靶標與疾病的聯系越緊密,若得到的靶標過多則按照score值>中位數的靶標作為該疾病的潛在靶標。
4 關鍵靶點的篩選
為明確變應性鼻炎相關靶點與麻黃附子細辛湯潛在靶點的相互作用,利用R軟件程序包對疾病靶點與麻黃附子細辛湯中藥物活性成分預測靶點取交集并繪出韋恩圖。
5 PPI拓撲學分析
以基因名的形式將篩選得到的關鍵靶點上傳到String平臺(https://string-db.org /),建立蛋白互作網絡圖(protein protein interaction,PPI),最后將獲得的PPI網絡圖導入Cytoscape軟件進行拓撲學分析。
6 藥物-疾病共同靶點基因本體功能(GO)與基因組百科全書(KEGG)通路富集分析
借助基迪奧生物信息云平臺(OmicShare)(https://www.omicshare.com/),對藥物-疾病共同靶點進行GO富集分析和KEGG信號通路分析,將結果按P值的大小排序,取前20條通路進行可視化分析。
7 麻黃附子細辛湯治療AR相關網絡圖的構建
依托Cytoscape(3.8.0)軟件分別建立出麻黃附子細辛湯的活性成分-靶點網絡圖和麻黃附子細辛湯治療變應性鼻炎的核心靶點-通路網絡圖。圖中的節點(node)是活性成分、靶點等,而節點與節點之間的連接則稱為邊(edge)。節點的大小及連接的線條代表節點之間的聯系,節點越大或線條連接得越多表示該節點越重要。
8 分子對接驗證
從PubChem平臺獲取麻黃附子細辛湯治療AR關鍵化合物的結構,再利用ChemOffice將其進行優化。在RCSB PDB平臺下載AR關鍵靶蛋白的分子結構,并利用PyMOL軟件去除水分子和無效小分子配體。依托AutoDock(1.5.6)工具和Vina進行分子對接,獲得關鍵化合物與關鍵靶蛋白的對接效果,并將最佳構象利用PyMOL工具進行可視化展示。
結 果
1 麻黃附子細辛湯中活性成分及預測靶點的獲取
在TCMSP平臺中共篩選出麻黃附子細辛湯的已知化學成分620種,包括麻黃363種,附子65種,細辛192種。在通過了以OB≥30%、DL≥0.18為篩選條件后,總共獲得了麻黃附子細辛湯52個活性成分,其中來源于麻黃23個,附子21個,細辛8個,列出主要的中藥活性成分,內容見表1。查詢出麻黃附子細辛湯蛋白靶點共計227個,并將預測出的所有蛋白靶點名稱借助UniProt平臺(http://www.uniprot.org/)轉換為基因名。

?
2 疾病靶點的獲取及核心靶點的篩選
依托DisGeNET、OMIM以及GeneCards平臺,分別在上述數據庫的網頁檢索框中輸入關鍵詞“allergic rhinitis”后,得到的靶點個數分別為446、1、1034,匯總去重后,得到301個疾病靶點。將得到的301個疾病靶點與227個藥物活性成分靶點借助R軟件取交集并繪制韋恩圖(見圖1)。結果獲得30個藥物活性成分與疾病的共同靶點,即:PTGS2、ADRB2、DPP4、PPARG、NOS2、BCL2、ICAM1、GSTP1、AHR、AKR1B1、VEGFA、PLAU、MMP9、MAPK1、HIF1A、IL1B、CCL2、CXCL8、IL2RA、PLAT、SERPINE1、IFNG、IL1A、PARP1、PPARA、SPP1、IL4、CHRM3、CAT、NOX1。將篩選得到的關鍵靶點以基因名的形式上傳到String平臺并進行拓撲學分析,獲得PPI網絡圖,見圖2。
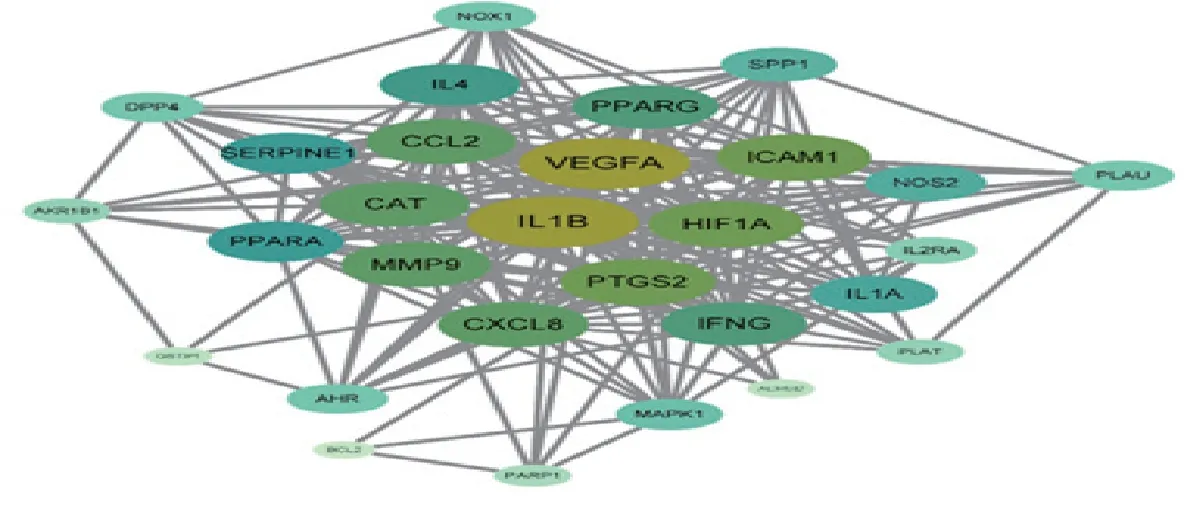
圖2 PPI拓撲學分析結果圖
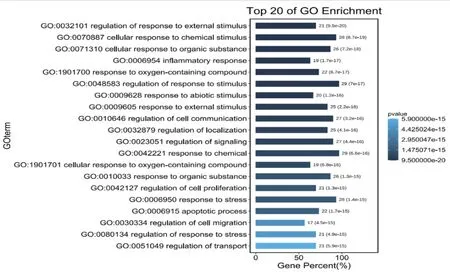
圖3 生物過程(BP)
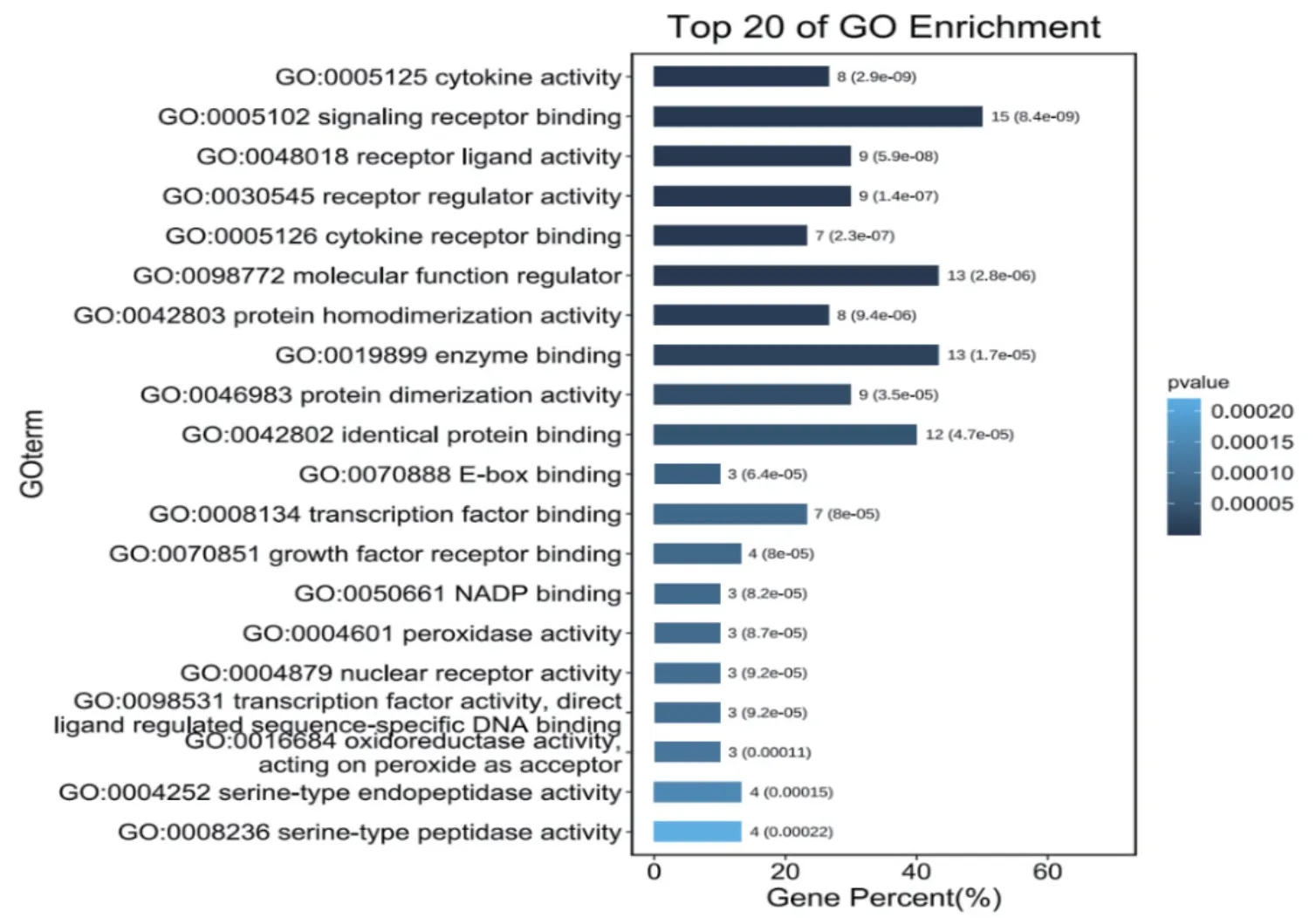
圖4 分子功能(MF)
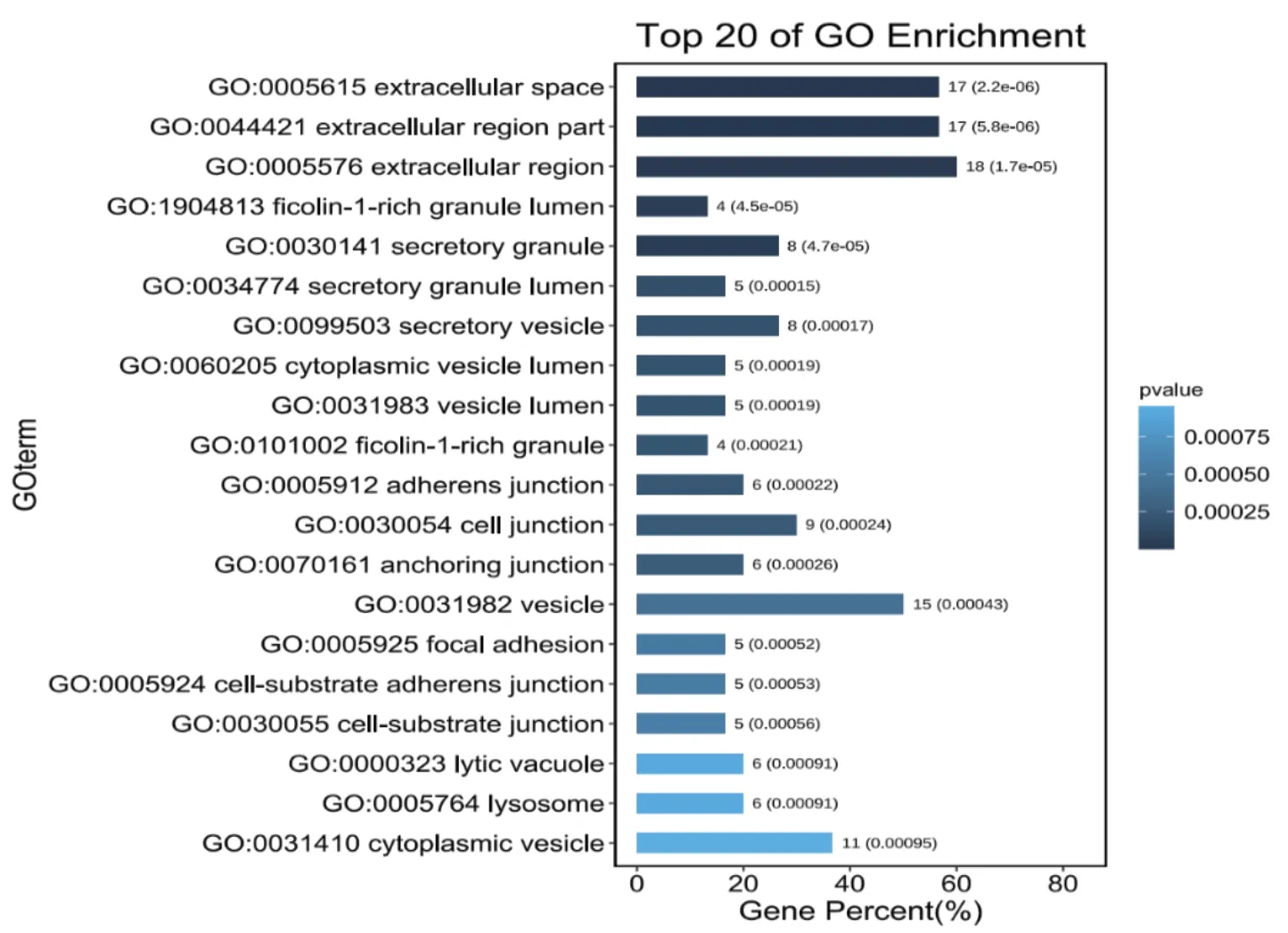
圖5 細胞組成(CC)
3 基因本體功能與通路富集分析
借助基迪奧生物信息云平臺(OmicShare)(https://www.omicshare.com/)對麻黃附子細辛湯與變應性鼻炎的30個共同靶點進行基因本體功能(GO)富集分析和KEGG通路分析。將所得的結果根據P值的大小排列,并依次以排序前20項的條目形式列出生物學過程(Biological Process,BP)、分子功能(Molecular Function,MF)以及細胞組成(Cellular Component,CC),并依次繪出柱狀圖,見圖3-5。結果顯示,在藥物-疾病共同靶點上共富集的生物學過程17743條,分子功能過程18408條,細胞組成18579條。其中主要涉及的生物學過程有:細胞對外界刺激的反應、細胞對化學刺激的反應、細胞對有機物的反應、炎癥反應、對含氧化合物的反應等;主要涉及的分子功能有:細胞因子活性、信號受體結合、受體配體的活性、受體調節器活性、細胞因子受體結合等;主要涉及的細胞組成有:細胞外間隙、胞外區部分、質膜外側、富含ficolin-1的顆粒管腔、分泌顆粒等;在進行藥物-疾病共同靶點KEGG通路分析后,共富集出197條通路,其中排名前20條的為:流體剪切力和動脈粥樣硬化、AGE- RAGE信號通路在糖尿病并發癥中的作用、IL-17信號通路、癌癥、美洲錐蟲病、Th17細胞分化、HIF-1信號通路等,見表2,將結果繪制成氣泡圖,見圖6。
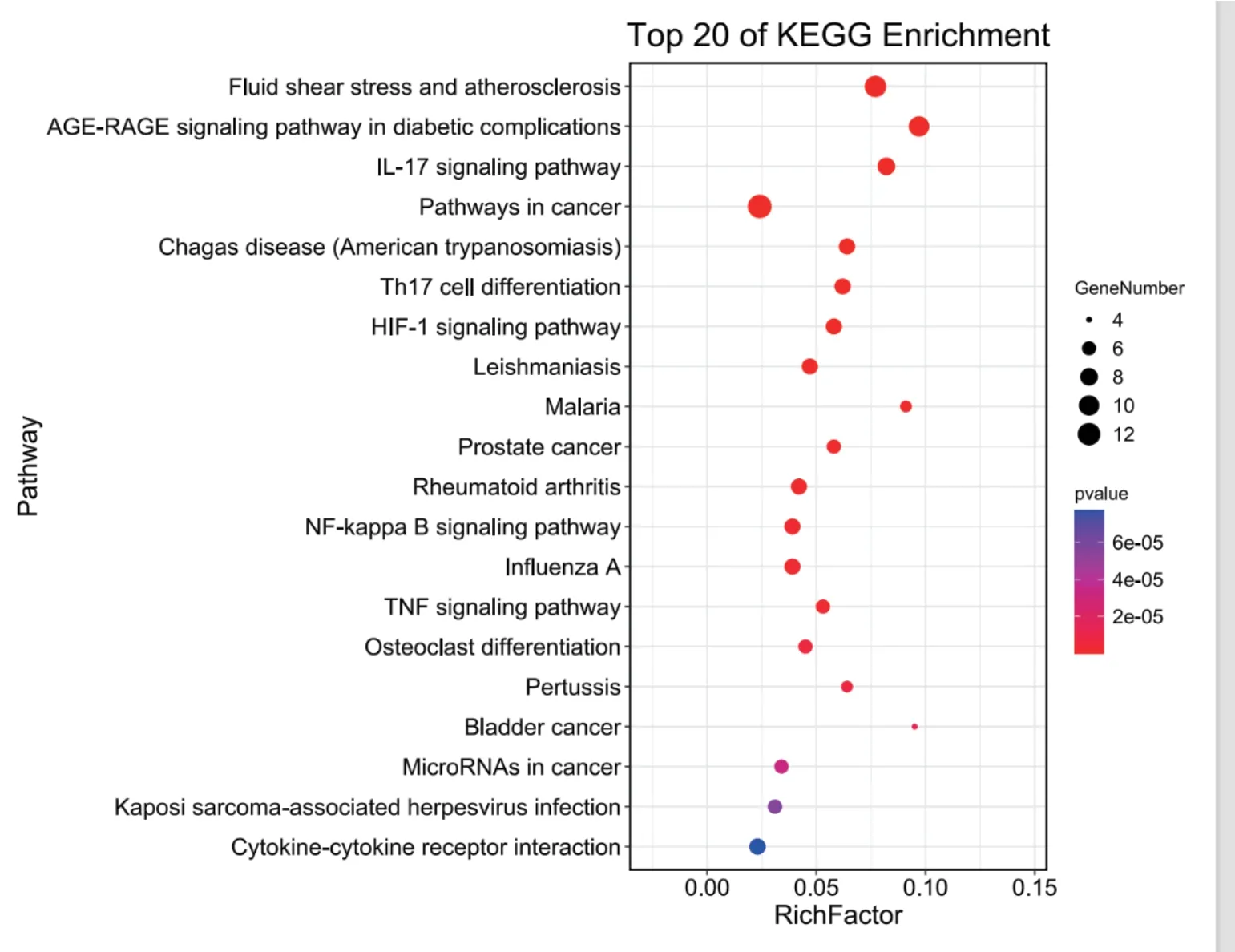
圖6 KEGG前20條氣泡圖
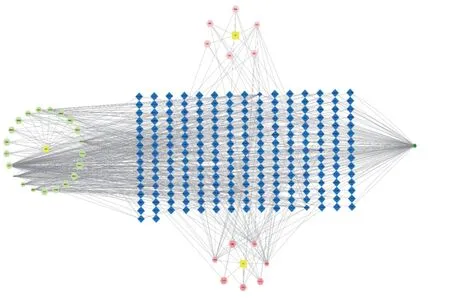
圖7 麻黃附子細辛湯活性成分-靶點網絡圖
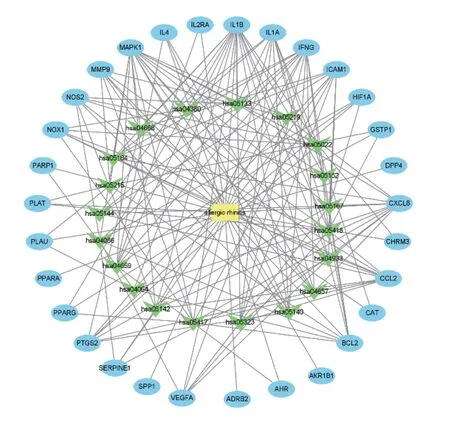
圖8 靶點-通路網絡圖

?
4 相關網絡圖的構建
依托Cytoscape(3.8.0)工具分別建立出麻黃附子細辛湯的活性成分-靶點圖和麻黃附子細辛湯治療變應性鼻炎的核心靶點-通路網絡圖,見圖7-8。其中,麻黃附子細辛湯的活性成分-靶點圖中共有60個節點(node)和104條邊(edge),麻黃附子細辛湯治療變應性鼻炎的核心靶點-通路網絡圖中共有51個節點和170條邊。
5 分子對接驗證結果
將PPI拓撲學分析結果中5個節點度最高的靶蛋白(IL1B、VEGFA、PTGS2、HIF1A、ICAM1)與“麻黃附子細辛湯活性成分-靶點網絡圖”中的主要化合物kaempferol(山奈酚)、quercetin(槲皮素)、luteolin(木犀草素)、naringenin(柚皮素)分別依次在AutoDock(1.5.6)軟件中進行分子對接驗證。結果見表3。當受體與配體的結合能<-5.0 kcal/mol時則表示分子與蛋白靶點之間具有較好的結合活性[11]。驗證結果顯示,麻黃附子細辛湯主要活性成分與AR疾病關鍵靶點的結合活性在-5.7kcal/mol至-9.6kcal/mol之間,表明麻黃附子細辛湯主要活性成分與AR疾病關鍵靶點之間形成的構象結構較穩定,具有較好的結合活性。另外,由表3可見,luteolin(木犀草素)與5個靶蛋白結合能最低,利用PyMOL軟件對木犀草素與核心靶蛋白的最佳結合構象進行可視化分析,見圖9。
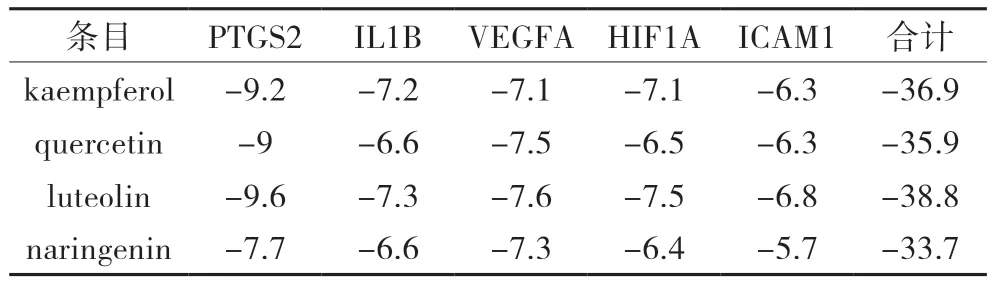
表3 主要化合物與核心靶蛋白分子對接結果
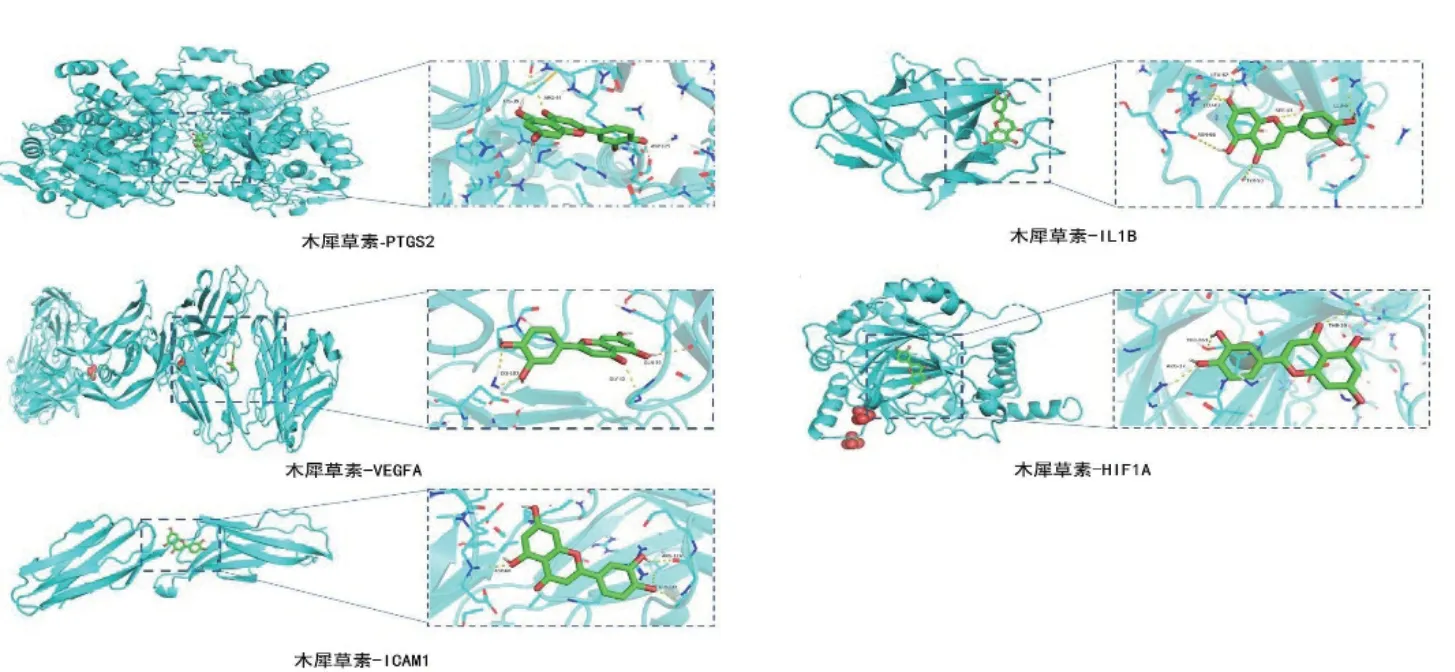
圖9 木犀草素與核心靶蛋白對接圖
討 論
變應性鼻炎屬于中醫“鼻鼽”“鼽嚏”等范疇,大量研究表明,運用麻黃附子細辛湯治療變應性鼻炎能取得一定的療效。方中麻黃是麻黃科植物的干燥草質莖,麻黃的主要化學成分為生物堿、黃酮類、揮發油類等,具有平喘、發汗、利尿、抗炎抗過敏等作用[12],其中,麻黃中的水提物和乙醇提取物可抑制肥大細胞和嗜堿性粒細胞釋放組胺等化學介質,具有抗變態反應的作用[13];現代藥理學研究顯示[14],附子具有強心、抗癌、抗炎等作用;細辛能夠抗病毒抗菌、抗炎鎮痛、免疫調節等,其中,細辛中的甲基丁香酚、芝麻脂素具有明顯的抗炎作用[15]。
本研究中藥物-疾病靶點網絡圖顯示,麻黃附子細辛湯治療AR的主要化合物依次為槲皮素、木犀草素、山柰酚、柚皮素、豆甾醇等。槲皮素是一種天然存在的多酚類黃酮化合物,它可以抑制組胺等化學介質的產生,可以調節Th1/Th2的穩定性,具有抗氧化、抗炎抗過敏以及免疫調節的作用,對相關的變應性疾病有著廣泛的應用[16]。木犀草素主要通過調節NF-κB、AP-1、STAT3等轉錄因子達到一定的抗炎作用,有研究表明木犀草素可通過調節變應性鼻炎大鼠的 TLR4/NF-κB 信號通路和調整Th1/Th2 失衡狀態以改善鼻黏膜炎癥[17]。山奈酚可降低小鼠血清中的組胺、腫瘤壞死因子-α、IL- 8等,具有抗過敏作用[18]。柚皮素能顯著改善變應性鼻炎大鼠的鼻黏膜組織,且能降低大鼠血清中IgE、IL4及IL5值,對變應性鼻炎大鼠具有一定的保護作用[19]。在本研究中,我們發現,在獲得的主要活性成分中,大多來源于麻黃,這可能與麻黃在研究變應性鼻炎方面更為廣泛有關。在對得到的30個核心靶點進行拓撲學分析后顯示,VEGF-A、IL1B、PTGS2、HIF1A、等可能是麻黃附子細辛湯發揮治療AR作用的重要靶點,其中血管內皮生長因子A(VEGF-A)是VEGF家族中研究最多的一種,具有促進血管生成、增加血管通透性、參與血管重塑以及促進受損黏膜組織修復等作用[20],相關研究顯示,血管內皮生長因子在變應性鼻炎患者中有較高的表達[21],說明VEGF-A與變應性鼻炎鼻黏膜重塑有關。IL1B基因中第5外顯子rs1143634使IL-1β分泌增加,而在變應性鼻炎患者抗原激發后其鼻腔分泌物中IL-1β水平會顯著增高,亦有研究發現IL-1β與過敏性疾病的炎癥進展呈現正相關,這說明IL1B與變應性鼻炎的炎癥有著密切的聯系[22-23]。綜上,麻黃附子細辛湯的多個核心靶點對變應性鼻炎的炎癥狀態、鼻黏膜重塑、免疫調節等方面發揮作用。
通過富集分析,得出197條麻黃附子細辛湯與變應性鼻炎相關的通路。其中流體剪切力和動脈粥樣硬化這一信號通路為麻黃附子細辛湯對變應性鼻炎的第一作用通路,流體剪切力和動脈粥樣硬化與NF-κB炎癥信號的激活有關[24]。AGE-RAGE信號通路與神經和外周血管的修復、再生密切相關[25],有研究報告,AGE-RAGEs影響著細胞的凋亡和增殖、參與細胞的氧化應激反應過程[26]。IL-17信號通路是變應性鼻炎機制研究較多的通路之一,是由T輔助細胞(Th17)產生,可激活NF-κB、MAPKs等多種信號通路以誘導促炎趨化因子和細胞因子的表達,在防御反應、過敏性疾病以及自身免疫疾病中起著重要作用[27-28]。從富集結果來看,對麻黃附子細辛湯治療變應性鼻炎的研究主要可以通過流體剪切力和動脈粥樣硬化、AGE-RAGE信號通路在糖尿病并發癥中的作用、IL-17信號通路、癌癥、美洲錐蟲病、Th17細胞分化、HIF-1信號通路等進行。
在得到的分子對接結合能中,我們發現木犀草素與5個關鍵靶蛋白的總結合能最高,說明木犀草素可能是麻黃附子細辛湯治療AR的核心化合物。
借助網絡藥理學與分子對接技術對麻黃附子細辛湯治療AR的分子機制從多成分、多靶點、多信號通路進行預測,為麻黃附子細辛湯治療變應性鼻炎的作用機制提供了一定的理論依據和研究方向。但由于本研究主要借助相關網絡平臺信息,對獲得的結論還需通過相關實驗進行進一步驗證。

