肺炎克雷伯菌肝膿腫與非肺炎克雷伯菌肝膿腫的特征比較研究*
徐 彤,張吟眉,魯敏儀,鄭佳佳
北京大學第三醫院檢驗科,北京 100191
肝膿腫是由多種病原微生物引起的臨床上較為常見的肝臟感染性疾病,臨床上以細菌引起的細菌性肝膿腫(BLA)較為常見[1-2]。既往研究表明,在美國和歐洲國家引起BLA的主要病原菌是大腸埃希菌和鏈球菌屬[3-4]。肺炎克雷伯菌(KP)是近年來引起社區獲得性血流感染的常見條件致病菌,并逐漸成為BLA的主要致病菌[5]。而在肺炎克雷伯菌肝膿腫(KPLA)患者標本中分離出的高毒力肺炎克雷伯菌(hvKP)又成為KPLA的主要病原菌。hvKP還可以引起除BLA外其他部位的轉移性感染[6]。本研究收集并分析了本院2016年1月至2020年12月收治的215例肝膿腫患者的臨床資料及實驗室檢查結果,比較KPLA患者和非肺炎克雷伯菌肝膿腫(NKPLA)患者,以及KPLA患者中合并糖尿病、膽道疾病、胃腸道疾病各亞組的臨床特征及實驗室檢查指標結果,為KPLA的診斷與治療提供參考依據。
1 資料與方法
1.1一般資料 回顧性分析本院在2016年1月至2020年12月收治的215例肝膿腫患者的臨床資料。BLA診斷標準:(1)患者常出現以發熱、畏寒或寒戰、肢體乏力為主的臨床表現或以肝區叩痛為主的體征;(2)腹部超聲等影像學檢查發現患者肝部有膿腫病灶;(3)患者的血培養或膿腫部位引流出的穿刺液細菌培養結果為陽性;(4)經抗菌藥物治療后患者的癥狀有所減輕;(5)經穿刺引流或手術后證實為肝膿腫;(6)排除其他相關疾病和其他類型肝膿腫[7]。糖尿病的診斷參照《中國2型糖尿病防治指南(2020年版)》中糖尿病診斷標準[8]:典型糖尿病癥狀加上隨機血糖≥11.1 mmol/L,或加上空腹血糖≥7.0 mmol/L,或加上口服葡萄糖耐量試驗(OGTT)2 h血糖≥11.1 mmol/L,或加上糖化血紅蛋白(HbA1c)≥6.5%。
1.2方法
1.2.1資料收集及分組 查閱215例肝膿腫患者的完整病歷資料,結合KPLA患者病歷信息,匯總分析其基本資料(年齡、性別)、臨床表現(發熱、寒戰或畏寒、腹痛等)、基礎疾病(是否患糖尿病、肝膽疾病、胃腸道疾病等)、有無并發癥;收集患者實驗室檢查指標[白細胞計數(WBC)、血紅蛋白(Hb)、血小板計數(PLT)、丙氨酸氨基轉移酶(ALT)、天門冬氨酸氨基轉移酶(AST)、堿性磷酸酶(ALP)、γ-谷氨酰轉肽酶(GGT)、中性粒細胞絕對值(NEUT#)、葡萄糖(GLU)、淋巴細胞絕對值(LYMPH#)]結果、治療方式、抗菌藥物藥敏試驗結果、治療時間及患者的預后情況等信息。患者按照病原學檢測結果分為KPLA組和NKPLA組。治療效果劃分如下:(1)好轉為病原學結果陰性及全身感染癥狀消失、膿腫病灶縮小、炎癥指標水平下降;(2)死亡;(3)其他(未愈/轉院等)。
1.2.2細菌培養、鑒定及藥敏試驗 使用BD BACTEC FX全自動血培養儀對血液標本進行培養,將血培養陽性瓶中的血液接種于中國藍平板上以分離細菌,使用VITEK2 Compact全自動微生物分析系統及BD-Bruker MALDI Biotyper微生物質譜快速分析系統對分離出的菌種進行鑒定。采用微量肉湯稀釋法(VITEK2 Compact全自動微生物分析系統)檢測常用抗菌藥物的最低抑菌濃度(MIC),采用紙片擴散法檢測抑菌環直徑。依據美國臨床和實驗室標準協會(CLSI)相關文件對KP的藥敏試驗結果進行判斷,將細菌的藥敏試驗結果分為敏感、中介和耐藥。
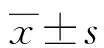
2 結 果
2.1患者基本資料 本研究收集的215例肝膿腫患者:98例病原學檢測結果陽性,即診斷為BLA,其中72例臨床標本細菌培養結果為KP陽性,26例為其他致病菌陽性;84例病原學檢測結果陰性;33例未做相關病原學檢查。肝膿腫患者平均年齡(57.66±16.06)歲,其中男140例,女75例。72例KPLA患者的平均年齡為(57.64±13.95)歲,其中男42例,女30例;26例NKPLA患者的平均年齡為(58.15±17.08)歲,其中男19例,女7例。KPLA組與NKPLA組的年齡與性別比較,差異無統計學意義(P>0.05)。
2.2肝膿腫患者病原學特征及KPLA藥敏試驗結果 215例肝膿腫患者中164例進行血培養,陽性59例(35.98%);75例進行引流液/穿刺液/膿液培養,陽性51例(68.00%);有12例患者血培養和引流液/穿刺液/膿液培養同時陽性。兩種樣本的陽性率差異有統計學意義(P<0.01)。72例KP陽性患者所分離的菌株對大部分β-內酰胺類、喹諾酮類、大環內酯類抗菌藥物敏感率較高,而其中有2株KP具有較高的耐藥性,KPLA患者分離的菌株藥敏試驗結果見表1。其他致病菌陽性有26例,包括:大腸埃希菌9例、奇異變形桿菌1例、舟形梭桿菌1例、具核梭桿菌1例、人葡萄球菌1例、糞腸球菌1例、戊糖片球菌1例、鶉雞腸球菌D群1例、鳥腸球菌1例、金黃色葡萄球菌2例、屎腸球菌1例、咽峽炎鏈球菌1例、中間鏈球菌3例、格氏鏈球菌1例、微小小單胞菌1例。
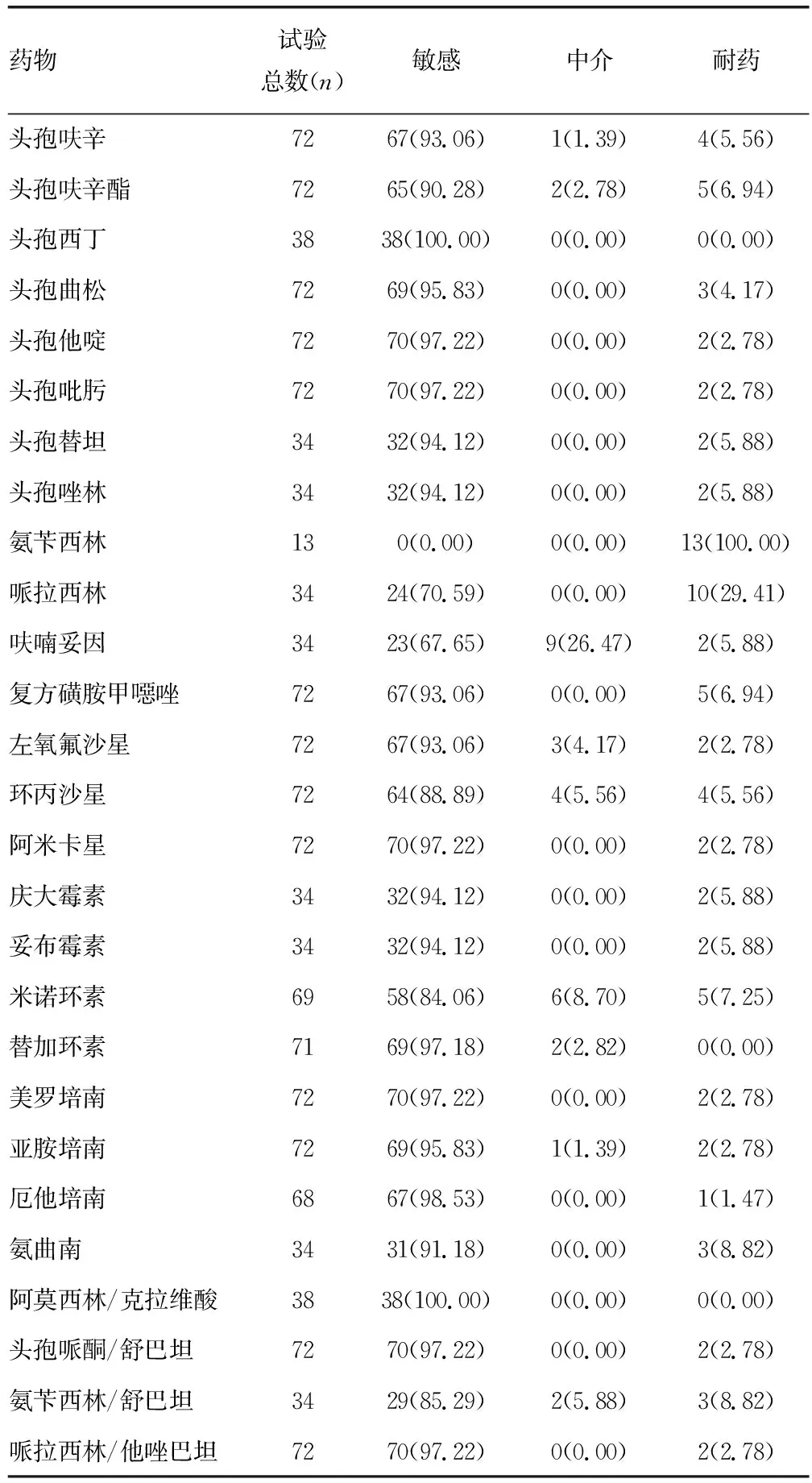
表1 72株KPLA患者分離的KP藥敏試驗結果[n(%)]
2.3KPLA組與NKPLA組的臨床特征及實驗室檢查結果比較 與NKPLA患者相比,KPLA患者多合并糖尿病,且患者臨床表現中畏寒或寒戰、乏力的比例較高(P<0.05),NKPLA患者多合并膽道疾病(P<0.05)。兩組患者治療方法、治療時間和治療效果比較,差異無統計學意義(P>0.05)。對KPLA組與NKPLA組的實驗室檢查結果進行比較,KPLA組的Hb、GLU、AST水平高于NKPLA組(P<0.05)。見表2、3。

表2 KPLA組與NKPLA組的臨床特征比較[n(%)或

表3 KPLA組與NKPLA組的實驗室檢查結果比較或M(P25,P75)]
2.4KPLA組不同合并癥患者的臨床特征分析 本研究中,72例KPLA患者中合并糖尿病的患者有37例(51.39%),合并膽道疾病的患者有11例(15.28%),合并胃腸道疾病的患者有11例(15.28%)。合并糖尿病的KPLA患者的治療時間相比未合并糖尿病的KPLA患者延長(P<0.05)。合并膽道疾病的KPLA患者治療后好轉的比例低于未合并膽道疾病的KPLA患者(P<0.05)。合并胃腸道疾病的KPLA患者年齡大于未合并胃腸道疾病的KPLA患者(P<0.05),二者治療時間及效果差異無統計學意義(P>0.05)。見表4~6。

表4 合并糖尿病與未合并糖尿病KPLA患者的臨床特征比較[n(%)或
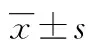
表5 合并膽道疾病與未合并膽道疾病KPLA患者的臨床特征比較[n(%)或或M(P25,P75)]
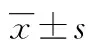
表6 合并胃腸道疾病與未合并胃腸道疾病KPLA患者的臨床特征比較[n(%)或或M(P25,P75)]
2.5不同合并癥情況KPLA患者的實驗室檢查結果比較 KPLA患者中,合并糖尿病患者的GLU、WBC、NEUT#高于未合并糖尿病患者(P<0.05),AST水平低于未合并糖尿病患者(P<0.05);合并膽道疾病的KPLA患者的PLT及GGT水平高于未合并膽道疾病的患者((P<0.05))。合并與未合并胃腸道疾病的KPLA患者實驗室指標比較,差異均無統計學意義(P>0.05)。見表7~9。

表7 合并糖尿病與未合并糖尿病KPLA患者的實驗室檢查結果比較或M(P25,P75)]

表8 合并膽道疾病與未合并膽道疾病KPLA患者的實驗室檢查結果比較[M(P25,P75)或

表9 合并胃腸道疾病與未合并胃腸道疾病KPLA患者的實驗室檢查結果比較或M(P25,P75)]
3 討 論
近30年來,KP已經成為BLA的主要致病菌[9],本研究結果顯示,本院2016年1月至2020年12月的98例BLA患者中73.47%(72/98)由KP引起,26.53%由其他致病菌引起,與既往多數研究結果一致[5,10]。
本研究中72例KPLA患者中有51.39%合并糖尿病,與NKPLA患者相比,比例顯著升高,這與以往的研究結果一致[11]。糖尿病患者容易感染KP、引起BLA的原因可能是機體長期處于高血糖狀態,使血液中的白細胞抗感染的趨化作用和吞噬作用被部分抑制,患者機體的免疫系統功能減弱,增加了機體感染細菌的風險[12]。實驗室檢查結果顯示,合并糖尿病的KPLA患者的WBC和NEUT#高于未合并糖尿病的患者,提示合并糖尿病患者的炎癥反應更為明顯。BLA患者可能發生應激性血糖升高,從而加重糖尿病病情[13];同時也有研究發現合并糖尿病的BLA患者隱源性感染率高于膽管感染率和血源感染率[12],以上原因可能導致合并糖尿病的KPLA患者治療時間延長。因此,對于合并糖尿病的KPLA患者,在治療期間更要注意控制患者的血糖水平。
本研究中,合并膽道疾病的KPLA患者比例顯著低于NKPLA患者。有研究發現,目前大腸埃希菌仍是引起膽道感染的主要致病菌[14]。最初認為BLA的致病菌可能來自膽道感染。當膽道或膽囊等部位發生炎癥感染時,引起膽道感染的細菌可以隨血液沿著膽管上行至肝臟,從而引起BLA[13]。將合并膽道疾病與未合并膽道疾病KPLA患者進行比較,發現合并膽道疾病患者的PLT及GGT水平更高。
近年來從KPLA患者血液或穿刺液標本中分離出的KP大多是hvKP。目前認為攜帶rmpA和氣桿菌素基因的KP通常具有高毒力,但是否為hvKP還需要結合患者的臨床癥狀加以分析。
KP的腸道定植也是引起KPLA的可能致病因素。通過對比BLA患者使用抗菌藥物前的糞便標本與健康人的糞便標本,發現部分患者糞便中分離的KP與健康人糞便中的KP具有相同的血清型和基因型,且同時具有毒力,表明健康人的腸道中也存在hvKP的定植[15]。目前已有動物模型證明了hvKP能夠從胃腸道易位到其他無菌部位,從而導致膿腫發生[16],但并不是所有定植于腸道的hvKP都可以引起以KPLA為首發癥狀的侵襲綜合征,常見的可能致病因素有是否患胃腸道疾病,是否有手術史等侵襲性操作。有研究發現,胃鏡等檢查可能會增加BLA的患病風險[17],KP定植數量增加及機體的免疫功能下降等因素可能在這一過程中發揮了作用。本研究將合并胃腸道疾病的與未合并胃腸道疾病的KPLA患者的臨床資料進行對比發現,合并胃腸道疾病的KPLA患者除年齡較大(P=0.034)外,其余方面差異無統計學意義(P>0.05),其具體的致病機制還需要進一步探究。
KPLA的常見治療方式有針對病原菌的抗菌藥物治療、液化后的膿腫穿刺引流和外科手術治療。發病初期還未明確病原菌時,臨床常選擇廣譜抗菌藥物,膿腫符合穿刺引流條件后可及時對膿腫進行穿刺引流,并將穿刺液或膿液進行細菌培養以明確致病菌。本研究分離出的72株KP中,大部分菌株對除氨芐西林外其他常見抗菌藥物敏感,有2株(2.8%)依據藥敏試驗結果判斷為耐碳青霉烯類腸桿菌科細菌(CRE)。目前臨床常用第2代、3代頭孢菌素對輕癥的BLA患者進行治療,重癥患者可采用碳青霉烯類藥物治療。近20年來,CRE的產生對全世界的公共衛生構成了嚴重威脅。有研究表明,感染CRE的患者預后差,病死率高[18]。近期研究發現hvKP的檢出率呈上升趨勢[19-20],因此在治療過程中應時刻關注細菌耐藥性的變化,避免耐藥株的流行。
綜上所述,合并糖尿病的KPLA患者炎癥反應更為明顯,在治療時應同時注重控制患者的血糖水平。未合并膽道疾病的KPLA患者的治療效果好于合并膽道疾病的KPLA患者。使用抗菌藥物治療感染高耐藥性菌株的KPLA患者時,需關注細菌耐藥性的變化。

