不同入路腹腔鏡保留腎單位腎腫瘤切除術(shù)的應(yīng)用效果比較
林山,黃令杰,朱顯鐘,張漢榮,李金雨
(中國人民解放軍聯(lián)勤保障部隊第九〇九醫(yī)院·廈門大學(xué)附屬東南醫(yī)院泌尿外科,福建 漳州 363000)
腎腫瘤極易癌變,腎癌位居中國泌尿系統(tǒng)惡性腫瘤疾病第二位,2002~2018年,全球每年新發(fā)病例增漲16.77萬,死亡病例數(shù)增漲7.3萬[1]。腹腔鏡微創(chuàng)手術(shù)治療腎腫瘤具有創(chuàng)傷小、術(shù)中出血量少、減輕疼痛程度以及促進術(shù)后恢復(fù)等優(yōu)勢,是治療T1期腎癌(直徑≤7 cm)的標準術(shù)式[2]。腹腔鏡下保留腎單位手術(shù)(nephron sparing surgery,NSS)是治療T1期腎癌的主要術(shù)式,較腹腔鏡根治性腎切除術(shù)能提高5年腫瘤特異生存率,降低5年腫瘤特異死亡率和轉(zhuǎn)移率[3]。NSS常見術(shù)式類別為腎部分切除術(shù),能最大程度保留腎臟組織,將腫瘤完整切除,減少正常腎實質(zhì)的損失,減低術(shù)后腎實質(zhì)萎縮程度,從而最大程度保護腎臟功能[4]。但目前,臨床針對NSS腎部分切除術(shù)是選擇經(jīng)腹腔途徑或經(jīng)后腹膜途徑治療T1期腎癌的安全性、有效性尚無明確定論。本研究擬探討經(jīng)腹腔入路和經(jīng)后腹膜入路腹腔鏡保留腎單位腎腫瘤切除術(shù)的治療效果。
1 資料與方法
1.1 一般資料
選取2019年6月至2021年6月中國人民解放軍聯(lián)勤保障部隊第九〇九醫(yī)院收治的82例腎腫瘤患者為研究對象。納入標準:(1)《腎癌的診斷及鑒別診斷》為腎腫瘤的診斷標準[5],術(shù)前經(jīng)CT或MRI影像學(xué)檢查和病理檢查確診為單發(fā)腎細胞癌,未發(fā)生遠處轉(zhuǎn)移,腫瘤直徑≤7 cm;2002年美國癌癥聯(lián)合委員會(AJCC)為TNM分期診斷標準[6],符合T1N0M0期者;(2)健側(cè)肝、腎功能處于正常者;(3)未出現(xiàn)淋巴結(jié)腫大者;(4)臨床資料完整,能完成本試驗要求及隨訪者。排除標準:(1)腎臟解剖結(jié)構(gòu)不清晰或解剖結(jié)構(gòu)變異、畸形者;(2)合并其他惡性腫瘤者;(3)術(shù)中行輸尿管切開取石、腎囊腫去頂手術(shù)者;(4)處于女性懷孕期間或母乳喂養(yǎng)期間者。根據(jù)手術(shù)入路不同分為經(jīng)腹腔入路組(n=41)和經(jīng)腹膜后入路組(n=41)。其中經(jīng)腹腔入路組中,男性26例,女性15例;年齡(56.15±5.29)歲;體質(zhì)量指數(shù)(BMI)(23.89±2.29)kg/m2;腫瘤直徑(2.69±0.62)cm;腫瘤部位左側(cè)22例,右側(cè)19例.經(jīng)腹膜后入路組中,男性24例,女性17例;年齡(56.89±5.68)歲;BMI(24.09±2.31)kg/m2;腫瘤直徑(2.73±0.59)cm;腫瘤部位左側(cè)20例,右側(cè)21例。兩組患者一般資料比較,差異均無統(tǒng)計學(xué)意義(P>0.05)。本研究獲得醫(yī)院倫理委員會審批,受檢者均簽署知情同意書。
1.2 方法
1.2.1 經(jīng)腹腔入路組 行全身麻醉手術(shù),將患者手術(shù)姿勢調(diào)整為健側(cè)臥位,先建立人工氣腹,在患側(cè)鎖骨中心點肋緣下方作切口,切口長度1 cm,再依次切開各層腹壁,置入氣腹針并維持人工氣腹壓力13~15 mmHg;選擇經(jīng)腹腔入路,在患側(cè)腹直肌外緣處距離臍上和臍下均3 cm處,以及髂前上棘內(nèi)上方距離3 cm處分別建立3個操作孔,并將10 mm、10 mm及5 mm的Trocar分別置入上述操作孔中。于結(jié)腸脾曲、肝曲處使用超聲刀和分離鉗進行逐步銳性分離,再降、升結(jié)腸旁溝將腹膜從側(cè)方切開,右側(cè)處將升結(jié)腸旁溝向上游離,直至游離在肝結(jié)腸韌帶處,以便將后方腎周筋膜顯露出來,并將其游離至腎蒂,腎蒂和輸尿管顯示良好。將血管鞘以及腎蒂周圍結(jié)締組織進行分離,并在雙側(cè)沿性腺靜脈和下腔靜脈處顯示腎動、靜脈,并用Hem-o-lok雙重夾閉阻斷腎動、靜脈。明確瘤體部位并于瘤體周邊緣0.5~1.0 cm處以電刀將腎包膜切開,將腫瘤組織鈍性分離并完整取出,采用可吸收線及肝針間斷縫合創(chuàng)面,夾閉縫線、代替打結(jié),傷口創(chuàng)面縫合完畢,解除受到阻斷的腎臟血管,腫瘤組織送病理檢查,選擇在腎臟局部將乳膠管常規(guī)放置引流。
1.2.2 經(jīng)腹膜后入路組 行全身麻醉手術(shù),調(diào)整病人手術(shù)姿勢為90 °健側(cè)臥位,腰下墊墊枕并妥善固定,常規(guī)消毒鋪巾,建立人工氣腹并維持氣腹壓力13~15 mmHg;在腋后線12肋緣下處方位、腋前線11肋下距腋后線75 cm處方位以及腋中線髂嵴上緣15 cm處方位分別建立3個操作孔,并將10 mm、10 mm及5 mm的Trocar分別置入上述操作孔中。沿長軸方向?qū)⒏鼓ず箝g隙銳性分離以及擴大,再將其朝內(nèi)側(cè)游離,沿著腹側(cè)牽開腎臟顯露腎蒂。將血管鞘以及腎蒂周圍結(jié)締組織進行分離,并在雙側(cè)沿性腺靜脈和下腔靜脈處顯示腎動、靜脈,并用Hem-o-lok雙重夾閉阻斷腎動、靜脈。沿著腎動脈前下方將腎靜脈及其屬支進行游離,并采用Hem-o-lok夾閉阻斷血流。在瘤體組織周圍0.5~1.0 cm處切開腎包膜,切除腫瘤,采用可吸收線及肝針間斷縫合創(chuàng)面,夾閉縫線、代替打結(jié),傷口創(chuàng)面縫合完畢,解除受到阻斷的腎臟血管,腫瘤組織送病理檢查,選擇在腎臟局部將乳膠管常規(guī)放置引流。
1.3 術(shù)后處理
術(shù)畢,嚴密觀察兩組患者的術(shù)后失血量、引流液情況、術(shù)后疼痛情況、是否存在切口感染以及是否存在發(fā)生尿漏等,并進行及時輸血處理、抗炎、適當(dāng)止痛藥肌注處理、使用抗生素消炎、血腫切開引流以及植入輸尿管支架等對癥處理。
1.4 觀察指標
1.4.1 手術(shù)相關(guān)指標 記錄兩組患者的手術(shù)時間、術(shù)中出血量、平均熱缺血時間、術(shù)后通氣時間、術(shù)后置管時間及平均住院時間。
1.4.2 術(shù)后并發(fā)癥 觀察并統(tǒng)計兩組患者在術(shù)后出現(xiàn)的并發(fā)癥情況。
1.4.3 腎功能 于術(shù)前、術(shù)后24 h及術(shù)后3個月清晨,采集兩組患者的尿液樣本,應(yīng)用全自動生化儀測定尿液中肌酐(Scr)及尿素氮(BUN)含量。
1.4.4 生活質(zhì)量 對兩組患者進行生活質(zhì)量評定,評定量表為歐洲癌癥研究與治療組織生命質(zhì)量測定量表(EORTC QOL-C30)[7],測評時間為術(shù)前及術(shù)后3個月,量表測評內(nèi)容涉及軀體功能、情緒功能、社會功能、認知功能及總體生活質(zhì)量5個維度,每個維度總分均為100分,得分越高,提示患者相應(yīng)維度的生活質(zhì)量越好。
1.5 統(tǒng)計學(xué)分析
2 結(jié)果
2.1 兩組患者手術(shù)相關(guān)指標比較
經(jīng)腹膜后入路組的手術(shù)時間、術(shù)后通氣時間及平均住院時間均短于經(jīng)腹腔入路組(P<0.05),術(shù)中出血量少于經(jīng)腹腔入路組(P<0.05)。見表1。
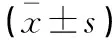
表1 兩組患者手術(shù)相關(guān)指標比較
2.2 兩組患者術(shù)后并發(fā)癥發(fā)生情況比較
兩組患者術(shù)后并發(fā)癥總發(fā)生率比較,無統(tǒng)計學(xué)差異(χ2=0.823,P=0.364)。見表2。

表2 兩組患者術(shù)后并發(fā)癥發(fā)生情況比較 [n(%)]
2.3 兩組不同時間點的Scr和BUN水平對比
術(shù)后24 h、3個月,兩組尿液Scr及BUN水平均先升高后下降,相鄰時間點間比較,差異均有統(tǒng)計學(xué)意義(P<0.05),但組間比較無統(tǒng)計學(xué)差異(P>0.05)。見表3。
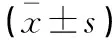
表3 兩組患者不同時間點的Scr和BUN水平比較
2.4 兩組患者術(shù)前及術(shù)后3個月的EORTC QOL-C30評分比較
術(shù)后3個月,兩組患者EORTC QOL-C30量表中關(guān)于軀體功能、情緒功能、社會功能、認知功能及總體生活質(zhì)量5項評分均下降(P<0.05),但組間差異無統(tǒng)計學(xué)意義(P>0.05)。見表4。
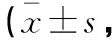
表4 兩組患者術(shù)前及術(shù)后3個月的EORTC QOL-C30評分比較分)
3 討論
腎部分切除術(shù)的適應(yīng)證為T1期腎腫瘤,術(shù)中選擇經(jīng)腹膜后或經(jīng)腹腔入路均能最大程度保留部分腎組織,可減少術(shù)中疼痛,提高腎腫瘤患者生存質(zhì)量[8]。針對腎部分切除術(shù)治療,如何縮短腎臟熱缺血時間以最大程度減少熱缺血范圍,是保護術(shù)后腎臟功能的關(guān)鍵[9]。本研究發(fā)現(xiàn),兩種入路均能阻斷腎段動脈,實現(xiàn)縮短正常腎臟實質(zhì)的熱缺血損傷時間,效果相同,均利于改善患者的術(shù)后腎臟功能。但本研究中經(jīng)腹膜后入路組患者的手術(shù)時間、術(shù)后通氣時間及平均住院時間均短于經(jīng)腹腔入路組,術(shù)中出血量少于經(jīng)腹腔入路組,究其原因可能是:(1)經(jīng)腹膜后入路對腹腔臟器干擾較小,更便于對腎血管實施分離、顯露與夾閉等操作,控制腎蒂血管,從而提高術(shù)中操作效率,縮短手術(shù)時間,利于術(shù)后胃腸功能恢復(fù)及康復(fù)出院[10];(2)經(jīng)腹腔入路對腹腔內(nèi)臟、血管的損傷較大,術(shù)中需松懈、游離腹腔臟器(結(jié)腸、十二指腸)和血管(腎靜脈、腔靜脈等),極易增加術(shù)中出血量,而經(jīng)腹膜后入路背靠腎臟側(cè)平面游離,腎周圍脂肪較薄,更容易切除背外側(cè)腎腫瘤、外生型腫瘤以及小體積腫瘤,術(shù)中操作更加安全、高效,從而減少術(shù)中出血[11-12]。
本研究發(fā)現(xiàn),經(jīng)腹膜后和經(jīng)腹腔入路兩種手術(shù)方式術(shù)后并發(fā)癥率和腎功能均未出現(xiàn)明顯差異。盧依剛等[13]研究指出,經(jīng)腹腔入路操作空間相對更大,解剖標志和視野更為清晰,腫瘤定位相對更容易;而經(jīng)腹腔入路由于術(shù)中極易造成氣體進入腹膜腔,導(dǎo)致術(shù)中操作空間相對狹小,手術(shù)視野不及經(jīng)腹腔入路。但周子健等[14]指出,經(jīng)腹腔入路操作更能順應(yīng)腫瘤性狀,更容易解剖分離腎腫瘤假包膜周圍薄層,可快速電凝止血,以減少腎實質(zhì)損傷,保留正常腎實質(zhì)程度更佳,術(shù)后并發(fā)癥更少,更利于腎功能保留和恢復(fù)。本研究結(jié)果差異不明顯,原因可能是本研究屬于非前瞻性研究,且隨訪時間相對較短。
本研究中,治療3個月隨訪結(jié)果,上述兩種入路治療T1期腎腫瘤患者,兩組術(shù)后生活質(zhì)量水平雖較術(shù)前有明顯下降,但兩組術(shù)后生活質(zhì)量水平相同,究其原因可能在于兩種手術(shù)入路治療均會對腎功能造成一定影響,甚至部分患者存在術(shù)后腎功能不全情況發(fā)生,但兩種手術(shù)入路方式在改善短腎臟熱缺血時間及保護術(shù)后腎功能的結(jié)果相似,致使兩組患者在隨訪3個月后的生活質(zhì)量水平相似。
綜上,NSS腎部分切除術(shù)中無論經(jīng)腹腔入路還是經(jīng)腹膜后路治療,T1期腎腫瘤病人均能縮短腎臟熱缺血時間,最大程度保護術(shù)后腎臟功能,減少術(shù)后并發(fā)癥和提升術(shù)后生活質(zhì)量,但經(jīng)腹膜后路在縮短手術(shù)操作時間、減少術(shù)中出血量以及促進術(shù)后胃腸恢復(fù)和康復(fù)出院的方面優(yōu)于經(jīng)腹腔入路,臨床選擇不同入路仍需結(jié)合腫瘤分期、大小及位置等實際情況。

