25-羥維生素D與兒童腎母細胞瘤的相關性及對疾病預后的評估價值分析
趙莉 馬旭凱 劉玉 岳迎賓 嚴媚
(新疆醫科大學第一附屬醫院兒內一科,新疆烏魯木齊 830000)
腎母細胞瘤又被稱為Wilms瘤,是一種病理組織結構為混合型的惡性腫瘤,該疾病的發生與腎臟、胚胎的發育異常有關[1]。兒童腎母細胞瘤的發病高峰期為1~5歲,年發病率約為7/10萬。既往研究指出,新疆地區是我國兒童腎母細胞瘤高發地區,但是由于地區醫療水平及經濟水平的限制,導致兒童腎母細胞瘤早期診斷率偏低,大多數兒童首次就診時瘤體均較大,錯過最佳手術時機[2]。伴有遠處轉移、腫瘤分期為Ⅱ~Ⅳ期的兒童預后欠佳,而臨床上尚缺乏靈敏度與特異度較高的用于評估腎母細胞瘤預后的指標,故而尋找新的預后評估指標對腎母細胞瘤早期輔助診斷與治療具有十分重要的臨床意義[3]。25-羥維生素D [25-hydroxyvitamin D,25-(OH)D]是血液循環中維生素D的主要代謝物質,可以作為評估人體是否缺乏維生素D 的診斷指標。既往研究指出,高水平的25-(OH)D是膀胱癌、乳腺癌、直腸癌等癌癥的保護因素[4]。也有研究指出,25-(OH)D 與腎癌的發生存在相關性[5]。兒童缺乏25-(OH)D 不僅會導致佝僂病的發生,還會增加其他疾病的發生風險[6]。Bersanelli 等[7]學者指出,腎癌患者的25-(OH)D 水平顯著低于健康人群。但是不同學者納入的樣本量及地區不同,導致結論存在一定差異。關于25-(OH)D 與兒童腎母細胞瘤的相關性研究報道較少,尚未見將25-(OH)D 用于兒童腎母細胞瘤預后評估的報道。基于此,本研究著重探討25-(OH)D 與兒童腎母細胞瘤的相關性及對疾病預后的評估價值,為臨床上治療兒童腎母細胞瘤提供新的視角。
1 資料與方法
1.1 研究對象
回顧性選取我院2018 年1 月—2022 年12 月收治的腎母細胞瘤患兒50 例為腎母細胞瘤組,納入同期我院體檢的健康兒童50 例為健康對照組。腎母細胞瘤組中,根據患兒術后病理類型,分為預后良好亞組(不含有間變的腎母細胞瘤,n=38)和預后不良亞組(彌漫間變型和局灶型腎母細胞瘤,n=12)。所有患兒或患兒家屬均知曉該研究方案且簽署同意書,該方案通過我院倫理委員會的批準(批號:211129-01)。
納入標準:(1)術后或腎臟穿刺后經病理診斷為腎母細胞瘤;(2)依從性良好,接受手術、化學藥物治療(簡稱化療),且按期復查;(3)年齡28 d至14歲;(4)無其他惡性腫瘤史。
排除標準:(1)失訪;(2)伴有影響本研究數據的基礎疾病;(3)病情復雜更改治療方案者;(4)臨床病例資料不完整。
1.2 研究方法
收集患兒的一般資料,包括:年齡、性別、身高、體重、腫瘤直徑、腫瘤部位、腫瘤分期,以及實驗室檢查[血鈉、血磷、血鈣、血肌酐及25-(OH)D]。所有患兒均在抽血前3 d停止口服維生素D,血清學指標與25-(OH)D 檢測分別于治療前及化療治療后,清晨空腹狀態下抽取,送我院檢驗科,經乙二胺四乙酸抗凝處理后,3 000 r/min,離心10 min 后,取上層血清凍存于-80℃待測。采用電化學發光法檢測患兒血清中25-(OH)D 水平,離子選擇電極法比色法檢測血鈉、血磷、血鈣、血肌酐。試劑盒均購自美國R&D 公司,嚴格按照說明書的標準進行操作,控制批內差異<10%,批間差異<15%。25-(OH)D 水平中,低于12 ng/mL 為缺乏,12~20 ng/mL 為不足,大于20 ng/mL 為充足[8]。兒童腎母細胞瘤治療療效反應分度參照中國小兒腫瘤專業委員會兒童腎母細胞瘤診斷治療方案CCCG-WT-2019-12 修正,分為(1)完全反應:影像學及細胞形態學檢查未發現殘留病灶;(2)完全反應(不能完全確定):影像學殘留,但不能與術后變化或感染后等完全鑒別,臨床綜合分析不能確定為有腫瘤殘留;(3)部分反應:腫瘤最大徑減少至少30%;(4)進展:腫瘤最大徑增長20%;(5)帶病穩定:部分反應與進展之間,并維持30 d以上。
1.3 統計學分析
所有數據均采用Excel 收集整理。數據處理采用SPSS 26.0 統計學軟件。計數資料以例數和百分率(%)表示,組間比較采用χ2檢驗。正態分布計量資料以均數±標準差(±s)表示,兩組間比較采用兩樣本t檢驗。25-(OH)D水平與兒童腎母細胞瘤預后的相關性采用Spearman 秩相關分析。影響兒童腎母細胞瘤預后的危險因素采用多因素logistic 回歸分析。采用受試者操作特征曲線(receiver operating characteristic curve,ROC 曲線)進行診斷效果評價。以P<0.05 為差異具有統計學意義。
2 結果
2.1 腎母細胞瘤組與健康對照組的一般資料比較
腎母細胞瘤組與健康對照組性別、年齡、身高、體重,以及血鈉、血鈣、血磷水平比較差異無統計學意義(P>0.05);腎母細胞瘤組血肌酐、25-(OH)D水平低于健康對照組(P<0.05)。見表1。

表1 腎母細胞瘤組與健康對照組一般資料比較
2.2 預后良好亞組與預后不良亞組患兒的一般資料比較
預后良好亞組與預后不良亞組患兒的性別、年齡、身高、體重、腫瘤部位,以及血鈉、血鈣、血磷水平比較差異無統計學意義(P>0.05);預后不良亞組腫瘤直徑、腫瘤分期為Ⅲ~Ⅳ比例、轉移比例高于預后良好亞組,血肌酐、25-(OH)D 低于預后良好亞組(P<0.05)。見表2。
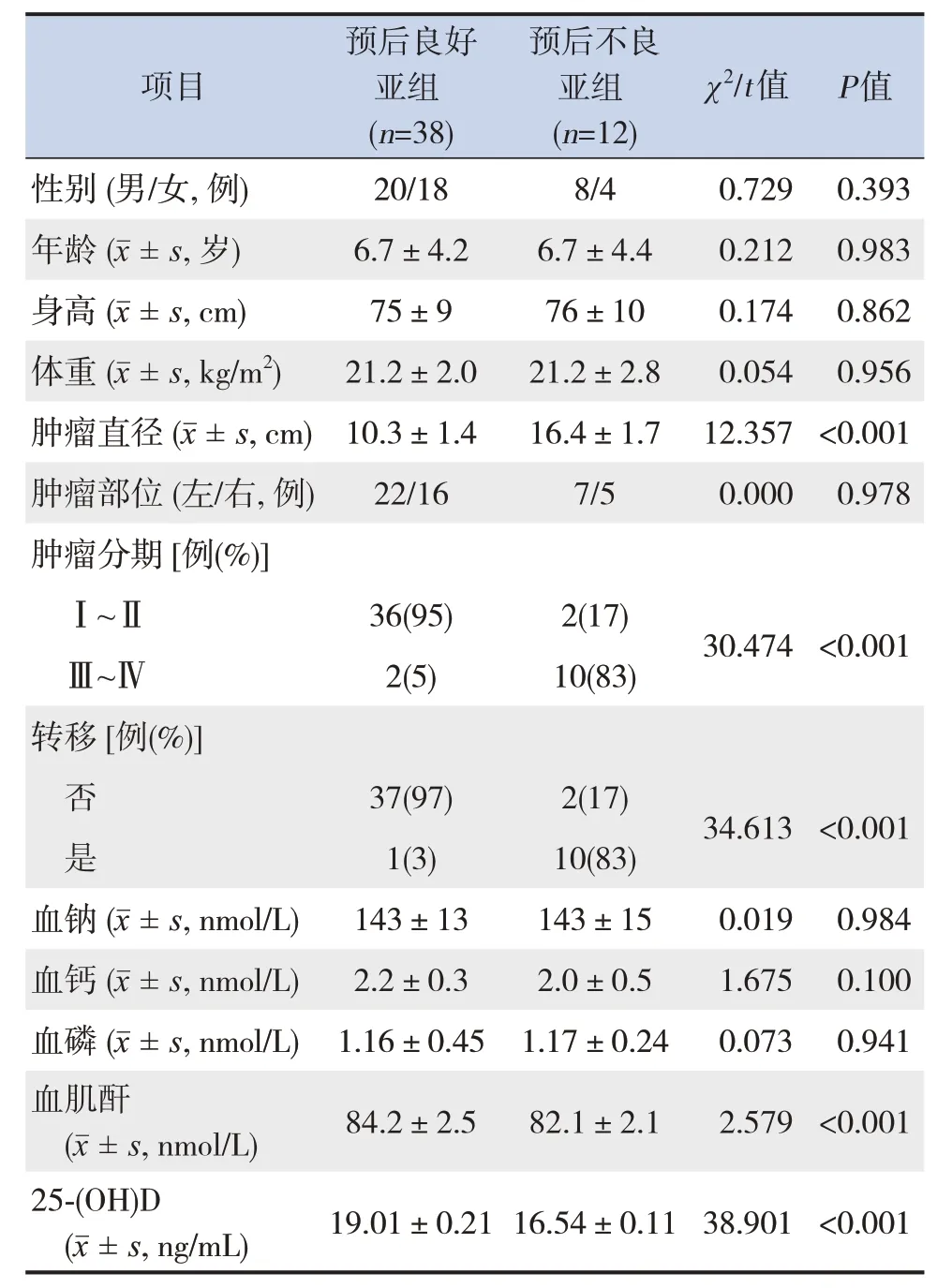
表2 腎母細胞瘤組中不同預后患兒的一般資料比較
2.3 血清25-(OH)D 水平與兒童腎母細胞瘤相關性分析
Spearman 秩相關分析顯示,血清25-(OH)D 水平與兒童腎母細胞瘤治療療效反應呈負相關(rs=-0.685,P<0.001),見圖1。
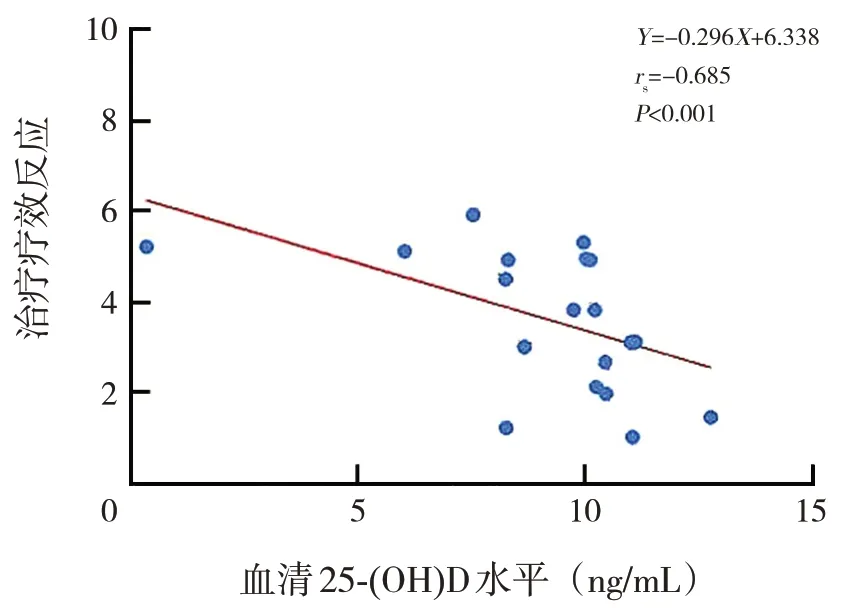
圖1 血清25-(OH)D水平與兒童腎母細胞瘤治療療效反應相關性分析圖 縱坐標表示兒童腎母細胞瘤治療療效反應分度,0~2分度:完全反應;2~4分度:完全反應(不能完全確定);4~6分度:部分反應;6~8分度:進展;8~10分度:帶病穩定。
2.4 影響兒童腎母細胞瘤預后的多因素logistic回歸分析
多因素logistic 回歸分析顯示,腫瘤直徑≥10 cm、腫瘤分期為Ⅲ~Ⅳ、存在轉移、25-(OH)D<19 ng/mL 與兒童腎母細胞瘤預后不良密切相關(P<0.05),見表3。
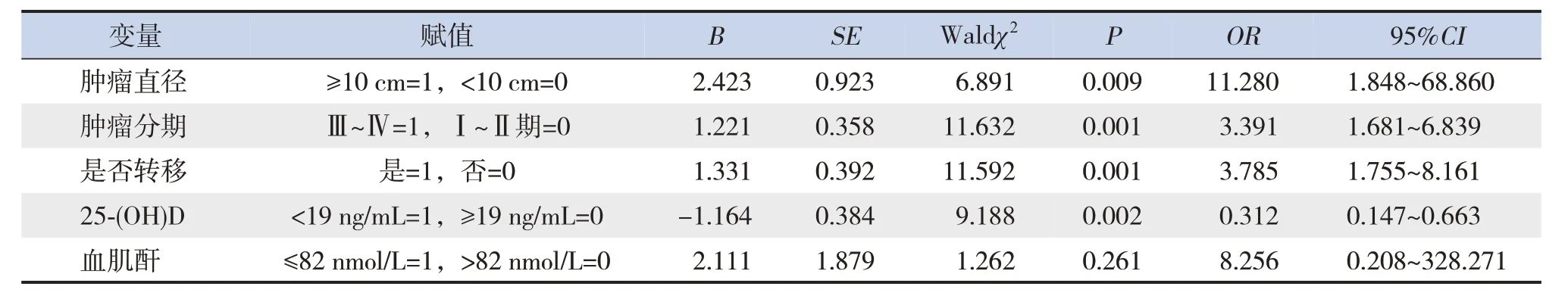
表3 影響兒童腎母細胞瘤預后的多因素logistic回歸分析
2.5 血清25-(OH)D 水平評估兒童腎母細胞瘤預后的ROC曲線
血清25-(OH)D 水平評估兒童腎母細胞瘤預后的 曲 線 下 面 積 為0.805 (95%CI:0.706~0.903,P<0.001),約登指數為0.512,最佳截斷值為1.764 ng/mL,靈敏度、特異度分別為0.938、0.575,陽性預測值、陰性預測值分別為0.638、0.920,見圖2。
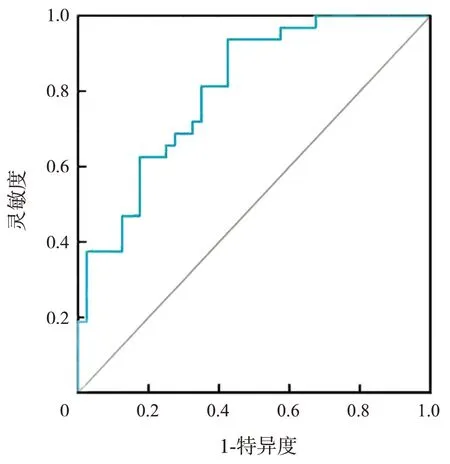
圖2 血清25-(OH)D水平評估兒童腎母細胞瘤預后的ROC曲線
3 討論
由于新疆地區醫療水平、經濟水平遠落后于我國經濟發達水平地區,導致兒童腎母細胞瘤的早期診斷與早期治療較為落后[9-10],極易造成漏診;且目前臨床上缺乏兒童腎母細胞瘤特異性診斷指標,導致早期確診率偏低,患兒極易錯過最佳診療時機[11]。目前,體內外的研究證實,25-(OH)D參與了腫瘤的增殖,在促進癌細胞凋亡、分化及抑制腫瘤血管侵犯中發揮了重要作用[12-13]。流行病學資料顯示,大多數國家與地區的人們普遍存在25-(OH)D 攝入不足的現象[14],且越來越多的研究指出,多種疾病、腫瘤的發生與25-(OH)D缺乏相關[15]。國內外已有多項基礎與臨床研究證實了25-(OH)D 能夠抑制腎癌的發展[16-20]。本研究中,腎母細胞瘤組血肌酐、25-(OH)D 水平低于健康對照組,25-(OH)D 具有免疫調節、抗炎和抗氧化活性作用,腎母細胞瘤患兒體內25-(OH)D 水平降低,可能與影響25-(OH)D 轉化為具有生物活性形式的1,25-(OH)2D 有關,且血清低25-(OH)D 狀態與腎母細胞瘤發生風險增加有關。
Nagakura 等[21]在1986 年開展了關于腎癌和維生素D關系的體外實驗,研究將維生素D加入人腎癌細胞株KU-2 中,發現維生素D 明顯抑制了腎癌細胞的增殖和集落形成。這也從側面證實了,低25-(OH)D 水平在一定程度上促進了腎母細胞瘤的發生與發展。而本研究中,預后良好與預后不良亞組患兒的25-(OH)D 水平存在顯著差異,這與患兒本身腫瘤直徑、腫瘤分期、是否轉移,以及腎功能水平有關,但是不可否認的是,25-(OH)D 一定程度抑制了兒童腎母細胞瘤的發生與發展。通過在體內、體外模型中驗證,25-(OH)D 可以有效地預防腎癌[22-23]。也有研究指出,25-(OH)D 有效地減小了腎癌腫瘤直徑[24]。結合上述學者及本研究結果,分析認為,骨化三醇是25-(OH)D 在體內轉化后的合成物,使得細胞周期處于停滯狀態,增加G0/G1 和G0 細胞數量,進而調節細胞周期蛋白依賴性激酶,有效地抑制促增殖信號分子,發揮抑制血管生成、誘導分化、調控表達,達到抑制兒童腎母細胞瘤的發生與發展的目的。
林光正等[25]對25-(OH)D與腎癌相關性進行分析,多因素logistic 回歸分析顯示25-(OH)D 及高血壓是影響腎癌發病的獨立危險因素。本研究顯示,血清25-(OH)D 水平與兒童腎母細胞瘤治療療效反應存在負相關。多因素logistic 回歸分析顯示,腫瘤直徑≥10 cm、腫瘤分期為Ⅲ~Ⅳ、存在轉移、25-(OH)D<19 ng/mL 是影響兒童腎母細胞瘤預后的獨立危險因素。ROC 曲線分析顯示,血清25-(OH)D 水平對兒童腎母細胞瘤預后評估有價值。25-(OH)D 可以通過多種機制調節腎母細胞瘤的發生發展,控制正常細胞避免轉化為癌細胞,而這種保護作用源于25-(OH)D 在體內的調節作用,在正常腎組織中,25-(OH)D 能夠與維生素D 受體激動劑干擾腎母細胞瘤細胞周期、分化和細胞凋亡,通過維生素D受體抑制細胞的生長與分化,進一步達到抑制腫瘤生長的目的。
綜上所述,25-(OH)D 水平與兒童腎母細胞瘤存在顯著相關性,25-(OH)D 水平可以作為兒童腎母細胞瘤輔助診斷指標之一,臨床上可以通過25-(OH)D水平綜合判斷患兒預后。受樣本量限制,本研究結果有待樣本量大的多中心試驗證實。
利益沖突聲明:所有作者均聲明不存在利益沖突。

