定向微孔鎂摻雜羥基磷灰石生物陶瓷降解及其生物學(xué)性能研究
趙雪妮,劉一佛,王鵬飛,魏森森,劉明玥,楊 智
(陜西科技大學(xué) 機電工程學(xué)院,陜西 西安 710021)
0 引言
人體骨骼具有很強的自我再生和重塑(舊骨吸收和新骨沉積)的能力,可以在受損后自發(fā)恢復(fù)其功能和結(jié)構(gòu).對于退行性骨疾病或較大的缺損,骨再生的要求超過了骨自發(fā)的自愈潛能,因此需要骨移植或骨替代材料來支持骨組織的再生[1,2].
理想的骨組織工程材料應(yīng)具有的特性是[3-5]:(1)具有良好的生物相容性和誘導(dǎo)成骨的能力,以支持細胞粘附、遷移和增殖,不產(chǎn)生免疫排斥作用;(2)具有生物活性,與宿主骨組織之間產(chǎn)生特殊的生物、化學(xué)反應(yīng),形成良好化學(xué)鍵合;(3)具有可控生物降解性,為了最終被宿主組織取代,支架需要在體內(nèi)降解為無毒產(chǎn)物,降解速度與植入部位的新組織生長速度相當;(4)具有類似松質(zhì)骨的高度互連的孔隙形態(tài)和結(jié)構(gòu),允許蛋白質(zhì)吸附,氧氣、營養(yǎng)物質(zhì)、信號分子的有效運輸和代謝廢物的移除,促進新骨組織向孔隙內(nèi)部長入.
孔隙的大小和形狀是決定骨缺損愈合的關(guān)鍵因素.研究發(fā)現(xiàn):孔徑尺寸為15≤d≤40 μm,允許纖維組織長入;孔徑為40≤d≤100 μm,允許非礦物類骨組織長入;d>100 μm,允許細胞穿透、血管和骨組織長入[6,7].微孔(d<10 μm)可以提供有效的營養(yǎng)物質(zhì)和成骨相關(guān)的信號分子,促進細胞和移植體之間的相互作用[8,9].因此獲得高度相似天然骨的孔隙結(jié)構(gòu),能夠在人體骨缺損修復(fù)中發(fā)揮重要作用.
本研究是在之前以CF(碳纖維)為造孔劑,制備微孔CF增強Mg摻雜HA(CF/Mg-HA)復(fù)合材料[10,11],為使材料更好地用于骨修復(fù)中,研究微孔Mg-HA材料體外生物相容性、降解性能,以及深入分析探討植入動物體內(nèi)后宿主骨組織的相互作用以及成骨機理.
1 實驗部分
1.1 實驗原料
直徑5~7 μm的CF購自日本東邦泰納克斯有限公司,六水硝酸鎂(Mg(NO3)2·6H2O)、四水硝酸鈣(Ca(NO3)2·4H2O)和磷酸氫二銨(NH4)2HPO4、氨水(NH4OH)國藥集團化學(xué)試劑有限公司,鹽酸(HCl)、濃硫酸(H2SO4)、濃硝酸(HNO3)購自國藥集團化學(xué)試劑有限公司.
1.2 Mg-HA粉體的制備
配置濃度為0.167 mol/L Ca(NO3)2·4H2O、0.05 mol/L Mg(NO3)2·6H2O和0.1 mol/L的(NH4)2HPO4水溶液.量取16.67 mL的Mg(NO3)2倒入到90 mL Ca(NO3)2溶液中,攪拌混合3~5 min,混合均勻后稱取100 mL的(NH4)2HPO4溶液逐滴加入混合溶液中.混合溶液pH穩(wěn)定后,加入氨水將PH值調(diào)整到10±0.02.將所得溶液倒入反應(yīng)釜中,在170 ℃下水熱反應(yīng)24 h至自然冷卻.隨后將反應(yīng)物溶液水洗三次,在80 ℃干燥4 h后,研磨得到Mg-HA粉體并干燥儲存.
1.3 CF/Mg-HA坯體的制備
連續(xù)CF分散成具有不同CF數(shù)量的纖維束(每束2根CF),CF束縱、橫交錯(正交)分布固定在銅版紙的指定位置.相鄰纖維束的距離設(shè)定為400 μm,獲得連續(xù)CF層.根據(jù)實驗所需的CF層數(shù)(10層)將的Mg-HA粉體和連續(xù)CF層銅版紙交替放置到模具中,獲得CF/Mg-HA坯體.
1.4 微孔Mg-HA生物陶瓷的制備
燒結(jié)工藝如圖1所示.具體過程為:將1.3節(jié)得到的連續(xù)CF/Mg-HA坯體放置到熱壓爐內(nèi)致密化燒結(jié),升溫至500 ℃開始施加30 MPa壓力,溫度900 ℃保溫30 min,然后降溫至500 ℃后,撤壓、隨爐冷卻,升溫和降溫速率均為10 ℃/min,獲得CF/Mg-HA復(fù)合材料.將連續(xù)CF/Mg-HA復(fù)合材料放置在微型箱式爐中,在600 ℃熱處理180 min,得到致密/微孔Mg-HA生物陶瓷

圖1 燒結(jié)工藝
1.5 表征與性能測試
1.5.1 體外降解性能測試
采用Tris-HCl(三羥甲基氨基甲烷鹽酸鹽)降解液浸泡法對HA、致密Mg-HA和微孔Mg-HA的降解性能進行表征.將試樣在37 ℃、pH=7.4的降解液中浸泡7~14天.隨后,取出試樣,用蒸餾水洗滌并在室溫下干燥.記錄浸泡前后試樣的質(zhì)量變化.采用掃描電子顯微鏡(SEM;AJEOL,JSM-6460)觀察HA、致密Mg-HA和微孔Mg-HA試樣在Trils-HCl緩沖液中浸泡7、14、28和56天的表面降解情況.提取浸泡后的上清液,檢測溶液pH值變化.通過ICP(電感耦合等離子體發(fā)射光譜儀)檢測濾液中離子釋放的濃度.
1.5.2 體內(nèi)成骨性能
選取體重為350±50 g的健康雄性大鼠10只作為實驗動物,對其進行麻醉和消毒處理.取后肢外側(cè)進行切口處理,切開皮膚、剝離骨膜,露出脛骨表面.用鉆頭(直徑:3 mm)垂直鉆出深度為3 mm的孔并植入材料,鹽水沖洗缺損部位逐層縫合,保持相同條件飼養(yǎng).
1.5.3 組織形態(tài)學(xué)分析
采用Micro-CT(Y.Cheetah,YXLON國際股份有限公司,德國)掃描脛骨標本,觀察骨組織-生物材料界面及生物材料周圍新生骨的生長情況.采用VG Studio2.1V分析骨體積密度(BV/TV)、骨小梁厚度(Tb.Th)、骨小梁數(shù)目(Tb.N)和骨小梁間距(Tb.Sp).對帶有植入物的脛骨組織標本在甲醛溶液中浸泡24 h進行固定,依次使用80%無水乙醇、丙酮和95%無水乙醇,進行脫水.處理后采用甲基丙烯酸甲酯(PMMA)進行包埋.用硬組織切片機(Leica SP1600)沿著樣品最大截面處(移植體軸向)切割組織標本,切片厚度約50~80 μm.將切片在研磨機上用砂紙打磨,得到大約30 μm的硬組織切片,進行Picric acid酸性復(fù)紅(Van Gieson,VG)和蘇木精-伊紅染色法(hematoxylin-eosin staining,HE)染色,用光學(xué)顯微鏡(OLYPUS,IX73)觀察并采集染色后圖像.
2 結(jié)果與討論
2.1 HA、致密/微孔Mg-HA陶瓷的體外降解性能
不同材料的質(zhì)量變化如圖2(a)顯示,三種材料在浸泡期間都逐漸降解,HA的質(zhì)量在浸泡7~28天內(nèi)幾乎沒有顯著改變,直至浸泡56天后,HA的質(zhì)量減少了0.59%.而致密Mg-HA和微孔Mg-HA在開始浸泡的7~14天內(nèi)質(zhì)量也無顯著變化,在浸泡28天的質(zhì)量分別減少了0.59%和1.096%,微孔Mg-HA的質(zhì)量損失是致密Mg-HA的2倍左右,是HA質(zhì)量損失的856.25%.隨著浸泡時間的延長(至56天后),微孔Mg-HA的質(zhì)量減少提高到2.74%,分別比致密Mg-HA和HA質(zhì)量損失率提高了43.3%和364.41%,呈現(xiàn)出最快的降解速率.
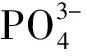

圖2 微孔Mg-HA、致密Mg-HA和HA在Trils-HCl中浸泡不同時間的質(zhì)量變化(a)及離子變化(b-c)
2.2 微觀形貌分析
HA、致密Mg-HA、和微孔Mg-HA浸泡7、14、28和56天后的表面微觀形貌如圖3~6所示.如圖所示,所有樣品都不同程度的降解.HA在浸泡0~28天材料表面可以觀察到輕微的降解.由于材料的溶解,在其表面形成大片微小的凹痕.隨著浸泡時間的延長,表面變得更加粗糙,到56天后HA表面可見一些分散的碎片,降解加劇.而致密Mg-HA和微孔Mg-HA在浸泡14天時材料表面就觀察到明顯的凹坑和縫隙,微孔Mg-HA的孔隙區(qū)域(黃色箭頭)溶解速率明顯快于基體區(qū)域.隨著浸泡時間的延長材料降解越明顯,直到56天后微孔Mg-HA的孔壁和基體區(qū)域都可以觀察到一些降解后的小碎屑.

圖3 Trils-HCl溶液中浸泡7天的SEM圖

圖4 Trils-HCl溶液中浸泡14天的SEM圖

圖5 Trils-HCl溶液中浸泡28天的SEM圖

圖6 Trils-HCl溶液中浸泡56天的SEM圖
2.3 HA、致密/微孔Mg-HA陶瓷的體內(nèi)降解性能


圖7 植入大鼠脛骨缺損部位8周后試樣的Micro-CT三維重建圖
2.4 HA、致密/微孔Mg-HA陶瓷的體內(nèi)成骨性能
植入大鼠脛骨8周后的三維重建和位矢圖如圖8~10所示.材料牢固的固定在脛骨內(nèi),沒有松動和脫出的現(xiàn)象產(chǎn)生,圖中白色區(qū)域是φ3×3 mm的試樣,黃色區(qū)域代表新生骨組織(選擇的感興趣區(qū)域為:樣品表面100 μm以內(nèi)).各實驗組的骨缺損區(qū)域可明顯觀察到更均勻致密的一層黃色新生骨,且新生骨組織與移植體骨界面緊密結(jié)合.從三種樣品(去除材料和骨組織)新生骨的位矢圖中可以看出微孔Mg-HA的新生骨量明顯高于致密Mg-HA組和HA組,而HA組黃色區(qū)較稀薄,新生骨量最低.微孔Mg-HA組和致密Mg-HA組的新生骨量之間沒有顯著差異,但明顯高于HA組,這表明8周之后骨愈合程度顯著.

圖8 HA植入大鼠脛骨缺損部位8周后的Micro-CT三維重建圖

圖9 致密Mg-HA植入大鼠脛骨缺損部位8周后的Micro-CT三維重建圖

圖10 微孔Mg-HA植入大鼠脛骨缺損部位8周后的Micro-CT三維重建圖
植入脛骨8周后骨缺損區(qū)的3D重建形態(tài)計量學(xué)分析結(jié)果如圖11所示.HA、致密Mg-HA和微孔Mg-HA植入8周后的骨體積密度(BV/TV)分別為27.55%、32.5%和40.5%,微孔Mg-HA和致密Mg-HA的骨體積密度分別比HA高23.18%和40.14%.表明Mg2+的摻雜以及微孔道的引入明顯提高了材料的成骨能力,且植入8周后微孔Mg-HA顯示出最好的成骨愈合情況.營養(yǎng)物質(zhì)和成骨誘導(dǎo)因子等可以通過的微孔(5~14 μm)有效地輸送到新骨生長的缺損區(qū)域[15,16].因此,微孔Mg-HA的成骨誘導(dǎo)效果優(yōu)于致密Mg-HA和HA.三種材料的骨小梁數(shù)目(Tb.N)沒有顯著變化,而微孔Mg-HA的骨小梁間距(Tb.Th)是低于HA和致密Mg-HA.

圖11 骨缺損區(qū)的3D重建形態(tài)計量學(xué)分析結(jié)果
2.5 組織形態(tài)學(xué)分析
植入大鼠脛骨缺損部位8周的HA、致密Mg-HA、微孔Mg-HA的切片進行HE染色,結(jié)果如圖12所示.HA植入體與骨組織之間有明顯的間隙存在,而致密Mg-HA的間隙明顯比HA小,微孔Mg-HA植入體與宿主骨結(jié)合緊密.放大圖中,對于致密Mg-HA和微孔Mg-HA,可見清晰纖維組織和新生骨組織沿著材料周圍生長,而HA的宿主骨組織附近觀察到較少新生骨的形成.

圖12 HA、致密Mg-HA、微孔Mg-HA植入8周的HE染色圖
VG染色如圖13所示,可以觀察到新生骨的形態(tài)及植入體與骨組織的界面與HE染色圖片結(jié)果相似,HA在植入8周后與宿主骨組織之間觀察到較大的間隙,而致密Mg-HA和微孔Mg-HA與新骨組織緊密結(jié)合,沿著植入體表面生長著紅色的新骨組織,其中微孔Mg-HA周圍新生骨組織較其它兩組最多.在植入體-宿主骨界面沒有觀察到炎癥細胞和慢性炎癥反應(yīng),骨愈合情況良好.

圖13 HA、致密Mg-HA、微孔Mg-HA植入8周的VG染色圖
綜合考慮陽性細胞百分率和陽性染色程度等評價陽性表達的兩個因素,運用Image-Pro Plus圖像處理軟件計算HA、致密/微孔Mg-HA積分光密度(IOD)和圖像面積.推導(dǎo)陽性水平指數(shù)(positive level index,PLI)的計算公式,即陽性水平指數(shù)(PLI)=陽性細胞百分率×平均光密度(AOD),作為定量分析的指標[17,18].
通過表1、表2對比發(fā)現(xiàn),陽性水平指數(shù) PLI 的大小排序如下:HA <致密Mg-HA<微孔Mg-HA,這與實際的Micro-CT三維重建結(jié)果基本相吻合.個別染色出現(xiàn)的偏差是由于PLI參數(shù)的計算取決于很多因素,著色程度不僅取決于樣本的含量和分布密度,還與樣本的敏感性、切片厚度、顯色時間等多種技術(shù)因素有關(guān)[19,20].

表1 HE染色基于組合參數(shù)的分析結(jié)果

表2 VG染色基于組合參數(shù)的分析結(jié)果
2.6 成骨機制
微孔道對骨修復(fù)和骨重塑的影響機制如圖14所示.在骨修復(fù)和重建過程中,生理液體中有關(guān)的各種細胞(破骨細胞、成骨細胞等)、內(nèi)源性骨誘導(dǎo)生物分子、其他生物因子和一些營養(yǎng)物質(zhì)(蛋白質(zhì)、維生素等)在微孔的毛細作用力下被動遷移滲透到微孔中,通過連通的孔道運輸?shù)绞軗p傷部位[21,22].微孔道也可以為各種生物分子和生長因子提供出儲存空間,事實上,雖然人們普遍認為骨只能在100 μm或更大的大孔中生長,然而研究表明,在材料的微孔中也存在骨成分,即膠原、類骨質(zhì)、細胞或骨礦物質(zhì)[23].此外,在重建階段,當移植體被破骨細胞和相關(guān)細胞因子降解時會釋放大量鎂、鈣和磷酸鹽離子,這些離子不僅為新骨的生成提供原料,也可以調(diào)節(jié)成骨細胞表型,促進骨橋蛋白的表達,刺激局部新骨形成.

圖14 微孔Mg-HA中微孔道的成骨機制
3 結(jié)論
本研究通過熱壓燒結(jié)結(jié)合造孔熱處理工藝實現(xiàn)定向微孔Mg-HA生物陶瓷的制備,依次研究體內(nèi)外降解性能、體內(nèi)成骨性能及成骨機制,結(jié)論如下:
(1)微孔Mg-HA在大鼠體內(nèi)植入8周后,材料發(fā)生了明顯降解,表面的凹坑數(shù)目顯著增加.在體外Trils-HCl緩沖液中浸泡28天后,微孔Mg-HA的質(zhì)量損失是致密Mg-HA的2倍左右,是HA質(zhì)量損失率的856.25%.浸泡56天后,微孔Mg-HA的質(zhì)量減少量顯著提高,分別比致密Mg-HA和HA質(zhì)量損失率提高了43.3%和364.41%,含有微孔道的Mg-HA呈現(xiàn)出最快的降解速率.
(2)微孔Mg-HA和致密Mg-HA的骨體積密度分別比HA高23.18%和40.14%,具有微孔通道的Mg-HA呈現(xiàn)出最好的成骨能力.
(3)微孔Mg-HA生物陶瓷植入動物骨缺損部位后,骨組織與植入體緊密結(jié)合,無間隙并沿著材料表面生長,表明該材料具有較好的成骨性能,作為骨修復(fù)材料具有廣闊的應(yīng)用前景.

