急性食管靜脈曲張出血經內鏡下套扎術治療后再出血的危險因素分析
王紅梅 葉長根 梁 斌 楊智軍 劉佳興
江西省贛州市第五人民醫院消化內科,江西贛州 341000
盡管近年來急性靜脈曲張出血(acute variceal hemorrhage,AVH)導致肝硬化患者的病死率有所改善,但它的6周病死率仍達15%~20%[1]。此外,AVH的再出血率和不良事件發生率高于非AVH患者,如潰瘍出血[2]。據報道,在AVH第一次發作后的前6周內,早期再出血率為30%~40%[3],第一年再出血率可達60%[4]。AVH是一種緊急情況,需要使用血管活性藥物、抗生素、輸血和靜脈曲張結扎進行治療[5]。最近一項meta分析稱,內鏡下靜脈曲張套扎術(endoscopic variceal ligation,EVL)在減少再出血率、不良結局等方面優于內鏡下靜脈曲張硬化注射術[2]。然而,EVL治療AVH后的長期預后等相關報道目前較少。因此,本研究通過長期隨訪,旨在探討急性食管靜脈曲張出血(acute esophageal variceal hemorrhage,AEVH)患者接受EVL治療后的長期結局以及再出血的危險因素。
1 資料與方法
1.1 一般資料
回顧性分析2015年2月至2018年3月在贛州市第五人民醫院收治的140例均診斷為AEVH且行EVL治療的患者。納入標準:①經活檢證實或具有明顯臨床證據的肝硬化;②既往無靜脈曲張出血預防措施;③無脾切除手術史。排除標準:①首次EVL治療后隨訪時間不足3年或患者自覺退出;②胃腸道出血;③胃底靜脈曲張出血。本研究經醫院醫學倫理委員會通過。
1.2 方法
采用EVL治療時主要檢查在出血發生率最高的食管遠端5~7 cm區域。如果患者的血紅蛋白(Hb)水平低于7 g/dL,則建議輸血,目標水平為7~9 g/dL。此外,所有患者均以1 g/d的劑量靜滴注射用頭孢曲松鈉(齊魯制藥有限公司,國藥準字H37020573),最多給藥1周。盡早開始使用血管收縮劑,每4~8小時靜脈注射1~2 mg去氨加壓素注射液(深圳翰宇藥業股份有限公司,國藥準字H20064093)。
1.3 觀察指標
患者入院時記錄以下臨床資料:性別、年齡、肝功能分級、并發癥(慢性腎病或肝癌)、Hb值和肝硬化病因學等。內鏡檢查記錄紅色征是否陽性、靜脈曲張類型和曲張位置。所有患者均隨訪3年或直至死亡,主要觀察指標為再出血和死亡的原因以及每位入組者的EVL隨訪情況。
1.4 診斷標準
中、大型食管靜脈曲張分別被定義為直徑為3~5 mm和>5 mm的管狀靜脈通道[6]。再出血被定義為出院后發生明顯的胃腸道出血,生命體征不穩定[(收縮壓≤90 mmHg(1 mmHg=0.133 kPa)或脈搏≥110 bpm]、Hb顯著下降、需要輸血或經內鏡證實的胃腸道出血。由于臨床懷疑再出血可能需要再次內鏡檢查,因此本研究在再出血的定義中納入了其他消化道出血,如消化性潰瘍病、食管潰瘍和Mallory-Weiss綜合征等。
1.5 統計學方法
所得數據采用SPSS 23.0統計學軟件進行處理。計量資料用均數±標準差()表示,行t檢驗;計數資料用[n(%)]表示,行χ2檢驗或Fisher確切概率法;多因素分析采用logistic回歸模型。P< 0.05為差異有統計學意義。
2 結果
2.1 患者一般資料分析
本研究中男99例,女41例,平均年齡(55.41±9.83)歲,≥65歲者34例(24.29%)。患者的肝功能按Child-Pugh分級:A級20例(14.29%),B級64例(45.71%),C級56例(40%)。患 者合并慢性腎病者27例(19.29%),合并肝癌者25例(17.86%)。患者入院時的平均Hb為(99.33±29.62)g/L,發現97例(69.29%)有病毒感染,EVL發現紅色征者65例(46.43%),大型靜脈曲張者125例(89.29%),靜脈曲張位于食管下部者68例(48.57%)。
2.2 EVL后再出血及死亡原因分析
隨訪截止,29.29%(41例)的患者發生再出血,主要為食管靜脈曲張27例(65.85%),消化性潰瘍7例(17.07%)。39.29%(55例)的患者發生死亡,其中15例(27.27%)為食管靜脈曲張出血,12例(21.82%)因肝衰竭死亡,見表1。
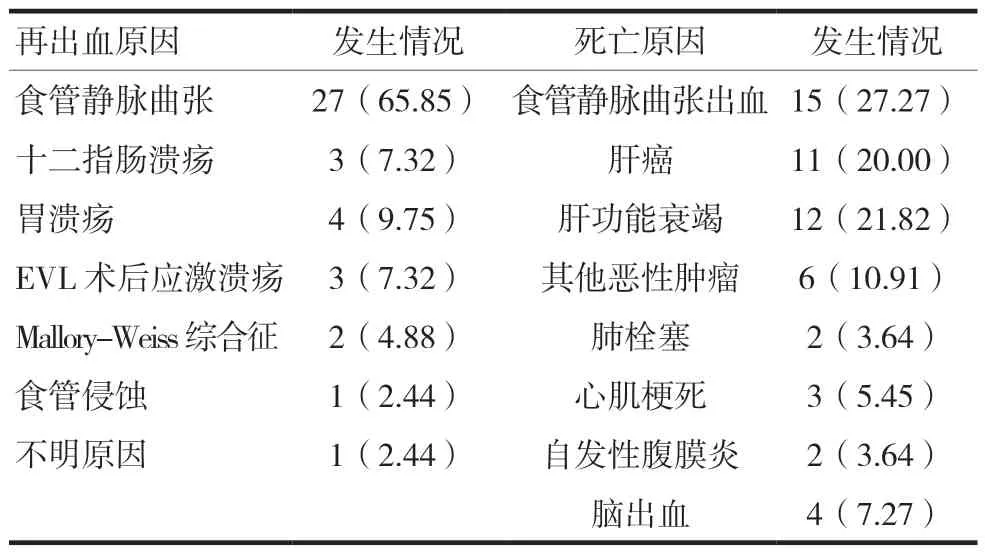
表1 EVL后再出血及死亡原因統計[n(%)]
2.3 EVL后再出血的單因素分析
單因素分析顯示,患者的性別、年齡、肝功能Child-Pugh分級、靜脈曲張類型以及EVL隨訪與再出血發生相關,差異有統計學意義(P< 0.05),而其他參數與再出血無明顯相關性,見表2。

表2 EVL后再出血的單因素分析
2.4 EVL后再出血的多因素分析
以是否發生EVL后再出血為因變量,與單因素分析有相關性的5項危險因素為自變量(賦值見表3)。logistic回歸分析顯示,肝功能Child C級(OR=3.793)、大型靜脈曲張(OR=2.592)、未EVL隨訪(OR=4.813)與患者發生再出血具有相關性,是其獨立危險因素(P< 0.05)。見表4。

表3 EVL后再出血的賦值說明
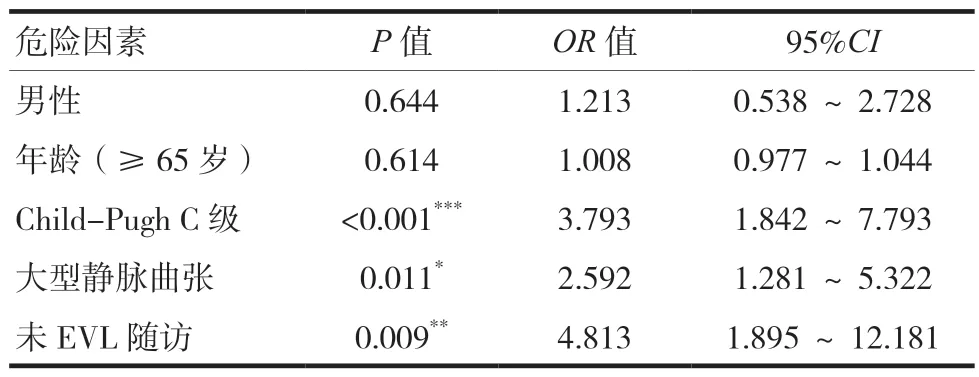
表4 EVL后再出血的Logistic回歸分析
3 討論
本研究結果表明,AEVH患者行EVL治療后發生再出血是一種相當常見的并發癥,本研究有29.29%的患者發生再出血,且3年病死率為39.29%,食管靜脈曲張出血是其主要原因。在前人的研究中,AEVH再出血率差異較大。在對128例患者進行平均17.3個月的隨訪后,Lopes等[7]報道了38.4%的患者出現反復出血,肝功能Child C級的患者發生再出血和死亡患者則更常見。最近的一項對174例行EVL治療的患者進行隊列研究顯示,1年累積再出血率和病死率分別為30%和26.6%。而在一項回顧性隊列研究中,Cho等[8]發現在患者首次出血后行EVL治療的2年內,AEVH再出血率明顯更低(4.6%),EVL是曲張患者的有效治療手段。
本研究中,肝功能Child-Pugh C級是3年內肝硬化患者再出血的獨立危險因素,這一發現與其他研究相一致。事實上,Child-Pugh分級被證實為早期治療AEVH患者失敗的不良預后指標[9]。因此,肝損傷的嚴重程度是出血復發的重要預測因素,這也得到了其他研究者的支持,他們認為終末期肝病模型預示著患者再出血[10]。雖然這些研究關注的是患者的早期結局,但與本研究結果是相似的,表明肝臟狀況是患者短期和長期復發出血的預后指標。
有研究表明,食管靜脈曲張類型及紅色征對再出血風險具有良好的預測價值[11]。與此相似的是,本研究單因素及多因素分析顯示,小中靜脈曲張的患者比大靜脈曲張患者更容易根除,曲張類型大小是患者再出血的獨立危險因素。本研究的另一個重要發現是,在未進行內鏡隨訪的情況下,患者再出血率較高(70%),未進行二次EVL是患者再出血的獨立風險,這一結果強調了對肝硬化患者進行內鏡隨訪的必要性。目前的指南建議在控制靜脈曲張出血急性發作后重復內鏡檢查,直到靜脈曲張被根除;之后,內鏡篩查應在食管靜脈曲張根除后1~3個月進行,并在6~12個月時再次篩查以檢測出血是否復發[12]。
國內關于EVL后再出血的危險因素研究較為廣泛。張妍等[13]認為,伴發門靜脈血栓、大量腹水及肝功能Child-Pugh C級是內鏡治療術后早期再出血的獨立危險因素。黃超等[14]的研究表明,國際標準化比值、Hb值、套扎數量是首次EVL術后早期再出血的單獨預測指標。黃理等[15]的一項多因素logistic回歸分析顯示,曲張靜脈數量、白蛋白、套扎點數、血鈉及脾臟厚度是EVL治療后早期再出血的獨立影響因素。而姬翠英[16]認為凝血酶原時間、大量腹水、門靜脈血栓形成、術后未應用普萘洛爾是EVL術后早期再出血的獨立危險因素。陳斯陽[17]的多因素分析顯示,存在大量腹水、凝血酶原時間延長、Child分級C以及低蛋白血癥為EVL術后早期再出血發生的共同獨立危險因素。以上與本研究有所不同,其研究對象均為肝硬化伴食管靜脈曲張患者,而無論有無AEVH,且觀察時間均為EVL術后6周內,也未對再出血原因進行分析。而與本研究更為契合的一項以178例乙肝肝硬化并發食管靜脈曲張破裂出血的患者為研究對象,通過EVL術后隨訪12~54個月建立的Cox風險模型分析顯示,Child-Pugh分級、腹水、糖化血紅蛋白、空腹血糖水平和肝性糖尿病是EVL術后再出血的獨立影響因素[18]。
綜上所述,AEVH患者EVL術后反復出血是一種較為常見的并發癥,顯著增加了患者的病死率。除了缺乏EVL隨訪和食管靜脈曲張類型之外,由Child-Pugh分級評估的肝臟狀況是這些患者再出血的獨立預后指標。因此建議在內鏡下對出血性食管靜脈曲張患者進行初步治療后進行密切隨訪,尤應注意終末期肝病和大靜脈曲張患者。

