對苯二甲酸乙二醇酯二聚體水/醇/氨解機理的理論研究
周 梅,李思佳,徐瑋峰,黃金保,羅小松,吳 雷
(貴州民族大學物理與機電工程學院, 貴陽 550025)
0 前言
聚對苯二甲酸乙二醇酯(PET)作為常用的熱塑性塑料之一,由于其具有優異的熱穩定性和耐磨性等性質,被廣泛應用于日常生活和食品包裝等各領域,給人們的日常生活帶來了極大的便利[1?4]。然而,PET塑料的大量生產和使用造成了PET塑料垃圾的數量急劇增加。PET廢塑料具有高穩定和耐腐蝕等特性,使其在不受外界因素影響的情況下難以降解[5],這不僅嚴重污染環境,同時還造成了資源浪費[6?8]。因此,有效回收利用廢塑料PET,對保護環境和節約資源具有重要意義。熱解是一種在無氧環境下使高分子聚合物發生裂解的熱化學轉化技術[9?11],被廣泛應用于聚合物的回收循環利用。聚合物熱解轉化成小分子化合物的過程需要較高的溫度,所形成的產物組分復雜,廢塑料原料回收利用的成本較高[12]。如果適當改變降解環境能夠有效控制聚合物降解過程中的產物組分和分布及降低熱解過程的能耗,則對有價值的化工產品具有較高選擇性[13?14]。水是自然界中最重要的溶劑,它來源廣泛且無毒,最后甚至無需從產物中除去,可代替那些易揮發和有毒的溶劑作為反應介質,以減少對環境造成污染[15]。甲醇作為分解反應的介質,具有反應條件溫和與分解反應相對完全等優點[16]。氨氣是一種還原性氣體,氨氣的存在會促進高分子主鏈酯鍵中的酰氧鍵位置發生斷裂形成端羥基的中間體[17]。因此,對PET廢棄物進行水/醇/氨解被認為是回收和高效利用PET塑料的可行方案。
目前對于PET水/醇/氨解已有較多的相關實驗研究[18?21]。Yoshioka 等[22]研究了 PET 固體顆粒在硝酸(HNO3)水溶液下于70~100 ℃反應溫度的常溫解聚情況,實驗結果表明,PET固體顆粒的尺寸與表觀速率成反比,反應活化能為 101.3 kJ/mol。Liu 等[23]研究了PET與正丁醇的醇解反應,結果表明,PET醇解反應生成了對苯二甲酸二丁酯與乙二醇等產物。楊華光等[24]通過金屬功能化離子液體催化PET胺解反應的研究表明,PET氨解能夠生成相應的對苯二甲酸二酰胺與乙二醇。姚浩余等[25]通過研究PET醇解協同催化體系的反應機理,獲得了PET在氧化鋅(ZnO)不同界面的作用機制及催化PET醇解的一級反應動力學,實驗結果表明,其表觀活化能為215.9 kJ/mol。
與實驗研究相比,通過量子化學方法進行理論研究可以更加詳細地詮釋PET水/醇/氨解反應過程及產物形成演化機理。然而,從分子層面對PET進行水/醇/氨解反應機理的理論研究鮮有報道。PET塑料是由對苯二甲酸與乙二醇縮聚而成具有酯鍵的高分子聚合物,對高分子聚合物的微觀機理通常采用各種模型化合物來研究,因此,本文采用密度泛函理論方法對二聚體的水/醇/氨解進行了理論研究,對水/醇/氨解可能反應路徑進行了熱力學計算與分析。從微觀上深入地研究對苯二甲酸乙二醇酯二聚體水/醇/氨解機理,對PET廢棄物的能源轉化回收利用技術具有重要的理論指導意義。
1 計算方法
所有計算均在Gaussian 09版程序中[26]完成,蒙含仙等[27]通過選取B3P86、M06?2X、B3LYP和BHandH?LYP等密度泛函方法對PET模型化合物鍵離能進行了理論計算研究,結果表明,B3P86和M06?2X方法比B3LYP和BHandHLYP方法計算PET模型化合物更加準確,且B3P86方法計算PET模型化合物鍵離能值總體上要低于M06?2X方法,最后選用B3P86密度泛函方法對PET模型化合物鍵離能以及PET熱降解機理[28]進行了理論研究。因此本文采用密度泛函理論B3P86/6?31++G(d,p)方法對參與反應的反應物、過渡態、中間體以及產物進行頻率分析和幾何結構優化。在同一計算水平上進行頻率計算以獲得標況下(273.15 K、101 kPa)的熱力學參數值。對熱力學量考慮了零點振動能(ZPE)校正。通過GaussView程序直接觀測或內稟反應坐標(IRC)計算進行驗證,確定反應物、中間體和產物的振動頻率均為正,過渡態有且只有一個虛頻。把標況下的過渡態與反應物的焓值能量差作為反應活化能,生成物與反應物的焓值(自由能值)能量差作為反應焓變(自由能變)。對于自由基反應,鍵離能近似為活化能。鍵離能的計算公式如式(1)所示[29?30]:

式中 BDE——考慮零點能修正后的鍵離能,kJ/mol
E——分子能量,kJ/mol
EZP——零點能,kJ/mol
2 結果與討論
2.1 對苯二甲酸乙二醇酯二聚體水解機理
PET水解相關研究文獻[31?33]表明PET水解主要通過主鏈酯鍵中酰氧鍵位置發生協同反應機理進行,因此本文主要對對苯二甲酸乙二醇酯二聚體主鏈酯鍵中酰氧鍵位置考慮了三條通過四元環過渡態進行的協同反應機理,并對對苯二甲酸乙二醇酯二聚體水解的可能反應路徑進行設計以及熱力學動力學計算與分析。對苯二甲酸乙二醇酯二聚體水解可能的反應路徑、反應能壘及主鏈酯鍵中酰氧位置初始裂解過渡態優化結構分別如圖1~3所示。
在反應路徑(1)中(如圖1所示),路徑(1?a)中,化合物1和H2O經過四元環過渡態TS1生成對苯二甲酸2和化合物3,該過程需要克服169.2 kJ/mol的勢壘,吸收5.2 kJ/mol較低的熱量。TS1的優化結構如圖3所示,反應前單獨優化水分子中的O—H鍵長為0.960 ?,對苯二甲酸乙二醇酯二聚體中酰氧鍵(C(4)—O(5))鍵長為1.341 ?,反應中過渡態TS1的O—H鍵長變為1.178 ?,酰氧鍵(C(4)—O(5))鍵長變為1.747 ?,從TS1的優化結構中可以看出,水分子的羥基(—OH)結合羰基中的碳原子C(4)形成對苯二甲酸,而氫原子結合乙烷基上的O(5)形成羥基端的化合物。化合物3可通過TS2水解生成乙二醇4和對苯二甲酸乙二醇酯5,其反應能壘為170.7 kJ/mol。對苯二甲酸乙二醇酯進一步經TS3降解形成PET主要產物[31?32]對苯二甲酸和乙二醇4。路徑(1?b)中,化合物1也可經過中間四元環過渡態TS4水解形成對苯二甲酸乙二醇酯,反應能壘為169.3 kJ/mol。路徑(1?c)中,化合物1可經過TS5裂解形成乙二醇和化合物6,該反應能壘為170.2 kJ/mol,化合物6可進一步通過TS6發生水解反應生成對苯二甲酸和對苯二甲酸乙二醇酯,該反應能壘為169.1 kJ/mol。

圖1 對苯二甲酸乙二醇酯二聚體水解可能反應路徑Fig.1 Possible reaction paths for ethylene terephthalate dimer hydrolysis

圖3 對苯二甲酸乙二醇酯二聚體初始水解過渡態優化結構Fig.3 Initial hydrolysis transition state optimization structure of ethylene terephthalate dimer
對對苯二甲酸乙二醇酯二聚體水解反應路徑的反應能壘進行對比分析可知,對苯二甲酸乙二醇酯二聚體主鏈中間和末端酯鍵中酰氧鍵位置水解的速控步反應能壘相差較小,分別為169.2、169.3、170.2 kJ/mol,這表明對苯二甲酸乙二醇酯二聚體水解反應可能是對苯二甲酸乙二醇酯二聚體主鏈隨機位置酯鍵中酰氧鍵發生多次裂解,最終形成對苯二甲酸和乙二醇等主要產物,這與相關PET水解實驗研究結果[32?35]相符。

圖2 對苯二甲酸乙二醇酯二聚體水解反應能壘Fig.2 Energy barrier of ethylene terephthalate dimer hydrolysis reaction
2.2 對苯二甲酸乙二醇酯二聚體醇解機理
基于PET水解實驗反應機理及相關醇解實驗文獻[36?40],本節對對苯二甲酸乙二醇酯二聚體醇解反應設計了3條可能的反應路徑。圖4~6分別描述了對苯二甲酸乙二醇酯二聚體醇解的可能反應路徑和相應的反應能壘以及初始降解過渡態優化結構。
在反應路徑(2)中(如圖4所示),路徑(2?a)中,化合物1和CH3OH經過四元環過渡態TS7生成對苯二甲酸單甲酯7和化合物3,該過程需要克服155.2 kJ/mol的勢壘。TS7的優化結構如圖6所示,反應前單獨優化甲醇分子中的O—H鍵長為0.960 ?,對苯二甲酸乙二醇酯二聚體中酰氧鍵(C(4)—O(5))鍵長為1.341 ?,反應中過渡態TS7的O—H鍵長變為1.171 ?,酰氧鍵(C(4)—O(5))鍵長變為1.765 ?,從TS7的優化結構中能夠看出,甲醇分子的甲氧(—OCH3)基結合羰基中的碳原子C(4)形成對苯二甲酸單甲酯,而氫原子結合乙烷基上的O(5)形成羥基端的化合物。化合物進一步通過TS8醇解生成乙二醇4和化合物8,反應能壘為156.9 kJ/mol。化合物8經TS9生成PET醇解主要產物乙二醇和對苯二甲酸二甲酯9,其過程需克服的勢壘為156.9 kJ/mol。在路徑(2?b)中,化合物1能夠通過TS10生成化合物8和對苯二甲酸乙二醇酯5,對苯二甲酸乙二醇酯進一經TS11醇解形成對苯二甲酸單甲酯和乙二醇,上述過程的反應能壘分別為155.3、156.4 kJ/mol。在路徑(2?c)中,化合物1和CH3OH通過TS12裂解形成乙二醇和化合物10,該過程的反應能壘為156.5 kJ/mol。化合物10既能通過TS13醇解生成對苯二甲酸單甲酯和化合物8,其反應能壘為155.3 kJ/mol。也能經TS14醇解生成對苯二甲酸二甲酯和對苯二甲酸乙二醇酯,該反應能壘為155.5 kJ/mol。
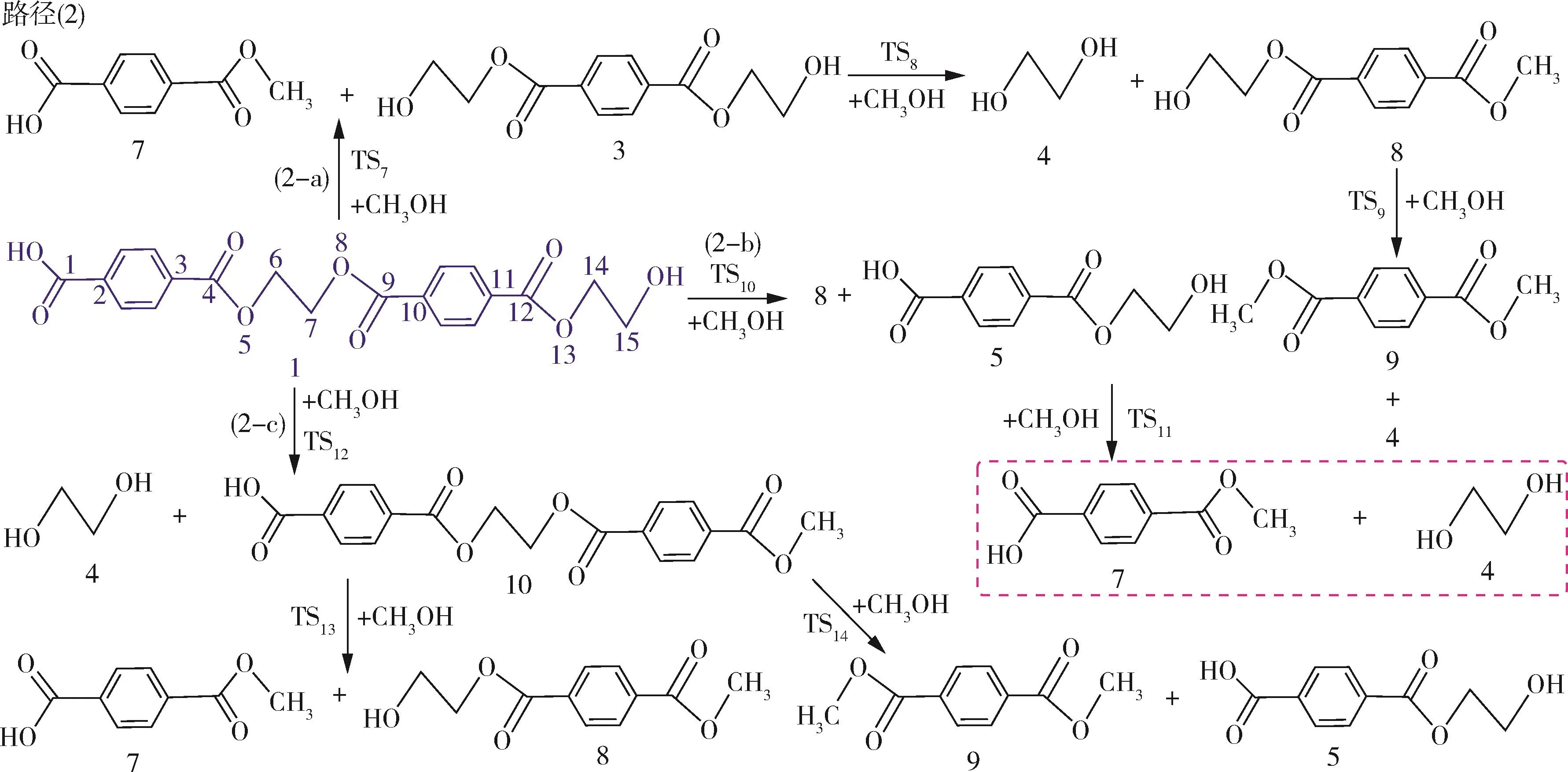
圖4 對苯二甲酸乙二醇酯二聚體醇解可能反應路徑Fig.4 Possible reaction paths for ethylene terephthalate dimer alcoholysis

圖5 對苯二甲酸乙二醇酯二聚體醇解反應能壘Fig.5 The energy barrier of ethylene terephthalate dimer alcoholysis reaction

圖6 對苯二甲酸乙二醇酯二聚體初始醇解過渡態優化結構Fig.6 Optimal structure of initial alcoholysis transition state of ethylene terephthalate dimer
對反應路徑(2)的反應能壘進行對比分析可知,對苯二甲酸乙二醇酯二聚體主鏈中間和末端酯鍵中酰氧鍵位置醇解的速控步反應能壘分別為155.2、155.3、156.5 kJ/mol,這表明對苯二甲酸乙二醇酯二聚體醇解反應可能是對苯二甲酸乙二醇酯二聚體主鏈任意位置酯鍵中酰氧鍵發生多次醇解,最終形成對苯二甲酸二甲酯和乙二醇等主要產物,這與相關PET醇解實驗研究結果[37?39]基本相符。
2.3 對苯二甲酸乙二醇酯二聚體氨解機理
根據PET在氨氣氣氛下的相關實驗結果[41?42],設計了3條可能的對苯二甲酸乙二醇酯二聚體氨解可能的反應路徑。圖7描述了對苯二甲酸乙二醇酯二聚體氨解可能的反應路徑,圖8描繪了對苯二甲酸乙二醇酯二聚體氨解過程的反應能壘示意圖,圖9為對苯二甲酸乙二醇酯二聚體主鏈酯鍵中酰氧鍵位置初始氨解過渡態的優化結構。
在反應路徑(3)中(如圖7所示),對化合物1降解過程設計了3條路徑,在(3?a)中,對苯二甲酸乙二醇酯二聚體化合物1經TS15氨解生成對苯二甲酸單酰胺11和化合物13,其過程需克服151.3 kJ/mol的勢壘。TS15的優化結構如圖9所示,反應前單獨優化氨氣分子中的N—H鍵長為1.000 ?,對苯二甲酸乙二醇酯二聚體中酰氧鍵(C(4)?O(5))鍵長為1.341 ?,反應中TS15的N—H鍵長變為1.136 ?,酰氧鍵(C(4)—O(5))鍵長變為1.902 ?,從TS15的優化結構中能夠看出,氨基(—NH2)結合羰基中的碳原子C(4)形成對苯二甲酸單酰胺,而氫原子結合乙烷基上的O(5)形成羥基端的化合物。對苯二甲酸單酰胺經兩次氨基中的氫原子轉移通過TS16和TS17裂解生成水和對氰基苯甲酸13,其反應能壘分別為167.8 kJ/mol和241.2 kJ/mol。化合物3和NH3通過TS18降解生成乙二醇和化合物14,其過程反應能壘為156.9 kJ/mol。化合物14進一步經TS19氨解生成乙二醇和對苯二甲酰胺15,反應能壘為156.9 kJ/mol。對苯二甲酰胺能經兩次氨基中的氫原子轉移通過TS20和TS21生成水和化合物17,反應能壘分別為167.0 kJ/mol和240.3 kJ/mol。同理,化合物17經兩次氫原子轉移通過TS22和TS23生成水和對苯二甲氰19,其過程反應能壘分別為168.4 kJ/mol和244.4 kJ/mol。在(3?b)中,化合物1和NH3通過TS24降解生成化合物14和對苯二甲酸乙二醇酯5,該過程需克服151.2 kJ/mol的勢壘。對苯二甲酸乙二醇酯進一步經TS25氨解生成乙二醇和對苯二甲酸單酰胺,反應能壘為156.6 kJ/mol。在(3?c)中,化合物1和NH3通過TS26降解生成乙二醇和化合物20,該反應能壘為156.6 kJ/mol。化合物20既能經TS27氨解生成對苯二甲酸單酰胺和化合物14,也能通過TS28生成對苯二甲酰胺和對苯二甲酸乙二醇酯,上述兩個過程的反應能壘分別為151.2 kJ/mol和151.2 kJ/mol。

圖7 對苯二甲酸乙二醇酯二聚體氨解可能反應路徑Fig.7 Possible reaction paths for ammonolysis of ethylene terephthalate dimer

圖8 對苯二甲酸乙二醇酯二聚體氨解反應能壘Fig.8 Ammonolysis reaction barrier of ethylene terephthalate dimer

圖9 對苯二甲酸乙二醇酯二聚體初始氨解過渡態優化結構Fig.9 Optimization of transition state for initial ammonolysis of ethylene terephthalate dimer
對苯二甲酸乙二醇酯二聚體氨解反應路徑的熱力學與動力學分析表明:對苯二甲酸乙二醇酯二聚體主鏈中間和末端酯鍵中酰氧鍵位置醇解的速控步反應能壘分別為151.3、151.2、156.6 kJ/mol,這表明對苯二甲酸乙二醇酯二聚體氨解反應可能是主鏈任意位置酯鍵中酰氧鍵發生多次降解,最終形成對苯二甲酰胺和乙二醇等主要產物,這與相關PET氨解實驗研究結果[42?43]基本相同。
通過對比對苯二甲酸乙二醇酯二聚體水/醇/氨解反應的熱力學與動力學計算結果可知:對苯二甲酸乙二醇酯二聚體主鏈酯鍵中酰氧鍵位置水/醇/氨解的速控步能壘分別約為169.0、155.0、153.0 kJ/mol,均要低于對苯二甲酸乙二醇酯二聚體熱解的速控步能壘(通過六元環、四元環過渡態發生的協同反應和自由基反應的能壘分別為184.0、267.0、345.0 kJ/mol)[29],由此可知,水/醇/氨解在一定程度上能降低對苯二甲酸乙二醇酯二聚體降解主要基元反應步的反應能壘,使反應更易于進行,且計算數據表明,對苯二甲酸乙二醇酯二聚體在氨氣氣氛中的裂解速控步能壘的最小,其次是在醇介質和水中的裂解。
2.4 溫度對對苯二甲酸乙二醇酯二聚體水/醇/氨解機理的影響
根據相關 PET 熱解相關文獻[29,44?45]可知:溫度對PET水/醇/氨解機理動力學(活化能)的影響不大,因此本文僅考慮溫度對對苯二甲酸乙二醇酯二聚體水/醇/氨解機理熱力學的影響。
從熱力學的角度去研究一個反應,只需考慮這個反應的始終兩態即可,而不用考慮它的中間過程[44]。故為了更加深入了解溫度對PET水/醇/氨解機理熱力學的影響,本節計算了對苯二甲酸乙二醇酯二聚體降解過程在不同溫度條件下(298、400、500、600、700、800、900 K)的反應自由能和焓變參數,反應自由能ΔG是判斷反應自發方向以及反應達到平衡時反應物轉化率大小的熱力學參數,當ΔG<0時,反應可自發進行,反應ΔG越小,反應達到平衡時,反應物的轉化率越大[45]。從反應能量的角度考慮時,ΔH>0表示是吸熱反應,反之是放熱反應[46]。表1為對苯二甲酸乙二醇酯二聚體模化物水/醇/氨解過程中不同溫度下降解過程的焓變(ΔH)、自由能變(ΔG)和熵變值(ΔS),圖10為對苯二甲酸乙二醇酯二聚體模化物/醇/氨解過程中降解過程的焓變、自由能變和熵變與溫度的相互關系。
在設定溫度范圍內,從表1數據可知,PET水解反應中,ΔH和ΔS恒大于零,ΔG當溫度在298~400 K時ΔG>0,在溫度500 K及以上時ΔG<0,故推測當溫度在500 K時,PET水解反應能夠自發進行,屬于吸熱反應,升高溫度能夠增加PET水解的自發性。而在PET醇解反應中,ΔH和ΔG恒小于零,ΔS大于零,故推測PET醇解可能屬于熱力學自發的放熱反應。在對PET氨解過程中發現,ΔH和ΔS恒大于零,ΔG在溫度400 K及以上時ΔG<0,故推測當溫度在400 K時,PET氨解反應能夠自發進行,屬于吸熱反應,且反應溫度升高能夠提高PET氨解的自發性。

表1 對苯二甲酸乙二醇酯二聚體在不同溫度下水/醇/氨解過程的ΔH/ΔG/ΔSTab.1 ΔH/ΔG/ΔS of ethylene terephthalate dimer during hydrolysis/alcoholysis/ammonolysis processes at different temperature
綜上所述,溫度對對苯二甲酸乙二醇酯二聚體水/醇/氨解過程的ΔH影響較小,ΔS均為正值,隨著溫度升高,所有路徑的吉布斯自由能ΔG均呈下降的趨勢[如圖10(a)所示],ΔG值越來越小,說明在PET水/醇/氨解反應過程中,升高溫度能夠增加其反應的自發性。

圖10 對苯二甲酸乙二醇酯二聚體水/醇/氨解的ΔH、ΔG、ΔS與溫度的相關性Fig.10 Relationship between ΔH,ΔG and ΔS in hydrolysis/alcoholysis/ammonolysis processes of ethylene terephthalate dimer and temperature
3 結論
(1)采用密度泛函理論B3P86/6?31++G(d,p)方法對對苯二甲酸乙二醇酯二聚體的可能水/醇/氨解路徑進行了理論研究,通過對比分析了對苯二甲酸乙二醇酯二聚體水/醇/氨解反應路徑的熱力學與動力學參數;
(2)對苯二甲酸乙二醇酯二聚體水解主要產物為對苯二甲酸和乙二醇;醇解主要產物為對苯二甲酸二甲酯和乙二醇;氨解主要產物為對苯二甲酰胺和乙二醇;
(3)對苯二甲酸乙二醇酯二聚體主鏈酯鍵中的酰氧鍵位置的水/醇/氨解過程中,升高溫度,ΔH變化較小,ΔG越來越小,因此在PET水/醇/氨解反應過程中,反應溫度的升高能夠增加其反應的自發性;
(4)與純熱解相比,水/醇/氨解能夠降低對苯二甲酸乙二醇酯二聚體降解過程中主要基元反應步的反應能壘[路徑(1)約為169.0 kJ/mol、路徑(2)約為155.0 kJ/mol、路徑(3)約為153.0 kJ/mol],使反應更易于進行,且對苯二甲酸乙二醇酯二聚體主鏈中間和末端酯鍵中的酰氧鍵發生水/醇/氨解的速控步能壘相差較小,因此PET水/醇/氨解可能是主鏈隨機位置酯鍵中的酰氧鍵進行的裂解反應。

