經典名方澤瀉湯基準樣品HPLC特征指紋圖譜分析研究*
姜恒麗,鐘鑫,王雙雙,馬向慧,劉燁,康亞娟,黃馥,張永和,曹麗娟
(1.盛實百草藥業有限公司,天津市中藥飲片炮制技術企業重點實驗室,天津 300301;2.天津津村制藥有限公司,天津 300301)
2008年國家食品藥品監督管理局發布“關于印發中藥注冊管理補充規定的通知”,明確了“經典名方”的概念,是指目前仍廣泛應用、療效確切、具有明顯特色與優勢的清代及清代以前醫籍所記載的方劑[1]。2018年國家中醫藥管理局官網公布包含澤瀉湯在內的第一批100首古代經典名方目錄[2]。澤瀉湯始載于漢代張仲景的《金匱要略·痰飲咳嗽病脈證并治第十二》,原文載“心下有支引,其人苦冒眩,澤瀉湯主之”[3],處方由澤瀉、白術組成,方中澤瀉氣平,味甘、淡,利水滲濕,化濁降脂,引水濕從小便排出而治其標,為君藥,白術苦、甘,健脾益氣、利水消腫,助脾運化水濕,則痰飲不得生,而治其本,為臣藥,兩者相須為用,祛濕又健脾,具有利水除飲、健脾制水的功效[4],后代因襲不衰。據文獻研究報道,從澤瀉中分離出的化合物達200多個,三萜和倍半萜類化合物是澤瀉的主要化學成分,其他還包括二萜類、含氮化合物、黃酮、糖類、脂肪烴及其衍生物、苯丙素等化合物。原萜烷型四環三萜類是澤瀉中研究最多的特征性成分,根據生物途徑,澤瀉醇A、澤瀉醇B、澤瀉醇C等單體及其衍生物等均可通過23-乙酰澤瀉醇B衍生獲得[4-6]。相關藥理研究顯示,澤瀉醇類成分如澤瀉醇A、澤瀉醇B、24-乙酰澤瀉醇A、23-乙酰澤瀉醇B等是澤瀉發揮降血壓、降血脂、利尿及抗炎等作用的主要成分[7]。白術的化學成分主要包括揮發油、多糖、內酯類、多種氨基酸和維生素等,其中重要的活性成分為白術內酯類,主要有白術內酯Ⅰ、Ⅱ、Ⅲ和雙白術內酯等。現代研究顯示,白術中的多種活性成分具有抗腫瘤、抗炎、改善胃腸功能、調節免疫等眾多藥理作用[8]。澤瀉湯組方雖簡,但臨床療效頗佳,中醫臨床主要用來醫治水停心下,清陽不升,濁陰上犯,頭目昏眩證,現代臨床多用于治療高血壓、高血脂癥、梅尼埃病、內耳性眩暈病等,經多年臨床實踐具有較好的臨床效果[9-10]。
經典名方主要為復方制劑,由多種化學成分復雜的中藥組成,在疾病治療方面不同于以單一化合物為主的化學制劑,通過“多靶點、多成分”進行協同作用。有研究表明,澤瀉湯包含多種藥效成分,僅用單一的化學成分對其進行質量控制研究,不能準確地反映其有效性和安全性[11-12]。隨著中藥質控體系的不斷完善,可以利用HPLC特征指紋圖譜,該方法技術十分成熟、穩定、科學和可靠,是一種可以表征中藥產品內在質量整體變化的評價手段,對全面控制中藥產品質量具有十分關鍵的意義,現在經常被用于中藥材、中藥飲片及中藥制劑的質量分析[13-15]。經典名方基準樣品研發是制劑研發的關鍵組成部分,為研發制劑提供了基準參照,保證古今工藝制劑的質量一致性[16-18]。本研究采用高效液相色譜法建立18批澤瀉湯基準樣品的特征指紋圖譜,以期為澤瀉湯基準樣品及復方制劑的質量評價提供科學依據和參考。
1 儀器與試藥
1.1 儀器 Agilent 1260 Series高效液相色譜儀、Agilent ZORBAX SB-Aq(250 mm×4.6 mm)色譜柱(美國安捷倫科技有限公司);LQ-C30002電子天平(上海瑤新電子科技有限公司);SKG便攜式電陶爐(廣東艾詩凱奇智能有限公司);全自動陶瓷壺(2 L,夏新科技有限責任公司);FDU1110型冷凍干燥機、PFR-100預備凍結槽(東京理化器械株式會社);1-14離心機(Sigma儀器有限公司);VORTEX 3000渦旋混合器(WIGGENS有限責任公司);XP205電子天平、PL403電子天平[梅特勒-托利多儀器(上海)有限公司];AS30600BDT超聲波清洗器(AUTO SCIENCE有限責任公司)。
1.2 試劑與試藥 試劑:乙腈(色譜純,德國默克股份有限公司);超純水(制水機型號為Milli-Q Reference)。對照品:白術內酯Ⅰ(批號:111975-201501,純度為99.9%),23-乙酰澤瀉醇B(批號:111846-201705,純度為99.7%)均購買于中國食品藥品檢定研究院;澤瀉醇A(批號:B21638,純度≥98%),澤瀉醇 B(批號:B21640,純度≥98%)均購買于上海源葉生物科技有限責任公司。樣品:18批次澤瀉藥材分別購于四川眉山、四川五通橋、湖北宜昌、湖北枝江4個產地,經盛實百草藥業有限公司曹麗娟研究員鑒定為澤瀉科植物澤瀉Alisma plantago-aquatica Linn.的干燥塊莖。18批次白術藥材分別購于浙江磐安、安徽亳州、安徽譙城3個產地,經盛實百草藥業有限公司曹麗娟研究員鑒定為菊科植物白術Astractylodes macrorephala Koide.的干燥根莖。澤瀉、白術對應飲片均按照2020年版《中國藥典》(一部)各藥材項下飲片的炮制要求加工。經檢驗均合格。18批澤瀉湯基準樣品原料澤瀉和白術的批號和產地明細如表1所示。

表1 18批澤瀉湯基準樣品原料的批號和產地明細Tab.1 Origin details of the raw materials of 18 batches of Zexie Decoction benchmark samples
2 方法與結果
2.1 澤瀉湯基準樣品的制備 稱取澤瀉15 g,白術6 g,加水 400 mL,加蓋,浸泡 30 min,以武火煮沸后,調節火力,保持微沸煎煮45 min,趁熱用150目濾網過濾,濾液冷凍干燥,即得。
2.2 色譜條件 色譜柱:Agilent ZORBAX SB-Aq C18(4.6 mm×250 mm,5 μm);流動相:乙腈(A)和超純水(B);梯度洗脫程序:0~5 min,35%~35%B;5~15 min,35%~55%B;15~30 min,55%~65%B;30~40 min,65%~75%B;40~47 min,75%~85%B。流速:1.0 mL/min;波長:208 nm;進樣量:10 μL;柱溫:30℃。理論塔板數按23-乙酰澤瀉醇B峰計算不低于10 000。
2.3 溶液的制備
2.3.1 混合對照品溶液的制備 精密稱取澤瀉醇A、白術內酯Ⅰ、澤瀉醇B、23-乙酰澤瀉醇B對照品適量,加甲醇配制成每1mL含澤瀉醇A、白術內酯Ⅰ、澤瀉醇B、23-乙酰澤瀉醇 B分別為20、30、100和500 μg的混合對照品溶液。
2.3.2 供試品溶液的制備 稱取約1 g的澤瀉湯基準樣品粉末,進行精密稱定,加10 mL水,稱得質量,超聲30 min,冷卻至室溫,稱質量,用溶劑補足減失的質量,精密吸取5 mL,置于10 mL的容量瓶內,加乙腈定容至刻度,搖勻,離心(12 000 rpm,5 min,離心半徑 20 cm),取上清液,用 0.22 μm 微孔濾膜過濾,即得。
2.3.3 單味藥材及飲片煎煮液的制備 按組方用量分別稱取澤瀉和白術藥材和飲片,按澤瀉湯基準樣品制法制備凍干粉末,按照“2.3.2”項下方法制備,所得供試品溶液即為單味藥材和飲片溶液。
2.3.4 單味飲片陰性供試品溶液的制備 按處方量稱取缺澤瀉、缺白術陰性處方,并按“2.1”項下澤瀉湯基準樣品制法制得相應的陰性凍干粉末,再按“2.3.2”項下方法制備,所得相應的單味飲片陰性供試品溶液。
2.4 方法學考察
2.4.1 精密度考察 取同一份澤瀉湯(S1號)供試品試液,按照“2.2”項下色譜方法連續進樣6次,記錄圖譜數據。選取23-乙酰澤瀉醇B(9號峰)作為參照,計算11個共有峰的相對保留時間和相對峰面積。各共有峰的相對保留時間的RSD值為0.08%,相對峰面積的RSD值為1.08%,結果顯示儀器精密度符合要求。
2.4.2 穩定性考察 取同一份澤瀉湯(S1號)供試品試液,分別在 0、2、4、6、8、12、24、32 h,按照“2.2”項下色譜條件進樣1次檢測,記錄特征指紋圖譜數據。選取23-乙酰澤瀉醇B(9號峰)作為參照,計算11個共有峰的相對保留時間和相對峰面積。各共有峰的相對保留時間的RSD值為0.09%,相對峰面積的RSD值為1.77%,結果顯示該樣品在32 h內穩定性符合要求。
2.4.3 重復性考察 稱取6份澤瀉湯基準樣品(S1號),制備供試品試液,分別按照”2.2”項下色譜方法進樣1次檢測,記錄特征指紋圖譜數據。選取23-乙酰澤瀉醇B(9號峰)作為參照,計算11個共有峰的相對保留時間和相對峰面積。各共有峰的相對保留時間的RSD值為0.03%,相對峰面積的RSD值為1.59%,結果顯示該方法重復性符合要求。
2.5 澤瀉湯基準樣品特征指紋圖譜測定
2.5.1 特征指紋圖譜建立 取按“2.1”項下澤瀉湯基準樣品制備方法所得的18批樣品,配置供試品試液,按“2.2”項下色譜條件進樣分析,記錄圖譜數據。將數據導入國家藥典委員會的《中藥色譜指紋圖譜相似度評價系統軟件》(2012版),對18批澤瀉湯基準樣品圖譜進行數據匹配,圖譜見圖1。從圖譜中可見其中11個峰為18批基準樣品所共有,因此確定這11個色譜峰為各基準樣品的共有峰,以平均值法確定共有模式,結果如圖2所示。
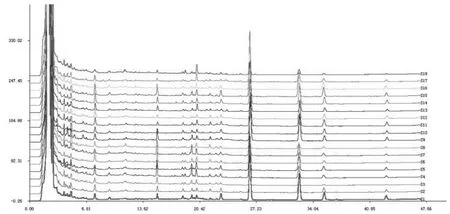
圖1 18批澤瀉湯基準樣品特征指紋圖譜Fig.1 Characteristic fingerprint of 18 batches of Zexie Decoction benchmark samples

圖2 澤瀉湯基準樣品特征圖譜(共有模式圖譜)Fig.2 HPLC characteristic of benchmark samples of Zexie Decoction(mutual mode)
2.5.2 色譜峰歸屬和確認 取“2.3”項下澤瀉湯基準樣品供試品試液、澤瀉和白術單味藥材及飲片溶液、單味飲片陰性溶液,按“2.2”項下色譜方法檢測,獲得各HPLC圖譜,結果如圖3和圖4所示。通過對比相對保留時間,對澤瀉湯基準樣品進行色譜峰追溯,確定了峰 1、峰 4、峰 7、峰 8、峰9、峰10 和峰11來自澤瀉,峰5和峰6來自白術,峰2和峰3為澤瀉和白術共有。

圖3 澤瀉色譜峰歸屬比較圖譜Fig.3 Chromatographic peak attribution comparison of alismatis rhizoma

圖4 白術色譜峰歸屬比較圖譜Fig.4 Chromatographic peak attribution comparison of atractylodis macrocephalae rhizoma
2.5.3 特征峰指認和參照峰選擇 通過與混合對照品比較進行特征峰指認,分別精密吸取配置的混合對照品溶液和供試品溶液,按“2.2”項下色譜方法檢測,記錄圖譜數據。見圖5。
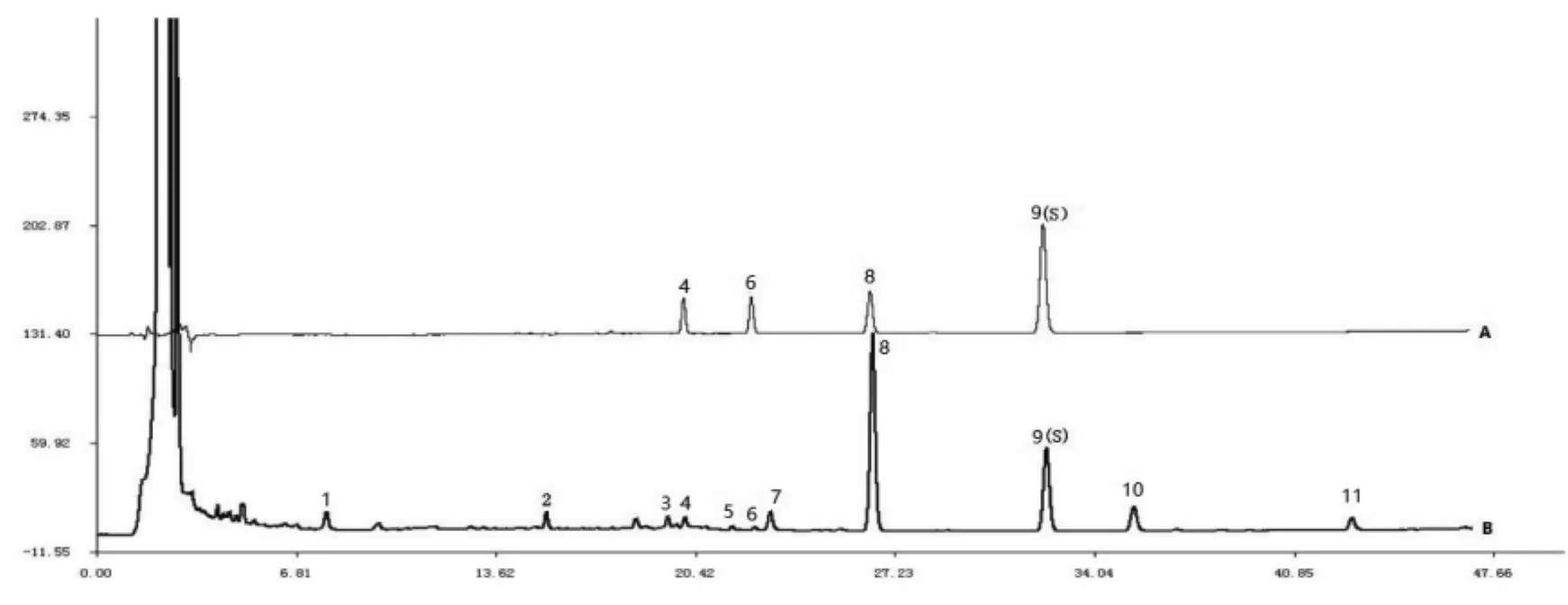
圖5 混合對照品(A)和基準樣品(B)對比圖譜Fig.5 Chromatographic peak comparison of mixed reference substance(A)and substance benchmarks sample(B)
由圖5可見,確定4號峰為澤瀉醇A,6號峰為白術內酯I,8號峰為澤瀉醇B,9號峰為23-乙酰澤瀉醇B。其中9號峰的23-乙酰澤瀉醇B是君藥澤瀉的重要活性成分,根據供試品溶液的特征圖譜可知,23-乙酰澤瀉醇B為已知化學成分,化學性質穩定,并且其在各色譜峰中,具有較好的分離度且較大的峰面積,因此選取9號峰(23-乙酰澤瀉醇B)作為基準樣品特征圖譜的參照峰。
2.5.4 相似度評價和共有峰計算 對“2.5.1”項下制得的18批澤瀉湯基準樣品的特征指紋圖譜數據,導入國家藥典委員會的《中藥色譜指紋圖譜相似度評價系統軟件》(2012版)進行分析,將對照特征指紋圖譜上標示的色譜峰作為匹配點,進行校正,并計算18批澤瀉湯基準樣品指紋圖譜相似度及共有峰的峰面積,選取23-乙酰澤瀉醇B峰(9號峰)的保留時間和峰面積為參照,計算11個特征峰的相對保留時間與相對峰面積,結果如表2、表3、表4所示。

表2 18批澤瀉湯基準樣品的指紋圖譜相似度Tab.2 Fingerprint similarity of 18 batches of Zexie Decoction benchmark samples

表3 18批澤瀉湯基準樣品共有峰的峰面積Tab.3 Peak area of common chromatographic peaks of 18 batches of Zexie Decoction benchmark samples

表4 澤瀉湯基準樣品共有峰的相對保留時間和相對峰面積Tab.4 Relative retention time and relative peak area of common chromatographic peaks of Zexie Decoction benchmark samples
根據表2相似度結果可知,18批澤瀉湯基準樣品的指紋圖譜相似度在0.912~0.997,選取23-乙酰澤瀉醇B對應峰(峰9)為S峰,計算各特征峰的相對保留時間,各相對保留時間應在要求值的±5%。具體要求值為:0.242(峰1)、0.473(峰2)、0.602(峰3)、0.620(峰4)、0.669(峰5)、0.693(峰6)、0.709(峰7)、0.817(峰8)、1.000(峰9)、1.092(峰10)、1.325(峰11)。
3 討論
3.1 劑量考證 澤瀉湯原方記載“澤瀉五兩,白術二兩。以水二升,煮取一升,分溫再服”。《中國科學技術史·度量衡卷》記載,并通過實測漢代出土器具,得到西漢1斤厘定為250 g,新莽權1斤厘定為245 g,東漢 1 斤厘定為 222 g,故東漢:1 兩=13.8 g[19]。但明代李時珍在《本草綱目》中就提出:“今古異制,古之一兩,今用一錢可也。”清代汪昂《湯頭歌訣》也遵李時珍之說,認為“大約古用一兩,今用一錢足矣。”由于李時珍在中國醫藥界地位崇高,對古方劑量的主張對后世影響甚大,“古一兩折今一錢”成了通例,為多數醫家所沿用。現代醫家李培生編著的《傷寒論講義》,其在書中的古今劑量折算表中也提到東漢時代的1兩折合為3 g。眾多學者對張仲景用藥的古今劑量折算關系進行了大量考證和核實[20-23],通過對古籍文獻和歷代度量衡演變考證,綜合分析后,本研究按照漢代1兩=3 g對處方劑量進行折算。
3.2 基準樣品制備工藝
3.2.1 浸泡工藝 古籍中對是否浸泡及時間并未明確說明,以澤瀉湯出膏率為考察指標,發現浸泡30 min后澤瀉湯樣品出膏率為26.73%,高于未浸泡樣品的出膏率23.96%。此外,浸泡30 min時藥材飲片吸水達到飽和,且吸水量與煎煮后的藥渣吸水量接近,所以確定浸泡時間為30 min。
3.2.2 煎煮工藝 關于加熱設備,對比了全自動陶瓷壺加熱盤和可調功率電陶爐,后者煎煮時間適中,制備的澤瀉湯的出膏率為18.93%,高于前者16.42%,且電陶爐受熱均勻,控溫準確,火候易掌控,所以確定可調功率電陶爐為制備物質基準的加熱設備。目前市面上的煎煮容器多數為陶瓷材質的煎藥壺,選擇2 L陶瓷壺作為澤瀉湯物質基準的制備容器,壺身壁的平均厚度為5 mm,其加水量為400 mL,液面高度為2.2 cm,符合《醫療機構中藥煎藥室管理規范》中規定的2~5 cm液面高度。
現代由于加熱方式的改變,根據加水量和煎煮時間的長短,通過調節加熱功率以達到同古代文武火基本一致的煎藥效果。以出膏率為指標,對澤瀉湯進行不同功率的煎煮考察發現,400 W煎煮的出膏率最高為26.21%,且煎煮時間適中,所以選擇400 W作為澤瀉湯物質基準的制備功率。此外,不加蓋煎煮時水量蒸發快,煎煮時間短,但對應出膏率較低,故確定煎煮時進行加蓋煎煮。
3.2.3 過濾工藝 通過對濾過方式、濾過材質、濾過目數對澤瀉湯出膏率的影響進行考察,發現常壓濾過出膏率較高,同時結合儀器可操作性及設備利用度,選擇濾網常壓濾過作為制備澤瀉湯物質基準的濾過方式。在采用4層紗布、100目濾布和100目濾網濾過的結果中,100目濾網出膏率相對較高,所以選擇濾網作為制備澤瀉湯物質基準濾過材質。同時考察100、150和200目濾網對出膏率的影響,150目濾網出膏率相對較高,所以最終選擇150目作為制備澤瀉湯物質基準的濾過目數。
3.2.4 干燥工藝 中藥提取液的成分和性質復雜,常用的干燥方式為減壓濃縮真空干燥和冷凍干燥。傳統的干燥會引起材料皺縮,破壞細胞,而冷凍干燥過程中樣品的結構不會被破壞,可以保持物料原化學組成和物理性質,除長期保存的穩定性以外,還保留了其固有的生物活性與結構,故選擇冷凍干燥。
通過對澤瀉湯制備過程中的一系列影響因素進行考察篩選,并制備3批澤瀉湯對該工藝進行驗證,結果表明該方法制備的澤瀉湯基準樣品質量穩定,因此確定澤瀉湯基準樣品的制備工藝,通過對18批澤瀉和白術飲片進行隨機組合,制備了18批澤瀉湯基準樣品凍干粉。
3.3 色譜條件篩選 澤瀉湯中成分主要有君藥澤瀉中的倍半萜類、三萜類,白術中的揮發油、內酯類成分,本研究采用DAD檢測器對樣品進行全波長掃描,同時對200、208、220 nm波長下的色譜圖進行比較發現,當波長在208 nm時,色譜圖中呈現的色譜峰數量最多,各指標成分色譜峰的吸收強度很平均,且分離度較好,因此,最終選用208 nm波長為檢測波長。
分別比較Agilent ZORBAX SB-Aq(250 mm×4.6mm,5μm),ZORBAX Eclipse Plus(250mm×4.6mm,5 μm),COSMOSIL C18-MS-II I(250 mm×4.6 mm,5 μm)3個型號的色譜柱,結果顯示,使用Agilent ZORBAX SB-Aq色譜柱時,各色譜峰呈現了較好的分離度,且特征峰很明顯,各峰形良好,因此選擇Agilent ZORBAX SB-Aq色譜柱作為HPLC特征指紋圖譜的色譜柱。
選用Agilent ZORBAX SB-Aq色譜柱,對不同柱溫條件(20、30和40℃)進行比較和篩選,結果顯示,在柱溫30℃條件下,各色譜峰具有較好的分離度,不易受干擾因素影響。所以,最終選擇柱溫30℃作為HPLC特征指紋圖譜的最佳柱溫條件。
以乙腈-水為流動相,考察了4個不同梯度洗脫條件下的色譜峰數目和各色譜峰分離情況,選出最佳梯度洗脫條件。考察了不同提取溶劑對澤瀉湯樣品的影響,篩選了純化水溶解、乙腈提取和50%乙腈提取法,結果發現,50%乙腈提取法樣品在色譜條件下色譜峰數目較多,且各色譜峰紫外吸收和分離度良好,因此最終選擇50%乙腈提取法為最佳前處理法。
3.4 測定結果分析 本研究采用HPLC法建立了18批澤瀉湯基準樣品的特征指紋圖譜,相似度在0.912~0.997,共標定11個共有色譜峰,確定了峰1、峰4、峰7、峰8、峰9、峰10和峰11來自君藥澤瀉,峰5和峰6來自臣藥白術,峰2和峰3為澤瀉和白術共有。指認了4個特征峰,其中4號峰為澤瀉醇A,6號峰為白術內酯I,8號峰為澤瀉醇B,9號峰為23-乙酰澤瀉醇B。選取23-乙酰澤瀉醇B對應峰(峰9)為S峰,計算各特征峰的相對保留時間,各相對保留時間應在要求值的±5%。具體要求值為:0.242(峰 1)、0.473(峰 2)、0.602(峰 3)、0.620(峰 4)、0.669(峰 5)、0.693(峰 6)、0.709(峰 7)、0.817(峰 8)、1.000(峰 9)、1.092(峰 10)、1.325(峰 11)。
本研究通過建立澤瀉湯基準樣品的HPLC特征指紋圖譜,為澤瀉湯基準樣品關鍵化學屬性的質量評價奠定了良好的基礎,同時對澤瀉湯復方制劑的質量評價和標準建立提供基準參照和控制依據。