神奇的手性螺環催化劑
——第54屆國際化學奧林匹克試題第8題解析
湯平平
南開大學化學學院,天津 300071
手性是指物體與其鏡像不能重疊的現象,如同人的左右手。構成生命體的基本物質如蛋白質、DNA、糖等都具有手性,所以能夠識別客體手性分子的對映異構體,這是手性化合物對映異構體具有不同生理活性的根本原因[1]。
手性直接關系到藥物的藥理作用,由于藥物和其受體之間的這種立體選擇性作用,使得藥物的一對對映體不論是在作用性質還是作用強度上都會有差別。在20世紀60年代,歐洲曾以消旋體的反應停(Thalidomide)作為抗妊娠反應的鎮靜劑,一些妊娠婦女服用此藥后,出現多例畸變胎兒。后經研究證實(R)-構型才真正起鎮靜作用,而(S)-構型則有強致畸作用。因此,通過不對稱合成的方法高效獲得具有手性的化合物,對于醫藥、農藥、精細化工等領域都有重要的意義[2]。
不對稱催化方法(asymmetric catalysis),是通過使用手性催化劑來實現不對稱合成反應的方法,一般指利用手性金屬配合物作為手性模板控制反應物的對映面,將大量前手性底物選擇性地轉化成特定構型的產物,實現手性放大和手性增殖。簡單地說,就是通過使用催化劑量級的手性原始物質來立體選擇性地生產大量手性特征的產物。它的反應條件溫和,立體選擇性好,(R)-異構體或(S)-異構體同樣易于生產,且潛手性底物來源廣泛,對于生產大量手性化合物來講是最經濟和最實用的技術。2001年、2021年,諾貝爾化學獎兩次授予給從事“不對稱有機催化發展”相關科學家[3-5]。
1 出題依據
不對稱催化是南開大學化學學科的重點研究領域之一,在周其林院士的帶領下,該團隊經過20年探索,發現了一類全新的手性螺環配體骨架結構[6]。在此基礎上,發展了一系列手性螺環催化劑,這些手性螺環催化劑具有廣譜性,在許多不對稱催化反應中都表現出優于其他手性催化劑的催化活性和對映選擇性[7]。比如在酮化合物的不對稱氫化中,手性螺環銥催化劑的催化轉化數達到了455萬[8],是目前“最高效的手性分子催化劑”。周其林教授團隊獲得2019年度唯一國家自然科學獎一等獎,相關的研究成果發表在Science、Nat. Catal.、JACS、Angew. Chem.、Chem. Sci.、CCS Chem.等頂級期刊上,受到學界的廣泛關注。
第54屆國際化學奧林匹克試題中第8題中[9],我們以周其林院士發展的手性螺環催化劑Ir-SpiroPAP為主要內容,逐次展開,考查了手性螺環配體SpiroPAP的合成路線,手性螺環催化劑Ir-SpiroPAP的制備以及手性螺環催化劑在合成中的應用。
2 題目及解析
手性化合物對人類健康至關重要,例如,目前臨床使用的藥物有50%以上是手性分子的單一對映體。然而,合成富含對映體形式的手性分子仍是一個巨大的挑戰。南開大學周其林教授團隊開發了一系列高活性的手性螺旋催化劑,將不對稱合成的效率提高到一個新的高度,在醫藥行業得到了廣泛的應用。這些催化劑催化獲得的手性化合物的ee可達99.9%,催化劑用量可降至0.00002 mol% (摩爾百分比)[8]。該系列研究成果獲得2019年中國國家自然科學獎一等獎。圖1示出一種基于過渡金屬銥的手性螺環催化劑及其在酮的不對稱催化氫化中的應用。
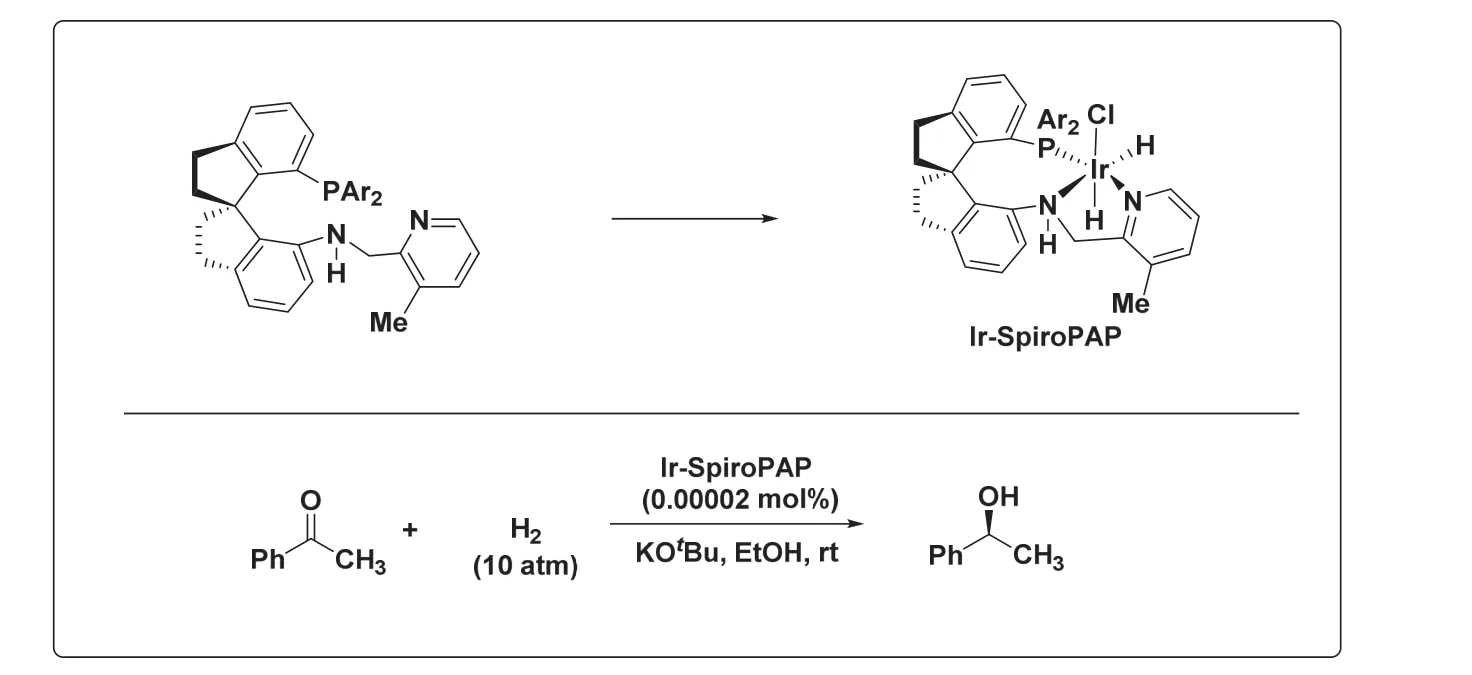
圖1 手性螺環金屬銥催化劑及其在酮的不對稱催化氫化中的應用(Ar = 3,5-(tBu)2C6H3)
2.1 手性配體SpiroPAP的合成
2.1.1 題目
手性配體SpiroPAP的合成路線如圖2所示[10]。

圖2 手性螺環配體SpiroPAP (+)-9的合成
8-1 (16分) 請畫出化合物1,2,4,5的結構式(不考慮立體化學構型)。
8-2 (2分) 在下列試劑中,哪種試劑A不能用于化合物8到9的轉化?
(a) NaBH(OAc)3;(b) NaBH3CN;(c) NH2NH2, NaOH;(d) NaBH4
外消旋螺環化合物6與(-)-氯甲酸薄荷酯(10)反應生成柱層析可分離的化合物11a和11b,再經肼解得到光學純的(+)-6和(-)-6,如圖3所示。

圖3 外消旋螺環化合物6的動力學拆分
8-3 (2分) 以下說法正確的是。
(a) 化合物11a和11b是一對對映異構體
(b) 化合物11a和11b是一對非對映異構體
(c) 化合物11a和11b是一對順反異構體
(d) 化合物11a和11b是一對構象異構體
2.1.2 答案與解析
這一部分主要涉及手性螺環配體SpiroPAP的合成路線。本題為經典的有機化學推斷題,根據反應條件推測合成過程中缺失結構或者填寫所需條件。而該類型的題目我們在有機的預備題第13題中也有體現。本題給出的合成路線中,從間甲氧基苯甲醛出發,在堿性條件NaOH下,與0.5當量的丙酮發生羥醛縮合反應,由于分子式已經給出,因此可以很方便地判斷出得到了不飽和酮化合物1,接著在Raney Ni的催化下利用H2將不飽和雙鍵氫化,生成化合物2,再在Br2和吡啶的條件下在芳環上引入兩個Br原子,得到化合物3。從3的結構逆推也能驗證1和2的結構。化合物3在TiCl4的條件下發生傅氏酰基化反應,生成螺環化合物4,緊接著在nBuLi的條件下發生鋰溴交換,隨后在EtOH的條件下水解得到化合物5,再在BBr3的條件下脫除甲基得到消旋的螺環配體(±)-6。
8-1小題的答案為:
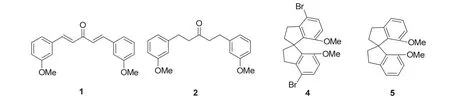
經過一系列轉化得到化合物8,隨后考察了一個還原胺化的條件A,得到化合物9,從8-2的選項中我們不難發現a、b、d都可以實現還原胺化反應,因此8-2的答案為c。
其中,光學純的手性螺環配體6,需要通過對消旋的螺環配體(±)-6進行拆分才能得到。通過與手性化合物10反應,得到一對非對映異構體11a和11b (8-3的答案為b),通過柱層析純化分離后再肼解得到光學純的手性螺環配體(+)-6和(-)-6。這里主要考查學生對非對映異構體概念的理解。
2.2 手性配體和Ir-SpiroPAP的制備、性質和應用
2.2.1 題目
用SpiroPAP與[Ir(cod)Cl]2(cod為環己烷-1,5-二烯)在甲醇中與氫氣反應制備Ir-SpiroPAP,如圖4所示。

圖4 催化劑Ir-SpiroPAP的制備(Ar = 3,5-(tBu)2C6H3)
8-4 (2分) 請寫出催化劑Ir-SpiroPAP中Ir的氧化態。
8-5 (2分) 請寫出催化劑Ir-SpiroPAP中Ir的d軌道價電子數。
在二萜類化合物Mulinane (22)全合成中,采用手性螺旋催化劑Ir-SpiroPAP催化的不對稱反應,如圖5所示[11]。

圖5 手性螺環催化劑Ir-SpiroPAP在二萜類化合物Mulinane (22)全合成中的應用(Ar = 3,5-(tBu)2C6H3)
8-6 (8分) 請畫出化合物15和16的結構式,包括其立體構型。
8-7 (2分) 從以下試劑中,選擇出最佳條件B。
(a) MeLi/CeCl3;(b) MeLi/CuI;(c) MePh3P+I-,nBuLi;(d) Me3S+I-, NaH
8-8 (2分) 從以下試劑中,選擇出最佳條件C。
(a) MeLi/CeCl3;(b) MeLi/CuI;(c) MePh3P+I-,nBuLi;(d) Me3S+I-, NaH
2.2.2 答案與解析
這一部分主要涉及手性螺環催化劑Ir-SpiroPAP的制備、性質與應用。首先考查學生對于絡合物中Ir金屬的氧化態和外層d軌道價電子的認知。從Ir-SpiroPAP結構中我們不難發現,Ir與六個配位原子結合,其中三個是電中性的,分別是兩個N原子和一個P原子,而另外的三個分別是Cl-離子和兩個H-離子,因此Ir的氧化態為+3,考慮到基態Ir原子的價層電子組態為5d76s2,失去3個電子后,Ir3+外層d軌道價電子為6。
8-4小題的答案為:+3;8-5小題的答案為:6。
隨后是考查手性螺環催化劑Ir-SpiroPAP在Mulinane型二萜天然產物全合成中的應用。本題仍為經典的有機化學推斷題,根據反應條件推測合成過程中缺失結構或者填寫所需條件。依據所給出的合成路線,從化合物12出發,在手性螺環催化劑Ir-SpiroPAP的不對稱催化氫化下,可以以高產率、高ee值一步構建三個連續手性中心,得到化合物13,隨后在PCC (氯鉻酸吡啶,Pyridinium Chlorochromate)的條件下將羥基氧化成羰基,獲得化合物14,緊接著在堿性條件下,化合物14與烷基碘代物發生烷基化反應,得到化合物15。這里需要注意的是新生成的手性中心的判斷,因為分子中異丙基是朝面上的,由于面下空間位阻較小,生成的烯醇負離子面下進攻烷基碘代物,因此引入的烷基是朝面下的結構,該手性中心也可以從后面的結構17中得到驗證。在MsOH的作用下,化合物15發生分子內傅氏酰基化成環,并消除得到化合物16,隨后在Pd/C氫化的條件下將雙鍵還原,得到化合物17。接下來在Na和NH3的條件下將苯環進行還原,生成化合物18,接下來是發生甲基對不飽和酮的1,4-加成,這里考查的是甲基對不飽和酮發生1,4-加成的最佳條件。從8-7的選項中我們不難判斷在CuI/MeLi存在下,甲基對不飽和酮發生1,4-加成得到正確的產物19。化合物20發生甲基對不飽和酮的1,2-加成,生成化合物21。這里考查的是甲基對不飽和酮發生1,2-加成的最佳條件。從8-8的選項中我們不難判斷在CeCl3/MeLi存在下,甲基對不飽和酮發生1,2-加成得到正確的產物21。最后經過多步反應得到化合物22。
8-6小題的答案為:

8-7小題的答案為b;8-8小題的答案為a。
Mulinane型二萜是1990年Rodriguez等從智利北部一種當地人用于治療糖尿病、支氣管炎、腸胃不適等疾病的傳統民間藥物傘形灌木Mulinium crassifolium中首次分離得到的。迄今為止,已分離得到的該家族成員達到30多個,生物活性測定表明其具有腸胃保護、抗瘧原蟲和抗菌等活性。2017年,南開大學周其林團隊利用所發展的手性螺環銥催化劑Ir-SpiroPAP催化的不對稱催化氫化反應(關鍵步驟),完成了7個Mulinane型二萜和2個類似物的不對稱全合成[11]。
3 結語
周期林院士團隊發展的手性螺環催化劑在許多不對稱催化反應中都表現出優異的催化效率和對映選擇性,成為為數不多的一類“優勢手性骨架”。手性螺環催化劑已經被國際同行成功應用于150余種有機合成反應中。國際知名制藥公司,如羅氏制藥和九州制藥等已經將手性螺環催化劑用于Aleglitazar和Rivastigmine等手性藥物的生產。國際著名試劑公司Aldrich、Strem、J&K等已將這些手性螺環配體和催化劑進行商品化生產和銷售。
本題結合南開大學周其林院士團隊在手性螺環催化劑的前沿研究,考查了手性螺環配體SpiroPAP的合成路線,手性螺環催化劑Ir-SpiroPAP的制備及其在合成中的應用。主要涉及的知識點包括羥醛縮合、雙鍵氫化、傅氏酰基化、醚的脫保護、還原胺化反應、烷基化反應、不飽和酮的1,2-加成,1,4-加成反應,以及金屬絡合物中Ir金屬的氧化態和外層d軌道價電子的判斷等。該題所涉及到的大部分知識點,都包含在預備題聯烯以及天然產物全合成的題目中。

