摻雜天然膠乳的鑒別及分析方法研究
林卓遠,鄧珍達,王兵兵,李高榮,廖祿生,3,林宏圖,3*
(1.中國熱帶農業科學院農產品加工研究所 農業農村部熱帶作物產品加工重點實驗室,廣東 湛江 524001;2.華中科技大學,湖北 武漢 430074;3.海南省天然橡膠加工重點實驗室,廣東 湛江 524001)
目前天然膠乳的收購多以干膠含量作為質量評價和交易議價指標。近年來一些產膠地區出現了天然膠乳摻雜現象,目的是增大干膠含量測定值,從而牟取暴利。楊映華等[1-2]認為天然膠乳中主要摻入了尿素、蔗糖、淀粉、膩子粉和滑石粉等物質。李寧寧[3]考察了在新鮮天然膠乳中摻入淀粉、小蘇打(碳酸氫鈉)、明膠、食鹽(氯化鈉)、底漆等物質的檢測方法。周聰等[4]研究了分別摻入淀粉、雙灰粉、石灰粉、尿素、蔗糖的天然膠乳在高溫烘烤后的外觀及氣味特征。經過走訪調查得知,天然膠乳中常用的摻雜物除了上述物質外,還有氯化銨、硫酸銨、碳酸鈣、高嶺土等。
測定天然膠乳干膠含量的方法很多,包括標準法、快速總固體法、相對密度法等,目前被廣泛使用的還有微波法,而通常會采用化學凝固法(標準法)作對檢和鑒定[5]。
本工作研究影響天然膠乳干膠含量測量值的白糖、食鹽、淀粉、尿素、氯化銨、硫酸銨、碳酸氫鈉、碳酸鈣、滑石粉、高嶺土和石灰粉11種可能的天然膠乳摻雜物檢測,重點討論摻入高嶺土、碳酸鈣、滑石粉和淀粉的天然膠乳的定性及定量分析方法,以利于收膠站及橡膠加工企業對天然膠乳的質量進行評定。
1 實驗
1.1 主要原材料
天然膠乳,廣東農墾勝利農場有限公司產品;白糖、食鹽、淀粉、尿素、氯化銨、硫酸銨、碳酸氫鈉、碳酸鈣、滑石粉、高嶺土和石灰粉,市售品;鉻天青S、鉻黑T和鎂試劑,分析純,廣東光華科技股份有限公司產品;鈣試劑,分析純,上海科拉曼試劑有限公司產品。
1.2 主要設備和儀器
DH925D型微波膠乳測試儀,北京大華無線電儀器有限責任公司產品;SN-LSC-40S型離心機,上海尚普儀器設備有限公司產品;SMR-640H型精密恒溫干燥箱,無錫施耐爾電子設備有限公司產品;722S型可見分光光度計,上海儀電科學儀器股份有限公司產品。
1.3 樣品制備
取白糖、食鹽、淀粉、尿素、氯化銨、硫酸銨、碳酸氫鈉、碳酸鈣、滑石粉、高嶺土和石灰粉各2 g,分別加入到11份100 g的新鮮天然膠乳中,攪拌均勻后得到11個摻雜天然膠乳樣品,立即使用微波法、快速總固法和標準法[6-7]測干膠含量。
取上述樣品,按照GB/T 8293—2019[8],通過離心法獲得橡膠非膠組分及不溶摻雜物的混合沉渣,用于后續的檢測;除去沉渣的摻雜天然膠乳樣品采用酸凝、烘干制成生膠樣品。
1.4 測試分析
摻雜天然膠乳定性及定量分析:(1)摻入高嶺土的天然膠乳采用鉻天青S溶液顯色法定性分析,采用分光光度法[9]定量分析;(2)摻入碳酸鈣的天然膠乳采用鹽酸反應法定性分析,采用滴定法[10]定量分析;(3)摻入滑石粉的天然膠乳采用鎂試劑顯色法定性分析,采用滴定法[11]定量分析;(4)摻入淀粉定性的天然膠乳采用碘試劑法定性分析。
2 結果與討論
2.1 天然膠乳的干膠含量測定
不同摻雜物天然膠乳樣品的干膠含量(質量分數)檢測結果如表1所示。
從表1可以看出:摻入食鹽、氯化銨的天然膠乳樣品未能使得微波法干膠含量測定值增大;摻入白糖、尿素、硫酸銨和碳酸氫鈉的天然膠乳樣品雖然使微波法干膠含量測定值增大,但由于摻雜物的水溶性較好,當使用標準法檢測干膠含量時由于摻雜物溶解于水中,不能增大標準法干膠含量測定值,表明收膠站及橡膠加工企業如果嚴格執行微波法與標準法對檢是可以鑒別大部分摻雜天然膠乳的;摻入石灰粉會使新鮮天然膠乳迅速凝固,無法采用這3種方法檢測干膠含量,這是由于鈣離子作用的結果。排除以上摻雜物,本工作主要討論影響天然膠乳干膠含量測量值的摻雜物淀粉、碳酸鈣、滑石粉和高嶺土的檢測,定性及定量分析摻雜天然膠乳。
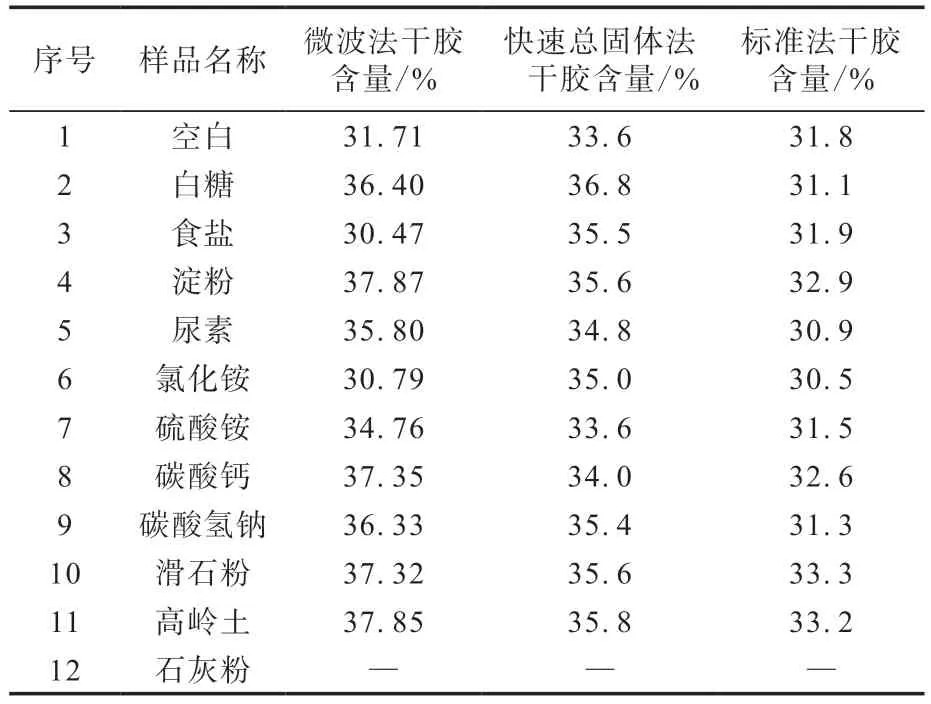
表1 天然膠乳樣品的干膠含量Tab.1 Dry rubber contents of natural latex samples
2.2 摻入高嶺土的天然膠乳的定性及定量分析
2.2.1 試驗原理
高嶺土的主要成分為Al2O3·2SiO2·2H2O,屬于不溶于水的鋁鹽,其酸溶解物能與鉻天青S形成呈紫色至玫瑰紅色的配合物,根據鋁離子的濃度不同,配合物溶液的顏色深淺有明顯梯度變化,因此本試驗采用顯色法定性分析以及分光光度法定量分析。
2.2.2 試劑配制
質量濃度為0.01 g·mL-1的鉻天青S溶液:取0.5 g鉻天青S,用50 mL 1/1的乙醇/水溶液溶解。
鋁離子標準溶液:準確稱取十二水硫酸鋁鉀0.467 6 g加入容量瓶中,定容至250 mL。
pH值為6的醋酸-醋酸銨緩沖液:取100 g醋酸銨溶于300 mL去離子水中,再加8 mL醋酸制備得到。
2.2.3 定性分析
檢測天然膠乳離心沉渣中是否有鋁鹽存在,從而鑒別天然膠乳中是否摻入高嶺土。試驗方法:取天然膠乳離心沉渣,向沉渣中加入少許體積比為1/3的鹽酸/水溶液進行浸泡溶解,于電爐上煮沸3 min,過濾,再向濾液中加入物質的量濃度為4 mol·L-1的氫氧化鈉溶液中和至pH值為6,滴入質量濃度為0.01 g·mL-1鉻天青S溶液,溶液呈現紫色到玫瑰紅色,表明天然膠乳中摻入高嶺土。在實際工作中,只要收膠站及橡膠加工企業的實驗室預先配制試劑,便可實現天然膠乳中是否摻入高嶺土的快速檢測。
2.2.4 定量分析
2.2.4.1 樣品處理
取烘干的天然膠乳離心沉渣3.782 1 g,研磨成粉末或碎屑狀,用1/3的鹽酸/水溶液進行浸泡溶解,于電爐上小火加熱處理1 h,過濾,再向濾液中加入物質的量濃度為4 mol·L-1的氫氧化鈉溶液中和至pH值為6,再加2 mL質量濃度為0.01 g·mL-1的鉻天青S溶液以及5 mL pH值為6的醋酸-醋酸銨緩沖液,定容至50 mL。
取生膠樣品4.955 7 g于電爐上加熱碳化,再于馬弗爐中600 ℃灼燒2 h,灰分溶于稀鹽酸/水溶液中,溶液于電爐上小火加熱處理11 h,過濾,按上述方法定容至50 mL。
2.2.4.2 建立標準工作曲線
取鋁離子標準溶液0,1.0,2.5,5.0,8.0和10.0 mL,加入醋酸-醋酸銨緩沖液,定容至50 mL,在波長為561 nm下測定鋁離子標準溶液的吸光度,結果如表2所示。
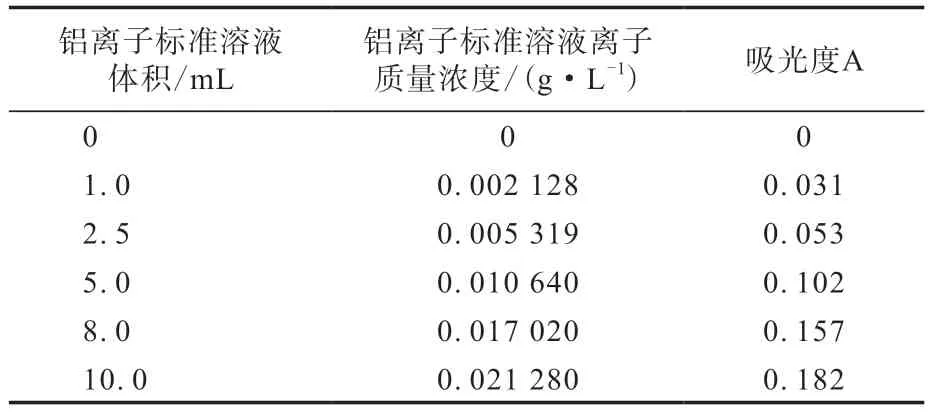
表2 鋁離子標準溶液的吸光度Tab.2 Absorbances of aluminumion standard solutions
根據表2繪制的鋁離子溶液的標準吸光度曲線的線性方程為y=8.976 6x,相關因數(R2)=0.989。
2.2.4.3 樣品檢測
分別測定生膠灰分溶解液和離心沉渣溶解液的吸光度,結果如表3所示。
通過表3可計算得到,生膠灰分溶解液和沉渣溶解液中鋁離子的質量濃度分別為0.003 565和0.013 81 g·L-1。換算為高嶺土在生膠成品中和沉渣中的含量分別為0.172和0.873 mg·g-1。說明摻入高嶺土的天然膠乳可通過離心沉降法除去大部分摻雜物,但仍有部分摻雜物存在于生膠成品中無法除去。

表3 樣品溶液的吸光度Tab.3 Absorbances of sample solutions
由于檢測摻雜高嶺土天然膠乳的定量分析方法比定性方法復雜,檢測需要一定時間,因此定量分析方法更適合后續的檢測及研究。
2.3 摻入碳酸鈣和滑石粉的天然膠乳的定性及定量分析
2.3.1 試驗原理
碳酸鈣是一種難溶于水的鈣鹽,為雙飛粉、膩子粉的主要成分;滑石粉的主要成分為Mg3[Si4O10](OH)2,也不溶于水。針對鈣鹽和鎂鹽一般可溶于強酸的特點,本試驗選擇對摻雜天然膠乳中的鈣離子和鎂離子同時進行檢測。摻入碳酸鈣的天然膠乳離心沉渣遇到鹽酸后會釋放出大量二氧化碳,摻入滑石粉的天然膠乳離心沉渣遇到鎂試劑時先呈深綠色,最后生成天藍色或者深藍色的絮狀沉淀物。雖然文獻[5]認為天然膠乳中自然存在著微量的鈣離子和鎂離子,但是通過試驗證明無人為摻雜鈣離子和鎂離子的天然膠乳離心沉渣不會有上述表現。
本試驗采用配位滴定法,用已標定濃度的乙二胺四乙酸二鈉溶液(EDTA)測定沉渣溶解液中鈣離子(Ca2+)和鎂離子(Mg2+)的含量,反應式如下:
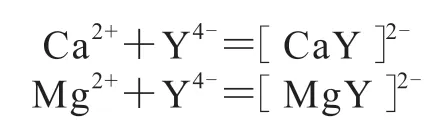
式中,Y為配位的EDTA。
本試驗使用的顯色劑為鈣試劑和鉻黑T。鈣試劑與鈣離子結合時,呈現紫紅色;當EDTA奪取鈣試劑中鈣離子后,溶液顯藍色;當EDTA奪取鉻黑T中與其結合的離子時,溶液由酒紅色變為純藍色。
2.3.2 試劑配制
pH值為10的氯化銨-氨水緩沖溶液:取13.5 g氯化銨,溶于少許去離子水中,再加入87.5 mL濃氨水,定容至250 mL。
質量濃度為0.01 g·mL-1的鎂試劑和鉻黑T試劑:取0.5 g鎂試劑和鉻黑T,分別溶于50 mL去離子水中。
物質的量濃度為0.01 mol·L-1的EDTA滴定溶液:取0.93 g EDTA溶于水,定容至250 mL,其標定后的物質的量濃度為0.010 17 mol·L-1。
2.3.3 定性分析
檢測天然膠乳離心沉渣中是否有碳酸鈣和滑石粉的存在,從而鑒別摻雜天然膠乳。試驗方法:取天然膠乳離心沉渣,加入體積比為1/3的鹽酸/水溶液進行浸泡溶解,沉渣中產生大量氣泡表明摻有碳酸鈣;過濾沉渣,向濾液中加入物質的量濃度為4 mol·L-1的氫氧化鈉溶液中和至中性或弱堿性,逐滴滴加質量濃度為0.01 g·mL-1的鎂試劑,溶液產生深藍色的絮狀沉淀物,即證明摻有滑石粉。收膠站及橡膠加工企業的實驗室也可以通過預先配制試劑,實現天然膠乳中是否摻入碳酸鈣和滑石粉的快速檢測。
2.3.4 定量分析
若樣品中同時含有鈣離子和鎂離子時,鈣離子和鎂離子將被同時滴定測出,此處以摻入碳酸鈣的天然膠乳樣品作為樣例說明。
2.3.4.1 樣品處理
取烘干的天然膠乳離心沉渣2.971 7 g,研磨成粉末或碎屑狀,用10 mL體積比為1/3的鹽酸/水溶液溶解,小火加熱浸煮1 h,加入物質的量濃度為4 mol·L-1的氫氧化鈉溶液中和至中性,定容至100 mL。
取生膠樣品5.076 6 g,于電爐上加熱碳化,再放入馬弗爐中600 ℃處理2 h,使之完全轉化為灰分。用少量稀鹽酸/水溶液溶解灰分,再加入氫氧化鈉溶液中和至中性,定容至100 mL。
2.3.4.2 樣品檢測
分別取一定量的天然膠乳離心沉渣溶解液和生膠灰分溶解液,加入5 mL pH值為10的氯化銨-氨水緩沖溶液、2滴質量濃度為0.01 g·mL-1的鉻黑T,用已標定的EDTA溶液滴定至體系由酒紅色變為純藍色即為終點。各組試驗平行滴定3次,試驗數據如表4和5所示。
由表4計算可知,沉渣溶解液中鈣離子和鎂離子的總物質的量濃度為0.098 22 mol·L-1,相對平均偏差為0.1%,換算為碳酸鈣在沉渣中的含量為3.3 mg·g-1。

表4 滴定天然膠乳離心沉渣溶解液消耗的EDTA溶液體積Tab.4 EDTA solution volumes consumed for titration of natural latex centrifuge sediment solution
由表5計算可知,灰分溶解液中鈣離子和鎂離子的總物質的量濃度為0.018 31 mol·L-1,相對平均偏差為1.2%,換算為碳酸鈣在生膠中的含量為0.36 mg·g-1。

表5 滴定生膠灰分溶解液消耗的EDTA溶液體積Tab.5 EDTA solution volumes consumed for titration of raw rubber ash solution
由兩種樣品的檢測數據比較可以看出,摻入碳酸鈣的天然膠乳采用離心沉降工藝能除去大部分的摻雜物。若要精確滴定生膠中碳酸鈣和滑石粉含量,可以配置濃度更低的EDTA溶液。
2.4 摻入淀粉的天然膠乳的定性分析
2.4.1 試驗原理
根據淀粉遇碘可形成藍色化合物的原理,可用碘化鉀試劑快速檢測新鮮天然膠乳中是否摻有淀粉,但未能找到定量檢測摻入淀粉的天然膠乳的合適方法。摻入淀粉的天然膠乳在經過離心沉降、酸凝固、壓縐等加工環節后,淀粉可能會分布在離心沉渣及成品生膠中。因此,本試驗同樣檢測離心沉渣及生膠樣品中是否含有淀粉。
2.4.2 樣品檢測
取一定量天然膠乳離心沉渣,在80 ℃的水浴中加熱1 h,過濾,得到離心沉渣浸出液;取一定量生膠樣品,在80 ℃水浴中加熱1 h,過濾,得到生膠樣品浸出液。樣品浸出液滴加碘化鉀的現象如表6所示。

表6 樣品浸出液滴加碘化鉀的現象Tab.6 Phenomenon of driping potassium iodide to sample leaching liquids
從表6可以看出:摻入淀粉的天然膠乳離心沉渣浸出液滴加碘化鉀后變藍;生膠樣品浸出液滴加碘化鉀后不變藍,其原因可能是淀粉被橡膠包裹,在80 ℃水中浸泡時淀粉難以析出,因此未能檢測出。
3 結論
摻入高嶺土的天然膠乳:向離心沉渣溶解液中滴入鉻天青S溶液,溶液呈顯紫色至玫瑰紅色,證明高嶺土的摻入;摻雜碳酸鈣的天然膠乳:離心沉渣加入鹽酸/水溶液溶解,離心沉渣中產生大量氣泡,證明碳酸鈣的摻入;摻雜滑石粉的天然膠乳:離心沉渣加入鹽酸/水溶液溶解后滴加鎂試劑,溶液產生深藍色的絮狀沉淀物,證明滑石粉的摻入;摻雜淀粉的天然膠乳:向離心沉渣浸出液滴加碘化鉀,浸出液變藍,證明淀粉的摻入。
在實際工作中,只要收膠站及橡膠加工企業的實驗室預先配制相應的試劑,便可實現摻雜天然膠乳簡單、快速、準確地檢測。

