淋巴瘤臨床研究—2022 年ASCO 會議報告*
陳馨蕊 石遠凱
淋巴瘤是中國常見惡性腫瘤之一,包括霍奇金淋巴瘤(Hodgkin’s lymphoma,HL)和非霍奇金淋巴瘤(non-Hodgkin’s lymphoma,NHL)。國內每10 萬人HL和NHL 的發病率分別為0.46% 和4.29%,死亡率分別為0.19%和2.45%[1]。傳統的化療藥物已不能滿足臨床需要,近年來腫瘤免疫治療藥物、細胞治療和靶向藥物的良好療效及安全性為淋巴瘤患者帶來新的希望。2022 年6 月召開的第58 屆美國臨床腫瘤學會(ASCO)年會報道了全球腫瘤領域研究的最新進展。本文將根據淋巴瘤不同組織分型對2022 年ASCO 年會中淋巴瘤臨床研究領域最新成果進行綜述。
1 HL
HL 患者在接受一線放化療后有較高的緩解率和較長的生存期,但仍有10%~15% 的患者出現復發,這部分患者通常對傳統化療不敏感[2]。近年,抗體偶聯藥物(antibody-drug conjugate,ADC)及免疫檢查點抑制劑的出現為這類患者提供了新的選擇。
維布妥昔單抗(brentuximab vedotin,Bv)是由抗CD30 單克隆抗體和MMAE 組成的ADC 藥物。多項研究結果表明,Bv 單藥或聯合化療方案在初治及復發/難治(relapse/ refractory,r/r)經典型霍奇金淋巴瘤(classic Hodgkin’s lymphoma,cHL)患者的治療中顯示出較高的緩解率[3-6]。2022 年ASCO 年會公布了應用Bv 聯合化療方案治療初治Ⅲ/Ⅳ期cHL 患者的ECHELON-1 研究的最新隨訪結果(摘要編號7503)。中位隨訪時間為73 個月,A+AVD(Bv,多柔比星,長春新堿,達卡巴嗪)組與ABVD(多柔比星,博來霉素,長春新堿,達卡巴嗪)組6 年總生存(overall survival,OS)率分別為93.9%與89.4%(P=0.009),6 年無進展生存(progression-free survival,PFS)率分別為82.3%和74.5%(P=0.002)。與ABVD 組患者相比,A+AVD 組患者的治療方案中無博來霉素,因此這組患者第二次惡性腫瘤發生率更低,在隨訪期間有更多的女性患者懷孕或生產。
淋巴細胞活化基因3(lymphocyte activation gene-3,LAG-3)為T 細胞表面抑制性受體。體內、外研究結果顯示,同時拮抗LAG-3 和程序性細胞死亡蛋白-1(programmed cell death protein-1,PD-1)可增強T 細胞抗腫瘤作用[7-9]。2022 年ASCO 年會公布了IgG4 LAG-3 抑制劑favezelimab 聯合帕博利珠單抗(pembrolizumab)治療r/r cHL 的Ⅰ/Ⅱ期臨床研究結果(摘要編號7516)。30例入組患者客觀緩解率(objective response rate,ORR)為73%,其中7 例患者為完全緩解,中位PFS(median PFS,mPFS)為19 個月。最常見的不良事件(adverse event,AE)是甲狀腺功能減退、疲勞、輸液相關反應、頭痛、關節痛、甲狀腺功能亢進、肌痛和惡心。3 級以上治療相關AE 發生率為20%。LAG-3 抑制劑聯合PD-1 抑制劑與既往PD-1 抑制劑單藥治療r/r cHL 結果相似[10-11]。因此,LAG-3 抑制劑能否使r/r cHL 患者獲益有待進一步探究。
2 NHL
2.1 彌漫性大B 細胞性淋巴瘤
彌漫性大B 細胞性淋巴瘤(diffuse large B-cell lymphoma,DLBCL)是NHL 最常見的病理類型,一線治療后有30%~50% 患者出現復發或難治[12]。2022年ASCO 年會上公布了多項DLBCL 免疫治療和細胞治療的研究結果(表1)。

表1 2022 年ASCO 會議中免疫療法治療DLBCL 相關研究匯總
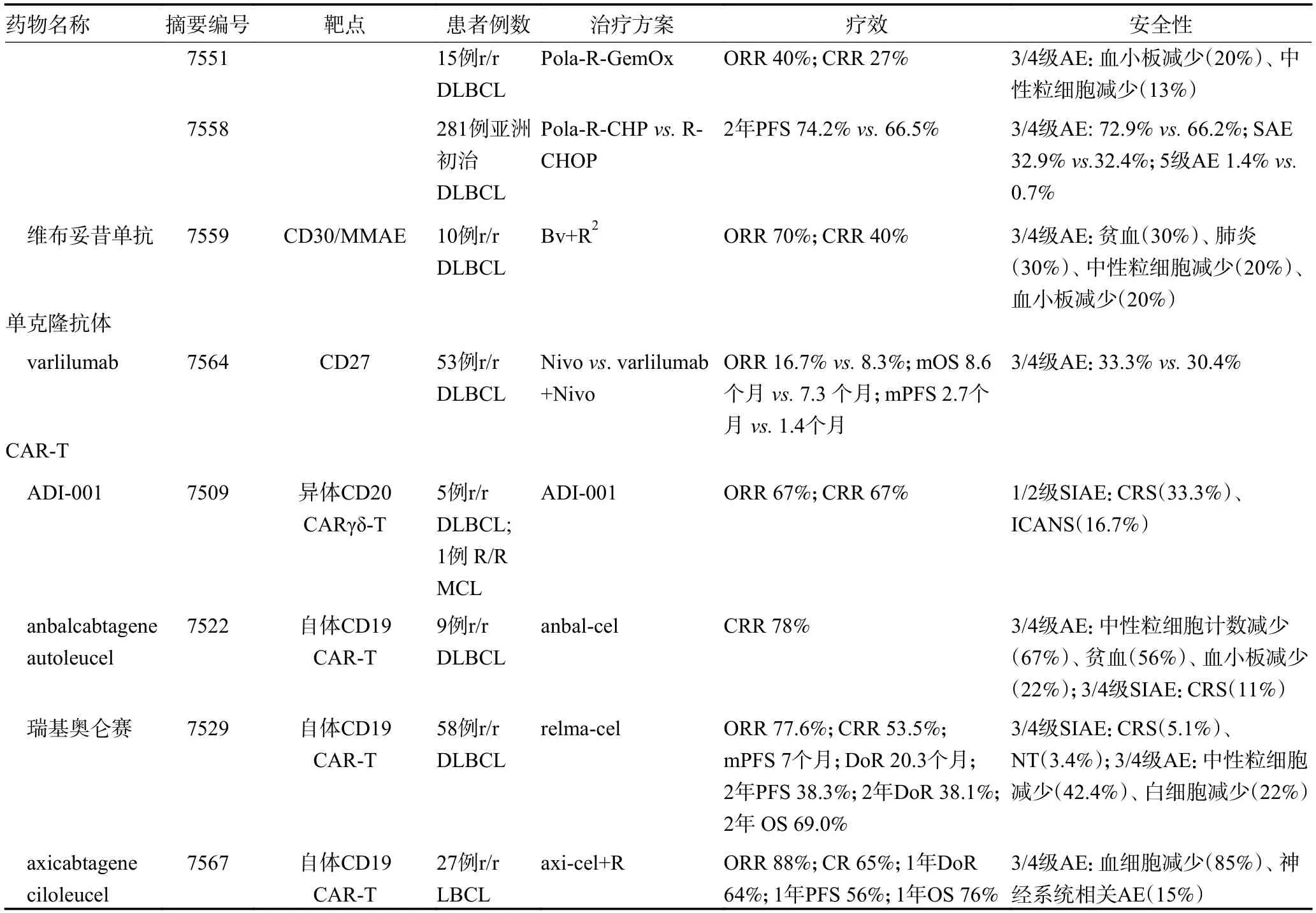
表1 2022 年ASCO 會議中免疫療法治療DLBCL 相關研究匯總 (續表1)
2.1.1 雙特異性抗體 雙特異性抗體(bispecific antibody )具有同時靶向細胞毒性T 細胞表面CD3 和腫瘤細胞表面特異性抗原的特性,通過這一機制激活T細胞殺傷腫瘤[13]。在2022 年ASCO 年會上,澳大利亞學者口頭匯報了glofitamab 單藥治療r/r DLBCL患者的關鍵Ⅱ期擴展研究結果(摘要編號7500)。Glofitamab 是一種新型雙特異性抗體藥物,以2∶1結構同時與B 細胞表面CD20 雙價和細胞毒性T 細胞表面CD3 單價結合發揮抗腫瘤作用。本研究納入155 例先前至少接受過2 線治療的DLBCL 患者,ORR 和完全緩解率(complete response rate,CRR)分別為51.6% 和39.4%,mPFS 為4.9 個月。雖然63%的患者發生了細胞因子釋放綜合征(cytokine release syndrome,CRS),但僅有3.9%為3 級以上。目前,glofitamab 在中國的注冊臨床研究正進行中(NCT0465 7302)。此外,另一種靶向CD3/CD20 的雙特異性抗體藥物epcoritamab,單藥治療r/r DLBCL 時ORR 為68%,CRR 為45%[14]。在聯合傳統方案治療初治及r/r DLBCL 的研究中均表現出較好的療效和安全性(表1)。靶向CD3/CD20 的雙特異性抗體在一線應用CD20 單抗治療后復發、不適合接受移植或接受嵌合抗原受體 T 細胞(chimeric antigen receptor T-cell,CAR-T)治療后復發的患者中表現出較好的療效。
2.1.2 抗體偶聯藥物 波妥珠單抗維多丁(polatuzumab vedotin,Pola)是首款CD79b 抗體偶聯甲基澳瑞他汀E(monomethyl auristatin E,MMAE)的ADC 類藥物,通過破壞B 細胞分裂發揮作用。在2022 年ASCO 年會公布的Pola-DA-EPCH-R 方案治療初治侵襲性B 細胞淋巴瘤的初步結果(摘要編號7546)顯示,納入的18 例患者ORR和CRR 分別為88%和24%。但嚴重AE 發生較多,包括1 例5 級敗血癥/腸炎,3 例發熱性中性粒細胞減少癥,1 例3 級結腸憩室穿孔。這與年會其他Pola 聯合治療方案(表1)及既往Pola 相關研究報道相似,盡管包含Pola 的治療方案在初治及r/r DLBCL 患者中顯示出較好療效,但治療相關AE 的增加可能會限制其臨床應用[15-16]。
2.1.3 嵌合抗原受體 T 細胞 近年來,基于JULIET、ZUMA-1 和TRANSCEND 的研究數據,靶向CD19的自體CAR-T 細胞產品axicabtagene ciloleucel、tisagenlecleucel、lisocabtagene maraleucel 已被美國食品藥物監督管理局(FDA)批準上市,用于復發或≥2 線方案無效的DLBCL 患者的治療[17]。但應用過程中的脫靶效應和腫瘤細胞免疫逃逸等問題仍待解決[18]。本次年會中,美國學者公布的ADI-001 的Ⅰ期研究報道異體CD20 靶向CARγδ-T 細胞療法用于治療成人r/rB細胞淋巴瘤(摘要編號7509)。利用γδ-T 細胞不需要與主要組織相容性復合物分子結合的特點,直接識別并結合腫瘤細胞表面抗原,補充CAR 的靶向作用,同時減少移植物抗宿主反應的發生。在可評價的6 例患者中,用藥第28 天ORR 為67%,且全部患者達到完全緩解。特別關注的AE(special interest AE,SIAR)中2 例患者出現1/2 級CRS,1 例患者出現1 級免疫效應細胞相關神經毒性綜合征(immune effector cellassociated neurotoxicity syndrome,ICANS)[19]。
RELIANCE 研究是應用國產瑞基奧侖賽(relmacabtagene autoleucel,relma-cel)靶向CD19 的自體CAR-T 細胞治療r/r 大B 細胞淋巴瘤(large B-cell lymphoma,LBCL)的臨床研究。在2022 年ASCO 年會上中國學者公布了RELIANCE 研究的2 年隨訪結果(摘要編號7529)。在可評價的58 例患者中,2 年最佳ORR 和CRR 分別為77.6%和53.5%。2 年OS率為69.0%。但3 級以上的AE 發生率是72.9%。
目前,自體CAR-T 細胞療法顯著改善了不可接受造血干細胞移植和多線治療后進展的B 細胞淋巴瘤患者的預后,異體CAR-T 細胞療法也顯示出廣闊的應用前景。但臨床研究樣本量較小且隨訪時間有限,有效性及安全性有待進一步探究。
2.2 濾泡淋巴瘤
濾泡淋巴瘤(follicular lymphoma,FL)是最常見的惰性NHL,多數患者對治療反應較好,但初始治療后24 個月內復發及多線治療后耐藥的患者預后較差[20]。
2.2.1 磷脂酰肌醇3-激酶抑制劑 近年來,靶向藥物磷脂酰肌醇3-激酶(phosphatidylinositol 3-kinase,PI3K)抑制劑idelalisib、copanlisib 和duvelisib 單藥已嘗試用于r/r FL 的治療,但僅展現出中等程度的活性(ORR 為43.8%~57.0%,CRR 為1.6%~15.0%)。且除血液學相關AE 外,感染及免疫相關AE 發生率較高[20]。在2022 年ASCO 年會上公布了兩項PI3K抑制劑的研究結果(摘要編號7511、7574)。兩種新型PI3Kδ 抑制劑zandelisib 及parsaclisib 單藥在治療r/r FL 中均表現出較好的療效,ORR 分別達到70.3%和86.9%,CRR 分別為35.2% 和31.1%。Zandelisib的研究結果顯示3 級SIAE(腹瀉,結腸炎,皮疹,口腔炎,轉氨酶升高)的發生率均≤5%。
2.2.2 Bruton 酪氨酸激酶抑制劑 澤布替尼(zanubrutinib,Z)為中國自主研發的Bruton 酪氨酸激酶(Bruton's tyrosine kinase,BTK)抑制劑,被批準用于套細胞淋巴瘤、成人慢性淋巴細胞白血病/小淋巴細胞淋巴瘤和華氏巨球蛋白血癥的治療。有研究顯示,單藥澤布替尼治療r/r FL 的ORR 僅為36.4%,CRR 為18.2%,mPFS 為10.4 個月[21]。意大利學者在本次年會上公布了ROSEWOOD 研究主要結果,比較Z 聯合奧比妥珠單抗(obinutuzumab,O)對比O 單藥治療r/r FL 患者的療效和安全性(摘要編號7510)。納入的217 例患者隨機分配到ZO 組(n=145)和O 組(n=72)。結果顯示,ZO 組的ORR 顯著高于O 組(68.3%vs.45.8%,P=0.002)。ZO 組mPFS 顯著長于O 組患者,分別為27.4 個月和11.2 個月(HR=0.51,95% CI:0.32~0.81,P=0.004)。18 個月的OS 率為85.4%(ZO 組)vs.72.6%(O 組,HR=0.37,95% CI:0.23~0.60,P<0.001)。常見≥3 級AE 是血液學相關AE。r/r FL 對ZO 聯合方案的療效優于Z 或O 單藥,且AE 無明顯增加[21]。
2.2.3 組蛋白去乙酰化酶抑制劑 在2022 年ASCO年會上公布了由中國醫學科學院腫瘤醫院牽頭開展的新型泛靶點口服組蛋白去乙酰化酶抑制劑(histone deacetylase inhibitor,HDACi)艾貝司他(abexinostat)治療r/r FL 的療效及安全性的Ⅱ期臨床研究結果(摘要編號7513)。在研究中艾貝司他采用“服用1 周,停止1 周”的方式用藥。在37 例可評價療效的患者中,ORR 為70%,CRR 為16%。其中≥60 歲的16 例患者ORR 為88%,CRR 為31%。常見3 級及以上治療相關AE 為血小板減少(41%)、中性粒細胞減少(27%)、白細胞減少(7%)、淋巴細胞減少(7%)、Q-T間期延長(7%)和貧血(5%)。
2.2.4 果蠅zeste 基因增強子人類同源物2 抑制劑2022 年ASCO 年會上還公布了組蛋白甲基轉移酶果蠅zeste 基因增強子人類同源物2(enhancer of zeste homolog 2,EZH2)抑制劑SHR2554 治療r/r 成熟細胞淋巴瘤的Ⅰ期研究結果(摘要編號7525),在納入的84 例r/r 成熟細胞淋巴瘤患者中(41 例FL,22 例外周T 細胞淋巴瘤和21 例cHL),FL 患者ORR 為58.5%,EZH2 突變型FL 患者的ORR 比野生型患者略高(62.5%vs.55.2%)。所有患者中位持續反應時間(duration of response,DoR)為9.3 個月。
2.3 套細胞淋巴瘤
套細胞淋巴瘤(mantle cell lymphoma,MCL)是一種罕見的NHL 亞型,免疫化療和造血干細胞移植是標準的一線治療策略。但是對于不可耐受高劑量化療的老年患者或進入r/r 階段的MCL 患者需要更有效且耐受性更好的治療方案[22]。伊布替尼(ibrutinib)聯合利妥昔單抗(rituximab)方案在初治老年MCL 患者中表現出較好的療效及較低的骨髓毒性。ORR 達到96%,CRR 為71%,3 年PFS 和OS 分別為87%和94%。3/4 級骨髓抑制發生率<5%[23]。2022 年ASCO年會Michael Wang 口頭報告在初治老年MCL 患者中應用伊布替尼聯合苯達莫司汀(bendamustine)和利妥昔單抗(Ibr+BR),后續利妥昔單抗維持治療的SHINE 研究結果引起了廣泛關注(摘要編號7 502)。將納入的523 例患者隨機分配至Ibr+BR 組(n=261)或安慰劑(Pbo)+BR 組(n=262),并在治療后采用利妥昔單抗維持治療。入組患者中位年齡為71 歲,Ibr+BR 組 的ORR 為89.7%,CRR 為65.5%,pbo+BR組ORR 為88.5%,CRR 為57.6% 。Ibr+BR 組與pbo+BR 組相比mPFS 顯著延長2.3 年(80.6 個月vs.52.9 個月,P=0.011)。雖然Ibr+BR 組房顫發生率較Pbo+BR 組稍高(13.9%vs.6.5%),但大出血、高血壓、關節痛和繼發性惡性腫瘤等其他AE 發生率兩組相似。目前,BTK 抑制劑仍是r/r MCL 有效率較高的靶向藥物,未來該藥聯合方案可能成為初治老年MCL 及r/r MCL 患者的新選擇。
2.4 外周T 細胞淋巴瘤
外周T 細胞淋巴瘤(peripheral T-cell lymphoma,PTCL)是起源于胸腺成熟T 細胞或NK/T 細胞的一組具有高度異質性的NHL,占我國淋巴瘤患者的23.3%[24]。
2.4.1 免疫檢查點抑制劑 結外自然殺傷/T 細胞淋巴瘤(extranodal natural killer/T-cell lymphoma,ENKTL)為PTCL 亞型,在亞洲國家發病率顯著高于西方國家[24-26]。對于晚期和復發的ENKTL 患者以化療為主的治療方法5 年生存率僅為40%[25]。2022 年ASCO 年會上中國學者口頭報告的GEMSTONE-201 研究旨在評價PD-L1 抑制劑舒格利單抗(sugemalimab)單藥治療成人r/r ENKTL 的有效性和安全性(摘要編號7501)。結果顯示在78 例可評價的患者中,ORR 為46.2%,CRR 為37.2%,1 年DoR 為86%,2 年OS 率為54.6%。39%的患者出現了3 級以上AE。2020 年Kim 等[27]發表的應用PD-L1 單抗avelumab治療r/r ENKTL 的Ⅱ期臨床研究結果顯示,ORR 為38%,CRR 為24%,mPFS 僅為2.7 個月,結果并不理想。而舒格利單抗在r/r ENKTL 患者中表現出相對持久的抗腫瘤活性,與其他PD-L1 單抗相比,具有更高的CRR 和良好的OS 獲益趨勢。
2.4.2 造血干細胞移植 造血干細胞移植治療PTCL的相關研究較少[28-29]。2019 年ASCO 年會德國學者公布了AATT 研究結果,該研究前瞻性地比較了初治PTCL 患者常規治療后接受異基因造血干細胞移植(allogeneic transplantation,alloSCT)與自體造血干細胞移植(autologous transplantation,autoSCT)作為鞏固治療的療效和安全性。結果顯示,初治PTCL 患者接受alloSCT 或autoSCT 鞏固均有較高的緩解率,且3 年PFS 和OS 均無統計學差異[30]。2022 年ASCO年會該團隊公布了7 年隨訪結果(摘要編號7534)。在AATT 研究中實際參與移植的患者(n=67)中,雖然兩組之間患者的生存仍無顯著差異(autoSCT 組vs.alloSCT 組:7 年無事件生存率為50%vs.61%,P=0.403,7 年OS 為72%vs.61%,P=0.349)。但autSCT組患者復發率較alloSCT 組患者高(42%vs.5%)。AutoSCT 后復發的15 例患者中,10 例患者接受allo-SCT 作為后線治療,其中8 例患者生存時間為39~94 個月;未接受alloSCT 的患者的5 年生存率僅為17%。因此,對較年輕符合SCT 條件的PTCL 患者,SCT 仍是首選的鞏固治療方案,接受autoSCT 后復發的患者行alloSCT 挽救治療方案可延長生存期。
3 結語
淋巴瘤的治療模式正在發生改變,靶向治療、免疫治療和細胞治療的進展十分迅速,基礎研究成果不斷向臨床轉化。新靶點和新作用機制的藥物、新療法和新方案在淋巴瘤患者中表現出較好療效和安全性,期待更多的研究成果問世,為初治及復發/難治的淋巴瘤患者帶來新的希望。

