256例ACI患者溶栓后早期神經功能惡化高危因素
吳丹霞
急性腦梗死(acute cerebral infarction,ACI)是因缺氧缺血、血液供應障礙而引發的局部腦組織缺血軟化或壞死,患病率、致殘率、死亡率較高,可給社會及患者家庭造成沉重負擔[1]。故提高ACI治療效果,改善預后是目前亟待解決問題。阿替普酶是常用溶栓藥,能有效疏通腦血管,改善血供,降低致殘率,已成為臨床首選ACI治療方法,其有效性、安全性已經臨床多項試驗證實[2-3]。但受多種因素影響,ACI患者溶栓后仍可能出現早期神經功能 惡 化(early neurological deterioration,END),甚至死亡[4]。因此深入探討溶栓后END發生的機制及有關原因顯得尤為重要。本研究通過分析ACI患者溶栓后END的高危因素,旨在為臨床早期預防、干預提供理論依據,現報告如下。
1 資料與方法
1.1 一般資料
選取2018年1月-2021年12月福建醫科大學附屬第一醫院256例ACI患者。納入標準:MRI或CT診斷證實為ACI,符合文獻[5]《急性腦梗死早期中西醫結合診療方案貴州專家共識》中ACI診斷標準;年齡>18歲,發病4.5 h內給予溶栓治療;顱腦CT診斷無腦出血征象。排除標準:顱內占位、顱內出血、顱內動脈瘤史;既往3個月內有腦卒中史或腦外傷史;血管內治療或靜脈溶栓史;嚴重心、腎、肺、肝功能不全;近3周有泌尿系統或胃腸出血史。其中女82例,男174例,年齡54~73歲,平均(63.82±4.29)歲。本研究經本院倫理委員會審核批準,患者或家屬知情研究,簽署同意書。
1.2 方法
1.2.1 資料收集 自制《一般資料調查表》收集患者年齡、性別、體重指數(BMI)、飲酒史、吸煙史、基線血壓、糖尿病、心房顫動、卒中史、基線美國國立衛生研究院卒中量表評分(NIHSS)及實驗室指標{脂蛋白(a)[LP(a)]、白蛋白(ALB)、白細胞計數、血小板計數、血尿酸、血肌酐、總膽固醇}等。
1.2.2 END評價 END指患者死亡或溶栓后1 d內NIHSS評分較溶栓前增加≥4分,并據此分為END組、非END組[6]。
1.3 觀察指標
(1)記錄ACI患者溶栓后END發生情況。(2)ACI患者溶栓后END的單因素分析。(3)對單因素分析中的相關因素進行多重共線性檢驗。(4)ACI患者溶栓后END的多因素分析。
1.4 統計學處理
采用統計學軟件SPSS 22.0處理數據,計數資料以率(%)表示,采用χ2檢驗,對單因素分析中P<0.05的因素進行多重共線性檢驗,方差膨脹因子(VIF)<5及容差>0.2時,認為不存在多重共線性;影響因素采用Logistic回歸分析。檢驗水準α=0.05,P<0.05為差異有統計學意義。
2 結果
2.1 END發生情況
256例ACI患者溶栓后共53例出現END,發生率為20.70%(53/256)。
2.2 END單因素分析
END組年齡、性別、BMI、飲酒史、吸煙史、舒張壓、卒中史、血小板計數、白細胞計數、血尿酸、血肌酐、總膽固醇與非END組對比,差異無統計學意義(P>0.05);但END組收縮壓、心房顫動史、糖尿病、基線NIHSS評分、血清LP(a)、ALB水平與非END組比較,差異有統計學意義(P<0.05),見表1。
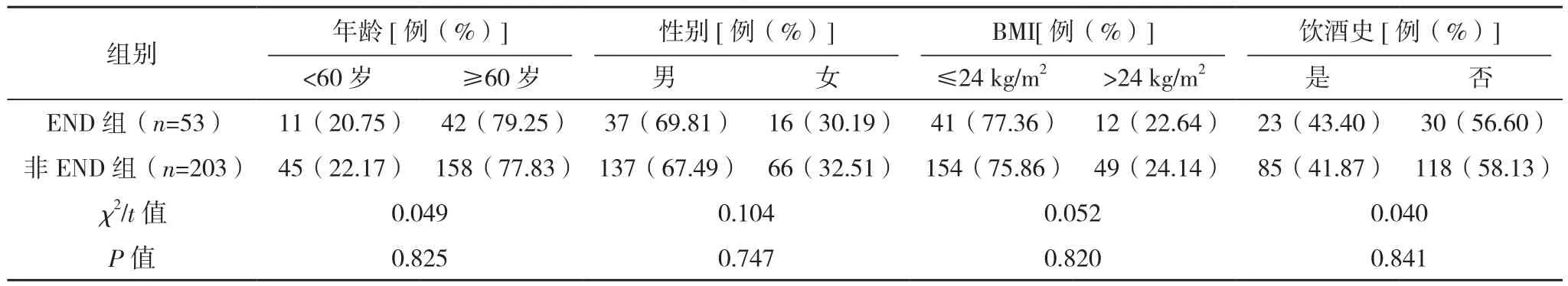
表1 END單因素分析

表1(續)
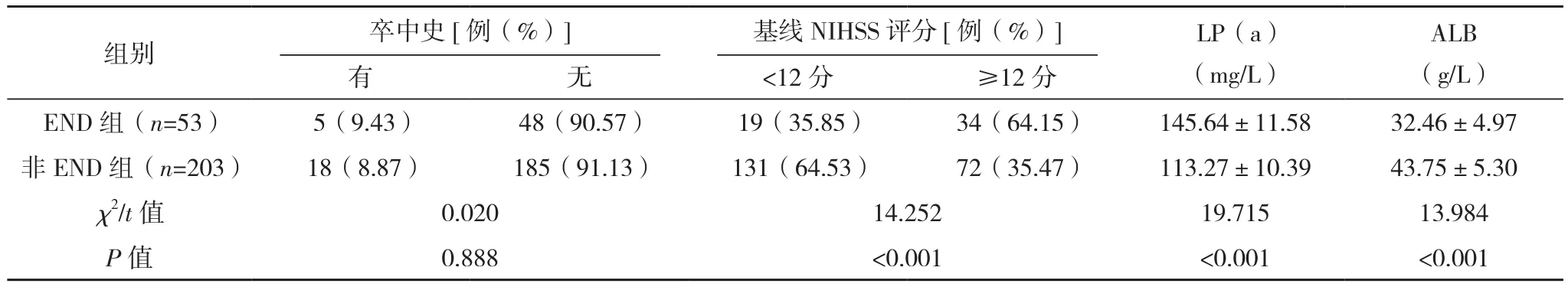
表1(續)
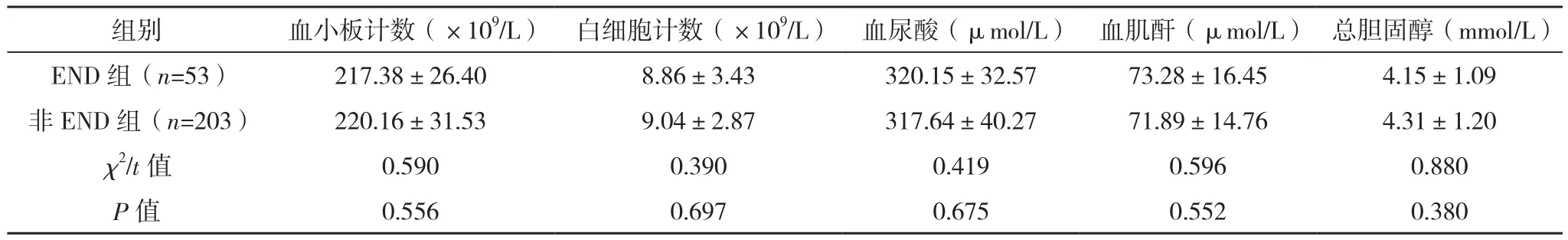
表1(續)
2.3 多重共線性檢驗
將表1中差異有統計學意義的項[收縮壓、心房顫動、基線NIHSS評分、糖尿病、血清LP(a)、ALB水平]進行多重共線性檢驗,發現6個因素容差在0.272~0.670,VIF在1.493~3.675,故以上因素多重共線可能性低,見表2。
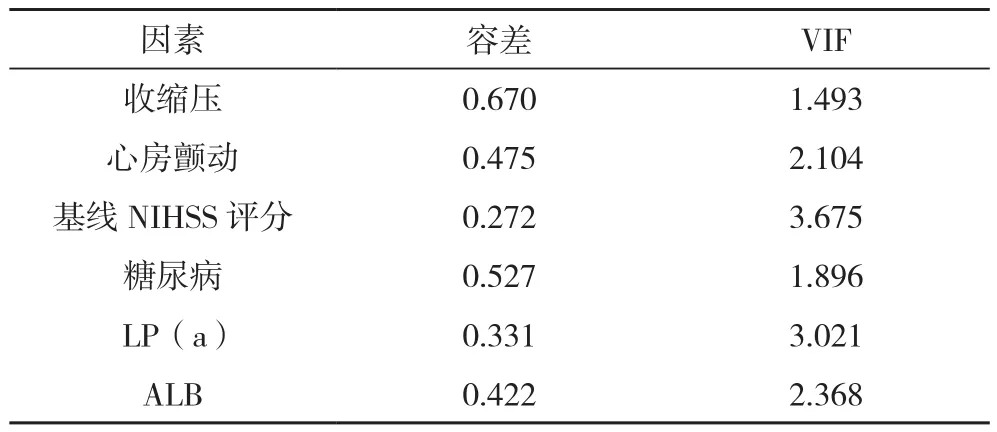
表2 多重共線性檢驗
2.4 變量賦值
以ACI患者溶栓后END為應變量,對上述差異有統計學意義的項為自變量,并賦值,見表3。
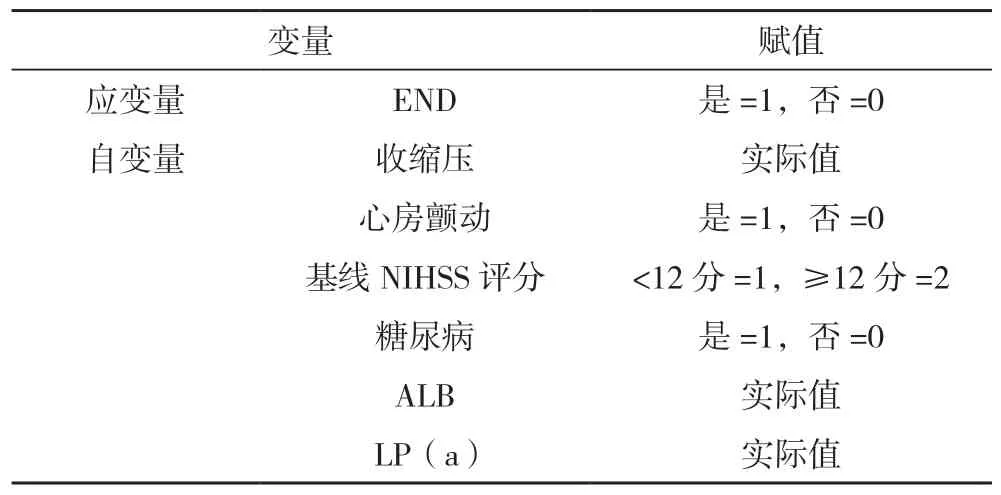
表3 變量賦值
2.5 END多因素分析
以ACI患者溶栓后END為應變量,收縮壓、心房顫動、基線NIHSS評分、糖尿病、血清 LP(a)、ALB水平為自變量,納入Logistic回歸模型,結果顯示,收縮壓高、心房顫動、基線NIHSS評分高、糖尿病、血清LP(a)高表達、ALB低表達是ACI患者溶栓后END的獨立危險因素(P<0.05),見表4。
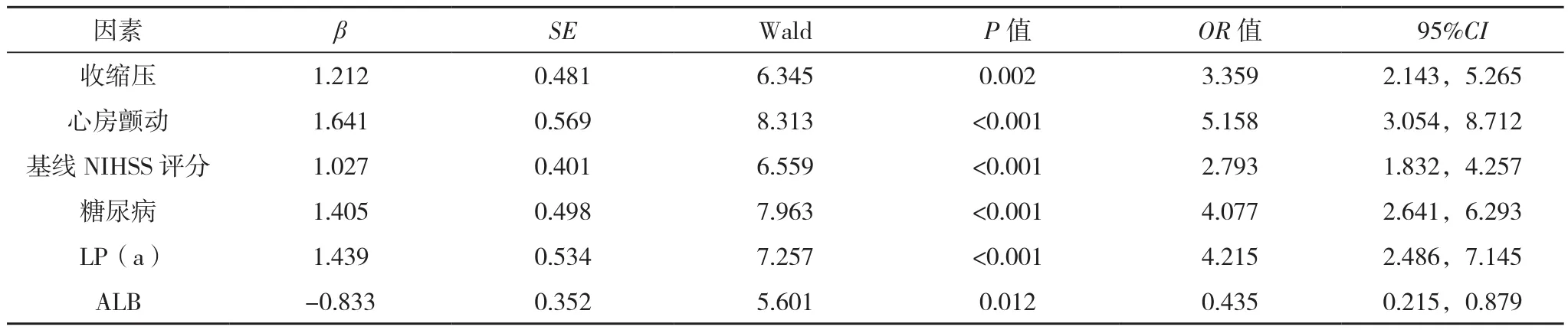
表4 END多因素分析
3 討論
END是ACI患者神經損傷加重、病情進展的一種表現,可影響溶栓效果,加重神經缺損,大幅增加致殘、致死風險,影響預后[7]。研究表明,卒中4.5 h內進行標準溶栓,部分患者病情仍可能未緩解,甚至進展加重,出現END,其發生率可達6%~38%[8]。本研究調查顯示,256例ACI患者溶栓后END發生率為20.70%,支持上述研究。故有必要找出溶栓后END的危險因素,及早進行干預,預防END發生。
END發生受多種因素影響,如溶栓前NIHSS評分、高血糖、心房顫動等。史寶光等[9]研究表明,基線NIHSS評分、心房顫動是卒中患者溶栓后出現END的危險因素,NIHSS評分≥10分、合并心房顫動更易出現END。郎豐龍等[10]研究顯示,糖尿病與溶栓后END顯著相關,Logistic模型計算糖尿病危險因素的95%CI:1.029,4.272,OR=2.097。本研究支持上述研究,END組基線NIHSS評分≥12分、伴有糖尿病、心房顫動者占比高于非END組。分析原因在于糖尿病者一般伴有血管病變,血糖持續增高可促進動脈硬化,且針對缺氧缺血腦組織,高血糖狀態具有毒性效應,可刺激腦水腫,進一步損害神經功能。心房顫動發生后左心房功能可顯著下降,減慢血流速度,心房內更易出現附壁栓子,而栓子脫落可阻塞大血管,改變血流動力學,導致腦組織低灌注,造成不可逆缺血半暗帶損傷[11]。NIHSS評分是神經缺損程度常用評價工具,包括麻痹凝視、意識水平、共濟失調、面癱、感覺障礙等,評分高提示神經缺損嚴重,梗死范圍大,若評分>8分即可能出現大血管閉塞,其溶栓再通率低,腦水腫、出血轉化風險高[12]。因此伴糖尿病、心房顫動及NIHSS評分≥12分者更易出現END。秦錦標等[13]研究表明,ACI患者溶栓后END受NIHSS評分、心房纖顫等影響,而與血壓無關。本研究表明,END組收縮壓高于非END組。分析原因可能與高血壓者抗氧化及氧化能力失衡有關[14]。另外本研究還發現,血清LP(a)水平升高、ALB水平下降與END發生有關。分析相關機制:(1)LP(a)是抑制血栓溶解、促進動脈硬化的重要物質,能抑制纖溶酶合成,影響纖維蛋白降解,介導泡沫細胞合成,具有促血栓形成、促動脈硬化作用[15]。(2)ALB能抑制內皮細胞凋亡,舒張毛細血管,改善缺血區血供,同時羥乙基淀粉與ALB協同作用,能下調凝血因子水平,調節凝血功能,促進微血栓溶解,起到抗血栓目的[16]。
針對上述因素,臨床需提高預警,及早進行防治干預,如:(1)合并糖尿病、高血壓者,溶栓前需積極控制血壓(收縮壓 140~159 mmHg)、血糖(7.7~10 mmol/L),以降低血糖,穩定血壓,預防END。(2)心房顫動者:學科室協同評價患者病情,明確溶栓方法,一定程度提高溶栓強度,抑制病情進展。(3)LP(a)過表達:溶栓前積極開展降LP(a)治療,溶栓后指導低糖、低脂飲食,調節LP(a)水平,減少END發生。(4)ALB低表達:溶栓前補充適量人血白蛋白,調節人體ALB,從而降低END風險。
綜上,ACI患者溶栓后END受收縮壓、心房顫動、糖尿病、基線NIHSS評分、血清LP(a)、ALB水平影響。

