中性粒細胞/淋巴細胞比率及血小板平均體積在慢性阻塞性肺病急性加重期細菌感染的診斷價值
陳家翠,彭 松,余志艷
(安徽省合肥市第一人民醫院全科醫學科,安徽 合肥 230031)
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)是以老年人為主要發病群體的常見呼吸系統疾病,氣流受限及持續呼吸道癥狀是其主要特征,COPD患者可在各種誘因作用下發生呼吸道癥狀急劇惡化,使得病情急性加重,這也是導致COPD患者病死的重要原因[1]。細菌感染是COPD急性加重的主要原因之一,目前痰培養陽性是診斷細菌感染的金標準,但存在耗時長、質量控制難度大弊端,尋找檢測方便、敏感度好的指標對指導臨床COPD急性加重期細菌感染診斷和治療具有重要意義[2]。中性粒細胞和淋巴細胞均為外周血白細胞重要組成部分,中性粒細胞/淋巴細胞比率(neutrophils to lymphocytes ratio,NLR)可反映二者動態平衡狀態,有越來越多研究顯示[3],NLR與多種炎癥性疾病、感染性疾病、惡性腫瘤等關聯密切。血小板平均體積(mean platelet volume,MPV)是一種可反映血小板功能及生成率的血小板形態學指標,當各種原因導致血小板破壞或消耗時,MPV可代償性升高,因此MPV在多種疾病輔助診斷也有一定應用[4]。鑒于此,本研究通過分析NLR、MPV在COPD急性加重期細菌感染中的診斷價值,從而為COPD急性加重期患者診療方案制定提供參考,現報告如下。
1 對象與方法
1.1研究對象:回顧性分析2019年2月至2022年2月101例老年COPD急性加重期患者臨床資料,納入標準:①符合指南中COPD急性加重期診斷標準,即患者自述呼吸系統癥狀急劇惡化,超出日常變異范圍,如咳嗽加劇、呼吸困難加重、咳痰變多或呈膿性,可伴發熱、全身不適、心悸、疲乏等癥狀,導致需改變藥物治療[5];②年齡65~85歲;③入院時急性加重病程72h以內;④入院前1月內無抗生素、免疫抑制劑、激素類藥物應用;⑤于本院接受規范治療;⑥病原學檢查、實驗室檢查等臨床資料完整。排除標準:①明確其他部位感染;②存在活動性肺結核、結締組織病、胰腺炎、潰瘍性結腸炎等其他炎癥性疾病;③合并惡性腫瘤、血液系統疾病、肝腎功能不全、心腦血管疾病等嚴重基礎疾病;④精神病史;⑤臨床資料不全。以痰液細菌學培養結果為金標準(即連續3次痰培養中,2次及以上相同病原菌培養陽性),101例患者可分為感染組62例和非感染組39例。感染組與非感染組性別、年齡、體重指數、COPD病程、急性加重病程、合并基礎疾病比較差異均無統計學意義(P>0.05),見表1。本研究經醫院倫理委員會批準(編號:LN2020-hall13),考慮到研究為回顧性分析,患者均免知情同意。
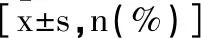
表1 感染組與非感染組一般資料比較
1.2觀察指標及方法
1.2.1一般資料:收集患者性別、年齡、體重指數、COPD病程、急性加重時間、合并基礎疾病等一般資料。
1.2.2血液指標:采集患者入院次日清晨空腹靜脈血標本3mL送檢,采用全自動血細胞分析儀(邁瑞BC5800型)檢測白細胞(white blood cell,WBC)計數、血小板(platelet,PLT)計數、中性粒細胞計數、淋巴細胞計數、MPV,計算NLR,檢測步驟均嚴格按照儀器說明書操作。
1.2.3治療原則:所有患者均參照相關指南[7]進行治療,對于無呼吸衰竭患者,主要采用支氣管擴張劑、糖皮質激素(口服)治療,膿性痰液者考慮開始使用抗菌治療;對于存在急性呼吸衰竭、但無生命危險患者,在支氣管擴張劑、糖皮質激素(口服)基礎上,對有細菌感染表現者,考慮口服抗生素治療,并聯合氧療、糖皮質激素定量吸入或霧化吸入,呼吸衰竭加重時考慮無創通氣,此外,治療期間重視血氣分析、監測液體平衡和營養、預防血栓以及相關合并癥(心律不齊、心力衰竭等)診療;對于存在急性呼吸衰竭且有生命危險患者,轉入ICU治療,在支氣管擴張劑、糖皮質激素(口服不耐受者使用靜脈滴注)基礎上,結合醫院細菌耐藥情況經驗性使用抗菌藥物,予以氧療或機械通氣支持,重視血氣分析、監測液體平衡和營養、預防血栓以及相關合并癥(心律不齊、心力衰竭等)診療,同時密切監測。治療后1周,再次檢測相關血液指標變化。
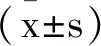
2 結 果
2.1感染組與非感染組血液指標比較:感染組WBC、NLR、MPV均顯著高于非感染組(P<0.05),但兩組PLT水平比較差異無統計學意義(P>0.05),見表2。

表2 感染組與非感染組血液指標比較
2.2血液指標對COPD急性加重期細菌感染診斷價值:以痰液細菌學培養結果為細菌感染診斷金標準,以是否診斷細菌感染為狀態變量,WBC、NLR、MPV水平為檢驗變量繪制ROC曲線,結果顯示,WBC、NLR、MPV診斷COPD急性加重期細菌感染的ROC曲線下面積分別為0.743、0.855、0.849(P<0.05),臨界值分別為10.5×109L-1、8.5、9.5 fl。見圖1、表3。

表3 WBC NLR MPV對COPD急性加重期細菌感染的診斷價值
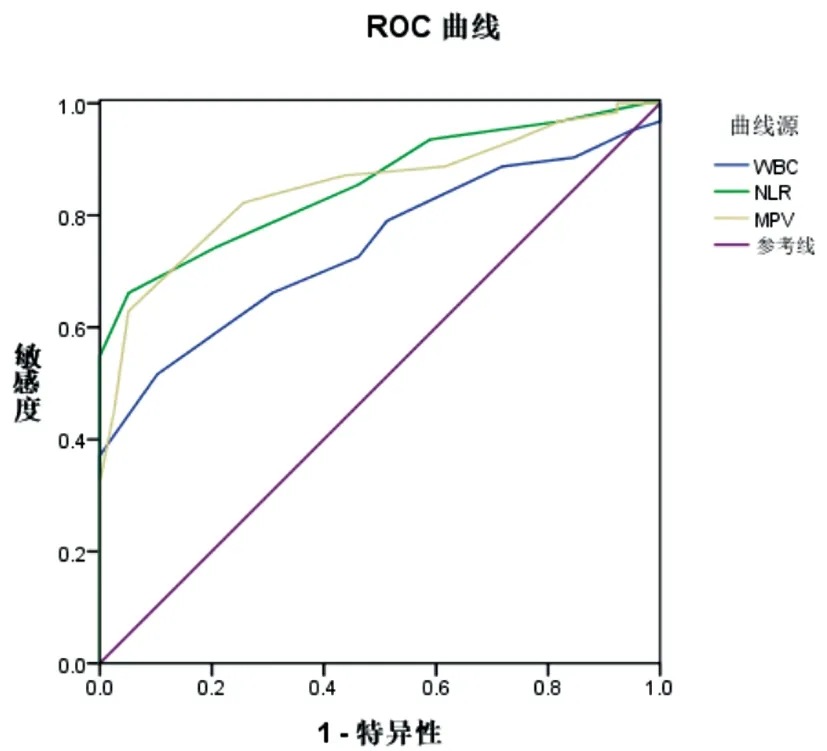
圖1 WBC、NLR、MPV診斷COPD急性加重期細菌感染的ROC曲線
2.3NLR聯合MPV的診斷價值:NLR聯合MPV串聯時特異度最高,誤診率為2.6%;NLR聯合MPV并聯時敏感度最高,漏診率為9.7%,見表4。

表4 NLR聯合MPV的診斷價值
2.4COPD急性加重期患者治療前后血液指標變化:治療后,COPD急性加重期患者WBC、NLR、MPV均較治療前降低(P<0.05),但PLT與治療前比較差異無統計學意義(P>0.05),見表5。

表5 COPD急性加重期患者治療前后血液指標變化
3 討 論
文獻顯示[6],COPD患者每年可出現0.5~3.5次急性加重,其中因下呼吸道細菌感染導致的急性加重可占1/3~1/2,尤其是老年患者,因肺功能、自身免疫功能等下降,更容易出現急性加重。細菌感染導致COPD急性加重的機制主要在于感染可激活淋巴細胞、巨噬細胞等免疫細胞,誘導大量炎癥細胞因子釋放,進而加劇肺血管內皮細胞炎癥損傷,使得患者肺部病變程度及肺功能進一步惡化[7]。因此,探究與COPD急性加重期細菌感染密切相關的免疫炎癥指標,對患者感染早期診斷具有指導意義。
NLR為外周血中性粒細胞計數和淋巴細胞計數的比值,能反映炎癥激活與調節間的平衡狀態,其值越高,意味著機體炎癥應激反應強度越大,因此NLR常作為炎癥指標用于多種炎癥相關疾病預測,而且考慮到NLR臨床檢測快速、方便、成本低,其適用性較為廣泛[8]。研究表明[9],細菌感染相較非細菌感染如病毒感染所致的炎癥應激反應更強烈,因此NLR在細菌感染中升高更為明顯。MPV可反映血小板體積變化,當機體發生細菌感染時,可導致血小板破壞增加,而且感染可影響凝血-纖溶系統功能,與微循環障礙、局部血栓生成管理密切,這些過程均可導致血小板大量消耗,因此血小板可出現代償性增大,使得MPV值升高[10]。研究顯示[11],膿毒癥患者MPV可持續升高,且是患者預后不良的危險因素。已有研究報道[12],COPD急性加重期患者NLR、MPV相較穩定期患者、健康體檢者均明顯升高,這可能與急性加重期氣道炎癥反應、組織低灌注、缺氧狀態有關。本研究發現,感染組NLR、MPV均顯著高于非感染組,提示NLR、MPV還與COPD急性加重期細菌感染有關。進一步分析發現,NLR、MPV診斷COPD急性加重期細菌感染的ROC曲線下面積分別為0.855、0.849,且較常規反映細菌感染的參數WBC的診斷價值更高。另外,本研究顯示,將NLR、MPV串聯用于COPD急性加重期細菌感染診斷時,誤診率僅為2.6%,而將二者并聯時,漏診率僅為9.7%,因此臨床可通過綜合比較來輔助診斷,從而更好指導臨床對該類患者細菌感染的初步篩查或早期抗感染治療。PLT是反映血小板數量的指標,其不僅在機體凝血過程中發揮重要作用,還具有免疫細胞功能,因此理論上而言,細菌感染時可直接或間接影響機體PLT變化。不過本研究發現,感染組與非感染組PLT計數并無明顯差異,提示直接檢測PLT計數對COPD急性期細菌感染并無明顯診斷價值,可能因為PLT表達可受多種生理、病理因素及感染病原菌種類影響,故COPD急性期細菌感染患者PLT計數變化并不明顯的原因。此外,本研究還發現,治療后COPD急性加重期患者NLR、MPV均較治療前降低,說明NLR、MPV或許對患者預后也有一定評估價值,后期研究可進一步探討。
綜上所述,COPD急性加重期合并細菌感染者NLR、MPV明顯升高,將二者并聯診斷細菌感染時可減少漏診率,串聯診斷時可減少誤診率,因此,NLR、MRV可作為COPD急性加重期細菌感染的早期輔助診斷指標。

