原發性高血壓患者血清RORγt mRNA、salusin-β水平及其與冠心病的相關性研究*
郭建霞,田 爍,徐 奕,俞 芳,肖紅珍,李 莎,楊曉琳,劉閣玲
1.河北省唐山中心醫院感染性疾病科,河北唐山 063000;2.河北省唐山市工人醫院內分泌科,河北唐山 063000
原發性高血壓是一種全球高疾病負擔的慢性疾病,據統計,2012-2015年我國18歲及以上居民高血壓患病率為27.9%,且呈升高趨勢[1]。血壓升高與心血管病發病和死亡密切相關,收縮壓增高10 mm Hg可使無心血管疾病患者的冠狀動脈事件風險增加20%[2]。合并冠心病(CHD)的高血壓患者較未合并CHD的患者血壓波動性更大[3],冠狀動脈病變程度更嚴重,病變范圍更廣。早期識別原發性高血壓合并CHD的風險有助于篩選高危人群,以便早期干預治療,改善預后。高血壓是一種慢性炎癥性疾病,先天性和適應性免疫反應觸發炎癥過程,導致血壓升高和器官損傷,輔助性T細胞17(Th17)參與和血壓升高相關的炎癥反應[4]。視黃酸相關孤兒受體(RORγt)是Th17發育必需及誘導白細胞介素(IL)-17表達的關鍵轉錄因子,RORγt表達異常可導致Th17分化異常,引起高血壓及其相關并發癥發生[5]。salusin-β是一種與血管平滑肌細胞增殖、血管纖維化和高血壓有關的生物活性肽,salusin-β過表達可導致血管平滑肌細胞增殖和血管纖維化,導致高血壓和心血管重塑[6]。RORγt、salusin-β是否與原發性高血壓合并CHD的發生及嚴重程度有關尚不完全明確,為此本研究擬檢測原發性高血壓患者血清RORγt mRNA、salusin-β水平,分析其臨床意義,以期為臨床診治提供借鑒,現報道如下。
1 資料與方法
1.1一般資料 本研究已獲得唐山中心醫院倫理委員會批準,選取2018年3月至2021年6月唐山中心醫院收治的109例原發性高血壓患者作為研究對象。納入標準:(1)符合《中國高血壓防治指南2018年修訂版》[7]中原發性高血壓診斷標準;(2)行冠狀動脈造影檢查,造影結果完整;(3)年齡18歲以上。排除標準:(1)腎動脈狹窄、皮質醇增多癥、原發性醛固酮增多癥等導致的繼發性高血壓;(2)急性冠脈綜合征、風濕性心臟病、心臟瓣膜病、心肌病等;(3)嚴重肝腎功能障礙、急慢性感染、惡性腫瘤。根據冠狀動脈造影檢查結果分為CHD組(52例)和非CHD組(NCHD組,57例)。CHD組患者均經冠狀動脈造影檢查提示主支血管狹窄程度≥50%,符合《臨床冠心病診斷與治療指南》[8]相關標準。另選取同期于唐山中心醫院門診體檢的61例志愿者作為對照組,均排除心血管疾病、原發或繼發性高血壓。所有受試者均知情同意并簽署知情同意書。
1.2方法
1.2.1實驗室檢查 所有受試者入組當天早晨采集空腹靜脈血3 mL注入干燥試管,血標本垂直放置30 min,待血液凝固后離心(3 000 r/min,半徑15 cm,時間10 min)取上清液,以ML-dr3518酶標分析儀(上海酶聯生物有限公司)采用酶聯免疫吸附試驗檢測血清salusin-β水平,試劑盒購自上海酶聯生物有限公司。采用BS-280全自動生化分析儀(深圳邁瑞醫療電子股份有限公司)檢測甘油三酯(TG)、總膽固醇(TC)、尿酸(UA)、同型半胱氨酸(Hcy)水平;采用己糖激酶法檢測空腹血糖(FPG)水平。采用實時熒光定量聚合酶鏈反應(qRT-PCR)檢測血清RORγt mRNA表達水平,采用TRIzolTMplus RNA Purification Kit(美國Invitrogen公司)提取總RNA,Agilent 2100 生物分析儀(美國Agilent公司)評估RNA質量,M-MLV反轉錄酶(美國Promega公司)將RNA反轉錄為cDNA。在StepOnePlusTMqRT-PCR系統(美國賽默飛Applied Biosystems)上重復3次qRT-PCR,反應體系,DNA模板2 μL,上、下游引物各1 μL,Premix Ex Taq DNA聚合酶25 μL,RNase-Free ddH2O 21 μL。反應條件:95 ℃預變性3 min,98 ℃變性2 s,67 ℃退火15 s,72 ℃延伸20 s,循環30次。采用2-ΔΔCt的方法計算RORγt mRNA相對表達水平。引物設計由上海捷瑞公司合成,引物序列:RORγt mRNA上游5′-CATCTCCAGCCTCAGCTTTGA-3′;下游5′-TCCCCCAGAA GTCCTTAAATCC-3′,擴增長度102 bp。β-actin(內參)上游5′-TGTCCACCTTCCAGCAGATGT-3′;下游5′-GCTCAGTAACAGTCCGCCTAGA-3′,擴增長度96 bp。
1.2.2冠狀動脈造影 采用標準Judkins法[9]進行冠狀動脈造影,自網站www.syntaxscore.com計算SYNTAX積分。根據SYNTAX積分評價冠狀動脈病變嚴重程度[10]并進行分組:輕度組(0~22分)15例,中度組(>22~32分)26例,重度組(>32分)11例。
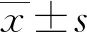
2 結 果
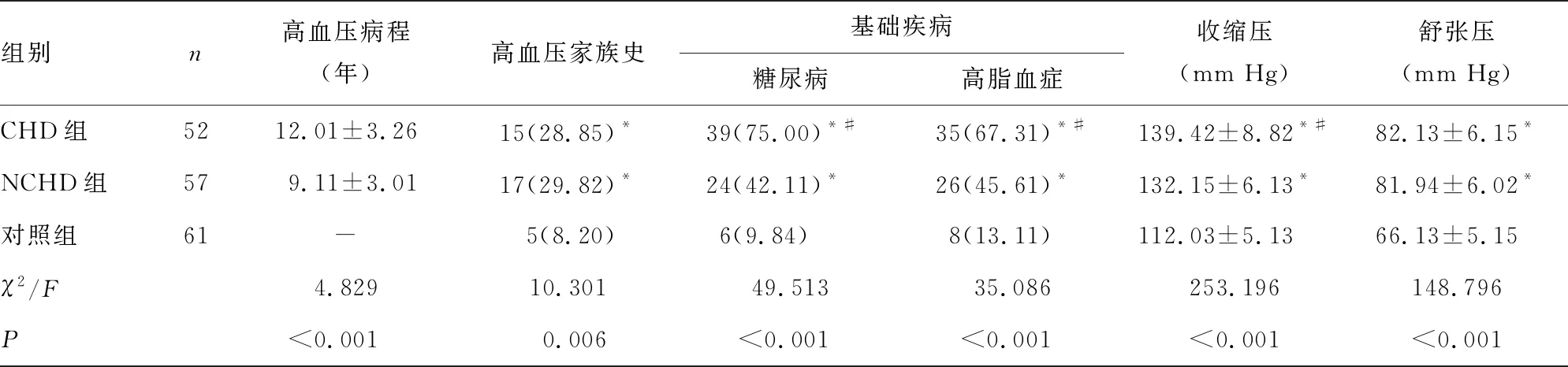
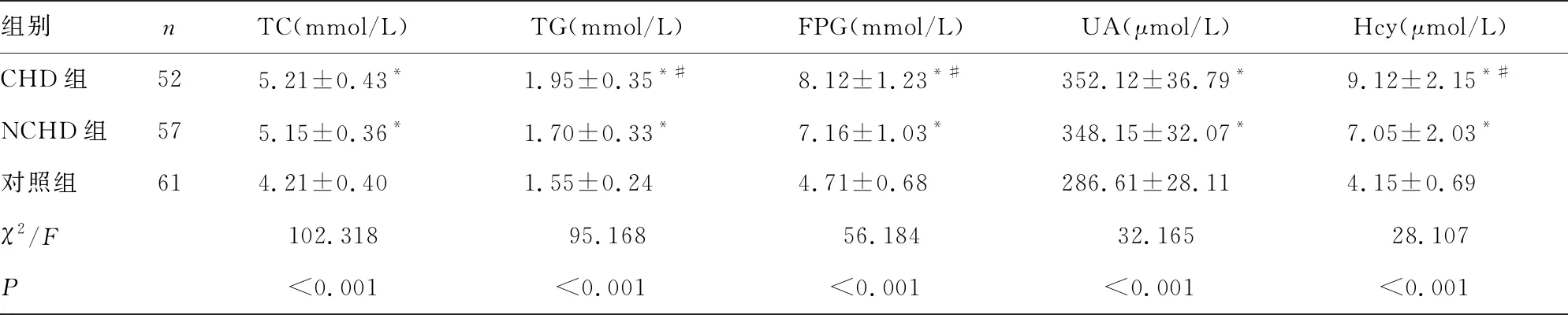
2.1CHD組、NCHD和對照組基線資料和實驗室指標水平比較 3組年齡、性別比較,差異均無統計學意義(P>0.05);CHD組和NCHD組吸煙史患者比例、飲酒史患者比例、體質量指數、高血壓家族史患者比例、糖尿病患者比例、高脂血癥患者比例、收縮壓、舒張壓、TG、TC、FPG、UA、Hcy、RORγt mRNA、salusin-β水平均高于對照組,差異均有統計學意義(P<0.05);CHD組體質量指數、高血壓病程、糖尿病患者比例、高脂血癥患者比例、收縮壓、TG、FPG、Hcy、RORγt mRNA、salusin-β水平均高于NCHD組,降壓藥物治療比例低于NCHD組,差異均有統計學意義(P<0.05);CHD組和NCHD組吸煙史患者比例、飲酒史患者比例、高血壓家族史患者比例、舒張壓、TC、UA及Ⅱ受體拮抗劑治療比例比較,差異均無統計學意義(P>0.05)。見表1。
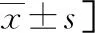
表1 CHD組、NCHD和對照組基線資料和實驗室指標水平比較[n(%)或
組別n高血壓病程(年)高血壓家族史基礎疾病糖尿病高脂血癥收縮壓(mm Hg)舒張壓(mm Hg)CHD組5212.01±3.2615(28.85)*39(75.00)*#35(67.31)*#139.42±8.82*#82.13±6.15*NCHD組579.11±3.0117(29.82)*24(42.11)*26(45.61)*132.15±6.13*81.94±6.02*對照組61-5(8.20)6(9.84)8(13.11)112.03±5.1366.13±5.15χ2/F4.82910.30149.51335.086253.196148.796P<0.0010.006<0.001<0.001<0.001<0.001
組別nTC(mmol/L)TG(mmol/L)FPG(mmol/L)UA(μmol/L)Hcy(μmol/L)CHD組525.21±0.43*1.95±0.35*#8.12±1.23*#352.12±36.79*9.12±2.15*#NCHD組575.15±0.36*1.70±0.33*7.16±1.03*348.15±32.07*7.05±2.03*對照組614.21±0.401.55±0.244.71±0.68286.61±28.114.15±0.69χ2/F102.31895.16856.18432.16528.107P<0.001<0.001<0.001<0.001<0.001
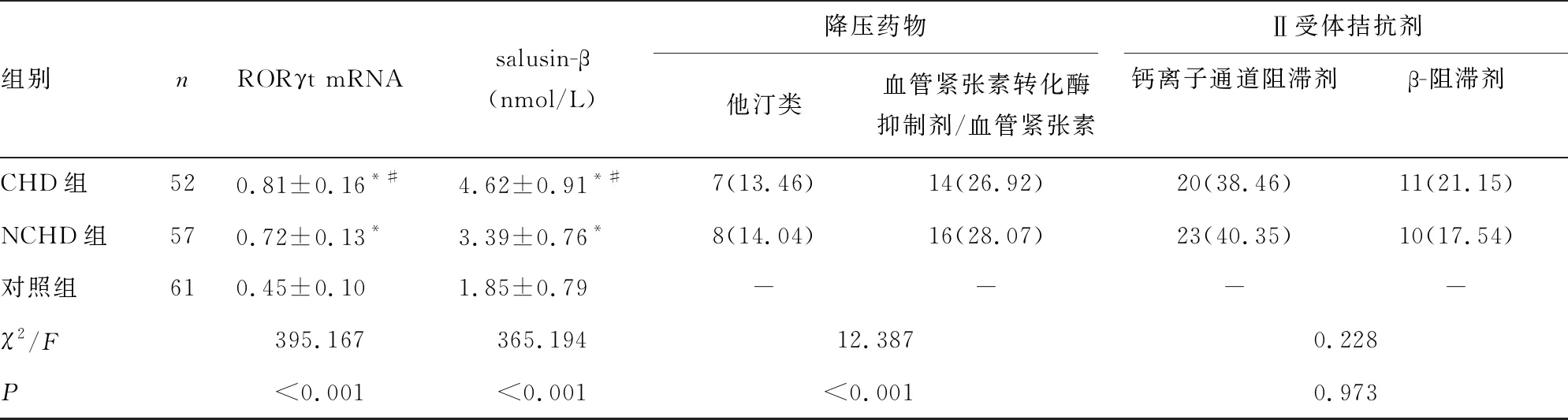
注:與對照組比較,*P<0.05;與NCHD組比較,#P<0.05;-表示無數據。
2.2輕度組、中度組和重度組患者血清RORγt mRNA、salusin-β水平比較 重度組患者血清RORγt mRNA、salusin-β水平均高于中度組和輕度組,差異均有統計學意義(P<0.05);中度組患者血清RORγt mRNA、salusin-β水平均高于輕度組,差異均有統計學意義(P<0.05)。見表2。
表2 輕度組、中度組和重度組患者血清RORγt mRNA、salusin-β水平比較
2.3影響原發性高血壓發生CHD的多因素Logistic回歸分析 將體質量指數、高血壓病程、糖尿病(賦值:0=否,1=是)、高脂血癥(賦值:0=否,1=是)、收縮壓、TG、FPG、Hcy、RORγt mRNA、salusin-β作為自變量(連續性變量原值代入),將原發性高血壓是否發生CHD作為因變量(賦值:0=否,1=是),采用ENTER法篩選變量,結果顯示,高表達RORγt mRNA、高水平salusin-β、高水平Hcy、糖尿病是原發性高血壓發生CHD的危險因素(P<0.05)。見表3。
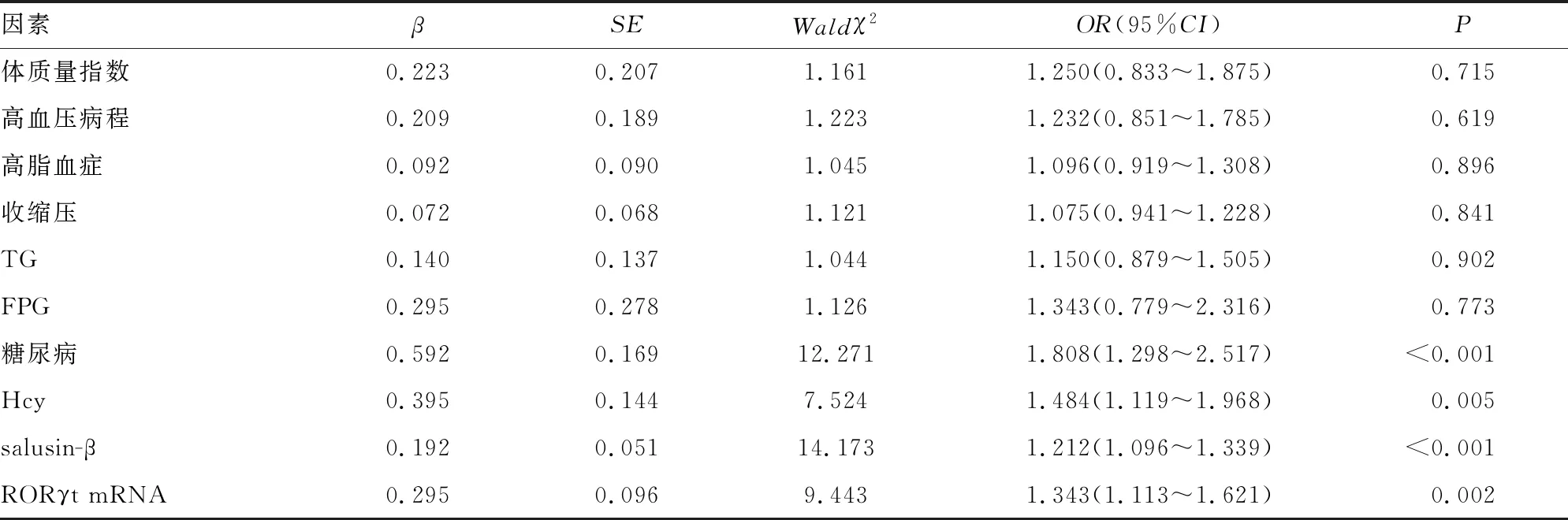
表3 影響原發性高血壓發生CHD的多因素Logistic回歸分析
2.4RORγt mRNA、salusin-β診斷原發性高血壓患者發生CHD的價值 RORγt mRNA、salusin-β診斷原發性高血壓患者發生CHD的截斷值分別為0.752、4.02 nmol/L,靈敏度分別為61.54%、67.31%,特異度分別為73.68%、77.19%,曲線下面積(AUC)分別為0.628、0.693,基于多因素Logistic回歸計算RORγt mRNA、salusin-β水平聯合檢測診斷原發性高血壓患者發生CHD的AUC為0.910,二者聯合檢測診斷原發性高血壓患者發生CHD的AUC高于RORγt mRNA、salusin-β單項檢測(Z=5.056、4.231,P<0.001)。見圖1、表4。
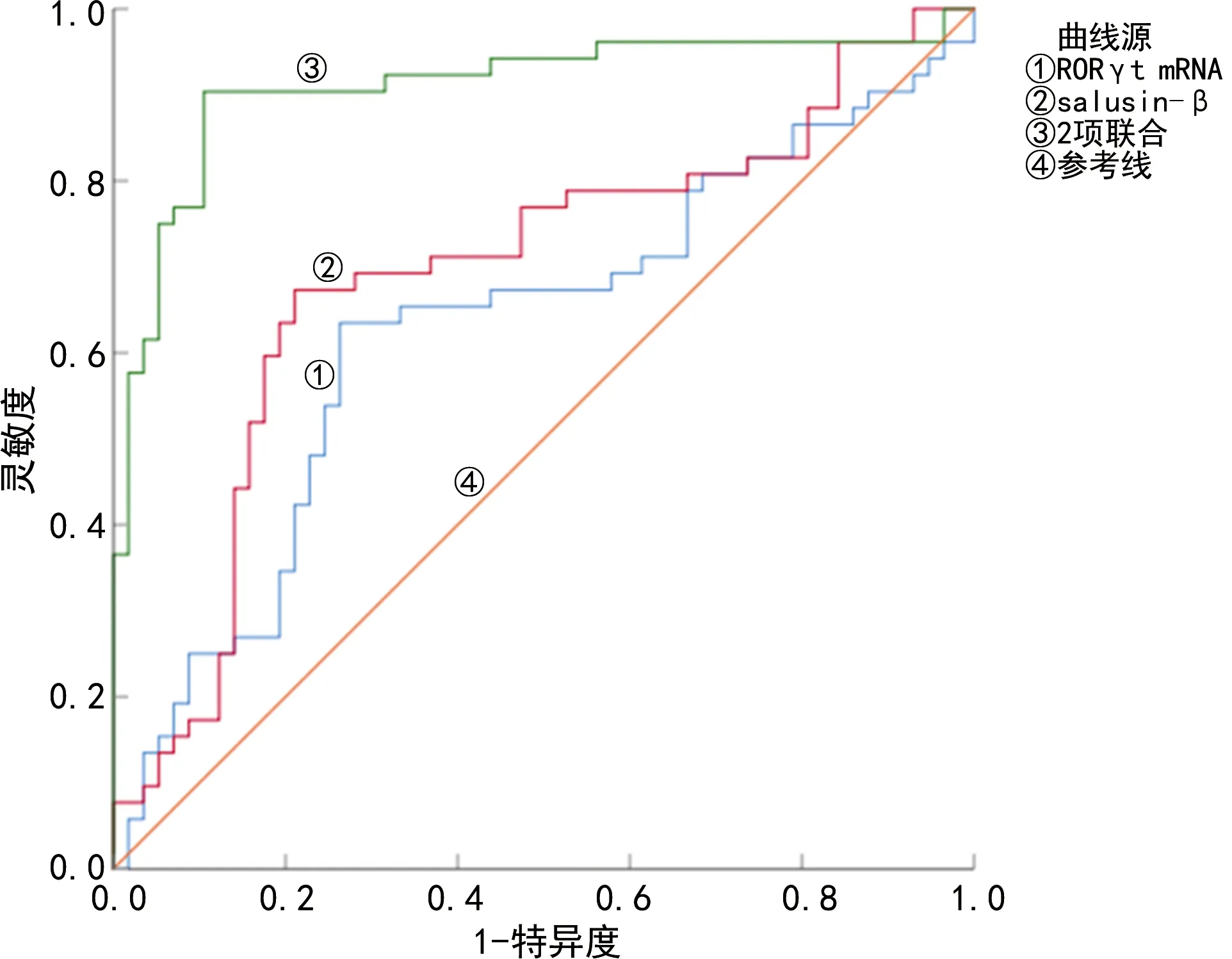
圖1 RORγt mRNA、salusin-β檢測診斷原發性高血壓患者發生CHD的ROC曲線
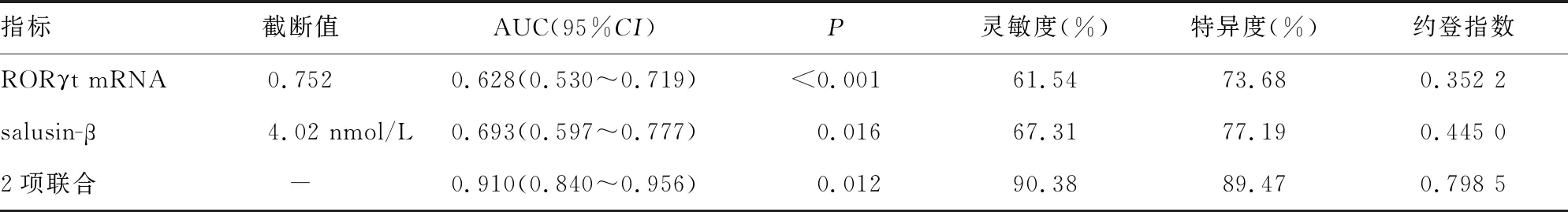
表4 RORγt mRNA、salusin-β檢測對原發性高血壓患者發生CHD的診斷效能
3 討 論
長期高血壓可導致血流剪切力變化,損傷血管內皮細胞,導致血小板激活、聚集黏附,巨噬細胞釋放炎癥因子,最終引起平滑肌細胞增殖和動脈粥樣硬化斑塊形成[11]。免疫炎癥反應和高血壓發病密切相關,Th17活化導致動脈巨噬細胞和T細胞浸潤,外周循環血中促炎因子水平升高,長期炎癥反應過程會增加活性氧的產生,引起氧化應激,導致內皮功能障礙,對一氧化氮生物利用度降低,使血管松弛和血管舒張作用減弱[12],最終引起血壓升高及心血管損傷。
RORγ是人類基因組中核受體超家族的成員,RORγt是RORγ的亞型,RORγt可促使T細胞分化為Th17,并調節Th17的細胞因子IL-17基因轉錄,參與免疫應答和調節過程[13]。有研究發現,過表達IL-17可誘導全身內皮功能障礙、血管氧化應激及動脈高血壓[14],而RORγt可通過促使IL-17表達驅動炎癥反應,參與高血壓的發病機制[15]。RORγt是否與原發性高血壓及合并CHD有關尚不清楚,本研究發現,CHD組患者血清RORγt mRNA表達水平明顯增高,高于NCHD組和對照組,且RORγt mRNA表達水平隨冠狀動脈病變加重而增高。多因素Logistic回歸分析結果顯示,高表達RORγt mRNA是原發性高血壓患者發生CHD的危險因素之一,說明RORγt可能與原發性高血壓及高血壓介導的冠狀動脈病變發生有關。有研究顯示,RORγt參與Th17發育分化及IL-23R產生,IL-23R和IL-23結合促使Th17分泌IL-17并維持病理形態,RORγt/IL-23R信號通路通過誘導病理性Th17分化參與高血壓的發病過程[16]。Th17過度活化及IL-17過量合成可加速動脈粥樣硬化進程,CHD患者外周血Th17占比、IL-17mRNA表達水平均明顯增加[17],提示RORγt可能通過誘導Th17活化及其特征性細胞因子IL-17合成,參與原發性高血壓合并CHD的發病過程。
salusin-β是具有血流動力學和促有絲分裂作用的生物活性肽,由20個氨基酸組成,在中樞及外周組織中廣泛表達,中樞salusin-β參與交感神經激活、精氨酸加壓素釋放和高血壓調節[18]。臨床研究顯示,原發性高血壓患者血清salusin-β水平明顯升高,salusin-β水平與頸動脈病變嚴重程度有關[19]。本研究結果顯示,原發性高血壓患者血清salusin-β水平較對照者升高,且CHD組患者血清salusin-β水平高于NCHD組患者,說明salusin-β與原發性高血壓患者冠狀動脈病變有關。分析可能的原因為salusin-β在人血管平滑肌細胞中也有表達,salusin-β可通過激活煙酰胺腺嘌呤二核苷酸磷酸,促使活性氧產生,下調抗衰老基因Klotho表達,促使血管鈣化[20]。salusin-β還可上調miR155表達水平,促使p65-核因子-κB核易位,增加膽固醇酰基轉移酶-1和血管細胞黏附分子-1的表達和活性,促使脂質在血管平滑肌細胞中積累,單核細胞黏附,泡沫細胞形成[21],導致動脈粥樣硬化形成。本研究多因素Logistic回歸分析結果顯示,高水平salusin-β是原發性高血壓患者發生CHD的危險因素,說明salusin-β可作為診斷原發性高血壓合并CHD的生物學標志物。WANG等[22]報道指出,salusin-β水平與冠狀動脈狹窄有關,是評估冠狀動脈疾病的潛在標志物。
本研究ROC曲線分析結果顯示,RORγt mRNA、salusin-β鑒別原發性高血壓患者發生CHD均具有一定價值,RORγt mRNA、salusin-β聯合檢測鑒別原發性高血壓患者發生CHD的效能明顯提高,說明RORγt mRNA、salusin-β水平均升高可能警示更高的冠狀動脈病變風險,聯合檢測對臨床識別冠狀動脈病變風險更有價值。多因素Logistic回歸分析結果顯示,糖尿病、高水平Hcy也與原發性高血壓患者發生CHD有關。王哲輝等[23]報道指出,高血壓合并糖尿病患者并發CHD的風險高于單獨高血壓和糖尿病,提示高血壓、糖尿病并存可加速冠狀動脈病變。陰淑瑩等[24]研究指出,Hcy水平與冠狀動脈病變程度呈正相關,Hcy水平升高是原發性高血壓合并冠心病的危險因素。
綜上所述,原發性高血壓合并CHD患者血清RORγt mRNA、salusin-β水平均升高,RORγt mRNA、salusin-β水平升高與冠狀動脈病變及病變程度均有關,是原發性高血壓合并CHD的危險因素。RORγt mRNA、salusin-β可作為診斷原發性高血壓合并CHD的生物學指標。

