應重視對糖尿病腎病(DKD)患者的血壓管理
首都醫科大學附屬北京朝陽醫院 那開憲
北京市朝陽區小紅門社區衛生服務中心 楊海燕
慢性腎臟病(CKD)是危害人民身體健康的常見慢性疾病,而我國2012年的抽樣調查顯示我國約有1.195億CKD人群。CKD患者的高血壓患病率遠遠高于無CKD人群。糖尿病腎病(DKD)占全球慢性腎臟病(CKD)病例的40%以上。高血壓是DKD進展以及發生心血管疾病和死亡的主要危險因素。因此,管理好高血壓對延緩DKD進展和降低心血管疾病風險至關重要。在治療時對降壓藥物的選擇不僅要看降壓效果,還要考慮到降壓藥物對心臟、腦、腎臟等重要的靶器官進行保護。因此,對糖尿病腎病合并高血壓患者不僅要控制血糖,還要考慮到降壓效果以及降壓藥對糖代謝、胰島功能和腎功能的影響。然而,在臨床實踐過程中,國內外對糖尿病腎病患者的血壓管理卻差距甚遠。
病例
趙先生,78歲,身高1.74米,體重88公斤,有煙酒嗜好及喜食用油膩食品30余年,發現糖尿病20年。20年前單位組織體檢無意中發現空腹血糖高(8.2mmoL/L),低密度脂蛋白膽固醇及甘油三酯偏高。次日,趙先生到三甲醫院內分泌科看病,經檢查診斷為二型糖尿病、高脂血癥,給予二甲雙胍、舒降之治療。醫生囑咐他,戒煙、限酒、減肥及少吃油膩食品。趙先生服藥后血糖、血脂得以滿意控制。趙先生曾經幾次嘗試戒煙,每次僅僅維持1-2個月,均以失敗告終。在家屬的監督下能夠節制油膩食品及限酒。5年后一天早上,趙先生無任何原因感到頭暈、頭沉,到醫院看病測量血壓高(180/100mmHg),醫生立即給予他硝苯地平緩釋片含服,不久后血壓降至正常,做頭部CT正常,醫生囑咐他,回家后常測量血壓,如果高就服用硝苯地平緩釋片。趙先生回家后多次測量血壓均正常,也沒有服藥。一天晚上,趙先生起床解小便,感到頭暈,測量血壓160/100mmHg,自己認為血壓高與憋尿有關,休息就會好轉。次日,趙先生晨起測量血壓150/90mmHg,起床到戶外活動后再測量血壓正常。因血壓正常趙先生未理會,但是他把這個情況告訴了愛人,其愛人是一個有心人,連續幾天清晨都給趙先生測量血壓,血壓均在150/90mmHg左右。在家屬催促下,趙先生到醫院看病,做24小時血壓監測示夜間高血壓,血壓從晚上10點開始升高,至次日凌晨4-5時下降至正常。醫生給予硝苯地平緩釋片10mg,囑咐他每晚睡前服用。服藥后一周,再次做24小時血壓監測夜間血壓恢復正常。爾后,趙先生一直堅持每天晚上睡前服用一片硝苯地平緩釋片。兩年后一天中午,趙先生無任何原因感到頭暈、頭沉,測量血壓高(160/100mmHg),立即到醫院看病,做24小時血壓監測示凌晨開始血壓高,持續至夜間11時。醫生建議早晚服用硝苯地平緩釋片,每次一片(10mg)。服用降壓藥物后,趙先生多次測量血壓并做24小時血壓監測,血壓控制滿意。因血壓、血糖控制滿意,趙先生放松了對血壓、血糖的監測。三年后,趙先生到醫院做例行檢查發現餐前血糖(7-8mmoL/L),餐后血糖(12-13.6mmoL/L),糖化血紅蛋白7.5%,24小時血壓監測示凌晨至上午10時血壓高(160/90mmHg左右),下午5時至11時血壓高(150-160/80-90mmHg),做尿白蛋白/肌酐比值(ACR)>30mg/g,肝腎功能正常。醫生給予二甲雙胍及亞莫利降血糖,拜新同及引達泊胺降壓。服藥后趙先生血壓、血糖得以控制,但是多次復查ACR>30mg/g。趙先生多次問醫生如何消除尿微量白蛋白,醫生告訴他微量白蛋白尿是糖尿病及高血壓所致,必須把血糖及血壓控制好,才能夠消除微量白蛋白尿,這需要較長時間治療,不能著急。三年間趙先生曾經多次在當地找過醫生看病,均同意目前治療方案。兩年后趙先生多次檢查ACR>200-300mg/g,腎小球濾過率(eGFR)<55ml·min-1·(1.73m2)-1,餐后血糖13.8mmoL/L、糖化血紅蛋白7.6%,做24小時血壓監測示凌晨4時開始血壓高(140-150/90-100mmHg)至上午10時許。醫生考慮患者血壓以凌晨高血壓為主,血糖表現餐后高,蛋白尿、腎功能受損,給予二甲雙胍、亞莫利及格列喹酮降糖,拜新同早晚各一片,睡前服用鹽酸特拉唑嗪2mg。服用藥物后患者血糖、血壓控制達標,多次檢查ACR及eGFR均無變化。趙先生及其家屬十分著急,在朋友介紹下找筆者看病。在細致查看了他所有檢查及其治療藥物之后,筆者告訴他,根據我國近期糖尿病指南及糖尿病腎病指南,筆者將他原先治療方案做一些較大變動,建議給予二甲雙胍、達格列凈及西格列汀降低血糖,給予沙庫巴曲纈沙坦、螺內酯及絡活喜降壓,阿托伐他汀降脂治療。筆者依據指南耐心給他及家屬講解新的治療方案,為什么有這么大的變動以及每一個藥物的作用。他們聽了筆者的講述后,同意這個治療方案。經過近兩年的治療,患者血糖、血壓、血脂控制滿意。多次檢查ACR>90-100mg/g,腎小球濾過率在正常范圍內。
教訓
①糖尿病腎病合并高血壓降壓及降糖藥物選擇一定要遵循以下原則:糖尿病腎病合并高血壓患者在選擇降糖及降壓藥物時,應優先考慮具有心臟、腎臟獲益證據的藥物,同時應充分考慮患者的心、腎功能情況,并根據eGFR調整藥物劑量;盡量避免使用血糖風險較高的藥物;還應考慮其他并發癥、體重、經濟狀況及患者偏好等因素。
②對于血壓高患者緊急降壓禁忌應用硝苯地平或硝苯地平緩釋片含服,因這種藥物短時間內使血壓急劇下降,可致心、腦、腎供血不足,致心血管事件發生。
③24小時動態血壓監測應作為血壓高患者的常規監測手段,對于診斷高血壓,判斷高血壓類型,指導治療及評估治療效果具有極其重要的地位。該患者如果盡早進行24小時動態血壓監測,就不會漏診夜間高血壓。
④該患者糖尿病腎病合并高血壓,降壓藥物應優先選擇ACEI或ARB對腎臟、心臟有保護作用的藥物,聯合治療時應選擇包含一種ACEI/ARB,聯用形式包括不同藥物自由聯合或單片復方制劑。
⑤該患者體胖,應優先選擇能夠減體重、避免血糖風險高、降低蛋白尿,對腎臟、心臟有保護作用的藥物。格列喹酮、亞莫利均增加體重,引達泊胺使血糖增加。
糖尿病腎病發生高血壓的機制
糖尿病患者易患高血壓的主要機制比較復雜,與多種因素有關,主要包括以下幾個方面:胰島素抵抗;鈉排泄障礙導致細胞外液容量負荷過重;RAS系統異常激活,興奮交感神經系統;交感神經系統興奮導致血管收縮效應,刺激腎素分泌等因素。這些因素中RAS系統異常激活及胰島素抵抗是其主要原因。由于RAS系統異常激活及胰島素抵抗導致交感神經系統亢進、水鈉儲留,引起血壓升高。長期高血糖可致腎功能損傷進而引起高血壓,初發糖尿病者如并發高血壓應視為腎病發生的一個易感標志。研究發現,約20%-60%的糖尿病患者都會發生DKD,并且進行性發展,75%的2型DKD患者在20年內進展至終末期腎病。從全國CKD患者高血壓流行病學調查中可以發現,男性CKD患者高血壓患病率高達76.4%,女性為65.7%。CKD患者高血壓患病率隨著年齡增長顯著增加(P<0.05)。
糖尿病腎病與高血壓二者的關系
眾所周知,血壓是DKD整個過程中一個決定性因素,高血壓是糖尿病腎病進展的重要危險因素,高血壓作為危險因素與腎病發生發展有密切關系,持續高血壓會加重腎臟負擔,促進糖尿病腎病進展。高血壓不僅是DKD的一種臨床表現,也是加重DKD的促發因素。長期高血壓可引起腎臟損傷,絕大多數糖尿病腎病患者均伴有不同程度的高血壓。臨床上高血壓與DM并存十分常見,2型糖尿病(T2DM)患者高血壓的患病率為20%-60%,與非DM人群相比,DM高血壓的患病率高2-3倍,且DM和高血壓互為因果,均可損害腎臟,導致糖尿病腎病(DN)發生。高血壓可使腎小球血流壓力升高,腎小球濾過壓及GFR增高,從而導致白蛋白濾過增加,進而出現系膜腎小球硬化癥和蛋白尿,腎臟病變又可加重高血壓而形成惡性循環,故高血壓是糖尿病腎病發生發展的一個重要因素。糖尿病患者心血管病變的危險性是健康人群的2倍,一旦并發高血壓則增至4倍,并會加速心血管病、視網膜病,尤其是腎病的進程,是引起終末期腎衰竭的重要原因。糖尿病腎病是糖代謝異常引起的以微血管病變為基礎的腎臟并發癥,在臨床上屬于晚期2型糖尿病的常見并發癥。微量白蛋白尿、高血壓與持續性蛋白尿等癥狀是此病的主要表現。患者一旦發生持續性蛋白尿,則提示患者的腎臟出現損傷,如果不進行干預,會很快進入終末期腎衰竭階段,這是導致患者死亡的主因。同時高血壓是造成腎功能損害的獨立危險因素,若糖尿病患者合并高血壓,發生糖尿病腎病和腎功能惡化的概率無疑會比無高血壓者明顯增加,糖尿病腎病合并高血壓發生ESRD的風險相當高。國外的大樣本研究發現,以理想的血壓為參考,正常高值血壓發生ESRD風險增加1.9倍,隨著高血壓分級的增加,發生ESRD的風險顯著增加。研究還表明,高血壓和糖尿病腎病共同促進心血管疾病的發生、發展。在CKD發生、發展的不同時期會出現水鈉潴留、腎小球硬化、高尿酸血癥、內皮細胞損傷,動脈彈性減退及自主神經調節異常等病理改變,這些病理改變使糖尿病腎病和高血壓成為互為因果的關系。糖尿病腎病會引起貧血、系統炎癥、電解質紊亂、代謝性酸中毒及礦物質代謝異常的癥狀;高血壓也會引起血管阻力增加、左心室肥厚、動脈閉塞及血管重建等病理變化。這些改變致糖尿病腎病合并高血壓是導致心血管疾病和ESRD死亡的重要原因。
糖尿病腎病血壓管理十分重要
對糖尿病腎病(DKD)患者而言,高血壓是蛋白尿、腎功能惡化、終末期腎臟病(ESRD)和心血管疾病的主要可逆性危險因素。T2D患者的高血壓患病率是健康患者的3倍,高血壓是DKD進展以及發生心血管疾病和死亡的主要危險因素。研究表明,血壓從115/75mmHg開始,每增加20/10mmHg,心血管終點事件發生率翻倍,心肌梗死和腦卒中風險增加8-10倍。糖尿病患者群體中,高血壓與任何心血管疾病事件風險增加57%和全因死亡風險增加72%相關。在T2D合并高血壓患者中,微血管和大血管并發癥明顯高于無高血壓患者。管理好高血壓對延緩DKD進展和降低心血管疾病風險至關重要,控制血壓已被證實有利于DKD患者腎臟保護。所以有效地控制血壓、減少蛋白尿、保護腎功能是延緩糖尿病腎病患者病情進展的重要手段。血壓是除血糖之外的又一個重要原因,高血壓在糖尿病腎病的發生和發展中起到重要的作用。積極降壓可明顯減少糖尿病患者心、腦、腎事件的發生。2021年11月13日,于《柳葉刀》發表的一項系統回顧和meta分析顯示:降低血壓,除外已知的可預防2型糖尿病(T2DM)的血管并發癥外,其本身也可以預防糖尿病的發病。收縮壓每降低5mmHg,糖尿病風險相應降低11%。英國前瞻性糖尿病研究(UKDPS)發現,嚴格控制血壓可使糖尿病相關性病死率明顯降低32%,微量白蛋白尿發生率下降29%,蛋白尿發生率下降39%,微血管終點事件(視網膜疾病和腎病)減少37%,大血管復合終點事件(心肌梗死、猝死、腦卒中和外周血管疾病)發生率減少34%,而強化控制血糖僅使糖尿病相關終點事件下降12%。因此,對于糖尿病或糖尿病腎病患者,降壓治療對減少心血管事件的作用優于降糖治療。歐洲收縮壓試驗(SYSTEur)研究亦指出,接受降壓治療的糖尿病高血壓患者,發生蛋白尿的風險顯著下降了71%,與非糖尿病患者相比,糖尿病患者在這方面的受益更大。同樣,Bakris等行薈萃分析提示,積極降壓可顯著延緩糖尿病及非糖尿病患者慢性腎臟病進展速度。國內外研究證實在糖尿病腎病患者中,嚴格控制血壓至130/80mmHg以下可有效減少蛋白尿,對于預防和減緩腎臟并發癥有非常重要的作用。抗高血壓治療是減緩以及阻止糖尿病腎病發展的有效手段。
糖尿病腎病合并高血壓降壓的目標值
根據患者糖尿病類型、腎功能情況以及患者年齡將個體化的降壓目標總結于表1中。
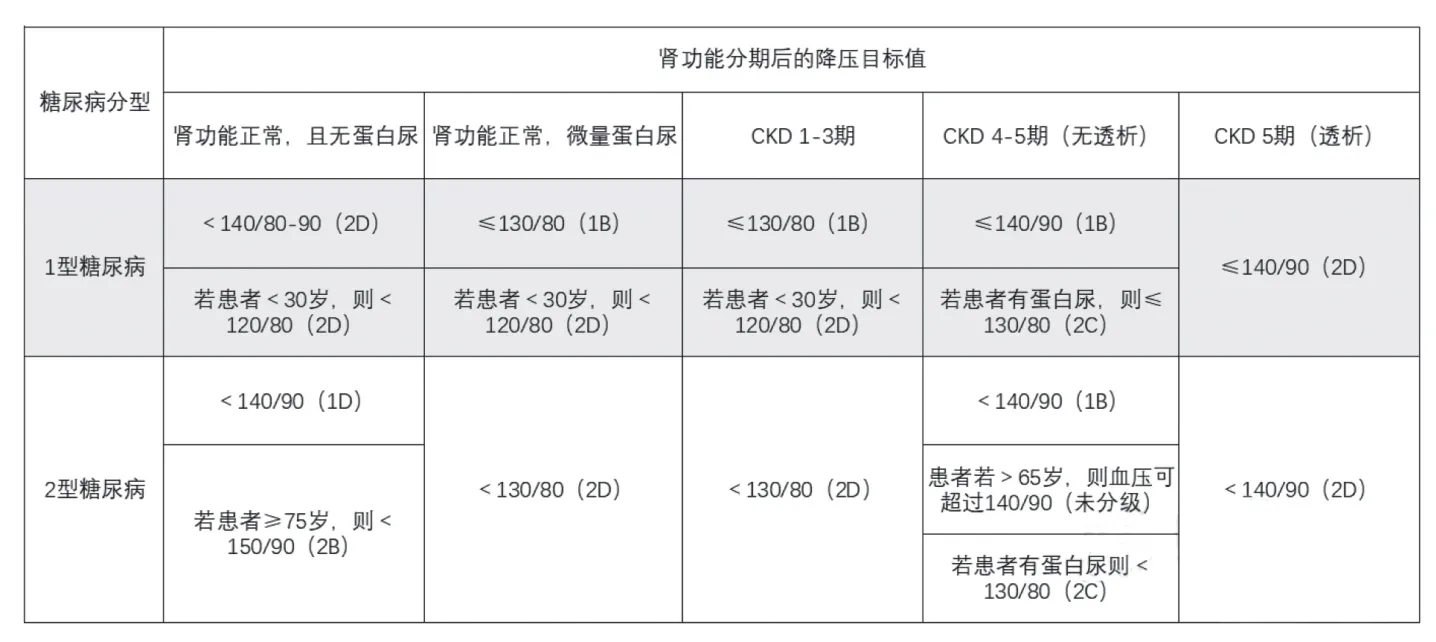
表1 糖尿病腎病合并高血壓降壓的目標值
當前我國糖尿病腎病高血壓管理存在的問題
最近,在JAMA net work Open上的一篇研究表明,盡管糖尿病患者CKD患病率較高,但患者未服用對腎臟有益的藥物,相反,許多患者服用了腎毒性藥物。該研究表明,約1/8的CKD患者患有蛋白尿,同時,只有1/5的患者服用腎素-血管緊張素系統抑制劑,更重要的是超過1/3的患者服用了非甾體抗炎藥或質子泵抑制劑,即腎毒性藥物。從我國CKD患者高血壓流行病學調查中可以發現,男性CKD患者高血壓患病率高達76.4%,女性為65.7%。由此可見,我國CKD患者高血壓患病率相當可觀,但是血壓的控制率較低。根據我國CKD患者高血壓流行病學調查顯示:我國CKD住院患者血壓控制率并不理想,33.1%的患者血壓控制在140/90mmHg以下;14.1%的患者血壓控制在130/80mmHg以下。隨著CKD分期增加,血壓控制率下降(P<0.05)。分析其血壓控制率低的原因,該調查報告歸納起來主要有以下3個方面原因:①利尿劑使用不足;②聯合降壓藥物治療比例低;③降壓藥物治療方案不合理。ACEI/ARB是CKD人群降壓治療的基礎用藥。高血壓合并糖尿病腎病患者降壓藥物的選擇除了需要注意普遍適用的降壓療效、安全性及依從性外,還需要綜合考慮是否合并糖尿病、蛋白尿、心腎保護作用,以及對特殊人群如血液透析、腎移植、妊娠、老年等藥物選擇方面的注意事項。在臨床實踐過程中,筆者發現有的醫生在對糖尿病腎病合并高血壓患者治療中往往忽視了上述應用降壓藥物的宗旨。就高血壓疾病而言,它是一種可治療的危險因素。但從目前的知曉率、治療率及達標率的統計數據來分析,中國乃至全世界各個國家的情況都不盡如人意。應積極使用合理的降壓藥物及采取有效降壓方案是完全可以控制CKD患者的血壓,進而延緩患者的腎功能減退。
經典降壓藥物治療糖尿病腎病合并高血壓應注意的問題
經典的抗高血壓藥包括血管緊張素轉換酶抑制劑(ACEI)、血管緊張素受體阻滯劑(ARB)、鈣通道阻滯劑(CCB)、噻嗪類利尿劑、鹽皮質激素受體拮抗劑(MRA)和β受體阻滯劑這5類。臨床選擇降壓藥物時需要考慮多種因素,如共病、年齡、糖尿病類型、CKD分期、eGFR、心腎保護、副作用等。國內外指南強烈建議將ACEI或ARB作為高血壓、糖尿病、慢性腎病和冠狀動脈疾病患者的一線治療用藥,并一致推薦ACEI或ARB作為糖尿病合并嚴重蛋白尿(白蛋白與肌酐比值,ACR>300mg/g)患者血壓控制的第一選擇,當ACR在30-299mg/g之間時應予以優先考慮,因為它們可以降低腎病進展的風險。研究表明,在標準降壓治療中加入螺內酯可以降低糖尿病合并糖尿病腎病患者的蛋白尿水平、延緩eGFR下降。此外,與在相同劑量的ACEI中添加氯沙坦相比,在最大劑量的賴諾普利中添加螺內酯可提高糖尿病腎病患者的腎保護作用。使用噻嗪類利尿劑(如氯沙利酮)治療可能會導致高血糖,因為藥物特性會影響胰島素抵抗。不推薦大多數β受體阻滯劑作為糖尿病患者的一線治療,因為它們對心臟代謝有負面影響,如增加甘油三酯水平、降低高密度脂蛋白膽固醇水平、隱藏低血糖癥狀和損害胰島素敏感性。此外,β受體阻滯劑也可能增加患糖尿病的風險,尤其是在高體重患者使用時。近年來,經過對藥物類別的深入分析發現,不同類別的降壓藥對于糖尿病風險,表現出了截然不同的影響:ACEI和ARB分別降低了新發糖尿病風險16%;相反,噻嗪類藥物增加了20%的糖尿病風險,β-受體阻滯劑增加了48%的糖尿病風險;鈣通道阻滯劑則對于糖尿病事件的發生沒有影響。故指南認為ACEI、ARB、CCB和噻嗪類利尿劑都是糖尿病患者可接受的初始降壓治療方案。但需要強調的是,并非所有β受體阻滯劑都對葡萄糖穩態產生如此不利的影響。卡維地洛、奈比洛爾、拉貝洛爾不僅能阻斷β-腎上腺素受體,而且還具有促進血管舒張的其他特性,對代謝的不良影響較小。CKD患者高血壓的發生涉及多個發病機制,常常需要聯合使用2種或2種以上降壓藥物。對血壓≥160/100mmHg或高于目標血壓20/10mmHg的高危人群,初始治療即需要應用2種降壓藥物。對于CKD患者,初始治療聯用方案中應包含一種ACEI/ARB,聯用形式包括不同藥物自由聯合或單片復方制劑。單片復方制劑使用方便,可改善治療的依從性及療效,是聯合治療的新趨勢,2020ISH指南中明確推薦單片復方制劑應作為優先選擇。
哪一些新興“降壓藥”能夠有益于糖尿病腎病血壓管理
除了上述降壓藥物外,還有許多新藥顯示出額外的降壓特性,而這些特性對糖尿病腎病患者尤其有利。①非奈利酮:非奈利酮是一種新型非甾體鹽皮質激素受體激動劑,相比螺內酯和依普利酮具有更高的選擇性和活性。它可以防止醛固酮激活鹽皮質激素受體,有助于減少重塑、纖維化和炎癥過程,尤其是在心臟、腎臟和外周血管系統中。非奈利酮主要用于心力衰竭治療,可使NT-proBNP水平下降。除此之外,由于非奈利酮能夠減少蛋白尿,因此可以使用非奈利酮治療難治性高血壓和糖尿病腎病。由于非奈利酮的高選擇性,因此不會導致血清鉀水平顯著升高。FIDELIO-DKD、FIGARO-DKD等多項試驗證明了非奈利酮在治療糖尿病腎病患者中的有益作用。②埃沙西林酮(esaxerenone):埃沙西林酮是另一種新型非甾體鹽皮質激素受體激動劑,已在日本獲批用于治療高血壓和糖尿病腎病。由于與依普利酮和螺內酯相比,埃沙西林酮對鹽皮質激素受體的效力和選擇性較高,因此對高鉀血癥、女性乳房發育、閉經和陽萎風險較小。研究表明,埃沙西林酮單藥治療,從基線檢查到治療結束,坐位血壓降低-18.5/-8.8mmHg;埃沙西林酮作為腎素-血管緊張素系統抑制劑的附加療法時,血壓降低幅度為-17.8/-8.1mmHg;此外,在2型糖尿病合并微量白蛋白尿患者中進行的三期臨床試驗表明,在T2D和微量白蛋白尿患者中,在高血壓治療中添加埃沙西林酮可減少蛋白尿的進展。③鈉-葡萄糖共轉運蛋白-2抑制劑(SGLT-2):SGLT-2是新型的抗糖尿病藥物,通過降低SGLT2對葡萄糖的轉運,減少腎小管葡萄糖重吸收,加強/修復腎臟致密斑管球反饋和腎小囊腔血流靜壓,改善腎小球高濾過狀態,降低腎小球內壓力,減少白蛋白尿和炎癥的發生。對伴糖尿病腎病的T2DM患者,推薦在eGFR≥45ml/min/1.73m2的患者中使用SGLT2,以降低糖尿病腎病進展和(或)心血管事件的風險。它還具有體重減輕、降尿酸和降壓的益處。④胰高糖素樣肽1受體(GLP-1RA):GLP-1類似物主要通過腸促胰島素效應發揮作用,刺激胰島素釋放,抑制胰高血糖素分泌,延遲胃排空和增加飽腹感,達到降低血糖作用,其利尿和利鈉作用起到降壓效果。它還能減少糖尿病患者新發大量白蛋白尿的風險,具有廣泛的心腎臟保護及體重減輕益處。⑤沙庫巴曲/纈沙坦:這是一種新型藥物,同時具有腦啡肽酶(NEP)抑制劑—沙庫巴曲和血管緊張素II(AngII)AT1受體阻斷劑—纈沙坦的雙重作用,其通過抑制NEP及(AngII)AT1受體的雙重作用機制,導致全身血管擴張、利尿和利鈉作用增強,發揮降低血壓和改善心力衰竭(HF)癥狀等重要作用。這種藥物又同時干預RAAS和利鈉肽系統,因此具有較強的降壓作用,且其降壓作用隨劑量增加而增強,還具有降低蛋白尿、保護腎功能作用。研究還證實這種藥物通過改善胰島素敏感性來改善血糖控制,可明顯改善糖尿病和心血管疾病風險。

