基于HPLC-QAMS及化學計量學的利膽石顆粒質量評價研究
劉艷芬,段 芳,張 翹,郭 丹*
基于HPLC-QAMS及化學計量學的利膽石顆粒質量評價研究
劉艷芬1,段 芳1,張 翹2,郭 丹1*
1. 南方醫科大學南方醫院 藥學部,廣東 廣州 510515 2. 廣東食品藥品職業學院中藥學院,廣東 廣州 510520
建立HPLC一測多評法(quantitative analysis of multi-components by single-marker,QAMS)法聯合化學計量學對利膽石顆粒質量控制的方法。采用HPLC-QAMS對3個廠家的10批利膽石顆粒中雙去甲氧基姜黃素、去甲氧基姜黃素、姜黃素、柚皮蕓香苷、橙皮苷、川陳皮素、3,5,6,7,8,3′,4′-七甲氧基黃酮、橘紅素、香附烯酮、圓柚酮和α-香附酮含量進行同時檢測;再利用SPSS 26.0、SIMCA 14.1軟件對上述指標的QAMS法計算數據進行層次聚類分析(hierarchical cluster analysis,HCA)、主成分分析(principal component analysis,PCA)及偏最小二乘-判別分析(partial least squares-discriminant analysis,PLS-DA),綜合評價利膽石顆粒質量及標志性成分。11種成分分別各自范圍內線性關系良好(>0.999 3);平均加樣回收率在96.87%~100.08%,RSD在0.66%~1.56%;HPLC-QAMS法所測結果與外標法(ESM)無顯著性差異;通過化學計量學分析,10批利膽石顆粒聚為3類,同一廠家聚為一類,不同廠家的質量存在一定的差異,柚皮蕓香苷(VIP=1.745)、橙皮苷(VIP=1.470)、香附烯酮(VIP=1.350)和姜黃素(VIP=1.188)可能是影響利膽石顆粒產品質量差異的標志物。所建立的HPLC-QAMS法多指標成分定量控制及化學計量學模式識別專屬性強,可用于利膽石顆粒質量控制和綜合評價。
利膽石顆粒;一測多評法;偏最小二乘-判別分析;化學計量學;質量評價;雙去甲氧基姜黃素;去甲氧基姜黃素;姜黃素;柚皮蕓香苷;橙皮苷;川陳皮素;3,5,6,7,8,3′,4′-七甲氧基黃酮;橘紅素;香附烯酮;圓柚酮;α-香附酮;層次聚類分析;主成分分析
中醫藥是中華民族智慧的結晶,在預防與治療疾病方面發揮了重要的作用。但目前中藥復方制劑質量評價標準不完善、均一性差一直是行業發展的首要問題,中藥制劑由多種藥味根據中醫藥配伍理論組方,中藥材本身受基原多、品種多、產地廣、成分繁雜、作用復雜(或制約或協同)的影響,質量和療效的一致性不能保證。
利膽石顆粒具有疏肝利膽、和胃健脾的功效,由郁金、陳皮、青皮、枳殼、香附、神曲、茵陳、紫蘇梗等15味中藥材加工而成,主要用于膽囊結石、膽道感染、膽道術后綜合癥的治療。其處方源于衛生部藥品標準中藥成方制劑第十二冊[1],質量標準未制定含量測定項,相關文獻報道[2]僅對橙皮苷進行定量控制。對于由15味中藥材組方的制劑來說,僅測定單一成分難以準確評價其綜合質量,也不能從根本上保證產品質量,更不能保證療效和安全性。但中藥成分對照品不易提純、不穩定、價高也造成多指標多成分質量控制模式難以推廣,一測多評法(quantitative analysis of multi-components by single-marker,QAMS)是采用一種相對易得、價廉的內參比物質對照品,實現對多個成分的同時測定;化學計量學應用數學、統計學與計算機科學的工具和手段及其最新成果進行設計或選擇最優測量方法,主要包括層次聚類分析(hierarchical cluster analysis,HCA)、主成分分析(principal component analysis,PCA)、判別分析(discriminant analysis,DA)和人工神經網絡。可以根據多變量數值分析把同類與異類中藥材區別開,近年來,HPLC-QAMS法[3-4]及化學計量學[5]越來越多地應用于中成藥復方制劑質控研究中。
本實驗參考中藥質量標志物[6-7]確認依據,以君藥香附和陳皮為首選,同時兼顧臣藥青皮、郁金和神曲及佐藥枳殼,選取它們所含主要成分進行分析,其中香附疏肝解郁、理氣寬中,主要藥效成分為香附烯酮、圓柚酮和α-香附酮等[8],陳皮、青皮和枳殼理氣健脾、寬中行滯、疏肝,主要含黃酮苷類成分柚皮蕓香苷、橙皮苷、川陳皮素、3,5,6,7,8,3′,4′-七甲氧基黃酮(3,5,6,7,8,3′,4′-heptamethoxyflavone,HMOF)和橘紅素[9],郁金利膽退黃、行氣解郁、清心涼血,主要含姜黃素類成分雙去甲氧基姜黃素、去甲氧基姜黃素和姜黃素[10],綜合考慮,最終選取質穩價廉的橙皮苷為內參比物質,采用HPLC- QAMS法并結合化學計量學對利膽石顆粒中雙去甲氧基姜黃素、去甲氧基姜黃素、姜黃素、柚皮蕓香苷、橙皮苷、川陳皮素、HMOF、橘紅素、香附烯酮、圓柚酮和α-香附酮含量進行同時檢測及評價分析,以期完善該制劑的控制手段,確保產品質量穩定和臨床療效的一致性。
1 儀器與材料
1.1 儀器
Thermo Ultimate 3000型高效液相色譜儀,美國Thermo Fisher公司;Waters e2695型高效液相色譜儀,美國Waters公司;Venusil XBP C18柱,博納艾杰爾公司;Cosmosil C18柱,Nacalai Tesque公司;Kromasil 100-5-C18柱,Akzo-Nobel公司,規格均為250 mm×4.6 mm,5 μm;Sartorius CP225D型電子天平,賽多利斯科學儀器有限公司。
1.2 試藥
對照品雙去甲氧基姜黃素(批號112004- 201501,質量分數95.0%)、去甲氧基姜黃素(批號112003-201501,質量分數98.5%)、姜黃素(批號110823-202107,質量分數98.1%)、橙皮苷(批號110721-202019,質量分數95.3%)、川陳皮素(批號112055-202102,質量分數99.7%)和α-香附酮(批號110748-201815,質量分數99.7%)購于中國食品藥品檢定研究院;對照品柚皮蕓香苷(批號PRF9062802,質量分數99.8%)、HMOF(批號PRF10032041,質量分數99.7%)、橘紅素(批號PRF8063048,質量分數98.7%)、香附烯酮(批號PRF20073022,質量分數98.0%)和圓柚酮(批號PRF8072622,質量分數97.4%)購于成都普瑞法科技開發有限公司。
陰性試驗所用中藥材來源于安國市神禾中藥材飲片有限責任公司,經廣東食品藥品職業學院中藥學院張翹教授鑒定為正品,郁金(批號20210802,產地浙江)為姜科姜黃屬植物溫郁金Y. H. Chen et C. Ling的干燥塊根,陳皮(批號20201203,產地湖北)為蕓香科柑橘屬植物橘Blanco及其栽培變種的干燥成熟果皮,青皮(批號20210801,產地江西)為蕓香科柑橘屬植物橘及其栽培變種的干燥幼果或未成熟果實的果皮,枳殼(批號20200704,產地湖南)為蕓香科柑橘屬植物酸橙L.及其栽培變種的干燥未成熟果實,香附(批號20210103,產地遼寧)為莎草科莎草屬植物莎草L.的干燥根莖,茵陳(批號20201201,產地陜西)為菊科艾屬植物濱蒿Waldst. et Kit.的干燥地上部分,紫蘇梗(批號20191103,產地湖北)為唇形科紫蘇屬植物紫蘇(L.) Britt.的干燥莖,山楂(批號20200901,產地山東)為薔薇科山楂屬植物山楂Bge.的干燥成熟果實,川楝子(批號20211001,產地甘肅)為楝科楝屬植物川楝Sieb. et Zucc.的干燥成熟果實,麥芽(批號20200903,產地河南)為禾本科大麥屬植物大麥L.的成熟果實經發芽干燥的炮制加工品,稻芽(批號20210901,產地江蘇)為禾本科稻屬植物稻谷L.的成熟果實經發芽干燥的炮制加工品,萊菔子(批號20210203,產地河南)為十字花科蘿卜屬植物蘿卜L.的干燥成熟種子,法半夏(批號20200601,產地四川)為天南星科半夏屬植物半夏(Thunb.) Breit.的干燥塊莖的炮制加工品,皂莢(批號20211003,產地河北)為豆科皂莢屬植物皂莢Lam.的干燥成熟果實。
乙腈和甲酸均選用色譜純級別,其余試劑為分析純;利膽石顆粒(規格:每袋裝25 g),分別購于云南云龍制藥股份有限公司,批號20200905、20210207、20210211、20210309,編號S1~S4;華潤三九醫藥股份有限公司,批號2102138D、2103072D、2103094D,編號依次為S5~S7;江西保利制藥有限公司,批號200901、201102、210203,編號依次為S8~S10。
2 方法與結果
2.1 混合對照品溶液的制備
取雙去甲氧基姜黃素、去甲氧基姜黃素、姜黃素、柚皮蕓香苷、橙皮苷、川陳皮素、HMOF、橘紅素、香附烯酮、圓柚酮和α-香附酮對照品適量,用甲醇制成0.126、0.142、0.258、0.976、1.210、0.392、0.178、0.156、0.480、0.094、0.212 mg/mL的混合儲備液。將混合儲備液用甲醇稀釋20倍得混合對照品溶液(雙去甲氧基姜黃素6.3 μg/mL、去甲氧基姜黃素7.1 μg/mL、姜黃素12.9 μg/mL、柚皮蕓香苷48.8 μg/mL、橙皮苷60.5 μg/mL、川陳皮素19.6 μg/mL、HMOF 8.9 μg/mL、橘紅素7.8 μg/mL、香附烯酮24.0 μg/mL、圓柚酮4.7 μg/mL和α-香附酮 10.6 μg/mL)。
2.2 供試品溶液的制備
取利膽石顆粒適量,研細,精密稱定約2 g,置具塞錐形瓶中,精密加甲醇25 mL,稱定質量,加熱回流處理30 min,放冷,補足減失的質量,搖勻,濾過,即得利膽石顆粒供試品溶液。
取按處方和制法制備的缺郁金和神曲陰性樣品、缺陳皮、枳殼、青皮和神曲陰性樣品、缺香附和神曲陰性樣品各適量,按上述方法制得3種陰性供試品溶液。
2.3 色譜條件
Venusil XBP C18(250 mm×4.6 mm,5 μm)色譜柱,柱溫30 ℃;檢測波長分別為420 nm(0~24 min檢測雙去甲氧基姜黃素、去甲氧基姜黃素和姜黃素)[11-15]、300 nm(24~47 min檢測柚皮蕓香苷、橙皮苷、川陳皮素、HMOF和橘紅素)[16-19]和242 nm(47~75 min檢測香附烯酮、圓柚酮和α-香附酮)[20-22];流動相為乙腈-0.1%甲酸水溶液,梯度洗脫:0~12 min,17.0%乙腈;12~24 min,17.0%~46.0%乙腈;24~47 min,46.0%~61.0%乙腈;47~67 min,61.0%~68.0%乙腈;67~75 min,68.0%~17.0%乙腈;體積流量1.0 mL/min;進樣量10 μL。理論板數按各成分色譜峰計均≥5500。
2.4 方法學驗證
2.4.1 專屬性試驗 依法進樣“2.1”項下混合對照品溶液及“2.2”項供試品溶液,記錄色譜圖(圖1)。結果表明,利膽石顆粒供試品溶液中11種成分與相鄰色譜峰分離良好(分離度均≥1.5);陰性樣品不干擾檢測。
2.4.2 線性關系考察 精密吸取“2.1”項下儲備液0.1、0.2、0.5、1.0、2.0、5.0 mL,置不同的20 mL量瓶中,用甲醇定容得6個混合對照品溶液,依法進樣,以雙去甲氧基姜黃素、去甲氧基姜黃素、姜黃素、柚皮蕓香苷、橙皮苷、川陳皮素、HMOF、橘紅素、香附烯酮、圓柚酮和α-香附酮質量濃度對峰面積進行線性回歸,得回歸方程、線性范圍及相關系數分別為雙去甲氧基姜黃素=7.088 2×105-506.90,=0.999 6,線性范圍0.63~31.50 μg/mL;去甲氧基姜黃素=9.162 8×105+1 454.6,=0.999 3,線性范圍0.71~35.50 μg/mL;姜黃素=1.813 4×106-217.70,=0.999 7,線性范圍1.29~64.50 μg/mL;柚皮蕓香苷=1.652 5×106-960.10,=0.999 4,線性范圍4.88~244.00 μg/mL;橙皮苷=1.537 1×106+1 242.10,=0.999 6,線性范圍6.05~302.50 μg/mL;川陳皮素=2.076 8× 106+641.60,=0.999 3,線性范圍1.96~98.00 μg/mL;HMOF=1.439 3×106+1 061.80,=0.999 4,線性范圍0.89~44.50 μg/mL;橘紅素=1.213 3×106-744.90,=0.999 6,線性范圍0.78~39.00 μg/mL;香附烯酮=2.456 4×106+972.80,=0.999 3,線性范圍2.40~120.00 μg/mL;圓柚酮=4.939 9×105+139.50,=0.999 5,線性范圍0.47~23.50 μg/mL;α-香附酮=1.565 2×106+645.30,=0.999 4,線性范圍1.06~53.00 μg/mL。
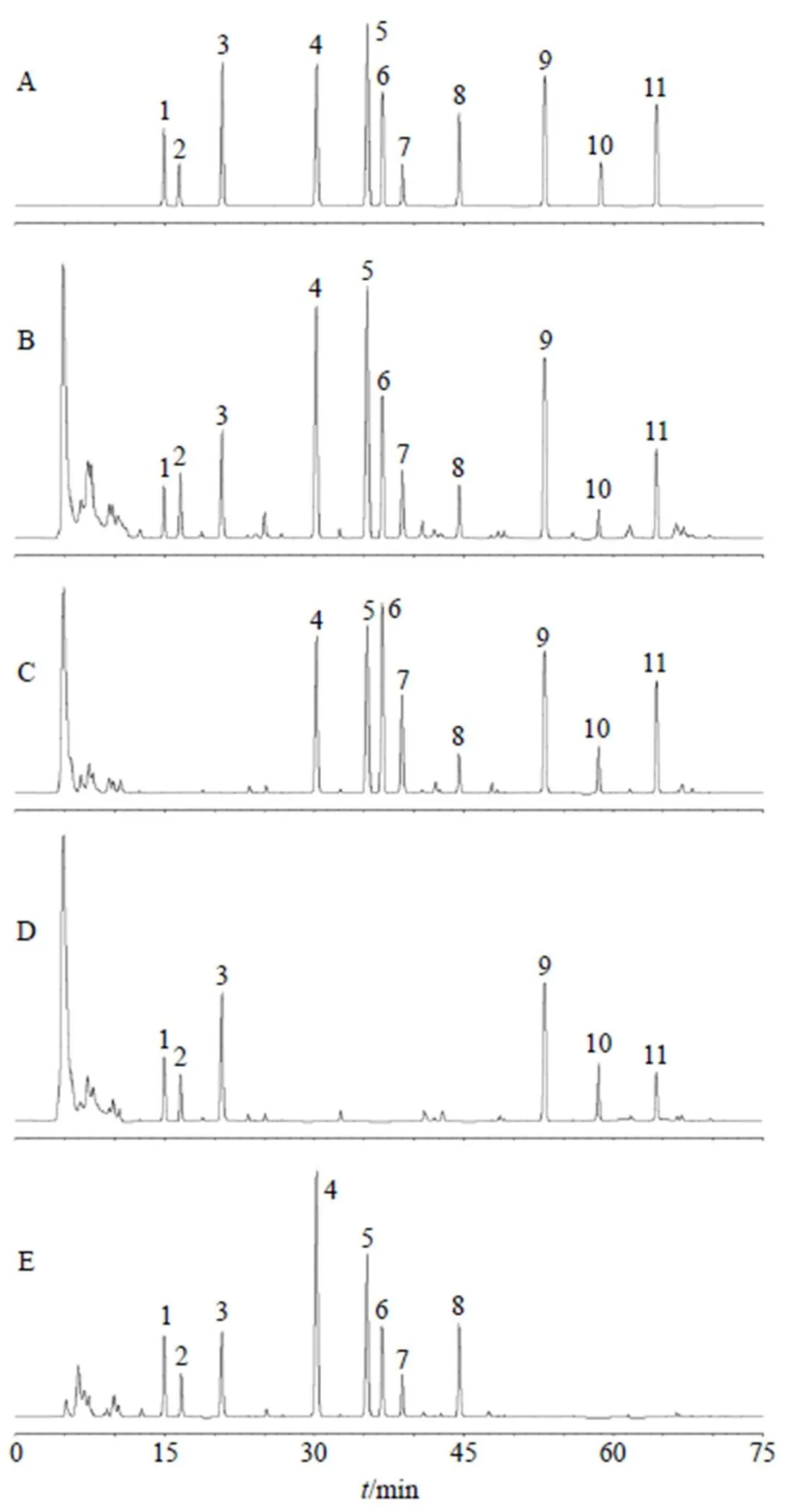
1-雙去甲氧基姜黃素 2-去甲氧基姜黃素 3-姜黃素 4-柚皮蕓香苷 5-橙皮苷 6-川陳皮素 7-HMOF 8-橘紅素 9-香附烯酮 10-圓柚酮 11-α-香附酮
2.4.3 精密度試驗 依法重復進樣利膽石顆粒(編號S1)供試品溶液6次,每次10 μL,得雙去甲氧基姜黃素、去甲氧基姜黃素、姜黃素、柚皮蕓香苷、橙皮苷、川陳皮素、HMOF、橘紅素、香附烯酮、圓柚酮和α-香附酮峰面積的RSD值依次為1.35%、1.18%、1.12%、0.77%、0.59%、1.06%、1.20%、1.26%、0.81%、1.42%、1.30%,表明精密度良好(RSD小于2.0%)。
2.4.4 重復性試驗 依法制備6份利膽石顆粒(編號S1)供試品溶液,進樣10 μL檢測分析,用外標法計算含量,得雙去甲氧基姜黃素、去甲氧基姜黃素、姜黃素、柚皮蕓香苷、橙皮苷、川陳皮素、HMOF、橘紅素、香附烯酮、圓柚酮和α-香附酮質量分數的RSD值依次為1.79%、1.66%、1.58%、1.05%、0.93%、1.28%、1.32%、1.45%、1.11%、1.85%、1.63%,表明重復性良好(RSD小于2.0%)。
2.4.5 穩定性試驗 取利膽石顆粒(編號S1)供試品溶液,于制備后0、2、5、9、16、24 h依法進樣10 μL,得雙去甲氧基姜黃素、去甲氧基姜黃素、姜黃素、柚皮蕓香苷、橙皮苷、川陳皮素、HMOF、橘紅素、香附烯酮、圓柚酮和α-香附酮峰面積的RSD值依次為1.31%、1.14%、1.09%、0.80%、0.61%、1.04%、1.18%、1.29%、0.84%、1.43%、1.27%,表明利膽石顆粒供試品溶液24 h內穩定(RSD小于2.0%)。
2.4.6 加樣回收率試驗 取已知待測成分含量的利膽石顆粒(編號S1),研成細粉,精密稱定1.0 g,精密加入混合對照品溶液(雙去甲氧基姜黃素0.067 mg/mL、去甲氧基姜黃素0.082 mg/mL、姜黃素0.174 mg/mL、柚皮蕓香苷0.749 mg/mL、橙皮苷0.886 mg/mL、川陳皮素0.218 mg/mL、HMOF 0.117 mg/mL、橘紅素0.091 mg/mL、香附烯酮0.343 mg/mL、圓柚酮0.051 mg/mL和α-香附酮0.149 mg/mL)0.8、1.0、1.2 mL,每個質量濃度制備3份,再按“2.2”項方法制成加樣供試品溶液,依法檢測,得上述11種成分的平均加樣回收率及RSD分別為97.28%(1.28%)、98.03%(1.56%)、98.18%(0.91%)、99.82%(0.84%)、100.08%(0.70%)、97.32%(1.07%)、97.43%(1.36%)、99.00%(1.19%)、100.01%(0.66%)、96.95%(0.88%)、96.87%(1.16%)。
2.5 HPLC-QAMS的建立
2.5.1 相對校正因子(k/s)的計算 依法進樣“2.4.2”項6個混合對照品溶液各10 μL,用對照品質量濃度與峰面積之比計算各成分k/s,即k/s=k/s=(k/k)/(W/A)=(kA)/(WAk)(其中、、、k和依次代表、質量濃度、峰面積、內參物和其他待測成分)。以橙皮苷為內參物,分別計算其他10種成分的(表1)。
2.5.2 儀器及色譜柱對k/s的影響 分別選用儀器(Thermo Ultimate 3000型和e2695型高效液相色譜儀)和色譜柱(Venusil XBP C18柱、Cosmosil C18柱和Kromasil 100-5-C18柱),進樣“2.1”項下混合對照品溶液10 μL,結果(表2)測得各成分k/s的RSD在0.79%~1.97%,表明儀器與色譜柱對所建立的k/s無影響。
2.5.3 體積流量對k/s的影響 在體積流量0.8、1.0、1.2 mL/min條件下,依法進樣“2.1”項下對照品溶液10 μL,結果(表3)測得各成分k/s的RSD在0.85%~1.92%,表明體積流量對所建立的k/s無影響。
2.5.4 柱溫對k/s的影響 在柱溫25、30、35 ℃條件下,依法進樣“2.1”項下對照品溶液10 μL,結果(表4)測得各成分k/s的RSD在0.68%~1.94%,表明柱溫對所建立的k/s無影響。
2.5.5 色譜峰定位 依法進樣“2.1”項下對照品溶液10 μL,采用相對保留時間值法對待測成分色譜峰進行定位,考察儀器(Thermo Ultimate 3000型和e2695型高效液相色譜儀)和色譜柱(Venusil XBP C18柱、Cosmosil C18柱和Kromasil 100-5-C18柱)對相對保留時間值()的影響,結果(表5)測得雙去甲氧基姜黃素、去甲氧基姜黃素、姜黃素、柚皮蕓香苷、川陳皮素、HMOF、橘紅素、香附烯酮、圓柚酮、α-香附酮和橙皮苷相對保留時間值()的RSD在0.84%~1.72%,表明采用相對保留時間值法可以對目標化合物色譜峰進行準確定位。
表1 利膽石顆粒中11種成分的fk/s
Table1 fk/s of 11 component in Lidanshi Granules
混合對照品溶液f橙皮苷/雙去甲氧基姜黃素f橙皮苷/去甲氧基姜黃素f橙皮苷/姜黃素f橙皮苷/柚皮蕓香苷f橙皮苷/川陳皮素f橙皮苷/HMOFf橙皮苷/橘紅素f橙皮苷/香附烯酮f橙皮苷/圓柚酮f橙皮苷/α-香附酮 12.175 41.637 40.862 50.920 40.724 01.055 11.291 50.618 53.090 50.972 2 22.169 31.634 00.838 00.920 20.726 01.055 31.254 40.609 83.089 30.972 4 32.198 81.638 60.862 00.924 10.725 51.057 81.264 50.610 53.099 40.965 3 42.172 01.649 30.847 80.917 30.731 61.056 31.262 70.617 83.079 40.968 0 52.164 31.713 40.843 00.945 90.756 61.081 51.274 30.641 43.141 31.001 1 62.169 71.672 70.848 30.928 50.738 21.066 31.266 40.624 03.108 20.979 9 平均值2.174 91.657 60.850 30.926 10.733 71.062 01.269 00.620 33.101 30.976 5 RSD/%0.561.861.181.121.690.981.011.870.711.33
表2 儀器及色譜柱對fk/s的影響
Table 2 Effects of instruments and columns on fk/s
儀器色譜柱f橙皮苷/雙去甲氧基姜黃素f橙皮苷/去甲氧基姜黃素f橙皮苷/姜黃素f橙皮苷/柚皮蕓香苷f橙皮苷/川陳皮素f橙皮苷/HMOFf橙皮苷/橘紅素f橙皮苷/香附烯酮f橙皮苷/圓柚酮f橙皮苷/α-香附酮 Thermo Ultimate 3000Venusil XBP C182.172 01.654 30.847 60.924 20.731 91.060 51.267 20.618 53.100 10.974 3 Cosmosil C182.140 51.617 90.825 30.907 70.718 01.038 21.240 10.604 33.070 60.950 6 Kromasil 100-5-C182.189 21.708 60.856 90.941 30.750 61.084 71.287 50.635 93.143 90.998 0 e2695Venusil XBP C182.166 91.632 80.841 50.919 00.724 41.055 01.253 90.614 03.0954 0.967 4 Cosmosil C182.155 71.650 10.837 20.915 60.720 81.047 91.254 80.606 73.088 20.958 1 Kromasil 100-5-C182.178 31.679 50.848 10.936 40.743 21.072 61.271 00.625 23.129 70.982 7 平均值2.167 11.657 20.842 80.924 00.731 51.059 81.262 40.617 43.104 70.971 9 RSD/%0.791.971.291.381.781.591.301.920.881.76
表3 體積流量對fk/s的影響
Table 3 Effects of flow velocitys on fk/s
體積流量/(mL?min?1)f橙皮苷/雙去甲氧基姜黃素f橙皮苷/去甲氧基姜黃素f橙皮苷/姜黃素f橙皮苷/柚皮蕓香苷f橙皮苷/川陳皮素f橙皮苷/HMOFf橙皮苷/橘紅素f橙皮苷/香附烯酮f橙皮苷/圓柚酮f橙皮苷/α-香附酮 0.82.195 81.696 30.870 20.935 60.751 01.072 61.290 90.637 83.141 90.991 2 1.02.176 31.659 00.851 50.928 80.736 11.064 31.271 50.622 23.103 60.978 4 1.22.159 01.632 70.848 10.912 30.724 51.050 91.256 70.614 33.076 20.956 7 平均值2.177 01.662 70.856 60.925 60.737 21.062 61.273 00.624 83.107 20.975 4 RSD/%0.851.921.391.291.801.031.351.911.061.79
表4 柱溫對fk/s的影響
Table 4 Effects of column temperature on fk/s
柱溫/℃f橙皮苷/雙去甲氧基姜黃素f橙皮苷/去甲氧基姜黃素f橙皮苷/姜黃素f橙皮苷/柚皮蕓香苷f橙皮苷/川陳皮素f橙皮苷/HMOFf橙皮苷/橘紅素f橙皮苷/香附烯酮f橙皮苷/圓柚酮f橙皮苷/α-香附酮 252.160 91.620 90.831 50.910 30.718 91.051 51.246 20.600 13.070 40.957 2 302.172 61.655 80.848 00.924 70.731 61.060 31.267 50.618 93.099 50.974 0 352.185 21.683 50.857 20.938 20.747 31.074 71.283 90.621 03.123 80.991 6 平均值2.171 21.653 40.845 60.924 40.732 61.062 21.265 90.613 33.097 90.974 3 RSD/%0.681.901.541.511.941.101.491.880.861.77
2.6 含量測定
為驗證所建立的QAMS法的準確性及可行性,取10批利膽石顆粒,依法制備利膽石顆粒供試品溶液,再依法進樣分析,分別運用外標法和HPLC QAMS法計算利膽石顆粒中各成分的含量,比較2種方法檢測結果的差異。結果(表6)2種方法無顯著差異(>0.05),表明HPLC QAMS法可用于利膽石顆粒中11種成分的含量測定。
3 利膽石顆粒的化學計量學質量分析
3.1 HCA
將10批利膽石顆粒中雙去甲氧基姜黃素、去甲氧基姜黃素、姜黃素、柚皮蕓香苷、橙皮苷、川陳皮素、HMOF、橘紅素、香附烯酮、圓柚酮和α-香附酮HPLC-QAMS法含量測定結果導入SPSS 26.0統計軟件進行聚類模式識別分析(分類:系統聚類;聚類方法:組間聯接;測量區間:Euclidean距離),得圖2。結果顯示,當間距為15時,10批利膽石顆粒供試品聚為3類,S5、S6和S7為第I類,S1、S3、S2和S4為第II類,S8、S9和S10為第III類,從聚類結果可以看出,同一廠家的產品聚成一類。
3.2 PCA
PCA通過降維處理對指標進行簡化,將10批利膽石顆粒中雙去甲氧基姜黃素、去甲氧基姜黃素、姜黃素、柚皮蕓香苷、橙皮苷、川陳皮素、HMOF、橘紅素、香附烯酮、圓柚酮和α-香附酮HPLC-QAMS法含量測定結果導入SPSS 26.0統計軟件及統計軟件SIMCA 14.1對主成分進行提取,得各主成分特征值和方差貢獻率,結果見表7、8和圖3。由表7可知前2個主成分特征值大于1,即7.463和2.227,對方差的貢獻率分別為67.848%、20.248%,累積方差貢獻率為88.096%,大于85%,表明選取前2個主成分即可代表利膽石顆粒88.096%的信息量。表8主成分矩陣可以看出第1主成分的信息來自雙去甲氧基姜黃素、去甲氧基姜黃素、橙皮苷、川陳皮素、HMOF、橘紅素、香附烯酮、圓柚酮等成分的綜合,第2主成分的信息來自姜黃素、柚皮蕓香苷的信息。從圖3可以看出,S8~S10、S1~S4以及S5~S7分別呈現一定關聯性,與“3.1”項聚類分析結果一致。
表5 儀器及色譜柱對ts/k的影響
Table 5 Effects of instruments and chromatographic columns on ts/k
儀器色譜柱t雙去甲氧基姜黃素/橙皮苷t去甲氧基姜黃素/橙皮苷t姜黃素/橙皮苷t柚皮蕓香苷/橙皮苷t川陳皮素/橙皮苷tHMOF/橙皮苷t橘紅素/橙皮苷t香附烯酮/橙皮苷t圓柚酮/橙皮苷tα-香附酮/橙皮苷 Thermo Ultimate 3000Venusil XBP C180.422 40.465 60.587 40.854 61.041 31.098 21.259 31.502 91.660 11.819 3 Cosmosil C180.420 80.451 10.581 60.842 11.029 61.071 91.230 51.483 21.642 81.796 6 Kromasil 100-5-C180.429 50.472 80.594 80.868 91.055 11.111 51.277 01.530 71.687 51.835 7 e2695Venusil XBP C180.417 70.460 30.582 60.850 21.035 91.080 41.241 81.489 61.653 91.802 8 Cosmosil C180.423 60.455 90.585 10.851 81.036 21.083 71.245 61.497 01.632 61.804 1 Kromasil 100-5-C180.425 00.467 40.590 70.857 31.048 01.092 21.262 11.514 51.671 21.825 9 平均值0.423 20.462 20.587 00.854 21.041 01.089 71.252 71.503 01.658 01.814 1 RSD/%0.941.720.861.040.891.291.331.161.190.84
表6 利膽石顆粒中11種成分含量測定結果(n = 3)
Table 6 Determination results of 11 components in Lidanshi Granules (n = 3)
樣品雙去甲氧基姜黃素/(mg?g?1)去甲氧基姜黃素/(mg?g?1)姜黃素/(mg?g?1)柚皮蕓香苷/(mg?g?1)川陳皮素/(mg?g?1)橙皮苷/(mg?g?1) 外標法QAMS外標法QAMS外標法QAMS外標法QAMS外標法QAMS外標法 S10.0690.0680.0810.0800.1720.1740.7560.7680.2170.2190.891 S20.0700.0720.1220.1250.2420.2480.8380.8560.2730.2740.953 S30.0570.0560.0870.0880.1760.1800.7360.7310.2320.2260.844 S40.0760.0780.1110.1130.2150.2090.8370.8150.2690.2660.974 S50.0700.0690.1090.1110.1520.1530.7260.7450.2130.2120.766 S60.0650.0640.1290.1320.1100.1090.7070.7020.1940.1970.709 S70.0600.0590.1190.1160.1020.1000.6590.6730.1860.1890.695 S80.0890.0870.0770.0780.1640.1600.6230.6380.3090.3051.073 S90.1050.1080.0680.0670.1890.1940.5900.6020.2990.2971.120 S100.0900.0920.0990.0970.1330.1360.5570.5660.3280.3251.142 P值0.9780.9590.9680.8750.964? 樣品HMOF/(mg?g?1)橘紅素/(mg?g?1)香附烯酮/(mg?g?1)圓柚酮/(mg?g?1)α-香附酮/(mg?g?1) 外標法QAMS外標法QAMS外標法QAMS外標法QAMS外標法QAMS S10.1190.1180.0920.0930.3470.3450.0520.0510.1450.146 S20.1250.1270.1200.1220.2630.2700.0330.0340.1930.188 S30.1210.1240.0900.092 0.3590.3640.0410.0420.1310.132 S40.1120.1110.1190.1170.3130.3080.0380.0390.1820.183 S50.1020.1030.0830.0820.2010.1990.0340.0330.1040.103 S60.0950.0940.0760.0770.1810.1800.0280.0270.1150.113 S70.0960.0970.0790.0800.1640.1600.0300.0310.0870.086 S80.1530.1510.1510.1480.5350.5280.0560.0570.1630.160 S90.1580.1600.1350.1370.5010.5140.0610.0600.1250.123 S100.1480.1450.1400.1420.4820.4910.0640.0630.1760.171 P值0.9920.9680.9830.9860.920
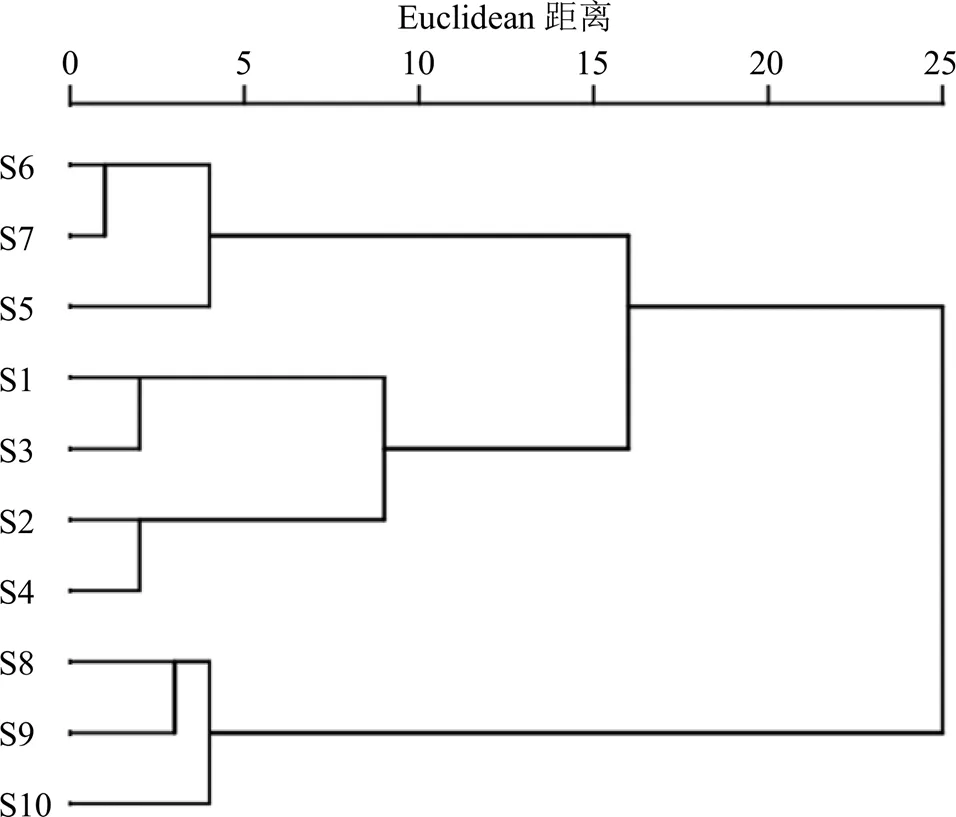
圖2 10批樣品聚類樹狀圖
表7 利膽石顆粒中主成分特征值和貢獻率
Table 7 Eigenvalue and contribution rate of principal components in Lidanshi Granules
主成分初始特征值提取載荷平方和 特征值方差貢獻率/%累積方差貢獻率/%特征值方差貢獻率/%累積方差貢獻率/% 17.46367.84867.8487.46367.84867.848 22.22720.24888.0962.22720.24888.096 30.7546.85294.949 40.3383.07798.026 50.1301.18399.209 60.0450.41399.622 70.0230.20699.828 80.0140.12699.954 90.0050.046100.000
表8 11種成分的成分矩陣
Table 8 Composition matrix of 11 components in Lidanshi Granules
成分主成分成分主成分1212 雙去甲氧基姜黃素0.877?0.167HMOF0.967?0.046 去甲氧基姜黃素?0.7200.334橘紅素0.9480.161 姜黃素0.3740.833香附烯酮0.967?0.123 柚皮蕓香苷?0.4950.826圓柚酮0.929?0.244 橙皮苷0.9810.143α-香附酮0.5530.746 川陳皮素0.9420.179
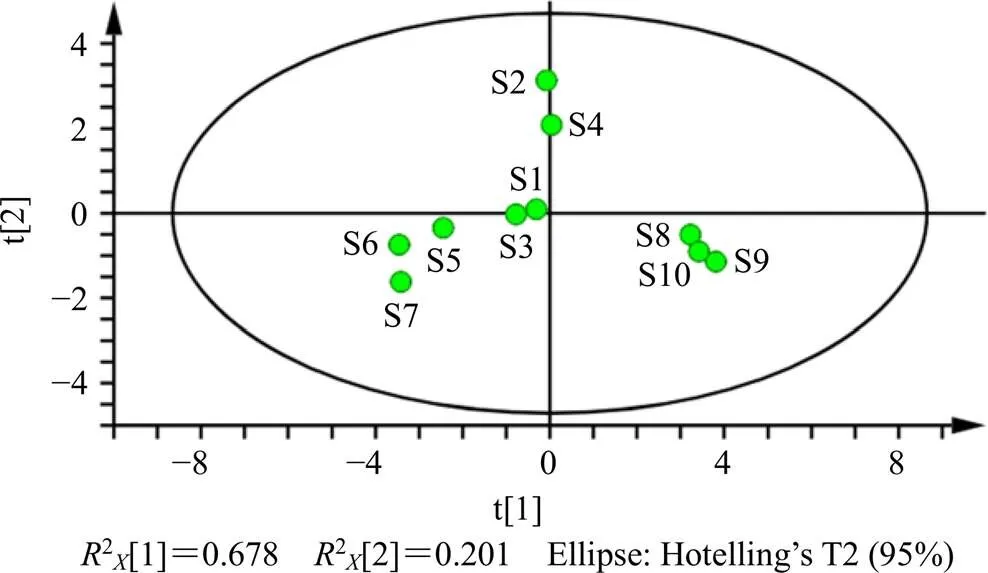
圖3 PCA得分圖
3.3 PLS-DA
PLS-DA通過對數據的分析,能夠查找出引起產品質量差異的特征成分,將10批利膽石顆粒中雙去甲氧基姜黃素、去甲氧基姜黃素、姜黃素、柚皮蕓香苷、橙皮苷、川陳皮素、HMOF、橘紅素、香附烯酮、圓柚酮和α-香附酮的QAMS法含量數據導入SIMCA 14.1統計軟件,進行PLS-DA分析,繪制PLS-DA模型得分圖(圖4),結果累積解釋能力參數(2、2)分別為0.927和0.848,預測能力參數2為0.757,均大于0.5,說明表明所建立的模型穩定可靠、預測能力強,可用于區分不同批次的利膽石顆粒。
由圖4可以看出10批利膽石顆粒的含量數據點均落在95%置信區間內,根據分布可分為3類,與聚類分析和主成分分析結果一致。
對建立的PLS-DA模型進行200次置換檢驗(圖5),結果顯示2擬合直線軸截距為0.133,小于0.3,表明所建立的模型結果可靠;2擬合直線軸截距為?0.275,小于0.05,表明所建立的模型不存在過度擬合,可有效判別分析10批利膽石顆粒的質量差異。
根據變量重要性投影(variable importance in projection,VIP)值篩選影響藥物炮制前后組方利膽石顆粒化學成分差異的標志性成分(圖6),結果VIP>1的有4個成分,即柚皮蕓香苷(VIP=1.745)、橙皮苷(VIP=1.470)、香附烯酮(VIP=1.350)和姜黃素(VIP=1.188)對利膽石顆粒樣品質量的影響較大,可能是影響利膽石顆粒產品質量的主要潛在標志物。
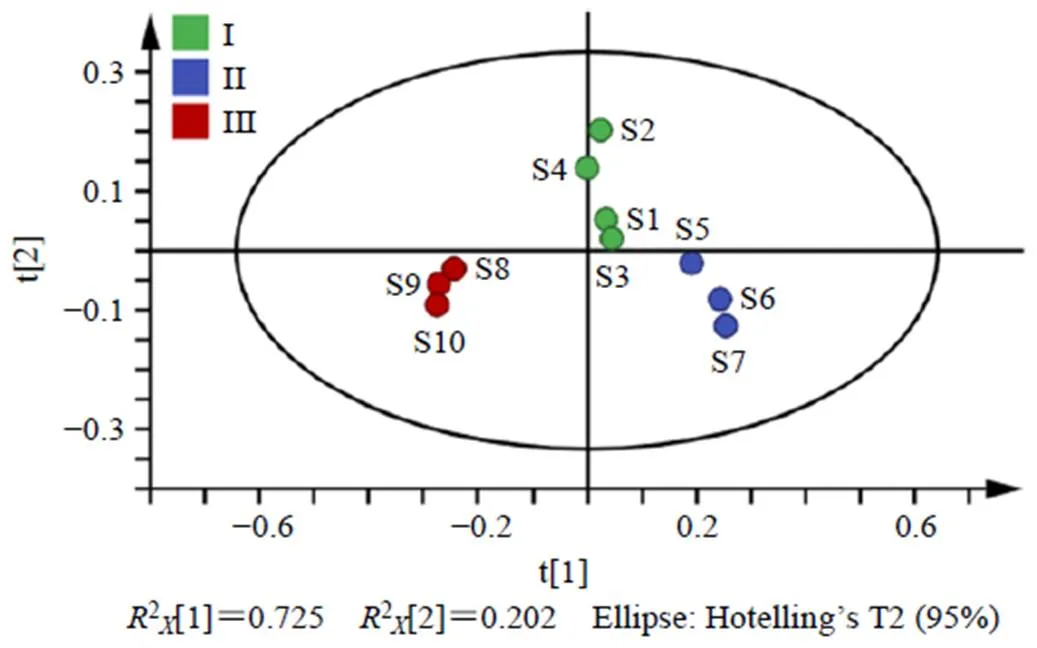
圖4 10批利膽石顆粒樣品的PLS-DA模型得分圖

圖5 PLS-DA置換檢測圖
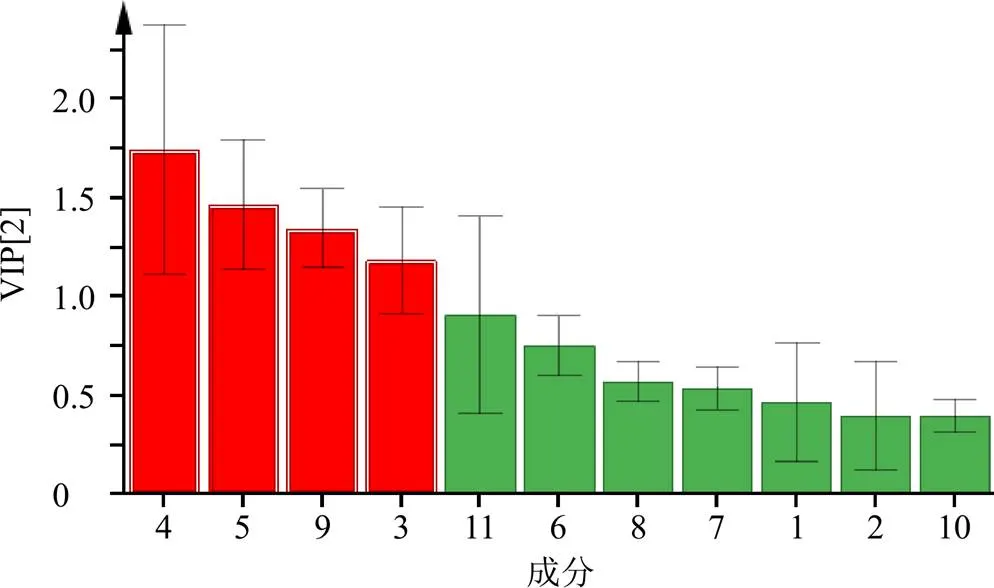
圖6 10批利膽石顆粒樣品的PLS-DA模型中共有峰的VIP值
4 討論
4.1 供試品處理方式的確定
本實驗在制備供試品溶液,以雙去甲氧基姜黃素、去甲氧基姜黃素、姜黃素、柚皮蕓香苷、橙皮苷、川陳皮素、HMOF、橘紅素、香附烯酮、圓柚酮和α-香附酮的提取效率為指標,結合雜質干擾情況,首先考察了溶劑水、甲醇和乙醇,分別采用超聲[12-15]、回流[17]、索氏[11]提取時11種成分的提取效率。結果發現,水作溶劑時,圓柚酮和α-香附酮幾乎未提取出,乙醇為溶劑時,橘紅素和圓柚酮基本未檢出,只有甲醇采用回流提取時,各成分提取效率較高,同時雜質干擾最少,進而對甲醇體積分數(50%[19]、70%[15]、85%[11]、100%[20-22])和提取時間(20、30、40、50 min)進行了篩選對比,發現甲醇加熱回流時11種提取率隨提取時間的延長有降低趨勢,但雜質卻在逐漸增加,綜合考慮確定以甲醇加熱回流提取30 min為最佳提取方式。
4.2 流動相系統的確定
本實驗在篩選流動相時,通過對乙腈-水、甲 醇-水的運行,篩選出乙腈-水系統優于甲醇-水系統,但有個別色譜峰出現了拖尾現象,進而對乙腈-0.4%磷酸水溶液[15]、乙腈-0.1%甲酸水溶液[17-18]、乙腈- 3%甲酸水溶液[11]、乙腈-1%冰醋酸水溶液[12]為流動相系統進行檢測利膽石顆粒供試品溶液,對比雙去甲氧基姜黃素、去甲氧基姜黃素、姜黃素、柚皮蕓香苷、橙皮苷、川陳皮素、HMOF、橘紅素、香附烯酮、圓柚酮和α-香附酮色譜峰的峰形及分離效果,結果乙腈-0.1%甲酸水溶液條件下可達到基線分離,峰形較好,因此,選擇乙腈-0.1%甲酸水溶液為流動相梯度洗脫對利膽石顆粒中11種成分含量進行同時檢測。
4.3 多指標成分定量控制及化學計量學結果評價
HPLC-QAMS法測定利膽石顆粒中雙去甲氧基姜黃素、去甲氧基姜黃素、姜黃素、柚皮蕓香苷、橙皮苷、川陳皮素、HMOF、橘紅素、香附烯酮、圓柚酮和α-香附酮的含量,從檢測結果可以看出HPLC-QAMS法結果與外標法實測值無明顯差異,表明所建立的HPLC-QAMS法結果準確,但各批次利膽石顆粒中11種成分含量存在一定的批間差異,表明建立多指標檢測的重要性。
分析含量差異的原因可能是廠家不同所導致,從HCA和PCA結果可以看出,10批利膽石顆粒聚為3類,同一廠家的樣品聚為一類,聚類結果與生產廠家具有一定關聯性,這可能與廠家生產工藝不盡相同,生產所用設備、原藥材也不相同有關,這也迫切要求有一個高水平的全面監控的產品質量標準來嚴格監管產品質量,從而實現質量均一性和療效一致性。PLS-DA方法篩選出4個差異性標志物,即柚皮蕓香苷、橙皮苷、香附烯酮和姜黃素是對利膽石顆粒樣品質量的影響較大的成分,與HCA、PCA相比,PLS-DA的預測能力更強,能夠更準確地進行利膽石顆粒的質量評價,也為后續生產廠家提升產品質量指明了方向。
本實驗以橙皮苷為內參物,建立了HPLC- QAMS法同時測定利膽石顆粒中雙去甲氧基姜黃素、去甲氧基姜黃素、姜黃素、柚皮蕓香苷、橙皮苷、川陳皮素、HMOF、橘紅素、香附烯酮、圓柚酮和α-香附酮的含量,方法簡便,結果準確、專屬性強,可多方位較全面地反映利膽石顆粒中化學成分信息,同時結合HCA、PCA、PLS-DA等化學計量學識別模式對含量檢測結果進行綜合分析,為完善利膽石顆粒控制方法,提升控制水平,為確保產品質量均一性和臨床療效一致性提供科學依據。利膽石顆粒方中君藥陳皮、臣藥青皮和佐藥枳殼均含有橙皮苷等成分,橙皮苷質量穩定,價廉易得,可作為該制劑多指標成分QAMS法內參物,《中國藥典》2020年版一部中陳皮和青皮均采用橙皮苷作為其定量控制指標成分,枳殼采用柚皮苷和新橙皮苷作為其定量控制成分,建議藥品生產企業建立枳殼中橙皮苷含量的內控標準,穩定該制劑的產品質量,以便于該制劑的臨床合理應用。
利益沖突 所有作者均聲明不存在利益沖突
[1] 國家食品藥品監督管理局國家藥品標準WS3-B-2330- 97 [S]. 1997: 67.
[2] 楊煒峰, 陳茂如, 劉學華. HPLC法測定利膽石顆粒中橙皮苷含量 [J]. 首都醫藥, 2008, 15(24): 38-39.
[3] 梁穎欣, 朱旦, 黃舒婷, 等. 一測多評法測定鉤藤中7種生物堿類成分的含量 [J]. 中藥材, 2019, 42(8): 1820-1823.
[4] Wang Z Q, Shen J, Li P,. Research on quality markers of: Quality evaluation and quality standards of[J]., 2017, 9(4): 307-320
[5] 高森, 王蘋, 唐鋮, 等. 基于HPLC指紋圖譜、多指標成分含量測定及化學計量學的濕熱痹片質量評價 [J]. 中草藥, 2020, 51(21): 5454-5461.
[6] 劉昌孝, 陳士林, 肖小河, 等. 中藥質量標志物(Q-Marker): 中藥產品質量控制的新概念 [J]. 中草藥, 2016, 47(9): 1443-1457.
[7] 劉昌孝. 中藥質量標志物(Q-Marker)研究發展的5年回顧 [J]. 中草藥, 2021, 52(9): 2511-2518.
[8] Mohamed-Ibrahim S R, Mohamed G A, Abdullah Khayat M T,. Anti-inflammatory terpenoids fromrhizomes [J]., 2018, 31(4 Suppl): 1449-1456.
[9] Chen H F, Zhang W G, Yuan J B,. Simultaneous quantification of polymethoxylated flavones and coumarins inandusing HPLC-ESI-MS/MS [J]., 2012, 59: 90-95.
[10] An Y W, Hu G, Yin G P,. Quantitative analysis and discrimination of steamed and non-steamed rhizomes ofby GC-MS and HPLC [J]., 2014, 52(9): 961-970.
[11] 周秋明, 王文華, 夏平, 等. HPLC法測定不同貯藏條件下莪術中6種化學成分的含量 [J]. 中國藥師, 2020, 23(8): 1669-1673.
[12] 高天慧, 廖婉, 傅超美, 等. 基于pH值動態變化的川產道地藥材蓬莪術醋制前后化學成分差異研究 [J]. 中草藥, 2017, 48(24): 5174-5178.
[13] 靳雅惠. 桂郁金種質資源姜黃素類化學成分分析 [J]. 陜西農業科學, 2021, 67(9): 61-64.
[14] 高紅寧, 殷奕, 毛春芹, 等. HPLC法測定不同產地醋莪術飲片中姜黃素、雙去甲氧基姜黃素和去甲氧基姜黃素的含量 [J]. 中國醫藥科學, 2021, 11(3): 67-70.
[15] 臧遠芳, 許麗麗, 劉洪超, 等. HPLC波長切換法測定莪術中8個主要有效成分的含量 [J]. 中國現代應用藥學, 2021, 38(18): 2227-2233.
[16] 邱烺, 吳曉玲, 謝子婷, 等. 濁點萃取-HPLC法測定陳皮中橙皮苷和川陳皮素的含量 [J]. 中藥材, 2017, 40(9): 2125-2127.
[17] 封宇飛, 張宏武, 鄒忠梅, 等. HPLC法同時測定陳皮飲片中5種黃酮類化合物的含量 [J]. 藥物分析雜志, 2009, 29(1): 10-15.
[18] 李影, 尚爾雨, 孫爽, 等. 陳皮HPLC指紋圖譜色譜條件優化 [J]. 黑龍江科學, 2021, 12(10): 8-10.
[19] 涂奇軍, 徐玲, 聶晶, 等. 蛇膽陳皮制劑中陳皮UPLC指紋圖譜 [J]. 中成藥, 2018, 40(10): 2233-2237.
[20] 王世宇, 李文兵, 盧君蓉, 等. HPLC法同時測定不同產地香附藥材中香附烯酮、圓柚酮和α-香附酮 [J]. 中成藥, 2015, 37(3): 588-591.
[21] 盧君蓉, 李文兵, 王世宇, 等. 香附醋制前后香附烯酮、圓柚酮和α-香附酮的含量比較 [J]. 中國實驗方劑學雜志, 2014, 20(20): 24-27.
[22] 喬璐, 張園園, 王若晨, 等. 不同炮制方法對香附中香附烯酮和α-香附酮的影響 [J]. 中華中醫藥學刊, 2022, 40(1): 49-53.
Quality evaluation of Lidanshi Granules based on HPLC-QAMS and chemometrics
LIU Yan-fen1, DUAN Fang1, ZHANG Qiao2, GUO Dan1
1. Department of Pharmacy, Southern Hospital of Southern Medical University, Guangzhou 510515, China 2. College of Traditional Chinese Medicine, Guangdong Food and Drug Vocational College, Guangzhou 510520, China
To establish a method for quality control of Lidanshi Granules (利膽石顆粒, LG) by HPLC-quantitative analysis of multi-components by single-marker (QAMS) combined with chemometrics.HPLC-QAMS was used to simultaneously detect the contents of bisdemethoxycurcumin, demethoxycurcumin, curcumin, narirutin, hesperidin, nobiletin, 3,5,6,7,8,3′,4′-heptamethoxyflavone, tangeretin, cyperenone, nootkatone and α-cyperone in 10 batches of LG from three manufacturers. SPSS 26.0 and SIMCA 14.1 software were used to conduct hierarchical cluster analysis (HCA), principal component analysis (PCA) and partial least squares-discriminant analysis (PLS-DA) on the QAMS calculation data of the above indexes, so as to comprehensively evaluate the quality and symbolic components of LG.The linear ranges of 11 components were good (> 0.999 3). The average recoveries were 96.87%—100.08%, RSDs were 0.66%—1.56%. There was no significant difference between HPLC-QAMS and external standard method (ESM). Through chemometrics analysis, 10 batches of LG were clustered into three categories, and the same manufacturer was clustered into one category. There was certain difference in the quality of different manufacturers, narirutin (VIP = 1.745), hesperidin (VIP = 1.470), cyperenone (VIP = 1.350) and curcumin (VIP = 1.188) might be the differential markers affecting the quality of LG.Establishment of HPLC-QAMS multi-index component quantitative control and application of chemometric pattern recognition are specific, which can be used for quality control and comprehensive evaluation of LG.
Lidanshi Granules; QAMS; discriminant analysis of partial least squares; chemometrics; quality evaluation; bisdemethoxycurcumin; demethoxycurcumin; curcumin; narirutin; hesperidin; nobiletin; 3,5,6,7,8,3′,4′-heptamethoxyflavone; tangeretin; cyperenone; nootkatone; α-cyperone; hierarchical cluster analysis; principal component analysis
R286.02
A
0253 - 2670(2022)19 - 6044 - 10
10.7501/j.issn.0253-2670.2022.19.011
2022-04-13
全國中藥特色技術傳承人才培訓項目(國中醫藥人教函[2019]43號T20194828003)
劉艷芬,女,本科,主管藥師,主要從事藥物質量控制及醫院藥學研究工作。E-mail: 757428953@qq.com
郭 丹,男,博士,主任藥師,主要從事藥物質量控制及抗腫瘤藥理研究工作。E-mail: wzaetn@163.com
[責任編輯 鄭禮勝]

