綠色還原硝基芳烴催化劑和催化機理研究進展
黃易旋,卓康基,徐娟,張燕輝
(閩南師范大學 化學化工與環境學院,福建 漳州 363000)
硝基芳烴化合物在眾多領域發揮著重要作用,但也是一類毒性較大并且難以降解的工業污染物[1]。處理水中硝基芳烴污染物的方法很多,催化技術以其簡單、高效、廉價的特點滿足了通過污水處理同時實現經濟效益與環境效益的雙重要求。然而,傳統的催化劑鐵粉容易在處理過程中產生大量鐵泥,不易處理,所以催化劑制備成為提高反應效益的關鍵[2-4]。基于此,大量的新型催化劑應運而生,進一步推動了催化硝基芳烴反應機理的完善。
綠色還原硝基芳烴的催化技術主要有室溫催化技術及光催化技術。單純的室溫反應下催化劑難以由自身激發出電子,常使用NaBH4作為氫源和供電子材料。NaBH4難以在室溫下長期保存且供應量有限,這極大地限制了催化反應的推廣應用[5-6]。相對于室溫催化,光催化技術避免了危險的還原劑參與反應,以質子溶劑作為氫源,不需要提供額外的供氫試劑,克服了NaBH4的使用帶來的弊端。半導體材料是該反應中常見的光催化劑[7]。可以發現催化還原反應實質是硝基芳烴轉移加氫還原的過程,所以,氫源及電子的轉移是機理探討的關鍵。同時,產物及副產物的再利用價值也成為了推進研究的重點。本文即以催化硝基芳烴還原胺化反應為脈絡,從催化劑及催化機理兩方面對還原硝基芳烴研究進展進行了綜述。
1 室溫催化
室溫催化還原法,在常溫常壓下以NaBH4為還原劑將硝基還原為氨基。室溫催化反應中的能量消耗低,同時可以獲得高產物收率和降低副產物的產生,反應分子之間的碰撞較少[8]。催化劑參與反應以獨特的方式降低反應的活化能。由此可見,催化劑性能的優劣是室溫催化還原硝基芳烴反應的關鍵。
1.1 室溫催化劑
1.1.1 貴金屬催化劑 硝基芳烴還原成亞胺需要經過脫氫、轉移加氫等步驟,而金屬催化劑具有很強的活化氫能力,因此金屬催化劑在該反應中被廣泛應用。金屬催化劑是指催化劑的化學組成中含有金屬元素,常用的金屬包括金、銅、鈀、鉑等。同時金屬催化劑又分為多種類型,如:還原型金屬催化劑,如鈀、鉑、鎳等;金屬氧化物型催化劑,如 ZrO2、 PdO2、 CeO2等;載體型催化劑如Pt/Al2O3、 Pt/TiO2,常用的載體有活性炭、絕緣體氧化物等[9]。
其中,還原型金屬納米粒子(NPs),具有很高的催化潛力,但它們的使用可能會導致稀有資源的消耗,環境污染和健康問題。此外,在催化反應期間,膠體金屬NPs的團聚通常不可避免。為了克服這些問題,常將NPs固定在高表面積無機載體上,例如碳納米管、石墨烯、TiO2和SiO2等。本課題組[10]報道了一種簡便的策略,用于將Au-Pd合金納米顆粒錨固到二維(2D)還原氧化石墨烯(RGO)納米片的平坦表面上。Au-Pd納米合金的形成和RGO的加載是同時完成的。將其用于選擇性還原硝基芳族化合物,Au-Pd/RGO的催化活性高于Au/RGO和Pd/RGO,催化活性的順序與Au,Pd和Au-Pd/RGO的貴金屬粒徑分布很好地吻合。
1.1.2 非貴金屬催化劑 盡管金屬催化劑具有很高的固有活性,但它們在催化還原對硝基苯酚的過程中會產生殘渣,分離困難,也存在包括選擇性低、穩定性差、雜質中毒以及影響環境等問題。此外,由于非金屬催化劑價格一般比貴金屬低很多,因此人們對開發無金屬催化劑給予了極大的關注。非金屬催化劑是指催化劑的化學組成中不含有金屬元素,通常是由N、C、P、S等元素所組成的。例如無金屬碳基催化劑(CMFCs)、六方氮化硼(h-BN)和過渡金屬二硫化(TMD),原子二維薄層結構等,由于其表面具有大量的官能團等特性得到廣泛應用[11]。
然而對于非金屬物質來說,由于它們本身沒有空軌道,普遍認為它們很難參與催化過程,所以為提高性能,常對它們進行摻雜、結構控制以及化學修飾。Jiang等[12]通過兩步煅燒工藝合成了富氧的介孔氮化硼(BNO)載體,通過典型的吸附還原程序將銅納米顆粒分散在其上。對硝基苯酚(p-NP)的還原是作為模型反應連續進行的,以確定Cu/BNO催化劑的催化性能。第一性原理計算表明,Cu/BNO的優異耐久性在很大程度上歸因于BNO在氧摻雜時的共軛作用減弱,從而增強了Cu納米粒子與BNO載體之間的相互作用。此外,摻雜的氧原子將顯著豐富Cu的電子密度,這有利于p-NP還原。所以,利用金屬與非金屬材料優勢互補,已成為催化材料研究的一大熱點。
1.1.3 金屬有機框架材料 金屬有機框架(MOF)是由具有多功能有機連接基的金屬離子/簇構成的有序多孔材料。其具有獨特的理化特性,例如結構多樣性、通用的化學組成和可調控的孔徑,MOF廣泛用于氣體分離或存儲、藥物釋放和感測。由于存在不飽和金屬位點(CUS)和催化活性有機配體,MOF可有效應用于催化領域。此外,通過MOF結構的功能化,可以用額外的活性位點修飾MOF[13-15]。
因此,MOF及其復合材料可以用作還原對硝基苯酚的有效催化劑。本課題組[14]通過簡單水熱反應制備了MIL-101(Fe)/SiO2,表現出優異的催化活性,還原對硝基苯酚,在4 min內轉化率為93.8%。SiO2和MIL-101(Fe)配合物之間的界面作用有助于提高催化活性。界面組分的增加使與結構有關的性質,例如離子價態和界面的電子運動傳遞發生了很大的變化。另外,MIL-101(Fe)/SiO2相較于MIL-101(Fe)在堿性條件下催化穩定性提高。此外,通過有機配體的官能化以及將COF與MOF有效結合,將為開發基于MOF的有效催化劑提供新的方向。
1.2 室溫催化機理
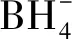
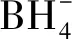
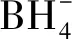
進一步地,本課題組[19]在研究了MIL-101(Fe)/SiO2催化還原對硝基苯酚協同產生氫氣的可能性后,完善此催化反應機理:添加MIL-101(Fe)催化劑后,NaBH4將吸附在不飽和金屬配位位點的表面上,并且供氫電子將解離。從BH4-吸附的氫原子與氫氧根離子結合形成H2O或與周圍的硼氫化物離子結合形成H2。然后,NaBH4與MIL-101(Fe)之間發生氧化反應,Fe表面上的電子通過共軛對硝基酚鹽離子轉移到硝基的反應中心。水的氫源用于將p-NP氫化物還原為p-AP。最后,—NO2從水中獲得質子,并通過一些中間體轉化為對氨基苯酚離子,見圖1。
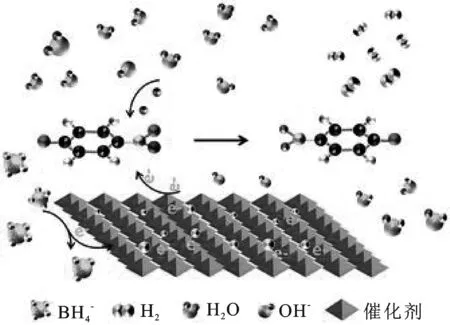
圖1 MIL-101(Fe)/SiO2催化還原硝基芳烴化合物協同產氫反應機理圖Fig.1 Schematic illustration of the proposed mechanism of simultaneous catalytic reduction of p-nitrophenol and hydrogen production on MIL-101(Fe)/SiO2
2 光催化
在NaBH4作用下將對硝基苯酚還原為對氨基苯酚是公認的模型反應,用于評估催化劑的催化活性,但對是否可以實現不添加NaBH4,以光驅動硝基芳烴轉化知之甚少。光催化是一種有望去除廢水中有機污染物的替代技術。光催化是在催化劑參與下的光化學反應。在光催化過程中,穩定高效的光催化劑是提高光催化效率的關鍵因素。在過去的幾十年中,已經開發出各種各樣的用于太陽能轉化的光催化劑,例如TiO2,Cu2O,C3N4等。
2.1 光催化劑
2.1.1 半導體 近年來,大量的研究工作致力于開發能夠以越來越有效的方式收集光子并誘導選擇性化學轉化的催化劑。其中,半導體代表了一種極有應用前景的材料,因為它們可以收集光子并啟動電荷分離過程。例如ZnO,CdS和Bi基納米等材料,可以吸收光輻射能激發出導帶電子(e-)和價帶空穴(h+),進一步與吸附在其表面上的物質發生化學反應[20]。相較于還原硝基芳烴,半導體材料光催化硝基芳烴大多表現為降解。
在各種氧化物半導體光催化劑中,二氧化鈦(TiO2)由于其生物和化學惰性,成本效益以及強大的氧化能力而備受關注。Vinu等[21]利合成了納米銳鈦型TiO2(CS TiO2)和商業二氧化鈦Degussa P-25,用于苯酚和對硝基苯酚的同時光催化降解以及銅(Cu2+)和鉻(Cr6+)等金屬離子的還原。他們發現金屬離子的存在降低了苯酚和對硝基苯酚的降解速率,而苯酚卻使Cu2+還原成Cu+的速度加快。同樣,苯酚或對硝基苯酚的存在也可以增強對Cr6+的吸附及其還原。Degussa P-25還原金屬離子的速度是CS TiO2還原速度的2倍。此外,Khan等[22]一種簡單的無毒表面活性劑的方法,合成了CdS納米片和納米棒。將這些納米粒子(NPs)用于光催化還原對硝基苯酚,發現納米棒比納米片活性更好,評估了所獲得的樣品的光催化活性。
2.1.2 半導體復合材料 小分子光催化劑和非均質材料,它們也可以組合以達到協同作用。半導體除了常與金屬原子及非金屬材料結合,還可以與其他類型半導體材料復合。可以吸收可見光的半導體,例如CdS, PbS, Bi2S3,CdSe和InP,常用作敏化劑,利用它們將電子轉移到TiO2或SnO2之類的大帶隙半導體中[23-24]。ZnO和TiO2半導體粉末的耦合或許有利于增強光反應性。Marcì等[25]通過不同方法制備了ZnO/TiO2多晶固體。用于對硝基苯酚光還原。ESR測量表明,鋅在負載的金紅石樣品中有助于穩定自由電荷載流子,這有利于光反應性的發生。兩個裸露ZnO樣品的光反應性主要取決于鋅的含量。Yang等[26]在模擬陽光下,發現Cu2O/TiO2p-n結可有效還原對硝基苯酚,該p-n結是通過對負載有Cu顆粒的TiO2納米管進行陽極氧化而制成的。與未改性的TiO2NTs(0.85 μg/min cm2)相比,Cu2O/TiO2具有更高的降解效率(1.97 μg/min cm2)。增強的光催化活性可以歸因于Cu2O納米線有利于可見光擴展吸收以及在Cu2O/TiO2p-n結界面處產生的光致電勢差驅動的光生載流子的有效分離。
2.1.3 聚合物材料 聚合物材料,即高分子材料,是由許多相同的、簡單的結構單元通過共價鍵重復連接而成的。按來源可分為天然高分子材料和合成高分子材料。其中,無定形微孔/多孔有機聚合物(POPs)是一類具有微孔的高度交聯的無定形聚合物,包括固有微孔性(PIM)的聚合物、多孔有機骨架(POF)和共軛微孔聚合物(CMP)等,已成為催化劑的通用平臺。POPs材料可分為三大類:POPs結合均相催化劑作為結構單元;POPs合成后進行改性;POPs封裝金屬顆粒。這些材料是無定形的,由于大量的微孔和中孔,它們通常具有相對較高的內部表面積[27]。Manna等[28]通過使用新開發的低成本催化聚合方法制備了3D聚咔唑基微孔有機聚合物(ACzMOP)。富氮ACzMOP與光氧化還原活性富電子的π共軛聚咔唑模塊集成在一起,材料具有大BET表面積(1 568 m2/g)以及孔體積(1.5 cm3/g)。該不含金屬的聚合物通過光催化途徑將有毒的對硝基苯酚有效還原為對氨基苯酚前體。在NaBH4存在下,硝基苯酚在70 min內完成了NP到AP的光還原(轉化率約99%)。
2.2 光催化機理
TiO2的銳鈦礦相和金紅石相的Ebg值分別為3.2 eV和3.0 eV。當光子的能量大于或等于TiO2表面的Ebg值時,就會發生分子激發結果,在光催化劑中產生電子-空穴對。Fatima等[29]認為TiO2在輻射下產生的主要反應物種包括空穴(h+),電子(e-) 和羥基自由基(H·)。羥基自由基在TiO2光催化硝基苯酚中起重要作用。硝基苯酚的降解遵循兩個步驟:羥基自由基的取代和TiO2破壞芳香環。光催化降解現象發生在溶液中靠近光催化劑和/或污染物分子表面的地方。第一步導致形成多羥基化的芳族化合物,而后一步導致形成有機酸和親水性化合物(例如,乙酸,甲酸,醛和酮)。Vinu等[21]發現苯酚與CS TiO2一起降解時,不會產生任何中間體,但會與Degussa P-25形成兩種中間體,即對苯二酚和鄰苯二酚。在存在Cu2+和Cr6+和CS TiO2的情況下也觀察到相同的中間體。當單獨降解以及在帶有CS TiO2的Cr6+存在下降解時,對硝基苯酚會轉化為對苯二酚和對硝基鄰苯二酚。伯羥基化的中間體經歷仲羥基化,然后開環形成直鏈脂肪族酸。在進一步暴露于紫外線下,這些礦物質最終礦化,產生CO2和水蒸氣。
對于半導體復合材料,Yang等[26]提出Cu2O(2.0 eV)的CB和VB高于TiO2(3.2 eV)的CB和VB。在輻射下,激發到Cu2O的CB的電子將轉移到TiO2,而TiO2中的VB產生的空穴與Cu2O中的空穴相反。在不同的半導體中分離h-e對可在p-n結界面處引起電勢差,從而阻礙h-e對重組并提高量子效率。對硝基苯酚首先與Cu2O(totalhVB+)生成的OH·之間發生反應。OH·在苯環上羥基的鄰位上發生親電攻擊,形成對硝基鄰苯二酚和氫自由基(H·)。H·與水反應并生成OH·后,通過光生電子將其還原為羥基離子。形成的亞硝基與光生電子結合,生成亞硝酸根離子,該亞硝酸根離子被溶解在溶液中的氧氣氧化成硝酸根離子。對硝基鄰苯二酚與氧自由基反應,生成苯醌。OH·優選通過遵循苯環上取代基的位置規則性來攻擊對硝基鄰苯二酚的鄰位對位,從而獲得1,2,4-三羥基苯。Yang等[30]合成了In2S3-GR納米復合材料,發現與裸露的In2S3納米顆粒和In2S3-GR-H相比,表現出更高的可見光光催化還原水中的硝基芳烴化合物的能力。他們認為In2S3-GR納米復合材料的光催化性能增強可以歸因于GR的引入以及In2S3與GR之間的緊密界面接觸,從而促進了界面電荷轉移速率和延長了光生載流子的壽命。同時,提出了一種可能的反應機理。在可見光照射下,電子在In2S3-GR納米復合材料的框架內從價帶(VB)激發到In2S3的導帶(CB),從而在VB中產生空穴。由于石墨烯/石墨烯的電勢約為-0.08 V(vs NHE),因此光生電子趨于轉移至GR,導致有效的電子空穴對分離并抑制了載流子的重組。同時,In2S3的VB中的空穴在N2氣氛中被甲酸銨(空穴捕獲劑)捕獲,抑制了硝基化合物基質上氧化過程的發生。
對于聚合物材料,Manna等[28]認為光、NaBH4、催化劑和惰性氣氛是成功進行反應的重要條件。在光照射下,電子給體NaBH4失去電子轉移到ACzMOP的光生空穴,然后激發態電子從ACzMOP的LUMO轉移到NP的LUMO中,從而形成一種活化的陰離子自由基類型的中間體,該中間體同時從NaBH4獲得氫源,從而轉化為AP。
此外,Khan等[22]測試合成的納米結構,在無惰性氣體保護下,以水為溶劑,以NaBH4為還原劑,也成功地光催化對硝基苯酚轉化為對氨基苯酚。他們認為硝基的胺化反應是通過與CdS的導帶電子作用來實現的。CdS價帶中的光生空穴被NaBH4分解產生的電子填充。可見,惰性氣氛的保護的影響有待探究。本小組在大量試驗后也發現惰性氣氛的保護并不是影響光催化反應的主要因素。在無惰性氣體保護下,反應依然可以順利進行。同時,使用適當的空穴捕獲劑可以對反應活性造成至關重要的影響,將更有利于通過光生電子還原硝基。
3 總結與展望
選擇合適載體進行催化劑負載,在原基礎上進行摻雜,都可以有效提高催化劑對催化還原硝基芳烴反應的催化效率及催化穩定性。催化還原硝基芳烴反應是一個常用于催化劑性能探究的反應體系,其中室溫熱催化常用NaBH4作為氫源及給電子體,光催化常添加空穴捕獲劑和使用惰性氣體,該反應催化劑的制備是熱點。盡管近年來已經取得了許多實驗和理論進展,特別是在催化劑的優化或催化方式的改進方面,但對于室溫熱催化及光催化還原硝基芳烴過程的理解及反應的應用還不夠深入。或許室溫熱催化及光催化還原硝基芳烴為氨基芳烴的反應過程已經明析,但是其反應過程中副產物的存在與否以及系列添加劑的影響是模糊的。例如,光催化中使用不同的空穴捕獲劑是否會針對各類催化劑產生不同的影響?是否需要進一步處理以分離水中催化劑?如果有不同的產物,可能會對應不同的反應路徑,是否可以加以調控?
今后還原硝基芳烴催化劑和催化機理的研究需要重點關注以下幾個方面:(1)進一步加強對反應副產物及其反應路徑可能性的研究;(2)不同添加輔助劑、硝基芳烴和催化劑之間的確切關系;(3)調控反應路徑,以增加目標產品的生成;(4)改進工藝,實現催化劑的綠色、循環、易回收以及規模化生產。這將有利于未來的工作從研究還原硝基芳烴過程的基本方面發展到其在各種領域的潛在影響,以擴展使用催化劑對硝基芳烴催化處理的實際應用的可選項。

