鐵活化過硫酸鹽降解水中污染物的研究進展*
黃 劍 ,王 良
(東北石油大學 化學化工學院,黑龍江 大慶 163318)
隨著科技的進步,環境污染問題也愈加嚴重,處理水中污染物成為了人們的研究熱點。傳統的高級氧化技術其機理主要依賴于羥基自由基(·OH),雖然對污染物表現出良好的去除性能,但仍存在能耗高和降解能力有限等問題。
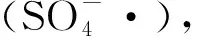
1 氧化體系狀態及作用機理
鐵作為一種環境友好、廉價、無毒的過渡金屬元素,已被廣泛應用于活化過硫酸鹽降解各種水中污染物。近些年來,鐵材料在活化過硫酸鹽方面的應用已經從均相擴展至非均相體系,從合成鐵氧化物擴展至天然鐵礦物質。對各種氧化體系的作用機理進行研究將有利于選擇合適的氧化體系,從而對污染物實現最大程度的降解。
1.1 均相體系
1.1.1 亞鐵離子
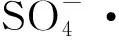
(1)
(2)
(3)

(4)
為了最大限度地減少自由基清除作用并提高均相活化過程的效率,一種常用的方法是對PS/PMS和Fe2+采用適當的物質的量比。正如Wang等[2]發現,1∶1的比率可能是Fe2+/PS和Fe2+/PMS體系的最佳物質的量比。另一個有效的方法是將Fe2+的投加方式從一次性投加改為逐漸投加,這樣可以減少副反應的發生。Ayoub等[3]發現,與一次性添加相比,反應過程中逐漸添加Fe2+雖然在前10 min對磺胺甲惡唑(SMX)的去除率較低,但是反應2 h后可使SMX的去除率提高一倍。
1.1.2 鐵離子
Fe2+的低穩定性限制了Fe2+/過硫酸鹽體系在高級氧化技術中的應用。據報道,Fe3+比Fe2+更穩定,因為Fe2+很容易被氧化成Fe3+。單獨的Fe3+不能像Fe2+一樣直接活化過硫酸鹽產生自由基,研究表明,PMS可以與Fe3+反應,生成的Fe2+可以活化過硫酸鹽,產生自由基降解污染物,見式(5)[4]。此外在某些有機物如醌類化合物存在或電場的條件下,Fe3+也可以還原為Fe2+。目前對Fe3+活化過硫酸鹽的研究較少,主要是在不加其他還原劑或電場的條件下,Fe3+很難被還原為Fe2+。
(5)
雖然利用氧化劑和有機化合物導致的Fe2+再生可以提高降解效率,但是整個過程相當緩慢。Fe3+在系統中的積累不僅會導致反應速率的下降,而且由于其溶解度較低還會形成沉淀。在這種情況下,可以通過引入螯合劑或還原劑提高PS/PMS的活化效率。目前為止,已經報道了用于該功能的各種材料,包括乙二胺四乙酸(EDTA),(S,S)-乙二胺-N,N-二琥珀酸三鈉鹽(EDDS),檸檬酸(CA)和草酸(OA)等[4]。Han等[5]報道,在CA、OA和EDDS中,CA具有中等螯合能力,可以通過其分子結構產生的空間位阻效應降低Fe2+的可及性,從而提高PS的活化效率,這使得其成為最合適的螯合劑。然而,降解效率提高的同時也可能會因為引入其他試劑而對系統產生一些不利影響。例如,腐殖酸(HA)可以與自由基反應,這可能會導致自由基與目標污染物發生競爭[6]。因此,應該謹慎選擇和添加螯合劑或還原劑。
1.2 非均相體系
1.2.1 零價鐵
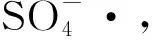

(6)
(7)
(8)
(9)

(10)

(11)

(12)
在Fe0/過硫酸鹽體系中,通過Fe0表面溶解生成Fe2+的速度取決于Fe0的粒徑大小。研究表明,合適的粒徑可以促進Fe0表面Fe2+的釋放。通常,粒徑越小,比表面積越大,反應性越高。反應過程中產生的腐蝕產物可能對過硫酸鹽的活化產生一定的抑制作用,這可能是因為表面形成的鐵(羥基)氧化物無法有效活化過硫酸鹽,并阻礙Fe0晶核與溶液的直接接觸。Kim等[8]報道在Fe0活化PS的過程中,由于受到Fe3+和在Fe0外殼上形成的鐵(羥基)氧化物的影響,Fe0的消耗速度減慢,PS的活化效率也大大降低。然而,也發現了腐蝕產物的一些促進作用。Cao等[9]觀察到,在Fe0/PMS體系中,沉積在Fe0表面的腐蝕產物會激活PMS或直接吸附污染物。
1.2.2 含鐵礦物
自然界中存在的鐵礦物較多,主要存在于地球表面。這些礦物價格低廉且易獲得,因而也被用作過硫酸鹽的活化劑。在活化過硫酸鹽的研究中,針鐵礦[FeO(OH)]、赤鐵礦(Fe2O3)、磁鐵礦(Fe3O4)和黃鐵礦(FeS2)等是主要的研究形式[4]。當電子從鐵礦物轉移到過硫酸鹽時,需要通過一個較寬的禁帶,導致其難以高效地活化過硫酸鹽。然而,鐵礦物對電子的傳遞效率較低,對Fe2+的淬滅效應可以產生一定的抑制作用,使其成為活化過硫酸鹽去除污染物的極佳候選物。
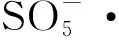
2 鐵活化過硫酸鹽降解水中污染物的影響因素
作為一種新型的高級氧化技術,鐵活化過硫酸鹽體系在降解水中污染物領域展現出了獨特的優勢和應用前景,但是,各種因素包括過硫酸鹽的濃度、溶液pH值、反應溫度和陰離子等,都會對體系中過硫酸鹽的活化和污染物的降解產生影響。深入了解各種因素對反應過程的影響將有利于開發出更加高效的高級氧化體系用來降解各種水中污染物。
2.1 過硫酸鹽的濃度
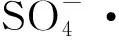
2.2 溶液pH值
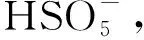
2.3 反應溫度
反應溫度會在很大程度上影響反應過程的進行,溫度升高可以促進溶液中的分子熱運動,加速過硫酸鹽自身的熱活化,同時也會使催化劑活化過硫酸鹽的速度加快,從而提高反應速率。Yao等[17]發現在Fe0/PMS體系中,高溫極大地促進了雙酚M(BPM)的降解。在t=50 ℃,經反應90 min后,BPM被完全去除,t=25 ℃時只有56.0%的BPM被去除。一般情況下,隨著溫度的升高,有機污染物的降解速率相應提高,但并不是所有的體系都是相同的情況。Gao等[9]研究發現,溫度的升高會導致自由基之間的淬滅作用,從而影響四環素(TC)的降解速率。t=30~60 ℃時,TC的最終去除率由88.5%降低到75.9%。因此,對于不同的反應體系,要根據催化劑類型、氧化劑穩定性和處理成本選擇適宜的反應溫度。
2.4 陰離子
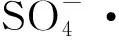

(13)
(14)

(15)

(16)
(17)
(18)

(19)
(20)
(21)
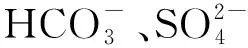
(22)
(23)
(24)
(25)
(26)
(27)
3 結束語
過硫酸鹽由于氧化還原電位高、成本低、環境友好等優點被認為是降解有機污染物的高級氧化劑,特別是被各種過渡金屬活化生成高活性自由基時。鐵是第四豐富的無毒金屬,能有效地以均相和非均相的方式活化過硫酸鹽。但作為一種新型的高級氧化技術,結合目前的研究現狀,鐵活化過硫酸鹽氧化技術仍有許多問題尚未解決,在今后的工作中,以下4個方面值得進一步研究。
(1)反應體系中,鐵泥的產生是不可避免的,處理不當可能會造成環境的二次污染,將初始鐵物種的損失最小化,充分利用鐵泥的剩余反應性成為研究重點。此外,Fe2+容易被氧化成Fe3+,避免氧化過程的發生,提高過硫酸鹽的利用率也是重中之重;
(2)不同的鐵材料對過硫酸鹽表現出了不同的活化效率,具有復雜分子結構的新型有機污染物不斷出現,根據污染物的性質及各種實際情況選擇合適的鐵活化過硫酸鹽體系,成為鐵活化過硫酸鹽氧化技術在應用中的關鍵問題;
(3)目前為止,大多數研究都只是停留在實驗室階段,對于實際廢水的處理需要進行更多的研究,并開發相關配套的技術手段,推進鐵活化過硫酸鹽氧化技術的實際應用;
(4)目前對各種鐵材料的安全性評價和生態毒理學效應的研究還不夠。在污染物降解方面,有必要加強對目標污染物降解后副產物的水環境毒性研究。

