基于UHPLC-Q-Exactive-MS/MS的酸棗仁總皂苷對失眠大鼠血清代謝物的影響
張文明,唐靜月,費倩倩,卞振華,,袁曉航,陳曉偉,胡敏敏,陸兔林
1.無錫市中醫醫院,江蘇 無錫 214000;2.南京中醫藥大學藥學院,江蘇 南京 210023
失眠是最常見的睡眠障礙性疾病,其主要表現是睡眠質量下降或睡眠時間紊亂。失眠發病原因和機制復雜,心理、生理、環境、藥物及多種疾病均可導致失眠。研究表明,失眠不僅與精神障礙(如抑郁、焦慮)有關,亦會導致內分泌失調(如肥胖、糖尿病)和心血管疾病(如高血壓、心臟病)。中醫藥因不良反應少、不易產生耐藥性及復發率低等特點,治療失眠具有一定優勢。酸棗仁來源于鼠李科植物酸棗Mill.var.(Bunge)Hu ex H.F.Chou的干燥成熟種子,具有養心補肝、寧心安神、斂汗生津作用。酸棗仁屬于原國家衛生部頒布的首批藥食同源兩用品,截至2016年,共有超過260個改善睡眠的保健產品以酸棗仁及其提取物為原料。酸棗仁總皂苷(Ziziphi Spinosae Semen saponins)是酸棗仁發揮藥理作用的主要活性物質,具有鎮靜催眠、抗抑郁、改善記憶等作用。目前對酸棗仁總皂苷的研究主要集中在提取純化、成分鑒別和藥效學等方面,缺乏關于其進入體內后內源性小分子化合物代謝的研究報道。
代謝組學是一種高靈敏度、高通量的研究體內小分子物質代謝特征變化的方法,可以全面展示代謝物和信號通路的變化及其相互作用。代謝組學的研究模式與中醫藥整體觀相契合,能更加可靠、靈敏地反映疾病或藥物作用引起的機體生物功能變化。因此,本研究以對氯苯丙氨酸(PCPA)腹腔注射建立失眠大鼠模型,并進行藥效學評價,探討酸棗仁總皂苷改善失眠的作用,結合代謝組學分析酸棗仁總皂苷干預后大鼠血清代謝物的變化,尋找主要相關靶點和通路,以期為酸棗仁總皂苷藥物開發和臨床應用奠定基礎。
1 實驗材料
1.1 動物
SPF級雄性SD大鼠30只,體質量180~220 g,購于北京斯貝福生物技術有限公司,動物許可證號SCXK(京)2019-0010。飼養于江蘇省血吸蟲病防治研究所,溫度(25±2)℃、相對濕度(55±5)%環境,自然晝夜節律光照,適應性飼養7 d后開始實驗。本實驗經無錫市中醫醫院實驗動物倫理委員會審批(SKJJ2020011707)。
1.2 藥物及制備
酸棗仁飲片(批號19121601,江蘇亞邦中藥飲片有限公司),經南京中醫藥大學中藥炮制重點實驗室陸兔林教授鑒定為鼠李科植物酸棗Mill.var.(Bunge)Hu ex H.F.Chou 的干燥成熟種子,符合2020年版《中華人民共和國藥典》相關規定。將飲片粉碎,稱取適量粉末,加入石油醚(60~90 ℃)索氏提取,制備酸棗仁脫脂粉末。稱取適量脫脂粉末,加入8倍量70%乙醇,95 ℃水浴回流3次,每次1.5 h,抽濾,合并濾液,濃縮得浸膏。采用D101型大孔吸附樹脂對浸膏進行洗脫,上樣液濃度0.05 g/mL,上樣速度2 mL/min,上樣量40 mL,上樣結束靜置1 h。以蒸餾水(2 BV/h,3 BV)、30%乙醇(2 BV/h,4 BV)、70%乙醇(2 BV/h,4 BV)分別進行洗脫,收集70%乙醇洗脫液,濃縮干燥即得酸棗仁總皂苷粉末。精密稱取酸棗仁總皂苷粉末5 mg置5 mL容量瓶中,加甲醇定容至刻度,作為供試品溶液。取酸棗仁皂苷A對照品(批號P13J9S65562,純度≥98%,上海源葉生物科技有限公司)適量,加甲醇溶解,制成1 mg/mL溶液,作為對照品溶液。取供試品溶液80 μL置于15 mL試管中,水浴蒸干,加10%香草醛溶液0.5 mL、60%硫酸溶液5 mL,混勻,60 ℃水浴加熱15 min,立即用冰水冷卻3 min。隨行試劑作為空白,分光光度法于波長543 nm處測定吸光度。分別取對照品溶液適量,制成不同濃度的系列對照品溶液,同法測定吸光度,繪制標準曲線,得回歸方程=3.956 2+0.000 5,R=0.999 5。計算酸棗仁總皂苷平均含量為50.96%,使用時蒸餾水配制成濃度為10.4 mg/mL溶液。
1.3 主要試劑與儀器
PCPA,批號20200914,國藥集團化學試劑有限公司;戊巴比妥鈉,批號030415,廣東臺城制藥有限公司;甲酸銨,色譜純,美國Sigma Aldrich公司;甲醇、乙腈、醋酸、甲酸,色譜純,美國Thermo Fisher公司;其他試劑均為分析純。Milli-Q 超純水儀,美國Millipore公司;Vanquish型液相色譜儀,美國Thermo Fischer 公司;Q-Exactive 型質譜儀,美國Thermo Fischer公司;H1850-R型冷凍離心機,湖南湘儀有限公司;QL-866 型混勻儀,美國Vortex Mixer 公司;5305型真空濃縮儀,德國Eppendorf公司;Eclipse CI型光學顯微鏡,日本尼康公司。
2 實驗方法
2.1 分組、造模及給藥
30只大鼠隨機分為對照組、模型組和酸棗仁總皂苷組(ZSSS組),每組10只。模型組和ZSSS組連續3 d腹腔注射PCPA溶液350 mg/kg建立失眠大鼠模型,注射體積10 mL/kg,對照組腹腔注射等量生理鹽水。以大鼠出現晝夜節律消失,即白天和夜晚煩躁不安、不斷活動,提示模型制備成功。第4日開始,ZSSS組予酸棗仁總皂苷溶液124.8 mg/kg灌胃,體積12 mL/kg,對照組和模型組灌胃等量生理鹽水,每日1次,連續7 d。
2.2 一般狀態觀察
每日早晚固定時間對3組大鼠的行為、精神狀況及毛發等一般狀態進行觀察并記錄。
2.3 戊巴比妥鈉睡眠實驗
末次給藥30 min后,參考文獻[14]方法,每組取4只大鼠腹腔注射戊巴比妥鈉溶液(35 mg/kg),記錄大鼠睡眠潛伏期(給藥到翻正反射消失的時間)和睡眠時間(翻正反射消失到翻正反射恢復的時間)。
2.4 取材
給藥結束后,各組剩余大鼠腹腔注射戊巴比妥鈉(45 mg/kg)麻醉,腹主動脈取血,室溫靜置30 min,3 500 r/min離心15 min,分離血清,置于-80 ℃冰箱保存。迅速分離大鼠下丘腦組織,置于4%多聚甲醛中固定24 h以上。
2.5 HE染色
將下丘腦組織從4%多聚甲醛中取出,常規脫水,石蠟包埋,切片(厚度4 μm),切片脫蠟至水,行HE染色,脫水封片,置于顯微鏡下觀察。
2.6 代謝組學分析
2.6.1 樣品制備
取出大鼠血清,室溫解凍。精密吸取100μL血清于2 mL離心管中,加入400μL甲醇,振蕩60 s充分混勻,4 ℃、12 000 r/min離心10 min,分離上清液,真空濃縮干燥。加入150 μL 80%甲醇溶液(含4 ppm PCPA)復溶,0.22μm濾膜過濾,即為待測樣品。
2.6.2 儀器條件
色譜柱:Waters ACQUITY UPLCHSS T3色譜柱(2.1 mm×150 mm,1.8 μm);正離子模式流動相:0.1%甲酸水(A)-0.1%甲酸乙腈(B),梯度洗脫(0~1 min,2%B;1~9 min,2%~50%B;9~12 min,50%~98%B;12~13.5 min,98%B;13.5~14 min,98%~2%B;14~20 min,2%B);負離子模式流動相:5mmol/L甲酸銨水(C)-乙腈(D),梯度洗脫(0~1min,2%D;1~9 min,2%~50%D;9~12 min,50%~98%D;12~13.5 min,98%D;13.5~14 min,98%~2%D;14~17 min,2%D);流速:0.25 mL/min;柱溫:40 ℃,進樣量:2 μL;離子源:電噴霧離子源(ESI),正、負離子模式;噴霧電壓:3.5 kV(正離子模式)、2.5 kV(負離子模式);碰撞電壓:30 eV;鞘氣:30 arb;輔助氣:10 arb;毛細管溫度:325 ℃。以70 000分辨率進行全掃描,采集范圍81~1 000(m/z),高能誘導裂解(HCD)進行二級裂解。
2.6.3 數據分析
采用Proteowizard3.0.8789軟件將采集的原始數據導出,利用R語言的XCMS程序進行峰識別、峰過濾、峰對齊等處理,得到代謝組學數據,導入SIMCAP14.1軟件進行主成分分析(PCA)和正交偏最小二乘判別分析(OPLS-DA),篩選變量重要性投影(VIP)>1且<0.05的代謝物作為潛在差異代謝物。根據精確分子量(分子量誤差≤30 ppm),結合MS/MS碎片信息對HMDB(http://www.hmdb.ca)、Metlin(http://metlin.scripps.edu)、Massbank(http://www.massbank.jp)、LipidMaps(http://www.lipidmaps.org)和mzClound(https://www.mzcloud.org)數據庫及自建數據庫進行確認注釋以獲得代謝物。采用Metabo Analyst 5.0(http://www.metaboanalyst.ca/)數據庫進行代謝通路分析,使用Cytoscape3.8.2軟件繪制代謝網絡并進行靶點篩選。
3 統計學方法

4 結果
4.1 酸棗仁總皂苷對模型大鼠一般狀態的影響
與對照組比較,模型組大鼠第2~5日行為興奮,皮毛蓬松且少有光澤,晝夜節律紊亂,第6日開始出現疲勞、精神不振和活動減少現象;與模型組比較,ZSSS組大鼠第2~5日晝夜節律紊亂,興奮性有所降低,第6日開始攻擊行為減少或消失,晝夜節律有所恢復,白天多倦臥,皮毛逐漸恢復光澤。
4.2 酸棗仁總皂苷對模型大鼠睡眠的影響
與對照組比較,模型組大鼠睡眠潛伏期顯著延長(<0.05),睡眠時間顯著縮短(<0.05);與模型組比較,ZSSS組大鼠睡眠潛伏期顯著縮短(<0.05),睡眠時間顯著延長(<0.05)。結果見表1。

表1 各組大鼠睡眠潛伏期和睡眠時間比較(,min)
4.3 酸棗仁總皂苷對模型大鼠下丘腦組織病理形態的影響
對照組大鼠下丘腦組織神經細胞豐富,結構完整,分布均勻;模型組大鼠下丘腦組織神經細胞邊界模糊,排列松散,有大量碎片細胞;ZSSS組大鼠下丘腦組織神經細胞較豐富,分布較均勻,細胞形態明顯恢復。見圖1。
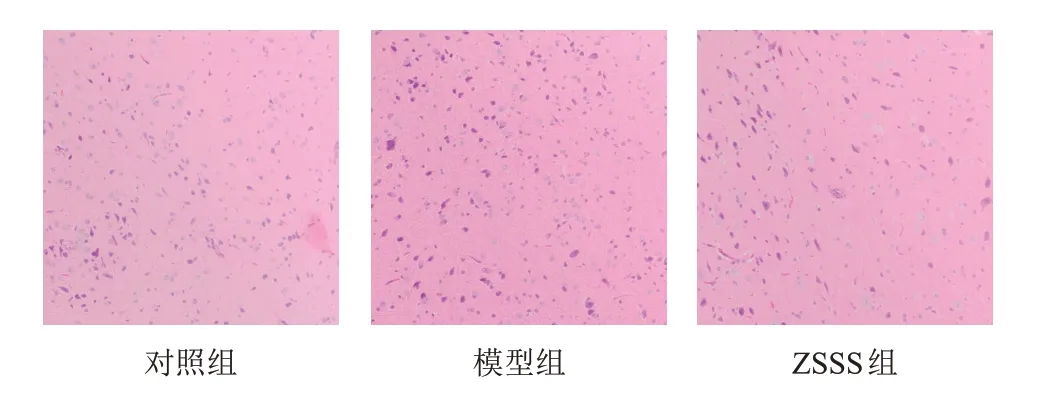
圖1 各組大鼠下丘腦組織形態(HE染色,×100)
4.4 酸棗仁總皂苷對模型大鼠血清代謝組學的影響
4.4.1 質譜檢測結果
將血清樣品處理后進行正負離子模式全掃描,樣品總離子流圖見圖2。
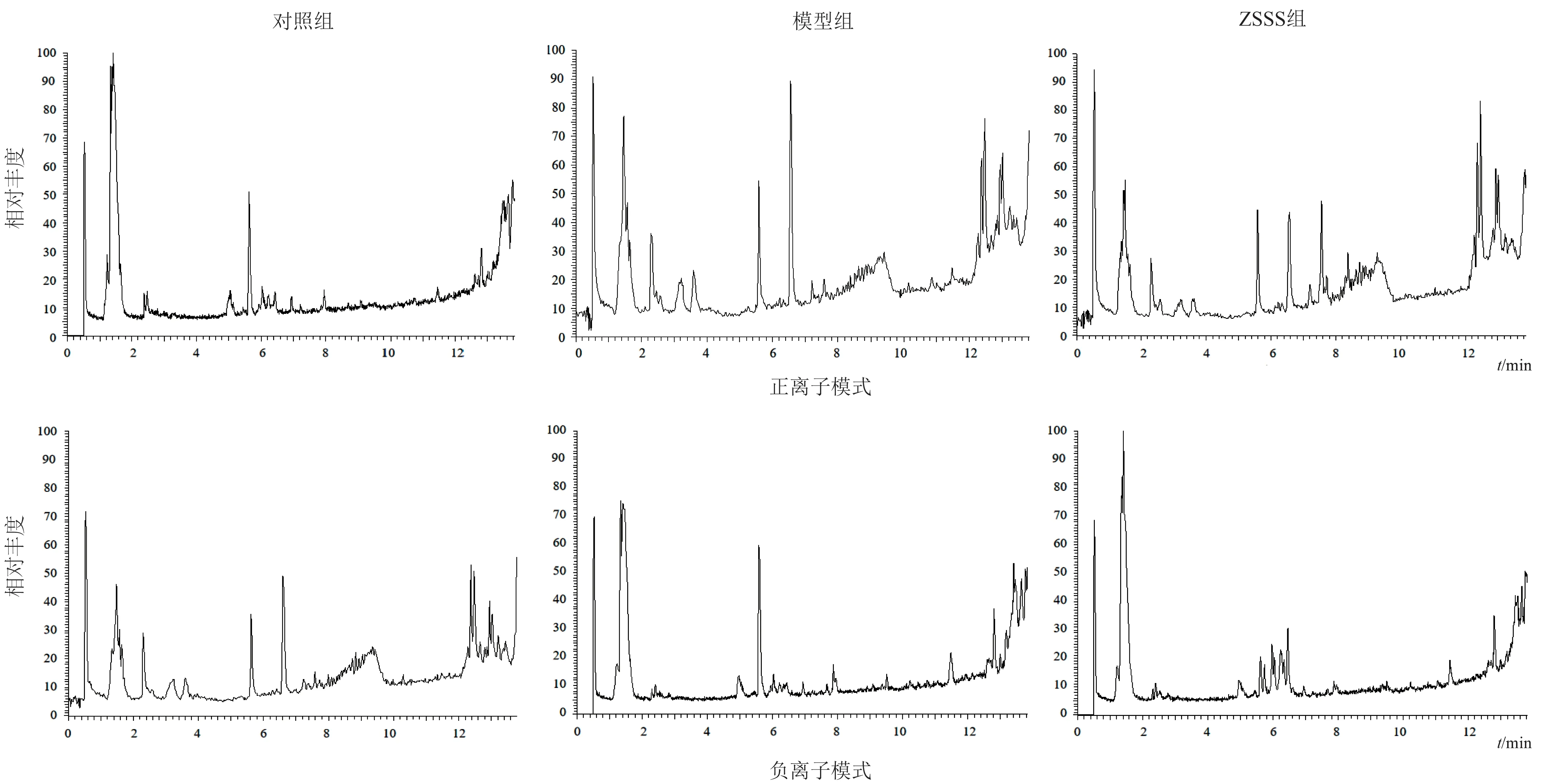
圖2 各組大鼠血清樣品總離子流圖
4.4.2 數據模式識別
無監督的PCA可以反映數據的原始狀態,有監督的OPLS-DA可直觀顯示各樣品的聚類及變化軌跡。由圖3、圖4可知,各組樣品有聚集成群的趨勢,表明各組大鼠血清代謝物產生了一定變化。為進一步篩選大鼠血清潛在差異代謝物,建立組間OPLS-DA模型。結果顯示,模型組和對照組、、分別為0.678、0.999、0.640,模型組和ZSSS組、、分別為0.687、0.998、0.631。表示模型預測效果,>0.5表示模型預測效果較好。由此可知建立的模型可靠,具有良好的預測能力。為避免過度擬合,進行模型驗證分析(=200),模型組和對照組、截距分別為0.986、-0.108,模型組和ZSSS 組、截距分別為0.987、-0.040 4,表示模型與數據的擬合程度,越接近1表明模型擬合越好,截距<0,表明本研究建立的模型有效,可用于PCPA致失眠大鼠血清差異代謝物的篩選。見圖5。
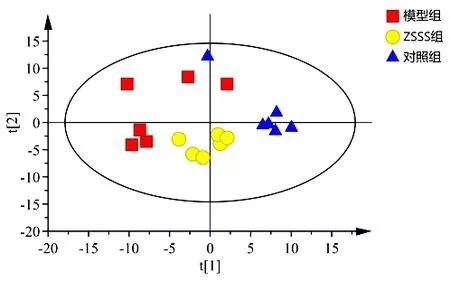
圖3 大鼠血清代謝組學數據PCA得分
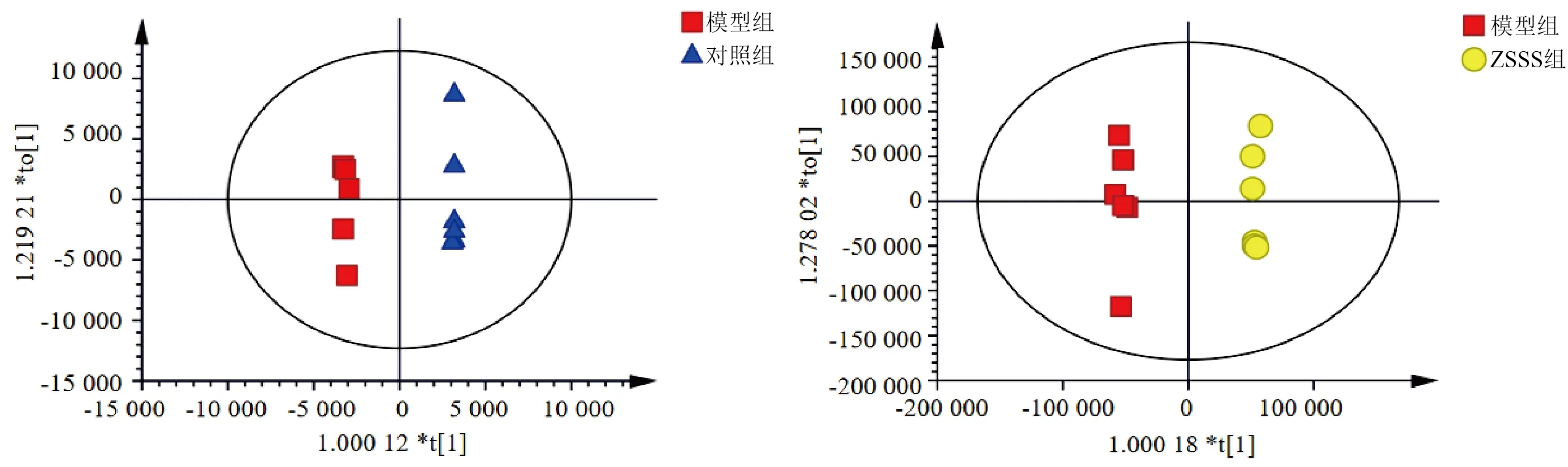
圖4 大鼠血清代謝組學數據OPLS-DA得分
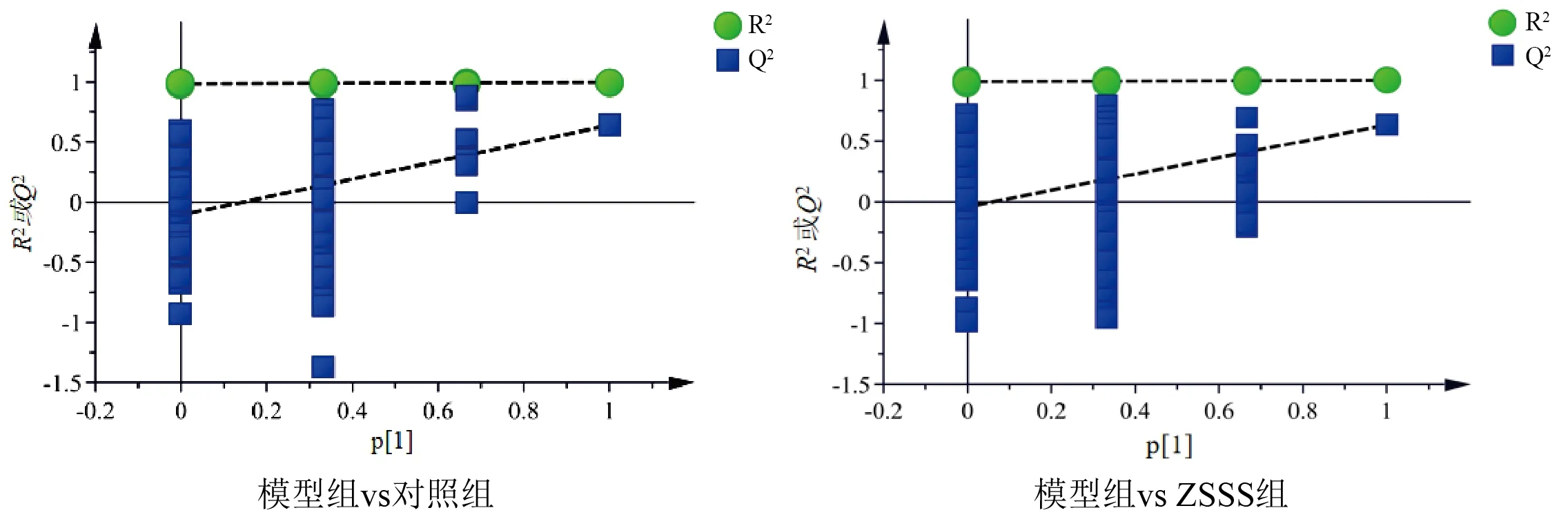
圖5 大鼠血清代謝組學數據OPLS-DA模型驗證
4.4.3 差異代謝物篩選
在OPLS-DA 基礎上,以VIP>1 且<0.05 為標準,選擇模型組和對照組大鼠血清差異代謝物,進而分析這些差異代謝物在對照組、模型組和ZSSS組的變化,在ZSSS組呈現明顯向對照組回調的成分即為潛在差異代謝物,最終篩選出8個潛在差異代謝物,見表2。為更直觀顯示各差異代謝物的變化,對其進行分層聚類分析,得到熱圖,見圖6。
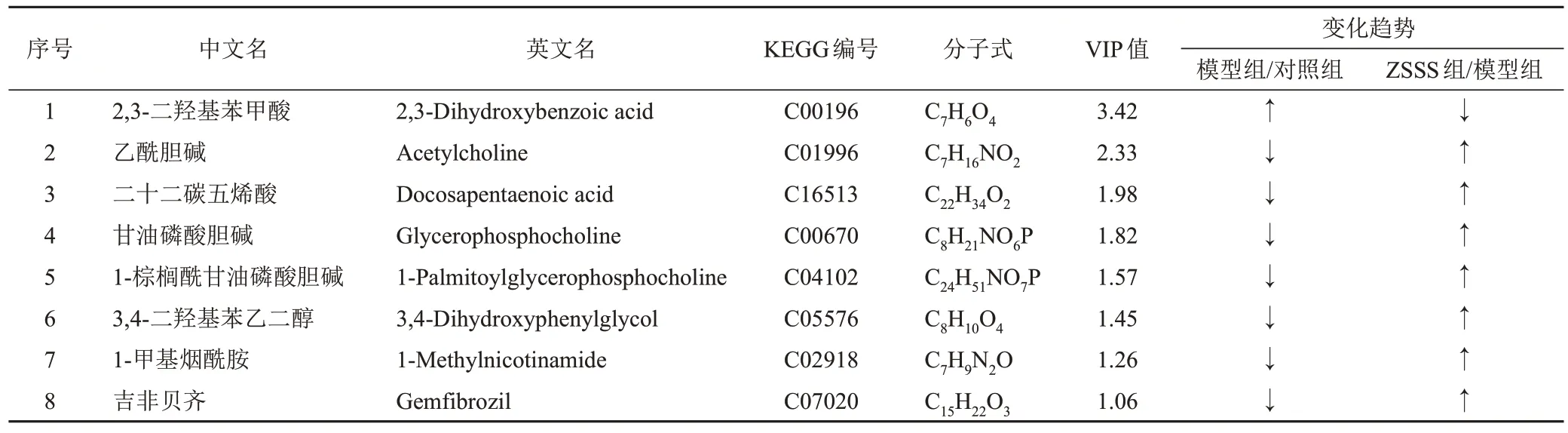
表2 大鼠血清潛在差異代謝物信息
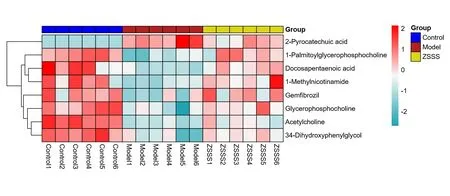
圖6 大鼠血清潛在差異代謝物熱圖
4.5 代謝通路分析
將篩選的差異代謝物輸入Metabo Analyst 5.0數據庫進行高通量代謝通路分析,得到3條相關代謝通路,分別為煙酸和煙酰胺代謝(涉及代謝物為1-甲基煙酰胺,其值、影響力值分別為0.075 011、0.138 16)、甘油磷脂代謝(涉及代謝物為乙酰膽堿和甘油磷酸膽堿,其值、影響力值分別為0.013 454、0.048 14)、酪氨酸代謝(涉及代謝物為3,4-二羥基苯乙二醇,其值、影響力值分別為0.197 700、0.012 70)。
4.6 代謝組學網絡構建
通過KEGG數據庫(https://www.kegg.jp)收集差異代謝物對應的酶和靶點基因,與代謝通路一起導入Cytoscape 3.8.2軟件,構建差異代謝物-代謝通路-酶-靶點基因相互作用網絡(見圖7)。使用Analyze Network插件對代謝網絡進行拓撲分析,獲得網絡中各節點的度值,度值越大,表明其對整個網絡的影響越大。度值大于均值(2.952)的潛在差異代謝物有5個,分別是2,3-二羥基苯甲酸、甘油磷酸膽堿、乙酰膽堿、1-甲基煙酰胺和3,4-二羥基苯乙二醇,涉及的代謝通路有甘油磷脂代謝、煙酸和煙酰胺代謝、酪氨酸代謝。度值大于均值的靶點基因有9個,利用度中心性、接近中心性和中介中心性衡量9個靶點基因在網絡中的重要性(見表3),這些靶點可能是酸棗仁總皂苷治療失眠的關鍵靶點。
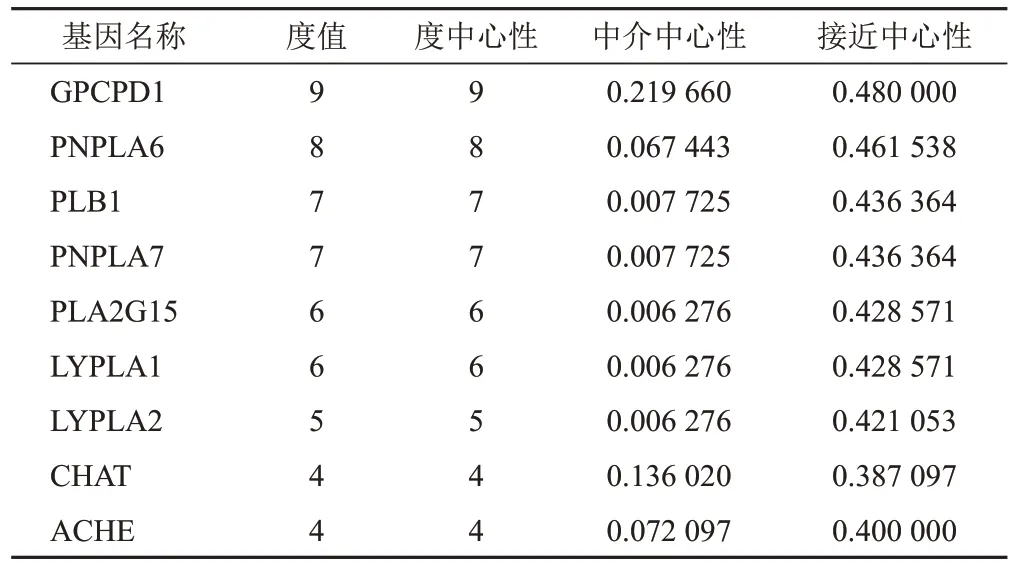
表3 酸棗仁總皂苷治療失眠的潛在靶點基因
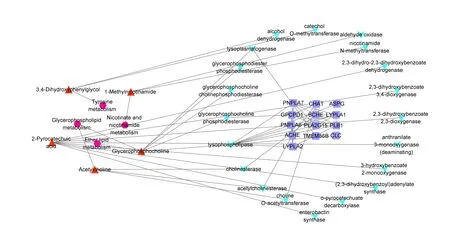
圖7 酸棗仁總皂苷治療失眠大鼠差異代謝物-代謝通路-酶-靶點基因相互作用網絡
5 討論
本實驗結果表明,酸棗仁總皂苷可明顯縮短模型大鼠睡眠潛伏期,延長睡眠時間,改善下丘腦組織病理損傷。為進一步了解酸棗仁總皂苷改善大鼠失眠的作用機制,本研究采用代謝組學技術結合模式識別分析對模型大鼠血清代謝物進行分析,結果得到8個潛在差異代謝物。對差異代謝物進行通路分析和代謝網絡分析,得到3條與失眠相關的代謝通路,包括煙酸和煙酰胺代謝、甘油磷脂代謝和酪氨酸代謝。煙酸和煙酰胺代謝、酪氨酸代謝通路>0.05,但其影響力值較大,研究表明失眠的發生與這2條通路密切相關。
1-甲基煙酰胺具有抗炎和抗糖尿病性腦血管疾病作用,可調節大鼠腦突觸體神經遞質釋放。煙酰胺N-甲基轉移酶(NNMT)催化S-腺苷甲硫氨酸的甲基轉移到煙酰胺上,可以認為1-甲基煙酰胺是煙酰胺的主要代謝物。煙酸和煙酰胺是人體輔酶Ⅰ(NAD)和輔酶Ⅱ(NADP)的組成部分,與糖脂代謝、能量代謝、氧化應激和炎癥調控等密切相關。研究表明,長期睡眠剝奪使SIRT3 表達顯著降低,煙酰胺作為NAD的前體,可以激活NAD-Sirtuins軸,進而上調SIRT1、SIRT2和SIRT3等基因表達。本研究中,與對照組比較,模型組大鼠血清1-甲基煙酰胺水平顯著降低;與模型組比較,ZSSS組大鼠血清1-甲基煙酰胺水平顯著升高,推測煙酸和煙酰胺代謝途徑與失眠發生關系密切,ZSSS可能通過影響1-甲基煙酰胺水平調控煙酸和煙酰胺代謝,從而發揮抗失眠作用。
磷脂酰膽堿與維持細胞膜結構完整性和信號傳導功能密切相關。研究表明,甘油磷酸膽堿通過肯尼迪途徑刺激磷脂酰膽堿合成,參與維持細胞膜結構的完整性。甘油磷酸膽堿也是神經遞質乙酰膽堿的前體,可改善認知功能和學習能力,有研究表明,甘油磷酸膽堿可刺激乙酰膽堿和磷脂酰膽堿的生物合成并激活突觸后膽堿能受體,從而增強中樞神經系統的中樞膽堿能功能。本研究顯示,模型組大鼠血清甘油磷酸膽堿和乙酰膽堿水平下降,提示大鼠中樞膽堿能功能出現紊亂,酸棗仁總皂苷能上調甘油磷酸膽堿和乙酰膽堿水平,通過調節中樞膽堿能功能紊亂改善失眠。
失眠的發生機制復雜,其中神經遞質紊亂被認為與失眠有關。3,4-二羥基苯乙二醇由去甲腎上腺素能神經末梢MAO-A同工酶催化氧化、脫氨基形成,是去甲腎上腺素能神經元內代謝的主要產物。研究發現,PCPA致失眠大鼠血清去甲腎上腺素水平顯著升高,去甲腎上腺素是由多巴胺催化產生,對神經活動、大腦皮層的醒覺和睡眠節律等有重要作用。去甲腎上腺素轉運蛋白的作用是將神經元釋放的去甲腎上腺素攝取回突觸前膜。由于3,4-二羥基苯乙二醇來源于去甲腎上腺素能神經元內代謝,因此去甲腎上腺素轉運蛋白抑制的結果表現為3,4-二羥基苯乙二醇減少。本研究中模型組大鼠血清3,4-二羥基苯乙二醇水平較對照組顯著降低,推測是由于去甲腎上腺素轉運蛋白受到抑制,而酸棗仁總皂苷能上調3,4-二羥基苯乙二醇水平。
綜上所述,酸棗仁總皂苷能提高失眠大鼠睡眠質量,改善下丘腦病理變化。本研究通過代謝組學技術篩選出與失眠相關的1-甲基煙酰胺、甘油磷酸膽堿、乙酰膽堿和3,4-二羥基苯乙二醇等生物標志物,涉及的代謝通路有煙酸和煙酰胺代謝、甘油磷脂代謝和酪氨酸代謝,GPCPD1、PNPLA6和PLB1等可能是酸棗仁總皂苷調節失眠的關鍵靶點,其具體作用機制還需實驗驗證。本研究進一步明確了酸棗仁總皂苷改善失眠的作用機制,可為其藥物研發提供依據。

