蛇足石杉主要活性成分及其生物合成研究進展
李籽杉,安周捷,王 婧,田 亞,徐志超,段寶忠*
·綜 述·
蛇足石杉主要活性成分及其生物合成研究進展
李籽杉1, 2,安周捷2,王 婧1,田 亞2,徐志超1, 2,段寶忠1*
1. 大理大學藥學院,云南 大理 671000 2. 東北林業(yè)大學生命科學院,黑龍江 哈爾濱 150000
蛇足石杉為我國珍稀瀕危藥用植物,可供利用的資源極其有限,其所含石杉堿甲對治療阿爾茨海默病、改善學習記憶等具有顯著的療效。對蛇足石杉的主要活性成分進行系統(tǒng)綜述,基于現(xiàn)有研究推導了其活性成分可能的生物合成途徑,為其資源開發(fā)利用和活性成分的生物合成提供科學參考。
蛇足石杉;石松生物堿;石杉型三萜;石杉堿甲;生物合成;轉(zhuǎn)錄組學
蛇足石杉(Thunb. ex Murray) Trevis.為石杉科石杉屬多年生蕨類植物,又名千層塔、蛇交子、鐵板草、矮羅漢等,為國家二級保護植物,主要分布于長江流域、云南、貴州、東北及兩廣地區(qū)。其藥用始載于《植物名實圖考》,以全草入藥,用于跌打損傷、內(nèi)傷出血、瘀血腫痛、燒傷燙傷、毒蟲叮咬、肌肉痙攣等[1],是生產(chǎn)石杉堿甲片、石杉堿甲注射液和石杉堿甲膠囊等藥物的重要原料。自然狀態(tài)下,蛇足石杉為一種小型蕨類植物,植株矮小,生長緩慢,其孢子萌發(fā)所需時間長達15年[2-3],而長期掠奪式的采挖導致野生蛇足石杉銳減,可供利用的資源極其有限,無法滿足市場需求[4]。現(xiàn)代研究表明,其化學成分主要為生物堿和三萜類成分,這2類成分與其他植物相比具有獨特的結(jié)構特點,其中石杉堿甲是一種高效的乙酰膽堿酯酶(acetylcholinesterase,AChE)抑制劑,主要用于阿爾茨海默病、老年患者術后認知和重癥肌無力等疾病的治療,亦可用于改善學習記憶能力[5-6],已成為國際生物合成和有機合成研究的熱點化合物,但由于植物體內(nèi)石杉堿甲含量甚微,僅0.006%左右,隨著工業(yè)需求量不斷加大,由于石杉堿甲開環(huán)的吡啶酮環(huán)和六氫吡啶環(huán)結(jié)構的復雜性,其全合成路線開發(fā)工藝難度極大,合成成本遠高于植物提取[7];在迄今已合成的100多種石杉堿甲類似物中,其抑酶活性大多不如天然石杉堿甲[8],導致石杉堿甲市場銷售價格昂貴。隨著合成生物學及代謝工程技術的飛速發(fā)展,開展生物轉(zhuǎn)化或半化學合成為石杉堿甲生產(chǎn)提供了新的途徑,但蛇足石杉三萜類和生物堿類化合物生物合成及代謝調(diào)控研究起步較晚,其生物合成信息相對有限,其綜述文章多關注于化學成分、藥理作用和石杉堿甲的生物合成等方面[9-11],蛇足石杉的組學研究呈現(xiàn)快速發(fā)展趨勢,對其活性成分生物合成途徑解析及合成生物學應用具有巨大推動作用。本文對蛇足石杉的主要活性成分進行了系統(tǒng)綜述,基于現(xiàn)有研究推導了其活性成分可能的生物合成途徑,以期為蛇足石杉科學研究和實踐應用提供理論支撐。
1 活性成分
目前已從蛇足石杉中分離鑒定出包括生物堿類、三萜類、黃酮類等化學成分。其中生物堿和三萜類是其主要成分。目前已從蛇足石杉中分離到生物堿類137種、三萜類69種以及其他化合物13種。
1.1 石松生物堿類
目前,從蛇足石杉中分離鑒定的生物堿成分超過130個,主要以石松生物堿為主,多數(shù)為C16N或C16N2骨架組成的三環(huán)或四環(huán)結(jié)構,少數(shù)為C27N3或少于C16[11]。按結(jié)構類型,其所含生物堿可分為fawcettimine型、lycopodine型、lycodine型、miseelaneous型4種類型[10,12],其母核結(jié)構如圖1所示。該類化合物主要具有抗AChE、細胞毒、抗炎和免疫抑制等作用。有關蛇足石杉的生物堿影響因素,已有研究表明,野生蛇足石杉引種至同一生物環(huán)境后,石杉堿甲的含量基本保持不變,提示含量高低是遺傳因素與環(huán)境條件共同作用的結(jié)果,但更受遺傳因素控制[13-14];此外,研究顯示不同生長階段的石杉堿甲的含量差異顯著,表現(xiàn)為幼苗>幼株>成株,且與年降雨量呈負相關[15],葉片中石杉堿甲和石杉堿乙的含量普遍高于根和莖[16]。

圖1 4種類型石松生物堿的母核
1.1.1 fawcettimine型生物堿 該類生物堿是蛇足石杉中最豐富的一類,目前已從蛇足石杉中分離到60個fawcettimine型化合物(1~60),約占蛇足石杉已分離到生物堿總數(shù)的50%以上。該類型生物堿結(jié)構變化多樣,通常具有7/5/6/6四環(huán)結(jié)構,根據(jù)C13位所連官能團可分為醇胺式和酮胺式[17],包括fawcettimine和huperserine A~D等,相關化合物信息見表1。該類化合物抗AChE活性較低,huperserine A~D對AChE無抑制作用[18]。
1.1.2 lycopodine型生物堿 該類型生物堿在蛇足石杉中的數(shù)量僅次于fawcettimine型,其母核一般為6/6/6/6四環(huán)結(jié)構,其排列方式與fawcettimine型生物堿相似,根據(jù)C12位氧化態(tài)的不同可分為lycopodine型和lycodoline型[17],包括6α,11α-dihydroxy-lycopodine、lycoposerramine K、huperzine O等化合物[50],目前該類生物堿的活性研究報道較少,相關化合物信息見表2。
1.1.3 lycodine型生物堿 該類型生物堿生物堿母核一般為含吡啶的6/6/6/6四環(huán)結(jié)構,偶有C9-C10斷裂的三環(huán)結(jié)構,其分子式大多為C16N2或C15N2[61]。lycodine型生物堿大多都具有抗AChE活性[62],如最具AChE抑制活性的huperzine A,以及活性較強的huperzine B、huperserine E和6β-羥基石杉堿甲均屬lycodine型石松生物堿。目前從蛇足石杉中僅分離到18個該類化合物,其研究主要集中在石杉堿甲類似物的人工合成和結(jié)構改造方面,藥效作用機制還有待繼續(xù)深入研究。相關化合物信息見表3。
1.1.4 miseelaneous型生物堿 miseelaneous型生物堿是其他類型石松生物堿的統(tǒng)稱,該類型生物堿在蛇足石杉中數(shù)量較少,又可分為phlegmarine型、lucidine型、氮雜十二元環(huán)型及其他4種類型,其中以phlegmarine型生物堿數(shù)量相對較多,phlegmarine型結(jié)構中的C4-C13鍵一般斷裂形成C4位為亞甲基的三環(huán)生物堿。相關化合物信息見表4。
表1 蛇足石杉中fawcettimine型石松生物堿
Table 1 Fawcettimine-type lycopodium alkaloids from H. serrata
編號化合物名稱分子式文獻編號化合物名稱分子式文獻 12α-hydroxyphlegmariurine BC16H23NO31929千層塔堿(serratine)C16H25NO330 27α-hydroxyphlegmariurine BC16H23NO32230dihydrolycopoclavamine AC16H25NO231 37α,11α-dihydroxyphlegmariurineC16H23NO42031千層塔寧堿(serratinine)C16H25NO332 48α-羥基馬尾杉堿乙(8α- C16H23NO32132千層塔尼定堿(serratinidine)C18H28N2O233 hydroxyphlegmariurine B) 33serratezomine AC16H25NO334 58β-羥基馬尾杉堿乙(8β-C16H23NO32234serratezomine BC16H25NO434 hydroxyphlegmariurine B) 35石杉堿I(huperzine I)C16H23NO235 68-deoxy-13-dehydroserratinineC16H23NO22336蛇足石杉新堿(neohuperzinine)C16H23NO336 7lycoposerramine AC18H29N3O22437馬尾杉堿甲(phlegmariurine A)C16H23NO219 8lycoposerramine CC16H23NO22538馬尾杉堿乙(phlegmariurine B)C16H23NO219 9lycoposerramine DC17H25NO326392-oxoyphlegmariurine BC16H21NO319 10lycoposerramine EC16H23NO3254011-oxophlegmariurine BC16H21NO319 11lycoposerramine PC16H25NO32541macleanineC16H26N237 12lycoposerramine QC16H25NO25427-過氧羥基馬尾杉堿乙(7- C16H23NO438 13lycoposerramine SC17H30N225 hydroperoxyphlegmariurine B) 14lycoposerramine UC17H25NO3254311α-過氧羥基馬尾杉堿乙(11α- C16H23NO438 15lycoposerramine RC16H22N2O27 hydroperoxyphlegmariurine B) 16lycoposerramine TC20H29NO52744石杉堿W(huperzine W)C14H21NO239 17N-methyl-lycoposerramine TC21H31NO52745石杉堿P(huperzine P)C16H21NO318 18N-formyl-lycoposerramine TC21H29NO62746石杉堿Q(huperzine Q)C16H25NO240 19法氏石松堿(fawcettimine)C16H25NO22747石杉堿R(huperzine R)C15H21NO341 20石杉堿S(huperzine S)C16H23NO32848石杉堿H(huperzine H)C16H21NO242 21石杉堿T(huperzine T)C16H23NO328494α-hydroxy-2,13-oxidofacettimineC16H23NO343 2211α-羥基佛石松堿(11α- C16H23NO229508-去氧千層塔寧堿(8-deoxy- C16H25NO244 hydroxy-fawcettidine) serratinine) 232α,11α-二羥基佛石松堿(2α,11α- C16H23NO32951huperserratinineC25H33NO545 dihydroxy-fawcettidine) 52N-oxyhuperzine Q C16H25NO346 248α,11α-二羥基佛石松堿(8α,11α- C16H23NO32953huperserine AC16H24NO247 dihydroxy-fawcettidine) 54huperserine BC17H26NO247 252β-羥基石松丟寧堿(2β- C16H23NO32955huperserine CC16H23NO47 hydroxy-lycothunine) 56huperserine DC16H23NO247 268α-羥基石松丟寧堿(8α- C16H23NO32957huperzimineC16H22N2O48 hydroxy-lycothunine) 58huperzine Y1C16H24NO349 27石松丟寧堿(lycothunine)C16H23NO22959huperzine Y2C15H22NO449 28千層塔他尼定堿(serratanidine)C16H25NO42960huperzine Y3C16H24NO349
1.2 三萜類
蛇足石杉中所含的三萜類化合物,又稱石杉型三萜、鋸齒石松烷三萜,是石松目植物三萜類物質(zhì)的代表成分,其化學結(jié)構屬特殊五環(huán)三萜,且骨架C環(huán)為七元環(huán)結(jié)構,C環(huán)的C27化學位移一般在C56左右,C14-C15位大多形成雙鍵結(jié)構,或形成C14β-C15β環(huán)氧結(jié)構,有些化合物的C16位為羰基,與C14和C15位的雙鍵形成共軛體系;此外C3和C21位一般分別有1個含氧官能團,按骨架上含氧官能團的數(shù)量,可分為二醇類、三醇類、多醇類和其他結(jié)構4種類型[9,76]。目前已從蛇足石杉中分離得到千層塔尼醇、16氧千層塔三醇、千層塔萜二醇、21氧千層塔萜烯三醇和千層塔三醇等70多種[77-78]。此外,從蛇足石杉中還分離到一些有特殊藥理活性的石杉型三萜,如serratenediol已被證實具有誘導人白血病細胞HL-60凋亡和抑制細胞增殖的作用[79]。相關化合物信息見表5。
表2 蛇足石杉中l(wèi)ycopodine型石松生物堿
Table 2 Lycopodine-type lycopodium alkaloids from H. serrata
編號化合物名稱分子式文獻編號化合物名稱分子式文獻 616α,11α-二羥基石松堿(6α,11α-dihydroxy- C16H26NO350 81lycoposerramine NC18H27NO455 lycopodine) 82lycoposerramine OC28H39NO655 625β,6β,15α-15-甲基石松堿-5,6-二醇(5β,6β, C16H27NO251 83lycodolineC16H25NO254 15α-15-methyllycopodane-5,6-diol) 846α-hydroxy-lycopodineC16H25NO254 6312β-12-羥基石杉堿G(12β-12-hydroxy- C18H26N2O451 85serratezomine CC16H25NO334 huperzine G) 864α,6α-dihydroxy-serratidineC16H23NO456 6412-脫氧石杉堿O(12-deoxyhuperzine O)C16H23NO223 874α-hydroxy-serratidineC16H23NO356 656α-羥基-5,15-氧化石松堿(6α,-hydroxy-5,15- C16H25NO223,43 886α-hydroxy-serratidineC16H23NO356 oxidelycopodane) 89serratidineC16H23NO256 662α-hydroxy-lycoflexineC17H25NO343 90石杉堿E(huperzine E)C16H21NO339 67N-氧化石杉堿E(N-oxidehuperzine E)C16H21NO352 91石杉堿F(huperzine F)C16H21NO352 68N-氧化石杉堿F(N-oxidehuperzine F)C16H21NO452 92石杉堿O(huperzine O)C16H23NO357 692-氯代石杉堿E(2-chlorohuperzine E)C16H20ClNO253 93石松洛寧(clavolonine)C16H25NO258 70石杉堿E′(huperzine E′)C16H19NO253 94石杉堿庚(huperzine G)C18H26N2O326 71石杉堿F′(huperzine F′)C16H19NO353 95石松文堿(lycoclavine)C18H29NO332 72石松堿(lycopodine)C16H25NO54 96亮石松靈(lucidioline)C16H25NO259 73lycoposerramine FC16H25NO455 974α,6α-dihydroxy-lycopodine/(6α,15R)-4,6-C16H25NO360 74lycoposerramine GC16H25NO355 dihydroxy-15-methyllycopodan-5-one 75lycoposerramine HC16H23NO255 98 7-hydroxy-lycopodine/(15S)-7-hydroxy-C16H25NO260 76lycoposerramine IC16H23NO255 15-methyllycopodan-5-one 77lycoposerramine JC16H25NO255 9912-epilycodoline N-oxide/(12α,15R)-12-C16H25NO360 78lycoposerramine KC16H23NO255 hydroxy-15-methyllycopodan-5-one N- 79lycoposerramine LC16H25NO255 oxide 80lycoposerramine MC16H25NO2551007α-hydroxy-lycopodineC16H25NO258
表3 蛇足石杉中l(wèi)ycodine型石松生物堿
Table 3 Lycodine-type lycopodium alkaloids from H. serrata
編號化合物名稱分子式文獻編號化合物名稱分子式文獻 101石松定堿(lycodine)C16H22N244109蛇足石杉堿(huperzinine)C17H22N2O65 102石杉堿甲(huperzine A)C15H18N2O26110異福定堿(isofordine)C15H18N2O64 103石杉堿乙(huperzine B)C16H20N2O26111N-demethylhuperzinineC16H20N2O66 104石杉堿U(huperzine U)C16H22N2O228112β-obscurineC17H24N2O66 1056β-羥基石杉堿甲(6β-hydroxy- C15H18N2O263113蛇足石杉堿丙(huperzinine C)C16h24N267 huperzine A) 114de-N-methyl-obscurineC16H22N2O54 106馬尾松堿M(phlegmariurine M)C17H20N2O364115huperserine EC18H22N2O347 107N-甲基石杉堿甲(N-methyl- C16H20N2O63116N-methyl-16-hydroxy-huperzine BC17H22N2O263 huperzine A) 1171-甲基石松嵩堿(1-methyllycodine)C17H24N263 108N-甲基石杉堿乙(N-methyl- C17H22N2O651188α-hydroxy-15,16-dehydro-des-N-C16H22N2O263 huperzine B) methyl-α-obscurine
表4 蛇足石杉中miseelaneous型石松生物堿
Table 4 Miseelaneous-type lycopodium alkaloids from H. serrata
編號類型化合物名稱分子式文獻 119phlegmarine型serratezomine EC18H32N2O68 120石杉堿J(huperzine J)C17H30N2O69 121石杉堿K(huperzine K)C16H28N2O69 122石杉堿L(huperzine L)C17H30N2O269 123石杉堿M(huperzine M)C17H30N2O270 124石杉堿N(huperzine N)C16H28N2O70 125lycoposerramine XC16H28N2O71 126lycoposerramine YC17H30N2O71 127lycoposerramine ZC16H28N2O71 128lucidine型serratezomine DC29H49N3O68 129石杉堿V(huperzine V)C28H47N3O72 130serratanine A/lucidine BC30H49N3O73 131serratanine B/oxolucidine BC30H49N3O273 132氮雜十二元環(huán)型huperserratine AC17H28N2O312 133huperserratine BC17H28N2O312 134其他蛇足石杉堿乙(huperzinine B)C10H15NO74 135馬尾杉堿N(phlegmariurine N)C11H11NO75 136(+)-huperzine ZC11H12NO249 137(?)-huperzine ZC11H12NO249
1.3 其他成分
除上述成分以外,蛇足石杉中還分離到黃酮類、甾醇類、二萜類、蒽醌類、醇類等化學成分[84,86]。其中黃酮類物質(zhì)主要為黃酮類和黃酮醇類[84,86]。相關化合物信息見表6。
2 生物合成
2.1 轉(zhuǎn)錄組學研究
目前,蛇足石杉的轉(zhuǎn)錄組學研究主要以2、3代或兩者結(jié)合技術手段進行。Luo等[89]基于表達序列標簽(expressed sequence tag,EST)分析,從其根、莖、葉中獲得140 930條ESTs,并注釋了16 274個轉(zhuǎn)錄本,其中182個參與植物激素代謝,115個參與生物堿、三萜和黃酮類成分的生物合成調(diào)控;通過差異表達分析篩選到20個編碼細胞色素P450(cytochrome P450,CYP450)的轉(zhuǎn)錄本,其中4個候選基因、、和與石松生物堿合成相關;何美娜[90]以蛇足石杉地上部分為樣本,共獲得111 251個unigenes,通過京都基因與基因組百科全書分析顯示,分別有4、154個unigenes參與了賴氨酸的合成與代謝;基于Illumina HiSeq 4000對蛇足石杉根、莖、葉、孢子囊的轉(zhuǎn)錄組測序結(jié)果,顯示共有105 516個去冗余后的轉(zhuǎn)錄本,N50值為2488 bp,預測了參與石杉堿甲前體生物合成和修飾的關鍵酶,如-賴氨酸脫羧酶(lysine decarboxylase,LDC)、酮胺氧化酶(copper amine oxidase,CAO)、聚酮合酶(polyketide synthase,PKS)和CYP450,對其編碼基因進行差異表達分析,結(jié)果顯示葉片中CAO、PKS、CYP450表達量較高,并通過實時熒光定量聚合酶鏈式反應進行了驗證[91]。基于RNA測序轉(zhuǎn)錄組測序分析,Peng等[92]注釋獲得49 923個unigenes,通過差異表達分析發(fā)現(xiàn),在幼葉、老葉和莖中分別有1158、1675、1326個基因特異性表達,結(jié)合轉(zhuǎn)錄組分析得到2個編碼LDC的unigenes(和),以及3個編碼CAO的unigenes(、和)。光照影響蛇足石杉的生長發(fā)育[93]。張林甦等[94]研究發(fā)現(xiàn),孢子和葉中有2321(3.3%)個基因表達上調(diào),2832(6.7%)個基因下調(diào),進一步對二者中差異表達基因進行分析,結(jié)果顯示共有294個基因參與了蛇足石杉的光周期途徑。而基于超高效液相串聯(lián)質(zhì)譜儀的綜合代謝組學研究,Wu等[95]從蛇足石杉中分離鑒定了118種生物堿,其中,有72種在不同組織中存在顯著差異;進一步分析發(fā)現(xiàn),生物堿huperzine A、huperzine B、lycoposerramine C和lycoposerramine D在莖和葉中的含量顯著高于根,且具有相同的變化趨勢。目前轉(zhuǎn)錄組研究多定位在石杉堿甲的生物合成過程中,催化賴氨酸和丙二酰輔酶A相關的LDC、CAO和PKS,這些轉(zhuǎn)錄組數(shù)據(jù)對進一步探討蛇足石杉生長發(fā)育和次生代謝的合成機制奠定了基礎。
表5 蛇足石杉中的三萜類化合物
Table 5 Triterpenoids from H. serrata
編號化合物名稱化學式文獻編號化合物名稱化學式文獻 138山芝三醇(tohogenol)C30H52O3801733α,21β-dihydroxy-serrat-14-en-24,29-diolC30H54O482 139tohogeninolC30H52O4801743α,21β-dihydroxy-serrat-14-en-16-oneC30H48O378 140山芝烯三醇(serratriol)C30H50O3811753α,21β,24-trihydroxy-serrat-14-en-16-oneC30H48O477 141serratinol AC39H58O4821763α,21β,24-trihydroxy-serrat-14-enC30H50O378 142serratinol BC39H58O5821773α,21β,24- trihydroxy-serrat-14-en-16-oneC30H48O478 143serratenediol-3-acetateC32H52O3261783α,21α-dihydroxy-serrat-14-en-24-oic acidC30H48O481 144serratenediol-21-acetateC32H52O38317921α-hydroxy-serrat-14-en-3β-yl-acetateC32H56O482 145山芝烯二醇(serratenediol)C30H50O28318021β-hydroxy-serrat-14-en-3β-yl-acetateC32H56O484 146serrat-14-en-3β,21β-diolC36H56O57718121β-hydroxy-serrat-14-en-3β-olC30H54O284 147serrat-14-en-3β,21α-diolC36H56O57718221α-hydroxy-serrat-14-en-3β-olC30H54O284 148serrat-14-en-3α,21β-diolC36H56O57718321α-hydroxy-serrat-14-en-3β-yl propanedioic acid C33H52O581 149serrat-14-en-3β,21β,29-triolC30H50O377 monoester 150serrat-14-en-3β,21β,24-triolC36H56O68418421α-hydroxy-serrat-14-en-3β-yl dihydrocaffeateC39H58O581 151serrat-14-en-3β,21α,24-triolC36H56O67718521α-hydroxy-serrat-14-en-3β-yl p-C39H58O481 152serrat-14-en-3α,21β,24-triolC36H56O677 dihydrocoumarate 153serrat-14-en-3α,21β,24,29-tetraolC30H50O47718621α-hydoxyserrat-14-en-3β-yl acetateC32H56O477 154seratenediol-3,21-diacetateC34H54O47818721-epi-serratenediolC30H50O283 155seratenediol-3-acetateC32H52O37818821-epi-serratenediol-3-acetateC32H52O378 1563β-hydroxy-serrat-14-en-21β-yl-acetateC32H56O38218916-oxo-serratriolC30H48O485 1573β-hydroxy-serrat-14-en-21α-yl-acetateC32H56O38219016-oxo-diepiserratenediolC30H48O383 1583β-hydroxy-serrat-14-en-21β-olC30H54O28219116-oxo-3β-hydroxy-serrat-14-en-21β-olC30H48O382 1593β-hydroxy-serrat-14-en-21α-olC30H54O28219216-oxo-3α-hydroxy-serrat-14-en-21β-olC30H48O382 1603β-hydroxy-serrat-14-en-21-oneC30H48O28219316-oxo-3α,21β-hydroxy-serrat-14-en-24-olC30H48O482 1613β-acetoxy-serrat-14-en-21-on-3-hydroxy-C32H50O38219416-oxo-3α,21β-hydroxy-serrat-14-en-24-oic acidC30H46O582 serratenon-acetat 19516-oxo-3α,21β-hydroxy-serrat-14-en-24-alC30H46O482 1623β,21β-dihydroxy-serrat-14-en-29-olC30H54O38219616-oxo-3α,21β-dihydroxy-serrat-14-en-24-olC30H48O482 1633β,21β-dihydroxy-serrat-14-en-24-olC30H54O38219716-oxo-3α,21β-dihydroxy-serrat-14-en-24-alC30H46O481 1643β,21β-dihydroxy-serrat-14-en-16-oneC30H48O37719816-oxo-3α,21β-dihydroxy-serrat-14-en-24-oic acidC30H46O581 1653β,21β,24-trihydroxy-serrat-14-enC30H50O37819916-oxo-21β-hydroxy-serrat-14-en-3β-olC30H48O382 1663β,21α-dihydroxy-serrat-14-en-24-olC30H50O38420016-oxo-21β-hydroxy-serrat-14-en-3α-olC30H48O382 1673β,14β-dihydroxy-serratan-21α-olC30H57O48220116-oxo-21β-hydroxy-serrat-14-en-3α-yl-acetateC32H50O484 1683β,14β,21α-trihydroxy-serratan-24-olC30H57O58220214β,15β-epoxyserratan-3β,21β,29-triolC30H50O477 1693β,21β-dihydroxy-serrat-14-en-29-olC30H50O38220314β,15β-epoxy-3β-hydroxy-serratan-21βC30H52O482 1703β-hydroxy-serrat-14-en-21β-yl-p-C39H58O47820414β,15β-epoxy-3β-hydroxy-serratan-21β-olC30H52O382 dihydrocoumarate 20514β,15β-epoxy-3β-hydroxy-serratan-21α-yl-acetateC32H54O482 1713α,21β-dihydroxy-serrat-14-en-24-olC30H50O38420614β,15β-epoxy-3β-hydroxy-serratan-21α-olC30H52O382 1723α,21β-dihydroxy-serrat-14-en-24-oic acidC30H54O482
表6 蛇足石杉中其他化學成分
Table 6 Other compounds contained in H. serrata
編號類型化合物名稱分子式文獻 207黃酮類5,5′-dihydroxy-2′,4′-dimethoxy-flavone-7-O-β-D-(6′′-O-Z-p-coumaroyl)-glucopyranosideC32H30O1487 2085,7,4′-trihydroxy-3′,5′-dimethoxyflavoneC17H14O784 209金圣草(黃)素(5,7,4′-trihydroxy-3′-methoxyflavone)C16H14O684 2105,7,2′,4′-tetrahydroxy-5′-methoxyflavoneC16H12O784 211芹菜素(apigenin)C15H10O584 212甾醇類β-谷甾醇(β-sitosterol)C30H52O26 213胡蘿卜甾醇(daucosterol)C35H60O626 214羽扇豆醇(lupeol)C30H50O84 215二萜類3β-hydroxy-isopimaric acidC20H30O388 21615R-12,16-epoxy-11,14-dihydroxy-8,11,13-abietanoid-7-oneC20H28O488 217蒽醌類大黃素甲醚(physcion)C16H12O584 218醇類三十烷醇(triacontanol)C30H62O78 2191-dibenzofuranolC12H8O278
2.2 生物堿和萜類生物合成
2.2.1 石松型生物堿 石松型生物堿是蛇足石杉的特征活性成分,目前有關其生物合成的研究主要聚焦于石杉堿甲,其生物合成途徑主要包括石松定堿骨架形成和下游后修飾階段。目前認為石榴堿(pelletierine)和4-(2-哌啶基)乙酰乙酸[4-(2-piperidyl) acetoacetate,4PAA]是石松定堿骨架形成的關鍵前體[96],其中石榴堿由4PAA自發(fā)脫羧形成;4PAA由Δ1-哌啶烯和3-氧戊二酸發(fā)生亞胺酮縮合反應生成;Δ1-哌啶烯的生物合成起始物為-賴氨酸[97],其被-賴氨酸脫羧酶(lysine decarboxylase,LDC)催化形成尸胺(cadaverine),尸胺在酮胺氧化酶(copper amine oxidase,CAO)作用下生成5-氨基戊醛(5-aminopentanal),后脫水并環(huán)化為Δ1-哌啶烯(1-piperideine);3-氧戊二酸的起始物為乙酸,其活化形成乙酰輔酶A(acetyl-CoA),經(jīng)系列反應生成丙二酰輔酶A(malonyl-CoA),隨后2分子丙二酰輔酶A與III型聚酮合酶(polyketide synthase III,PKS III)作用生成3-氧戊二酸(3-oxoglutaric acid)。下游途徑中,目前認為由3種雙加氧酶(dioxygenase,2OGD)參與合成,首先石松定堿骨架與相關酶反應轉(zhuǎn)化形成-甲基-α-玉柏堿(des--methyl-α-obscurine,DNMAO),但有關機制尚不清楚;隨后DNMAO在2OGD-3催化下形成具吡啶環(huán)的去-甲基-β-玉柏堿(des--methyl-β-obscurine,DNMBO),DNMBO發(fā)生氧化反應后轉(zhuǎn)化為石杉堿乙,石杉堿乙在2OGD-1催化下,哌啶環(huán)裂解形成中間產(chǎn)物石杉堿丙,在2OGD-2作用下石杉堿丙的雙鍵異構化形成石杉堿甲[98],見圖2。
2.2.2 石杉型三萜 石杉型三萜(鋸齒烷型三萜)是一類特殊的五環(huán)三萜,其生物合成途徑亦可分為三萜骨架形成和下游修飾階段。石杉型三萜骨架形成階段,之前有關學者認為芒柄花萜醇(α-onocerin)是三萜化合物合成的關鍵前體,其經(jīng)相關酶催化后形成具有七元環(huán)的山芝烯二醇(serratenediol)[99],但最新研究發(fā)現(xiàn),從東北石松L.中克隆鑒定出3種氧化鯊烯環(huán)化酶(oxido squalene cyclase,OSC)基因(、和),參與了山芝烯二醇及山芝三醇的生成;通過體外酶催化實驗,進一步證明芒柄花萜醇前體(pre-α-onocerin,POC)是石杉型三萜合成的關鍵前體[100-101],POC的形成以乙酰輔酶A為起始底物,經(jīng)甲羥戊酸(mevalonate,MVA)途徑生成異戊烯二磷酸(isopentenyl pyrophosphate,IPP)和二甲基烯丙基焦磷酯(dimethylallyl pyrophosphate,DMAPP),IPP和DMAPP在法尼基焦磷酸合酶(farnesyl pyrophosphate synthase,F(xiàn)PS)催化下,縮合生成法尼基二磷酸(farnesyl diphosphate,F(xiàn)PP),隨后2分子FPP在角鯊烯合成酶(squalene synthase,SQS)作用下生成角鯊烯(squalene),角鯊烯與角鯊烯環(huán)氧酶(squalene epoxidase,SE)作用催化形成2,3-氧化角鯊烯(2,3-oxidosqualene),2,3-氧化角鯊烯與OSC作用后,環(huán)化生成2,3,22,23-環(huán)氧角鯊烯(2,3,22,23-dioxidosqualene),2,3,22,23-環(huán)氧角鯊烯由LCC特異性催化形成具有A環(huán)和B環(huán)的POC[102]。下游途徑中,POC與LCD催化形成芒柄花萜醇,與LCE催化形成C14陽離子的6/6/7/6/6-稠合五環(huán)中間體(intermediate,IMD),隨后IMD脫質(zhì)子生成山芝烯二醇,或親核加成水生成山芝三醇[100],見圖3。
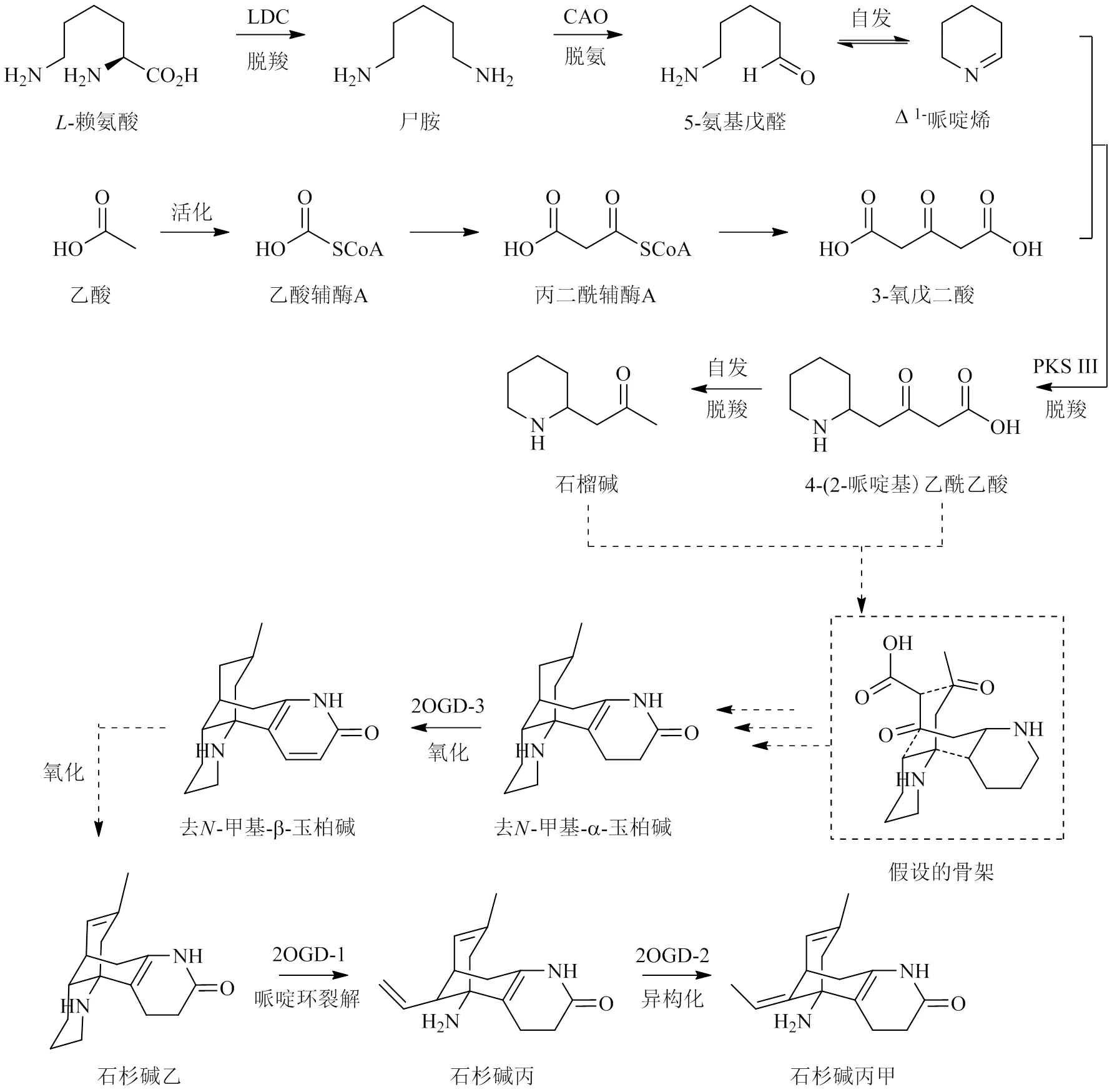
圖2 石松型生物堿的生物合成途徑
3 結(jié)語與展望
蛇足石杉作為一種重要的藥用植物,其所含的石杉堿甲為強效AChE抑制劑,對重癥肌無力癥的治療有效率高達99.2%,對老年癡呆癥、單純記憶障礙等療效顯著[103],是臨床治療上述疾病最有效的藥物之一。由于蛇足石杉野生資源有限,且石杉堿甲含量甚微,開展這一珍貴植物資源研究,探討合理開發(fā)利用途徑十分必要。化學合成是解決天然產(chǎn)物稀缺的重要手段,然而石杉堿甲的人工合成價格高昂,獲得產(chǎn)物純度較低,且大多數(shù)衍生物及類似物的生物活性較低甚至喪失等問題,均限制了石杉堿甲合成的發(fā)展和應用[104]。隨著分子代謝及生物技術的快速發(fā)展,有關天然產(chǎn)物生物合成及調(diào)控基因研究的不斷深入,為石杉堿甲生物合成提供了重要參考,但當前相關研究還存在一些問題,如蛇足石杉在全球分布廣泛,變種較多,關于該物種的分類和系統(tǒng)發(fā)育進化關系尚存較大爭議[105],有必要進一步開展深入研究。通過葉綠體基因組序列或轉(zhuǎn)錄組編碼基因的系統(tǒng)進化研究,有助于深入理解該物種及其近緣類群之間的演化關系;其次,目前蛇足石杉染色體的相關研究樣本采集范圍有限,基因組研究仍為空白,限制了其種間演變和進化關系的探索[106];關于蛇足石杉活性成分生物合成途徑相關研究,國內(nèi)外雖解析了蛇足石杉及其親緣種中石杉堿甲生物合成的大致途徑,并初步明確了參與上游合成途徑的關鍵酶基因,但涉及石榴堿和4PAA骨架形成的過程和關鍵酶尚不明確,且參與下游途徑中多個步驟的關鍵酶基因亦不清楚;此外,有關石杉型三萜的生物合成途徑,目前僅明確了七元環(huán)骨架形成的關鍵酶LCD和LCE,其骨架修飾相關過程關鍵酶還有待進一步研究。因此,蛇足石杉的基因組、轉(zhuǎn)錄組及代謝組研究仍亟待深入解析并挖掘,基于多組學的蛇足石杉活性成分生物合成研究,將為成分綠色合成提供重要基礎。
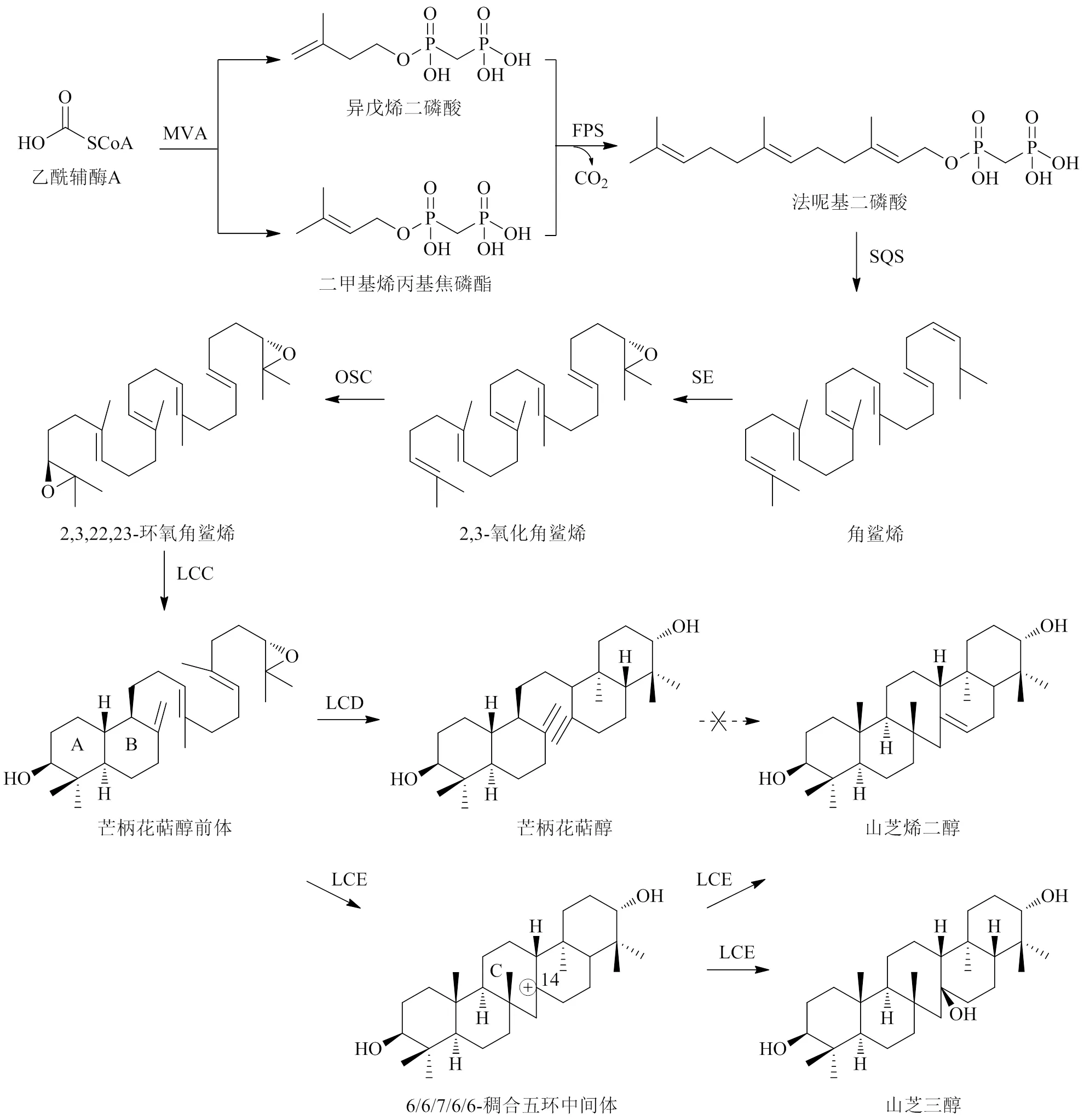
圖3 石杉型三萜的生物合成途徑
利益沖突 所有作者均聲明不存在利益沖突
[1] 趙剛, 胡光明, 吳平華, 等. 藥用蕨類植物蛇足石杉的研究進展 [J]. 上饒師范學院學報, 2018, 38(6): 67-73.
[2] 馬英姿, 劉江海, 張家玲. 林下珍稀藥用植物蛇足石杉繁殖的研究進展 [J]. 經(jīng)濟林研究, 2016, 34(2): 162-166.
[3] 齊耀東, 王德立. 蛇足石杉的種群結(jié)構和致危因素 [J]. 中國現(xiàn)代中藥, 2017, 19(1): 96-102.
[4] 王德立, 齊耀東. 蛇足石杉不同天然居群的土壤酶活性研究 [J]. 中國現(xiàn)代中藥, 2019, 21(10): 1407-1410.
[5] 張庭薈. 石杉堿甲提取工藝及藥理功效研究進展 [J]. 西部皮革, 2016, 38(2): 10.
[6] Ghassab-Abdollahi N, Mobasseri K, Dehghani Ahmadabad A,. The effects of huperzine A on dementia and mild cognitive impairment: An overview of systematic reviews [J]., 2021, 35(9): 4971-4987.
[7] 陳業(yè)高, 劉怡君, 蔣金和, 等. 石松類生物堿成分研究的新進展 [J]. 云南師范大學學報: 自然科學版, 2010, 30(6): 12-24.
[8] 易家寶, 顏杰, 李旭明. 石杉堿甲結(jié)構改造的研究進展 [J]. 天然產(chǎn)物研究與開發(fā), 2009, 21(6): 1080-1083.
[9] 周文昊, 董秋竹, 成飛, 等. 石杉型三萜類化合物及其生物活性研究進展 [J]. 中草藥, 2021, 52(12): 3736-3751.
[10] 袁經(jīng)權, 周小雷, 王碩, 等. 蛇足石杉化學成分和藥理作用研究進展 [J]. 中草藥, 2012, 43(2): 399-407.
[11] 謝峻, 張靜怡, 湯寧, 等. 加蘭他敏和石杉堿甲生物合成的研究進展 [J]. 中草藥, 2020, 51(3): 812-820.
[12] Wu X D, Li X N, Peng L Y,. Huperserratines A and B, two macrocyclic lycopodium alkaloids with an unusual skeleton from[J]., 2020, 85(10): 6803-6807.
[13] 黃驥, 趙愛玲. 蛇足石杉中石杉堿甲含量的動態(tài)變化分析 [J]. 中國中藥雜志, 2010, 35(19): 2511-2515.
[14] Yang Y, Dai L F, Wu D C,.propagation, huperzine A content and antioxidant activity of three genotypic[J]., 2021, 10(6): 1112.
[15] 王德立, 甘炳春, 齊耀東, 等. 蛇足石杉不同生長階段植株中石杉堿甲含量的地區(qū)差異及生境影響的比較觀察 [J]. 中國新藥雜志, 2014, 23(3): 326-332.
[16] 魯潤龍, 周忠澤, 鮑時來, 等. 藥用植物蛇足石杉的生物學特性 [J]. 中國科學技術大學學報, 1999(1): 121-124.
[17] 趙憲鶴. 生源啟發(fā)的Lycodoline型和Fawcettimine型石松科生物堿合成研究 [D]. 蘭州: 蘭州大學, 2017.
[18] Tan C H, Jiang S H, Zhu D Y. Huperzine P, a novelalkaloid from[J]., 2000, 41(30): 5733-5736.
[19] Tan C H, Chen G F, Ma X Q,. Three new phlegmariurine B type lycopodium alkaloids from[J]., 2002, 4(3): 227-231.
[20] Tan C H, Wang B D, Jiang S H,. New lycopodium alkaloids from[J]., 2002, 68(2): 188-190.
[21] 譚小健, 王海頃, 蔣華良, 等. 8α-OH馬尾杉堿B的結(jié)構鑒定: NMR譜分析及密度泛函理論研究 [J]. 化學學報, 2000, 58(11): 1386-1392.
[22] 袁珊琴, 趙毅民. 蛇足石杉中一個新的phlegmariurine型生物堿 [J]. 藥學學報, 2003, 38(8): 596-598.
[23] Yang Y F, Qu S J, Xiao K,.alkaloids from[J]., 2010, 12(11): 1005-1009.
[24] Takayama H, Katakawa K, Kitajima M,. A new type of lycopodium alkaloid, lycoposerramine-A, fromThunb. [J]., 2001, 3(26): 4165-4167.
[25] Takayama H, Katakawa K, Kitajima M,. Seven new lycopodium alkaloids, lycoposerramines-C, -D, -E, -P, -Q, -S, and -U, fromThunb [J]., 2002, 43(46): 8307-8311.
[26] 蔣金和, 劉瑩, 王利勤, 等. 蛇足石杉化學成分的研究 [J]. 云南師范大學學報: 自然科學版, 2010, 30(3): 59-65.
[27] Katakawa K, Kogure N, Kitajima M,. A new lycopodium alkaloid, lycoposerramine-R, with a novel skeleton and three new fawcettimine-related alkaloids from[J]., 2009, 92(3): 445-452.
[28] Tan C H, Ma X Q, Chen G F,. Huperzines S, T, and U: New lycopodium alkaloids from[J]., 2003, 81(4): 315-318.
[29] Katakawa K, Nozoe A, Kogure N,. Fawcettimine-related alkaloids from[J]., 2007, 70(6): 1024-1028.
[30] Inubushi Y, Harayama T, Akatsu M,. The structures of serratine and serratanidine [J]., 1968, 16(12): 2463-2470.
[31] Katakawa K, Mito H, Kogure N,. Ten new fawcettimine-related alkaloids from three species of[J]., 2011, 67(35): 6561-6567.
[32] 俞超美, 沈文照, 韓錦文, 等. 草藥蛇足草生物堿的研究 [J]. 藥學學報, 1982, 17(10): 795-797.
[33] Yasui B, Ishii H, Harayama T,. Structure of serratinidine: Correlation with serratinine [J]., 1966, 7(33): 3967-3973.
[34] Morita H, Arisaka M, Yoshida N,. Serratezomines A-C, new alkaloids fromvar.[J]., 2000, 65(19): 6241-6245.
[35] Gao W Y, Wang B D, Li Y M,. A new alkaloid and arbutin from the whole plant of[J]., 2010, 18(4): 614-616.
[36] 袁珊琴, 趙毅民, 馮銳. 蛇足石杉新堿的結(jié)構鑒定 [J]. 藥學學報, 2002, 37(12): 946-949.
[37] Ayer W A, Ma Y T, Liu J S,. Macleanine, a unique type of dinitrogenous lycopodium alkaloid [J]., 1994, 72(1): 128-130.
[38] Tan C H, Ma X Q, Zhou H,. Two novel hydroperoxylated lycopodium alkaloids from[J]., 2003, 45(1): 118-121.
[39] Cao H, Chai T T, Wang X,. Phytochemicals from fern species: Potential for medicine applications [J]., 2017, 16(3): 379-440.
[40] Hong B K, Hu D C, Wu J B,. Divergent total syntheses of (–)-huperzine Q, (+)-lycopladine B, (+)-lycopladine C, and (–)-4--lycopladine D [J]., 2017, 12(13): 1557-1567.
[41] Tan C H, Chen G F, Ma X Q,. Huperzine R, a novel 15-carbon lycopodium alkaloid from[J]., 2002, 65(7): 1021-1022.
[42] Gao, W Y,Li Y M,Wang B D,. Huperzine H, a new lycopodium alkaloid from[J]., 1999, 10(6): 463-466.
[43] 王海頃. 1. 石杉生物堿成分研究; 2. 烏頭生物堿成分研究[D]. 上海: 中國科學院上海生命科學研究院, 1999.
[44] 袁珊琴, 馮銳, 顧國明. 蛇足石杉生物堿成分的研究(II) [J]. 中草藥, 1994, 25(9): 595-596.
[45] Zhu D Y, Jiang S H, Huang M F,. Huperserratinine from[J]., 1994, 36(4): 1069-1072.
[46] Tan C H, Ma X Q, Chen G F,. Two novel lycopodium alkaloids from[J]., 2002, 85(4): 1058-1061.
[47] Jiang W W, Liu F, Gao X,. Huperserines A-E, lycopodium alkaloids from[J]., 2014, 99: 72-77.
[48] Yu C M,Calhoun L A,Konder R M,. Huperzimine, a novel lycopodium alkaloid from[J]., 2015 92(40): 406-410.
[49] Jiang F F, Qi B W, Ding N,. Lycopodium alkaloids from[J]., 2019, 137: 104277.
[50] Shan W G, Ren F Y, Ying Y M,. A new lycopodine alkaloid from[J]., 2012, 36(1): 15-16.
[51] Jiang J H, Liu Y, Min K,. Two new lycopodine alkaloids from[J]., 2010, 93(6): 1187-1191.
[52] Wang H B, Tan C H, Tan J J,. Two new-oxide lycopodium alkaloids from[J]., 2009, 23(15): 1363-1366.
[53] Wang H B, Tan C H, Tan J J,. Lycopodium alkaloids from[J]., 2007, 90(1): 153-157.
[54] 袁珊琴, 馮銳, 顧國明. 蛇足石杉生物堿成分的研究(III) [J]. 中草藥, 1995, 26(3): 595-596.
[55] Takayama H, Katakawa K, Kitajima M,. Ten new lycopodium alkaloids having the lycopodane skeleton isolated fromThunb. [J].(), 2003, 51(10): 1163-1169.
[56] Tan C H, Ma X Q, Jiang S H,. Three new hydroxylated serratidine alkaloids from[J]., 2002, 16(3): 149-153.
[57] 王保德, 滕寧寧, 朱大元. 石杉堿O的結(jié)構鑒定 [J]. 有機化學, 2000, 20(5): 812-814.
[58] Siengalewicz P, Mulzer J, Rinner U. Lycopodium alkaloids: Synthetic highlights and recent developments [J]., 2013, 72: 1-151.
[59] Lin L J, Lin L Z, Cordell G A,. NMR assignments of huperzine a, serratinine and lucidioline [J]., 1993, 34(5): 1425-1428.
[60] Tan C H, Zhu D Y. Lycopodine-type lycopodium alkaloids from[J]., 2004, 87(8): 1963-1967.
[61] Patil S P. Recently isolated lycodine-type lycopodium alkaloids and their total synthesis: A review [J]., 2020, 6: 99.
[62] 張青. 石松科Lycopodine型生物堿多樣性合成研究 [D]. 蘭州: 蘭州大學, 2021.
[63] Liu Y C, Zhang Z J, Su J,. Lycodine-type lycopodium alkaloids from the whole plants of[J]., 2017, 7(5): 405-411.
[64] 袁珊琴, 趙毅民. 蛇足石杉生物堿成分的研究(VI) [J]. 中草藥, 2003, 34(7): 595-596.
[65] 袁珊琴, 魏同泰. 蛇足石杉生物堿成分的研究 [J]. 藥學學報, 1988, 23(7): 516-520.
[66] Shan S M, Luo J G, Pan K,. Rapid screening and identification of lycodine-type alkaloids in Lycopodiaceae and Huperziaceae plants by ultra-performance liquid chromatography coupled with quadrupole time-of-flight mass spectrometry [J]., 2016, 30(11): 1861-1872.
[67] 袁珊琴, 趙毅民, 馮銳. 蛇足石杉堿丙的結(jié)構鑒定 [J]. 藥學學報, 2004, 39(2): 116-118.
[68] Kubota T, Yahata H, Yamamoto S,. Serratezomines D and E, new lycopodium alkaloids fromvar.[J]., 2009, 19(13): 3577-3580.
[69] Gao W, Li Y, Jiang S,. Three lycopodium alkaloid-oxides from[J]., 2000, 66(7): 664-667.
[70] Bosch C, Bradshaw B, Bonjoch J. Decahydroquinoline ring13C-NMR spectroscopic patterns for the stereochemical elucidation of phlegmarine-type lycopodium alkaloids: Synthesis of (?)-serralongamine A and structural reassignment and synthesis of (?)-huperzine K and (?)-huperzine M (lycoposerramine Y) [J]., 2019, 82(6): 1576-1586.
[71] Katakawa K, Kitajima M, Yamaguchi K,. Three new phlegmarine-type lycopodium alkaloids, lycoposerramines-X, -Y and-Z, having a nitrone residue, from[J]., 2007, 38(19): 177.
[72] Liu H Q,Tan C H,Jiang S H,. Huperzine V, a new lycopodium alkaloid from[J]., 2004, 15(3): 303-304.
[73] Siengalewicz P, Mulzer J, Rinner U.[M]. New York: Academic Press, 2013: 72.
[74] 袁珊琴, 趙毅民, 馮銳. 蛇足石杉生物堿成分的研究(V) [J]. 軍事醫(yī)學科學院院刊, 2001, 25(1): 57-58.
[75] 袁珊琴, 趙毅民. 蛇足石杉生物堿成分的研究(IV) [J]. 中草藥, 2000, 31(7): 20-21.
[76] 楊舜伊, 袁純紅, 蔣金和, 等. 石松類鋸齒烷型三萜成分及其生物活性研究進展 [J]. 浙江農(nóng)業(yè)科學, 2020, 61(4): 708-714.
[77] Zhou H, Li Y S, Tong X T,. Serratane-type triterpenoids from[J]., 2004, 18(5): 453-459.
[78] 鄭凱凱, 趙圓圓, 袁譜龍, 等. 蛇足石杉中非生物堿類化學成分研究 [J]. 中草藥, 2016, 47(1): 15-20.
[79] Ham Y M, Yoon W J, Park S Y,. Investigation of the component ofextract that inhibits proliferation and mediates apoptosis of human HL-60 leukemia cells [J]., 2012, 50(8): 2629-2634.
[80] Sano T, Tsuda Y, Inubushi Y. Structures of tohogenol and tohogeninol: Triterpenoids of[J]., 1970, 26(12): 2981-2986.
[81] Zhou H, Tan C H, Jiang S H,. Serratene-type triterpenoids from[J]., 2003, 66(10): 1328-1332.
[82] 羅超. 蛇足石杉化學成分研究 [D]. 蘇州: 蘇州大學, 2011.
[83] 李軍, 韓燕藝, 劉嘉森. 千層塔中三萜成分的研究 [J]. 藥學學報, 1988, 23(7): 549-552.
[84] 羅超, 陳重, 張文芳, 等. 蛇足石杉化學成分研究 [J]. 中草藥, 2011, 42(12): 2407-2409.
[85] Tsuda Y, Fujimoto T, Kimpara K. 16-Oxoserratriol and 16-oxolycoclavanol:triterpenoids [J]., 1970(5): 261.
[86] 魯翠濤, 梅興國, 鐘凡. 千層塔植物莖葉中黃酮類物質(zhì)的研究 [J]. 天然產(chǎn)物研究與開發(fā), 2002, 14(3): 27-29.
[87] 楊亞濱, 楊雪瓊, 徐艷群, 等. 千層塔中的一個新黃酮苷 [J]. 中國天然藥物, 2008, 6(6): 408-410.
[88] 楊亞濱, 楊雪瓊, 徐艷群, 等. 千層塔中的兩個二萜化合物[A] // 第七屆全國天然有機化學學術研討會論文集[C]. 成都: 中國化學會, 2008: 52.
[89] Luo H M, Li Y, Sun C,. Comparison of 454-ESTs fromandreveals putative genes involved in lycopodium alkaloid biosynthesis and developmental regulation [J]., 2010, 10: 209.
[90] 何美娜. 蛇足石杉轉(zhuǎn)錄組測序及基于SSR標記的遺傳多樣性分析 [D]. 西安: 西北大學, 2017.
[91] Yang M Q, You W J, Wu S W,. Global transcriptome analysis ofand identification of critical genes involved in the biosynthesis of huperzine A [J]., 2017, 18(1): 245.
[92] Peng Q Z, Long H, Du C,. RNA-seq of aboveground sporophyte’s transcriptome ofand transcriptional understanding of early steps associated with huperzine biosynthesis in forest [J]., 2020, 24: 100159.
[93] 駱冰潔, 姚茂君, 曹德華. 蛇足石杉芽胞萌發(fā)及生長發(fā)育的影響因素 [J]. 吉首大學學報: 自然科學版, 2016, 37(1): 64-68.
[94] 張林甦, 許義紅, 陸廷祥, 等. 基于蛇足石杉轉(zhuǎn)錄組測序篩選及分析光周期相關基因 [J]. 基因組學與應用生物學, 2020, 39(12): 5736-5743.
[95] Wu S W, Fan Z, Xiao Y L. Comprehensive relative quantitative metabolomics analysis of lycopodium alkaloids in different tissues of[J]., 2017, 3(1): 44-55.
[96] 陳作毅, 張君誠. 石杉堿生物合成與代謝途徑研究進展 [J]. 中華中醫(yī)藥雜志, 2013, 28(6): 1815-1818.
[97] Hemscheidt T.[M]. Berlin: Biosynthesis, 2000: 175-206.
[98] Nett R S, Dho Y, Low Y Y,. A metabolic regulon reveals early and late acting enzymes in neuroactivealkaloid biosynthesis [J]., 2021, 118(24): e2102949118.
[99] 張宇. 石松三萜成分的研究 [D]. 武漢: 中南民族大學, 2014.
[100] Saga Y, Araki T, Araya H,. Identification of serratane synthase gene from the fern[J]., 2017, 19(3): 496-499.
[101] Araki T, Saga Y, Marugami M,. Onocerin biosynthesis requires two highly dedicated triterpene cyclases in a fern[J]., 2016, 17(4): 288-290.
[102] 田榮, 谷巍, 韋陳彬, 等. 植物三萜類成分生物合成中氧鯊烯環(huán)化酶與細胞色素P450的研究進展 [J]. 南京中醫(yī)藥大學學報, 2021, 37(2): 303-310.
[103] Callizot N, Campanari M L, Rouvière L,.extract ‘NSP01’ with neuroprotective effects-potential synergies of huperzine A and polyphenols [J]., 2021, 12: 681532.
[104] Thu Ha T T, Khanh T D, Trung K H. Evaluation of genetic diversity and identification ofspecies collected in some different areas in Vietnam by molecular markers [J]., 2020, 80: 13-23.
[105] Yang Y H, Wang H, Yu H X,. Simultaneous separation and determination of three huperzine alkaloids inand its preparations by cyclodextrin-modified mixed micellar electrokinetic capillary chromatography [J]., 2021, 623: 114207.
[106] 陳思思, 張夢華, 王錦秀, 等. 藥用植物千層塔的基原物種及研究進展 [J]. 廣西植物, 2021, 41(11): 1794-1809.
Active compounds and their biosynthesis of
LI Zi-shan1, 2, AN Zhou-jie2, WANG Jing1, TIAN Ya2, XU Zhi-chao1, 2, DUAN Bao-zhong1
1. College of Pharmacy, Dali University, Dali 671000, China 2. College of Life Science, Northeast Forestry University, Harbin 150000, China
Due to theextremely limited resources available,is a rare and endangered medicinal plant in China. Moreover, clinical studies have shown that huperzine A fromis highly effective in treatment of Alzheimer’s disease and improving learning and memory abilities. Active compounds fromwere reviewed in this paper, and the possible biosynthetic pathway of active compounds ofwere concluded, in order to provide scientific reference for exploitation and utilization of its resources and biosynthesis of its active ingredients.
(Thunb. ex Murray) Trevis.; lycopodium alkaloids; serratene triterpenoids; huperzine A; biosynthesis; transcriptomics
R282.710.5
A
0253 - 2670(2022)11 - 3505 - 13
10.7501/j.issn.0253-2670.2022.11.029
2022-02-25
云南省院士專家工作站(202105AF150053);云南省重大科技專項(202002AA100007);云南省興滇英才支持計劃項目(YNWR-QNBJ-2020251)
李籽杉(1996—),女,碩士研究生,研究方向為中藥資源與鑒定。E-mail: lzs6623@163.com
段寶忠,教授,研究方向為中藥資源與種質(zhì)創(chuàng)新。Tel: (0872)2257411 E-mail: bzduan@126.com
[責任編輯 崔艷麗]

