殼聚糖聯合酶誘導碳酸鹽沉淀處理銅廢水的劣化現象和強化機理研究
徐銀龍,鄭文杰,王琳,薛中飛,謝毅鑫
(1 西安建筑科技大學土木工程學院,陜西西安 710055; 2 陜西省巖土與地下空間工程重點實驗室,陜西西安 710055)
引 言
隨著全球經濟的迅速發展及工業進程的加快,重金屬污染物通過各種途徑進入土壤和河水,導致大氣和水環境質量進一步惡化[1]。重金屬污染是一個國際上環境工程領域的關鍵問題,關乎人類健康和社會的可持續發展。礦山開采、印刷、電鍍、化工等行業產生的廢水中含有大量的銅離子(Cu2+),在自然環境中極易發生擴散和運移[2]。銅(Cu)進入人體內會形成富集,導致人體生長發育異常、致癌、智力低下并引發一系列其他疾病[3-4]。
銅廢水的主要處理技術包括化學沉淀法、離子交換法、電化學法、吸附法、微生物法等,但化學沉淀法無法形成穩定的沉淀從而產生大量的污泥并容易造成二次污染,離子交換法、電化學法、吸附法處理成本高昂,微生物法所使用的微生物對環境要求較高無法處理高濃度的銅廢水[5]。酶誘導碳酸鹽沉淀(EICP)是一項主要用于土壤改良的新興的修復技術,鮮少用于銅廢水的處理。相較于上述處理技術,這一方法可形成穩定的碳酸鹽沉淀結構從而避免污泥的產生,適應各種環境,操作簡單高效,因此備受同領域學者和從業人員關注[6-7]。
EICP 方法的實施原理即利用脲酶催化尿素水解為銨根離子(NH+4)和CO2-3[式(1)~式(3)],進而與鉛離子(Pb2+)、鋅離子(Zn2+)、鉻離子(Cr2+)、銅離子(Cu2+)等結合形成碳酸鹽沉淀從而防止重金屬離子擴散運移,最終達到處理、固化重金屬污染的目的[8-10]。Nam 等[11]應用EICP 技術固化重金屬和類金屬,研究結果表明砷、錳、鋅、鉛、鉻和銅的濃度分別大幅降低了31.7%、65.8%、50.6%、51.6%、45.1%和49.7%。Moghal 等[12-13]發現EICP 能有效沉淀鎘、鎳和鉛的碳酸鹽,同時還引用乙烯二胺四乙酸(EDTA)和檸檬酸對固化后的重金屬進行萃取,結果表明EICP技術可以有效降低重金屬的解吸水平。
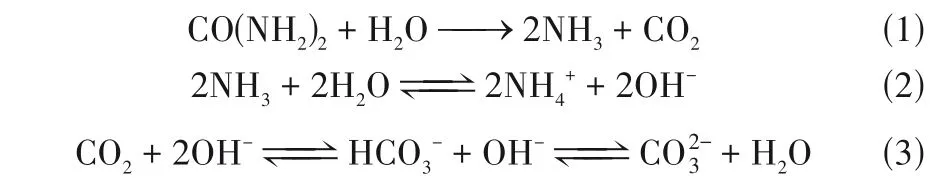
雖然EICP 在重金屬固化方面有很好的應用前景,但Wang 等[14]的研究表明在銅廢水濃度低于5 mmol/L 時EICP 方法才能發揮出較大作用,而就前人研究來看,實際的污染濃度早已超越這一范圍,因此在高濃度銅污染背景下的EICP 修復方法研究甚是缺乏。另外,高濃度的銅離子會顯著影響脲酶活性,進一步降低銅廢水處理效果[15-17]。因此,需尋找一種材料和方法來保護脲酶免受銅離子毒性作用影響。
殼聚糖是以蝦蟹外殼中的甲殼素為原料,經脫乙酰化得到的線性聚陽離子生物聚合物[18-21]。因其優異的吸附性、生物相容性和生物降解性而被廣泛應用于蛋白質的吸附與酶的固化[22-24]。以往的研究表明,殼聚糖多與微生物誘導碳酸鹽沉淀(MICP)技術聯用改善生物礦化的結構[25],卻鮮少用于重金屬污染的固化。殼聚糖作為一種大分子物質(分子量在5000 以上),Hamdan 等[26-27]進行試驗表明生物大分子膠體的加入會使碳酸鹽晶體之間的相互作用更緊密,并且可以延長EICP 反應時間,提高沉淀效率使得沉淀結構更為穩定。因此,基于以上研究現狀,本研究的主要目的是:(1)研究在酶誘導碳酸鹽沉淀處理銅廢水中,脲酶活性對處理效率的影響;(2)探求鈣源添加對沉淀形態和處理效率的影響;(3)揭示殼聚糖聯合酶誘導碳酸鹽方法處理銅廢水的強化和劣化機理。
1 試驗材料和方法
1.1 試劑與主要儀器
1.1.1 化學試劑 本試驗所用試劑均為分析純:尿 素[CO(NH2)2];氫 氧 化 鈉(NaOH);鈣 源[CaCl2;Ca(CH3COO)2];冰 醋 酸(CH3COOH);無 水 乙 醇(C2H5OH);硝酸銅[Cu(NO3)2];殼聚糖(chitosan,脫乙酰度≥95%);去離子水;干燥刀豆。
1.1.2 試驗儀器 粉碎機;電子天平;磁力攪拌器;冰柜;烘干機;pH 計(HANNA HI2003);電導率儀(HANNA HI2314);臺式高速離心機(常州市金壇勒普儀器TG16G);分光光度計(上海儀電分析儀器721G);原子吸收分光光度計(北京普析通用儀器TAS-990SVPERF)。
1.2 試驗方法
1.2.1 脲酶制備與活性測量 本研究所用脲酶提取步驟為:①將刀豆置于粉碎機中粉碎,過篩備用,儲存時應注意低溫、密封;②取豆粉溶于乙醇溶液中,置于磁力攪拌器上攪拌10~20 min 至均勻;③將豆粉溶液放入離心機離心30 min;④取離心管上清液,于冷柜中靜置4 h;⑤將靜置后的溶液再次離心1 h;⑥離心完成后分離上清液,沉淀即為所用脲酶。
電導率法測量脲酶活性:室溫下,將1 mol/L 尿素溶液30 ml和0.09 g 脲酶混合,使用電導率儀每隔5 min 測定混合溶液的電導率變化,連續測定3 次,取均值;根據Whiffin[28]提出的電導率法進行脲酶活性測量,即1 mS/(cm·min)的電導率變化對應11.1 mmol/(L·min)的尿素水解量,再乘以稀釋倍數,計算脲酶每分鐘水解尿素量,為刀豆脲酶活性的量化指標。脲酶活性(每克)=電導率(每分鐘)×11.1×稀釋倍數/脲酶濃度,得到尿素水解量為1.47 mmol/(g·min)。
1.2.2 殼聚糖膠體制備 將一定質量的殼聚糖加入質量分數為1%的醋酸溶液中,置于磁力攪拌器上攪拌至無肉眼可見顆粒,再加入NaOH 調節pH 至弱酸性即配制完成[29]。本試驗所使用的殼聚糖濃度為4 g/L和2 g/L。
1.2.3 銅廢水處理過程 將脲酶溶于去離子水中得脲酶溶液,將脲酶溶液與殼聚糖膠體混合攪拌均勻,再加入尿素溶液攪拌均勻即為本試驗所用的修復液,將上述修復液加入至不同濃度的硝酸銅和鈣源混合的污染液中,反應過后進行剩余銅離子濃度、銨根離子濃度、pH測量。剩余銅離子濃度通過原子吸收分光光度計測量,銨根離子濃度通過納氏試劑法測量,pH通過pH計測量。本試驗方案如表1所示。根據式(4)計算銅廢水處理效率:

表1 試管試驗方案Table 1 Testing scheme applied to the present work
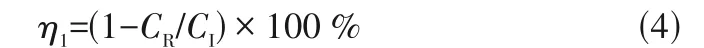
式中,CI為銅離子初始濃度,mmol/L;CR為處理后銅離子剩余濃度,mmol/L。
1.2.4 軟件模擬 為了評估脲酶活性和鈣源對銅廢水處理效率的影響,使用Visual MINTEQ 3.1 軟件進行模擬。脲酶催化尿素水解這一生物過程通過添加尿素水解產物,即銨根離子和碳酸根離子來體現,該軟件可通過添加由試管試驗中所測得的銨根離子和碳酸根離子來重現化學平衡反應的產物。數值模擬輸入參數如表2所示。
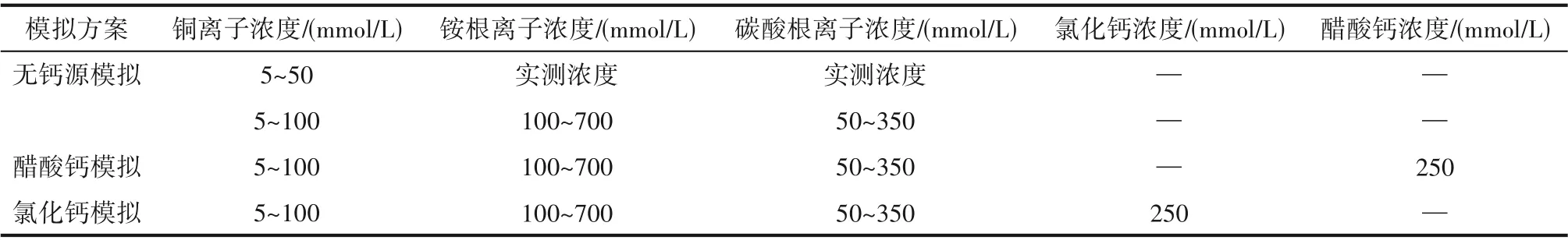
表2 數值模擬輸入參數Table 2 Simulation scheme applied to the present work
2 試驗結果與討論
2.1 脲酶活性對銅廢水處理的影響
由式(1)~式(3)可知,氫氧根離子和銨根離子作為脲酶催化尿素水解的產物,可以通過測量銨根離子濃度和pH 來反映脲酶活性和尿素水解程度,即銨根離子濃度和pH 越高,脲酶活性越高尿素水解程度越高。結果表明在未添加殼聚糖的試樣中均未檢測出NH4+,說明此時脲酶處于失活狀態,無法在EICP過程中實現尿素水解,故后續剩余銅離子濃度、處理效率沒有再進行測量和計算。脲酶失活的本質是銅離子結合脲酶上的巰基(—SH),從而改變其結構使其失活[28]。
基于前述量測結果,本研究擬添加不同濃度殼聚糖聯合酶誘導碳酸鹽沉淀技術開展后續試驗,結果如圖1 所示。在添加殼聚糖的試樣中,銨根離子濃度最高達330 mmol/L,并隨著殼聚糖濃度增加而增加,隨著銅離子濃度增加呈降低趨勢[圖1(a)]。另一方面,添加殼聚糖的試樣中,pH 的測量結果最高達9 以上,并且pH 隨殼聚糖濃度的增加而增加,同時隨銅離子濃度增加而降低[圖1(b)]。此結果說明殼聚糖能穩固脲酶活性進而保證尿素水解。根據剩余銅離子濃度和式(4)計算處理效率。如圖2所示,處理效率分布在18%~94%范圍,在尿素水解程度較高即銨根離子濃度較高(4 g/L 殼聚糖)和初始銅離子濃度較低(5 mmol/L 和10 mmol/L)的情況下,處理效率卻更低。在以往的研究中顯示,脲酶的活性越高,重金屬處理效率會越高[6]。然而本研究結果顯示脲酶活性與銅處理效率不成正比關系。
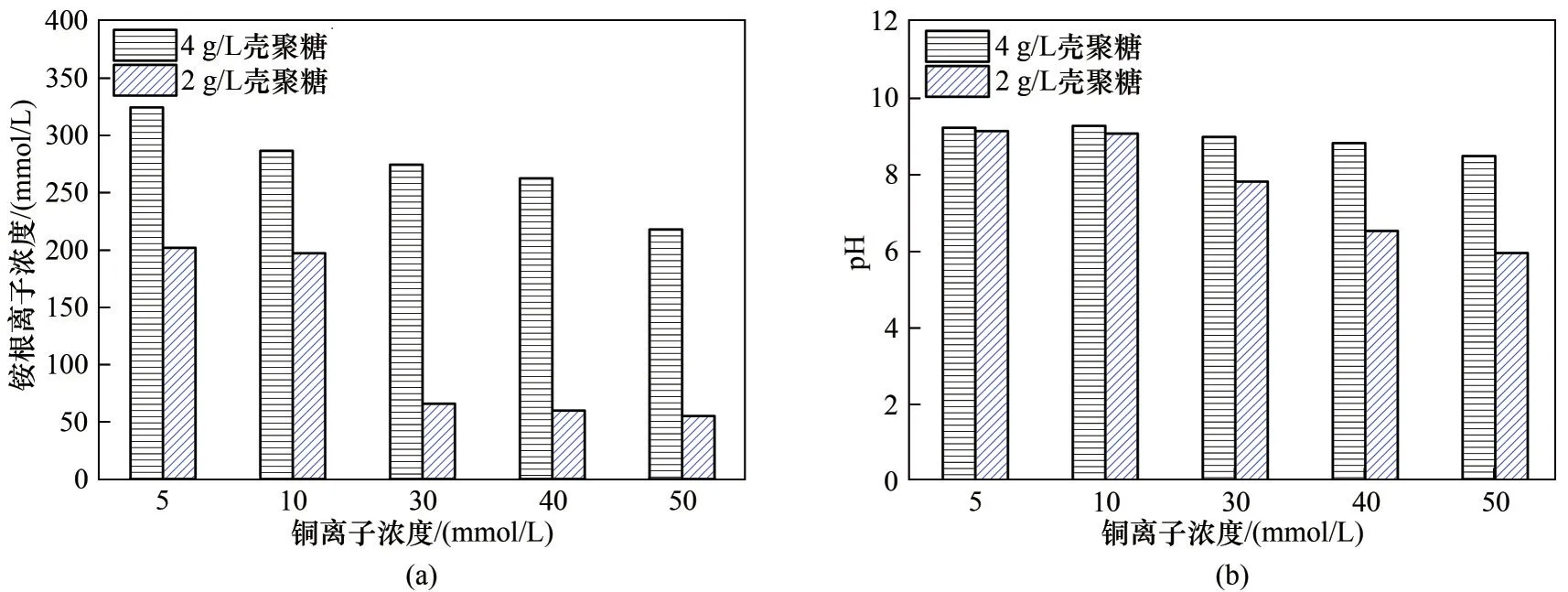
圖1 考慮添加殼聚糖銨根離子濃度和pH隨銅離子濃度的變化Fig.1 NH4+concentration and pH versus Cu2+concentration using the chitosan-assisted EICP method
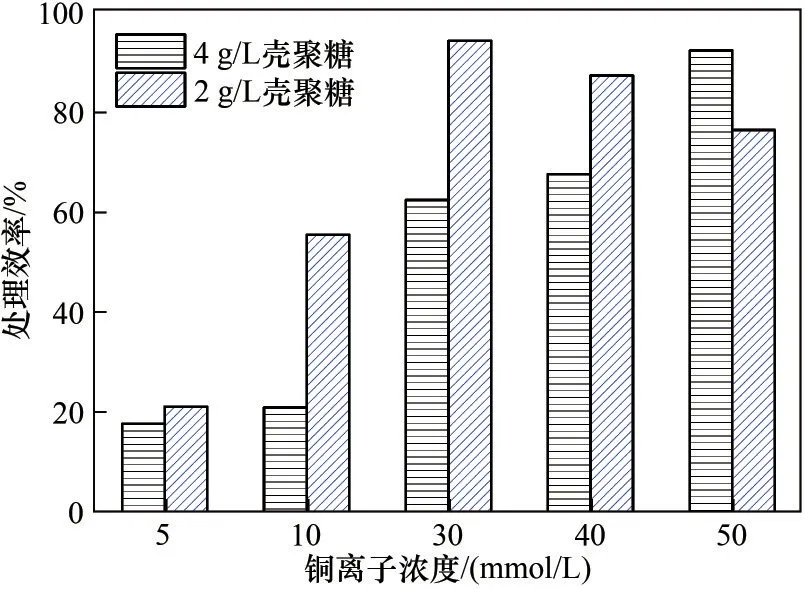
圖2 考慮添加殼聚糖處理效率隨銅離子濃度變化Fig.2 Treatment efficiency versus Cu2+concentration using the chitosan-assisted EICP method
進一步地,由數值模擬分析討論殼聚糖聯合酶誘導碳酸鹽沉淀的相關產物,探究影響銅處理效率的因素。數值模擬通過實際測量得出的銨根離子和碳酸根離子濃度作為輸入參數(圖1),考慮不同殼聚糖濃度下重現試管試驗EICP 過程。由圖3 可知,銅的相關產物主要為孔雀石[Cu2(OH)2CO3]、藍銅礦[Cu3(OH)2(CO3)2]和銅氨絡合物[[Cu(NH3)n]2+,n=1~4][式(5)~式(7)]。
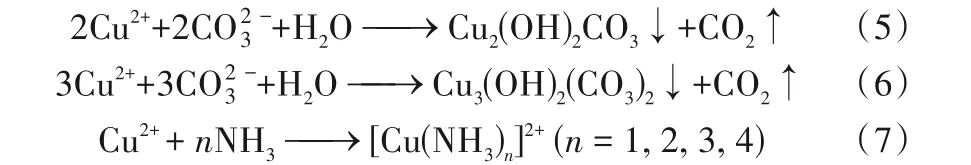
孔雀石和藍銅礦以沉淀形式存在,形態穩定且不易分解,而銅氨絡合物以離子形態存在,易擴散遷移,從而劣化處理效果[30]。由圖3(a)得,銅離子濃度為30 mmol/L時,銅相關的產物只有Cu3(OH)2(CO3)2,濃度接近于10 mmol/L,即沉淀了30 mmol/L 的Cu2+,此時處理效率接近100%(圖2)。銅離子濃度為5 mmol/L 時,銅產物為[Cu(NH3)n]2+,濃度接近于4 mmol/L,由式(4)計算處理效率低至20%(圖2)。由圖3(b)得,銅離子濃度為50 mmol/L 時,生成銅的沉淀只有Cu2(OH)2CO3,濃度接近于25 mmol/L,即沉淀了50 mmol/L的Cu2+,此時處理效率約為100%(圖2)。以上數值模擬得出的結果與試管試驗量測結果一致。由圖2 可得,銨根離子濃度越高處理效率反而越低的原因在于形成銅氨絡合物,造成游離銅的濃度較高從而劣化處理效率。銅氨絡合物的形成與氨的濃度緊密相關,本研究中氨主要來源于尿素水解,而尿素水解程度與脲酶活性密切相關。圖1、圖2的結果也證明殼聚糖濃度越高,脲酶活性越高,使得尿素水解程度較高,令溶液中的銨根離子和pH 較高,提供銅氨絡合物形成的優良條件。基于以上討論,本研究通過精細化數值模擬探究尿素水解程度以及銅氨絡合物的形成條件,以有效提高處理效率。
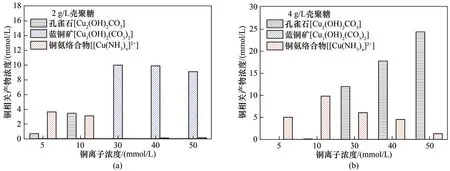
圖3 考慮添加殼聚糖碳酸鹽沉淀隨銅離子濃度的形態分布Fig.3 Speciation of carbonate precipitation versus Cu2+concentration using the chitosan-assisted EICP method
2.2 不同尿素水解程度下沉淀形態分析
2.2.1 未添加鈣源 從圖1(a)可知,殼聚糖能夠顯著提高脲酶活性,使銨根離子濃度高達330 mmol/L。為研究不同尿素水解程度對沉淀形態和處理效率的影響,數值模擬中引入銨根離子濃度范圍為100~700 mmol/L,對應的碳酸根離子濃度范圍為50~350 mmol/L。未添加鈣源時不同尿素水解程度下沉淀形態如圖4所示,主要沉淀形態包含藍銅礦、孔雀石和黑銅礦,其余均以銅氨絡合物和銅離子等離子形式存在。由分析結果可知銅濃度低于20 mmol/L,銨根離子濃度在300 mmol/L 以上時,形成了大量的銅氨絡合物,相應的處理效率接近于0,此時溶液pH在9以上(圖4)。銅離子濃度高于50 mmol/L,銨根離子濃度在200~300 mmol/L 范圍時,處理效率接近100%,此時銅主要以前述三種沉淀形式存在。由試管試驗和數值模擬的結果得,銨根離子濃度隨銅濃度增加而減少,當銅離子濃度較低時銨根離子濃度越高且pH越高[圖1(b)和圖4(c)],這種情況下形成了大量銅氨絡合物(圖3),說明堿性環境是銅氨絡合物形成的優良條件,Duarte-Nass 等[31]研究也發現pH在9以上時,銅離子偏向與氨絡合生成銅氨絡合物,而不是與碳酸根結合生成藍銅礦和孔雀石。綜合以上分析可知,高活性脲酶會產生一個偏堿性的多氨環境,并且使得溶液pH 超過9 時生成銅氨絡合物。由此發現可知,若能研發調控pH 的方法則可避免銅氨絡合物的形成,從而提高處理效率。

圖4 處理效率和pH與銨根離子濃度之間關系(未添加鈣源)Fig.4 Treatment efficiency and pH versus NH4+concentration(without calcium source addition)
尿素水解產生銨根離子和碳酸根,一部分碳酸根與銅離子結合生成碳酸鹽沉淀,剩余碳酸根大量水解,產生OH-造成pH 升高[式(8)~式(9)],因此阻止碳酸根水解即可對pH 進行調控。基于此猜想,本研究通過添加鈣源,使鈣離子與碳酸根結合進而阻止其水解,為了驗證此分析,本研究開展添加鈣源的數值模擬,相關的結果將在2.2.2 節進行分析討論。
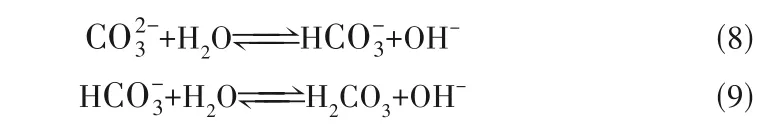
2.2.2 添加鈣源 圖5為氯化鈣作為鈣源時,不同尿素水解程度下的沉淀形態分析,其主要包含氯銅礦[Cu2(OH)3Cl]、藍銅礦和孔雀石三種形態,并且銨根離子在200~500 mmol/L 范圍時,各濃度的銅廢水處理效率接近100%[圖5(b)],此時沉淀主要以藍銅礦和孔雀石的形態存在[圖5(a)],這種形態的沉淀較為穩定,不易分解生成其他物質,是銅最佳的沉淀形態。另外,此時pH 基本在5~7 之間[圖5(c)],遠小于易形成銅氨絡合物的范圍。銅離子和銨根離子濃度為100 mmol/L 時,沉淀以氯銅礦的形態存在,這是因為這種條件下pH 過低[圖5(c)],尿素水解產生的50 mmol/L 碳酸根離子不足以使所有的銅離子沉淀,只能沉淀66 mmol/L 的銅離子,并由式(4)測算處理效率約為66%[圖5(b)]。從圖5(c)可以看出此時的pH 接近4,既有的研究表明過酸的環境不利于孔雀石和藍銅礦形成沉淀[31],故銅的沉淀形式只有氯銅礦一種,未沉淀的銅以銅離子的形式存在。此外,在銅離子濃度5 mmol/L、銨根離子600 和700 mmol/L,以及銅離子濃度10 mmol/L、銨根離子700 mmol/L 時,處理效率測算為0[圖5(a)、(b)] ,即無碳酸鹽沉淀形成,銅主要以銅氨絡合物的形式存在溶液中,此時pH 處于8~9 之間[圖5(c)]。添加鈣源的數值模擬結果表明,其不僅可以改變碳酸鹽沉淀形態,還可對pH進行調控,少部分處理效率的劣化主要是因為尿素水解程度不足(銨根離子濃度為100 mmol/L)而導致,但水解程度過高(銨根離子濃度為600 和700 mmol/L)提高了溶液pH亦會劣化處理效率。
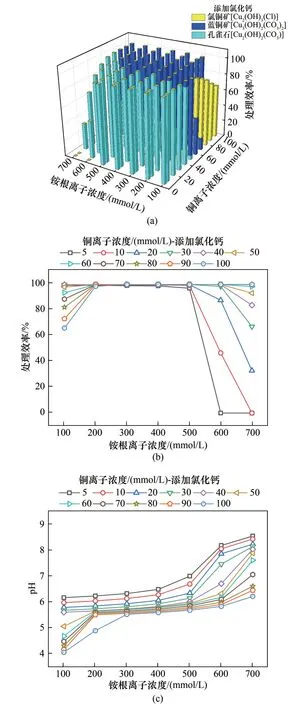
圖5 處理效率和pH與銨根離子濃度之間關系(鈣源為氯化鈣)Fig.5 Treatment efficiency and pH versus NH4+concentration(with CaCl2 addition)
圖6 為醋酸鈣作為鈣源時,不同尿素水解下的銅沉淀形態分析,主要包含藍銅礦和孔雀石兩種形態[圖6(a)],并未出現未添加鈣源時出現的黑銅礦沉淀[圖4(a)],對比藍銅礦和孔雀石,黑銅礦穩定性較差且易與其他化合物反應[31]。由圖6(b),銨根離子在200~500 mmol/L范圍,處理效率高達90%~100%,此時pH 介于5~8 之間[圖6(c)]。銅離子和銨根離子濃度為100 mmol/L 時,溶液pH 較低,尿素水解產生的50 mmol/L 碳酸根不足,只能沉淀76 mmol/L 的銅離子,由式(4)測算處理效率約為76%[圖6(b)]。此時pH 在5 以上,不利于銅氨絡合物形成。當銅離子濃度為5 mmol/L、銨根離子600 和700 mmol/L,以及銅離子濃度10 mmol/L、銨根離子700 mmol/L 時,處理效率測算為0[圖6(a)、(b)],處理效率劣化的原因與pH接近9時銅氨絡合物的形成緊密相關[圖6(c)]。
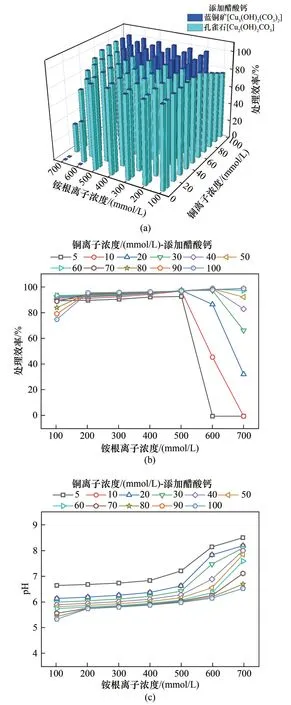
圖6 處理效率和pH與銨根離子濃度之間關系(鈣源為醋酸鈣)Fig.6 Treatment efficiency and pH versus NH4+concentration(with Ca(CH3COO)2 addition)
2.3 鈣源對處理效率的影響
由數值模擬結果得知添加鈣源能有效調控pH,避免銅氨絡合物的形成,且模擬結果與試管試驗有較好的一致性。圖7為考慮添加鈣源時不同殼聚糖濃度下銨根離子和pH 隨銅離子濃度的變化,銨根離子濃度隨殼聚糖濃度增加而增加,且隨銅離子濃度增加而減小[圖7(a)、(b)]。另外,醋酸鈣作為鈣源時,對比氯化鈣為鈣源時銨根離子濃度和pH 較低,原因是醋酸根水解產生的醋酸是有機酸,會破壞殼聚糖大分子的鏈式結構,降低殼聚糖對脲酶的保護作用,劣化脲酶活性[32]。當殼聚糖濃度為2 g/L 時,醋酸根水解產生的氫氧根會提高pH,因此圖7(c)中醋酸鈣作為鈣源時pH 高于氯化鈣作為鈣源時pH。當殼聚糖濃度為4 g/L時,由于兩種鈣源的銨根離子濃度差距較大,即尿素水解程度差距較大,從而弱化醋酸根水解的影響,導致圖7(d)中當醋酸鈣作為鈣源時pH低于氯化鈣作為鈣源時pH。

圖7 考慮添加鈣源時殼聚糖聯合酶誘導碳酸鹽沉淀方法銨根離子濃度和pH隨銅離子濃度變化Fig.7 NH+4 and pH versus Cu2+concentration using the chitosan-assisted EICP method(with calcium source addition)
圖8為添加鈣源時不同濃度殼聚糖下的處理效率隨銅離子濃度變化規律,較未添加鈣源時處理效率顯著上升。當殼聚糖濃度為2 g/L時,氯化鈣作為鈣源可使處理效率穩定提高至80%以上,當殼聚糖濃度為4 g/L 時,銅離子濃度為5 和10 mmol/L 時,處理效率顯著下降,原因為水解程度過高顯著提升了溶液pH,導致銅氨絡合物的形成。此外,對比兩種鈣源,醋酸鈣作為鈣源時的處理效率較低,普遍在80%以下。值得一提的是當殼聚糖濃度為4 g/L 時,盡管醋酸鈣作為鈣源時的pH 更低,但其處理效率也較低,主要與殼聚糖絮凝作用有關,將在2.4 節深入討論。

圖8 考慮添加鈣源殼聚糖聯合酶誘導碳酸鹽沉淀方法處理效率隨銅離子濃度變化Fig.8 Treatment efficiency versus Cu2+concentration using the chitosan-assisted EICP method(with calcium source addition)
2.4 殼聚糖聯合酶誘導碳酸鹽沉淀對處理效率的強化機理
試管試驗和數值模擬已表明處理效率的劣化現象,原因可歸結為:(1)水解程度不足無法沉淀所有銅離子;(2)較高的水解程度產生較多的氫氧根,導致溶液pH 升高從而形成銅氨絡合物。本節將深入討論殼聚糖聯合酶誘導碳酸鹽沉淀方法處理銅廢水的強化機理,如圖9 所示,其包含如下幾個作用。
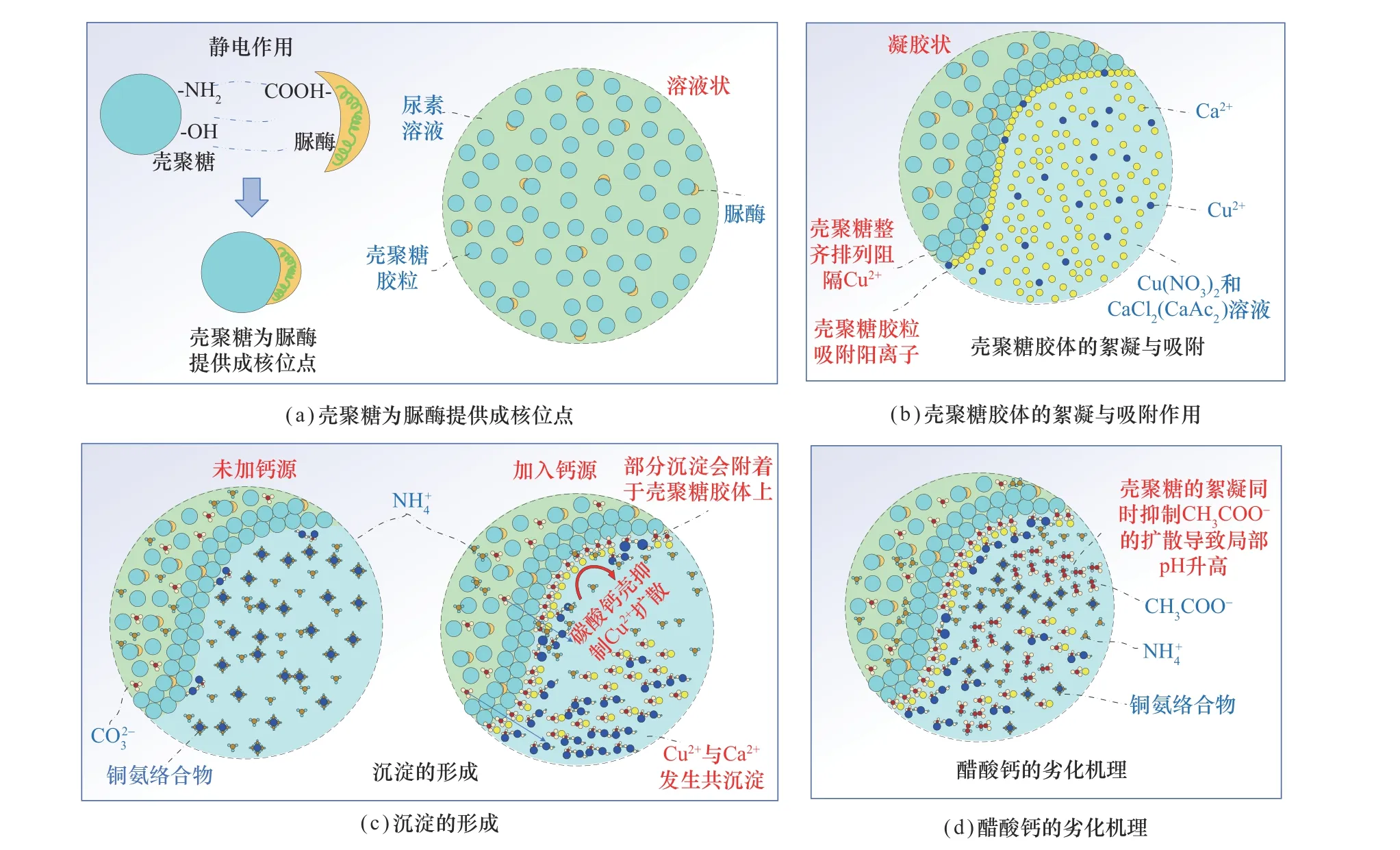
圖9 殼聚糖聯合酶誘導碳酸鹽沉淀處理銅廢水強化機理示意圖Fig.9 Enhancement mechanism of the chitosan-assisted EICP method for copper wastewater treatment
(1)殼聚糖為脲酶提供成核位點:由于殼聚糖分子中含有大量的氨基(—NH2)和羥基(—OH),可以與蛋白質分子中的羧基(—COOH)等活性基團產生靜電作用,所以殼聚糖與蛋白質之間有很好的親和性,可有效地吸附水中蛋白質分子[33-34]。因此,這種靜電作用使脲酶與殼聚糖膠體牢牢地結合在一起,避免其游離在溶液中因其他因素而失活,增強了脲酶的穩定性。
(2)殼聚糖膠體的絮凝與吸附作用:將殼聚糖和脲酶、尿素的混合溶液加入銅和鈣源的混合溶液后,殼聚糖膠體會產生絮凝作用,將銅離子和脲酶隔絕開,此時修復液呈凝膠狀,殼聚糖膠體會抑制銅離子的擴散并保護脲酶免受其抑制作用,為脲酶催化尿素水解提供足夠的時間,并且殼聚糖濃度越高這種絮凝作用就越強,進而尿素水解程度越高。這種絮凝作用的產生,是因為殼聚糖是一種陽離子多糖,在酸性溶液中帶正電荷,在接觸到含有銅和鈣源的混合溶液后,溶液中的反離子(即與帶電粒子表面電荷相反的離子)會影響分散系的穩定性,粒子雙電層的擴散層被壓縮,粒子間排斥位能降低而導致的[35-37]。因此在本文2.1 節中添加殼聚糖后脲酶活性顯著提高,為殼聚糖的絮凝作用將脲酶與銅離子隔離開提供了強而有力的證明。
(3)沉淀的形成:殼聚糖是一種線性聚陽離子聚合物,會吸附陽離子,即銅離子、鈣離子和尿素水解產生的銨根離子。未添加鈣源時,由于pH 范圍和銨根離子的緣故,銅離子會傾向于產生銅氨絡合物。添加鈣源后,鈣離子濃度為250 mmol/L,銅離子濃度最高為50 mmol/L,由于鈣離子濃度遠高于銅離子濃度,因此殼聚糖吸引鈣離子的量會高于銅離子的量,并且由于碳酸鈣(Ksp=10-8.54)和堿式碳酸銅(孔雀石和藍銅礦)(Ksp=10-9.86)的平衡常數相近,所以鈣離子會和碳酸根離子優先發生反應生產碳酸鈣沉淀,并在殼聚糖表面形成一層“碳酸鈣殼”,進一步地保護脲酶免受銅離子抑制作用,極大提高脲酶活性。因此,在本文2.3 節中添加鈣源后的銨根離子濃度會顯著提高。另一方面,碳酸鈣的形成會阻止碳酸根水解,pH 得以控制在9 以內,有效避免銅氨絡合物的生成。再者,受殼聚糖吸引的銅離子和尿素水解釋放的碳酸根離子會在殼聚糖絮凝處與碳酸鈣形成共沉淀,從而提高重金屬沉淀的穩定性。
(4)醋酸鈣作為鈣源處理效率降低:醋酸鈣作為鈣源,殼聚糖濃度為2 g/L 時,修復過程中醋酸根的水解會提高pH,如圖7(c),較高的pH 會促進銅氨絡合物的產生,因此醋酸鈣作為鈣源時的處理效率均小于氯化鈣作為鈣源。對于殼聚糖濃度為4 g/L 的情況下,雖然醋酸鈣作為鈣源時pH 較低,但由于殼聚糖的絮凝作用更強,抑制了醋酸鈣的影響。因此,無論殼聚糖濃度高低,醋酸鈣作為鈣源時進行銅廢水處理的效果都不如氯化鈣。
3 結 論
(1)銅離子對脲酶的抑制作用十分明顯,未添加殼聚糖時,脲酶處于失活狀態,而添加殼聚糖后,脲酶有較高活性,可使得銨根離子濃度最高達到330 mmol/L。但脲酶活性與處理效率不成正比關系,較高的脲酶活性會促使尿素水解產生較高的銨根離子,提高溶液pH,促使銅氨絡合物產生,進而降低處理效率。而較低的脲酶活性又無法滿足銅離子的完全沉淀,故較高和較低的脲酶活性都會劣化銅廢水處理。
(2) 未添加鈣源時,尿素水解使得pH 達到9 以上會大量生成銅氨絡合物,添加鈣源后會抑制pH的升高及銅氨絡合物的產生,顯著提高處理效率。銨根離子濃度在200~500 mmol/L 之間,pH 在5~8 之間利于產生孔雀石和藍銅礦這類理想的銅沉淀。相比于氯化鈣,殼聚糖的這種強絮凝作用使得醋酸鈣不合適作為鈣源進行銅廢水的處理,因此氯化鈣是強化銅廢水處理的較好鈣源。
(3)殼聚糖和脲酶之間的靜電作用使得脲酶吸附于殼聚糖之上,加入銅溶液后,殼聚糖的絮凝作用使脲酶和銅離子隔絕開,脲酶有活性催化尿素水解。殼聚糖作為一種線性聚陽離子聚合物,會吸引陽離子,未添加鈣源時,pH 的不斷升高會為銅氨絡合物的形成提供良好的環境從而劣化處理效率。添加鈣源后,會在殼聚糖表面產生“碳酸鈣殼”,進一步阻止銅離子的擴散,另外添加鈣源能夠有效降低pH阻止銅氨絡合物生成,有效提高處理效率。

