淺談脈動真空滅菌柜脈動滅菌和非脈動滅菌模式的不同及使用要點
藺建平 郭建軍 亢和平 張 淵
(金宇保靈生物藥品有限公司,內蒙古 呼和浩特 010111)
0 引言
脈動真空滅菌柜由于使用范圍廣、操作安全等優點,在制藥行業中被越來越多的使用,它不僅可以用于液體類物品的滅菌(對熱不敏感的溶液如MEM溶液等)、玻璃類用品用具的滅菌(各類血清瓶,取樣瓶,吸管等),還可以用于不銹鋼類用品用具的滅菌(反應器附屬用品用具如取樣T閥,離線過濾器等),而且針對不同的滅菌物品可以選擇不同的滅菌方式,作為制藥行業生產線中的重要滅菌設備,直接影響脈動滅菌柜的利用率和企業單位的直接能源成本。該文針對某公司所使用型號中的一種SHINVAXG1.DWT型脈動真空滅菌柜的工作原理、不同滅菌方式以及滅菌常用物品時的注意事項進行了詳細介紹和建議。
1 制藥行業常用的滅菌方法及微生物滅菌原理
1.1 常用滅菌方法概述
常用滅菌方法如圖1所示。
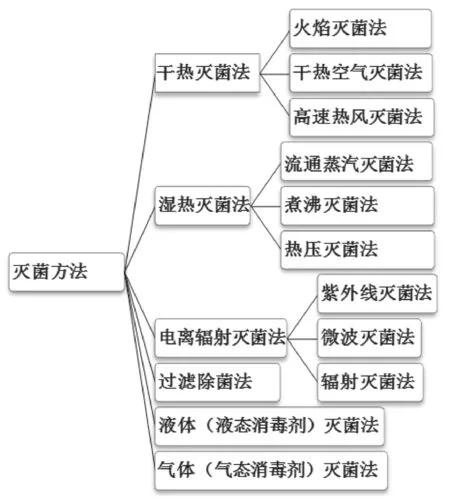
圖1 常用滅菌方法
1.2 滅菌基本原理
高壓蒸汽滅菌的原理是利用熱蒸汽穿透細胞使其蛋白質等物質變性而起到滅菌作用。高溫高壓滅菌,不僅可殺死一般的細菌、真菌等微生物。對芽孢、孢子也有殺滅效果,是最可靠、應用最普遍的物理滅菌法。主要用于能耐高溫的物品,如培養基溶液、蔗糖奶粉保護劑等一些溶液及丁基膠塞、搪瓷制品等制藥行業常用物品的滅菌。
2 設備使用前關鍵事項的準備及要求
2.1 蒸汽
蒸汽的質量、壓力直接影響滅菌的效果,所以使用前必須要保證純蒸汽的質量和壓力,純蒸汽壓力應控制在0.3MPa~0.5MPa,壓力過低不能保證滅菌程序的順利進行;壓力過高滅菌柜出于安全原因,程序會自動退出,無法滅菌。打開純蒸汽,在蒸汽進入夾層之前,應先將管道中的冷凝水排放干凈。
2.2 軟化水
打開軟化水閥,為真空泵和冷凝器用水做準備。若水源壓力低于0.1MPa,則不能啟動設備運行真空泵。 為及時方便觀察軟化水的壓力,建議在進滅菌器的水管道上安裝一塊0~0.6MPa量程的壓力表,便于觀看進水壓力。
2.3 滅菌效果檢測
滅菌效果的檢測是評價其滅菌方法是否合理、滅菌效果是否可靠的必要手段。 常規的檢測方式分為化學檢測、生物檢測、物理檢測三大類。
利用化學指示劑在一定溫度與作用時間條件下受熱變色或變形的特點,以判斷是否達到滅菌所需要求。
該原理是將一定量已知耐熱參數的耐熱孢子接入被滅菌的物品中,在預定的滅菌條件下滅菌,以驗證滅菌是否達到要求。常用的生物指示劑為嗜熱脂肪芽孢桿菌Bacillusstereathernophilus,其常規微生物耐熱參數值為121℃(1.5min~3.0min)。
物理驗證是對設備滅菌的溫度、壓力等指標進行驗證。就是在滅菌時通過直觀地觀察滅菌全過程的時間、溫度、壓力等相關參數,以判斷是否達到滅菌的要求。化學檢測、生物檢測、物理檢測這三種方法有著各自不同的目的和意義,因此不可互相替代,應互相結合使用。
3 SHINVAXG1.DWT型脈動真空滅菌柜的非脈動滅菌(液體程序)和脈動滅菌(織物程序)原理及實例
3.1 脈動滅菌(液體程序) 模式下的滅菌及滅菌效果驗證
非脈動滅菌(液體程序)模式下的滅菌主要是依靠蒸汽的重力,當純蒸汽進入內室時將內室的冷空氣從排氣口逐漸置換出去,使內室溫度逐漸升高,盡可能減少溫度死角,從而達到滅菌目的。
將待高壓驗證的MEM溶液分別分裝在帶有棉塞的1.5萬mL血清瓶中,每瓶建議分裝5000mL~6000mL,分裝完后用一層硫酸紙和兩層牛皮紙包扎瓶口并裝鍋,滅菌柜建議裝量是單層滿載量的50%~100%。
滅菌溫度:116℃~120℃。滅菌時間:900s~1800s。置換時間:2400s。內室壓力限度:93kPa~115kPa。
注意事項如下。1)用1.5萬mL血清瓶盛裝MEM溶液時為保證滅菌效果,不宜裝量太多,5000mL~6000mL為宜,瓶口一定要使用透氣的棉塞外加硫酸紙和牛皮紙包扎或使用無紡布包扎,切勿使用橡膠膠塞密封瓶口,防止因溶液高壓時瓶內液體體積膨脹而發生爆瓶或蹦塞現象,影響滅菌效果。2)容器內液體裝量建議不超過容器容積的80%。3)使用液體程序對MEM溶液進行滅菌時,在排汽結束后嚴禁開真空泵抽空,避免發生爆瓶及液體沸騰。4)液體程序置換時間的設定宜長不宜短,如果置換時間設置過短,將影響MEM溶液的升溫,進而可能會導致溶液滅菌不徹底。5)使用液體程序滅菌時,滅菌結束后請確認內室壓力略低于當地大氣壓(建議參考設備安裝時廠家設定的滅菌柜在開門狀態下屏幕顯示的內室壓力值為準)時再開門,防止高壓后的液體因內外壓差過大,導致蹦塞或溶液飛濺,影響滅菌結果。6)滅菌結束點開門,等真空泵運行結束后請勿立即開大鍋門,等待5min~10min再開大鍋門,要給高壓鍋內外留有一定的緩沖時間。
備注說明:下面滅菌效果驗證中使用的3種無菌檢驗用培養基分別按各自培養基的使用說明配制并分裝在6分管中,每支分裝6mL~8mL,蓋上膠塞經116℃,1800s高壓滅菌后無菌檢驗合格備用。
檢驗過程:將高壓滅菌后的MEM溶液(在室溫放置24h,然后移至層流罩(局百環境)下用5mL無菌注射器取樣,并分別接種硫乙醇酸鹽流體培養基2支、 胰酪大豆胨液體培養基1支和酪胨瓊脂培養基2支,每支接種0.2mL,分別在25℃(硫乙醇酸鹽流體培養基、 胰酪大豆胨液體培養基和酪胨瓊脂培養基各一支)和37℃(硫乙醇酸鹽流體培養基和酪胨瓊脂培養基各一支)條件下培養7天,每天觀察并記錄檢驗結果。
檢驗結果:觀察7天,無菌檢驗培養基中均無菌落生長,無菌檢驗合格。
檢驗過程:在高壓滅菌后的 MEM 溶液中加10%胎牛血清后貼壁培養MDBK細胞,并37℃培養3天,每天觀察細胞是否染菌。檢驗結果:3天后細胞生長良好,顯微鏡鏡檢細胞輪廓清晰,視野干凈,未見雜菌。
在高壓滅菌MEM溶液時選擇3個溫度可能最低的點分別放置生物指示劑,常用的生物指示劑嗜熱脂肪芽孢桿菌Bacillusstereathernophilus,其常規微生物耐熱參數值為121℃(1.5min~3.0min)。一同滅菌,滅菌結束后將滅菌后的生物指示劑及時取出并置于56℃培養箱中培養 48h,隨后取出培養后的生物指示劑, 觀察安瓿的內容物顏色,并與生物指示劑照片進行比較觀察。檢驗結果:48h培養后的生物指示劑顏色呈紫紅色且澄清, 說明該滅菌過程可有效殺滅孢子菌。
重復上述驗證,連續三次,結果均符合要求。
3.2 脈動滅菌(織物程序) 模式下的滅菌及滅菌效果驗證
采用機械強制脈動真空的排除方式, 程序運行后,首先進入的是脈動階段,真空泵運轉將設備內室氣體及冷凝水經抽空閥由真空泵抽出。當內室壓力達到脈動下限時,抽空閥關閉,停止抽空。當內室壓力達到脈動上限時,抽空閥再次開啟,又開始抽真空。這樣直至達到設定脈動次數。脈動次數達到后,抽空閥關閉,真空泵停止。經多次抽真空多次注入蒸汽,徹底消除滅菌室內的冷點,保證了可靠的滅菌效果。一般一次完整的滅菌程序建議脈動三次:一般情況,脈動上限為80kPa,脈動下限為-80kPa。抽空一次,排出量為80%;當抽空二次時,排出量為96%;當抽空三次時,排出量理論值可達99.2%。
將待高壓驗證的丁基膠塞分別分裝在無紡布袋中,每袋建議裝500~1000個,分裝完后用線繩捆扎無紡布袋口并裝鍋,滅菌柜建議裝量是單層滿載量的50%~100%。
滅菌溫度:121℃;滅菌時間:3600s;脈動次數:3次;干燥脈動次數:2次;干燥上限設定:+60kPa;干燥下限設定:-60kPa;干燥上限等待時間:60s;干燥下限等待時間:60s;內室壓力限度:11kPa~120kPa。
注意事項如下。1)丁基膠塞用自制的無紡布袋盛裝,裝量不宜太大,太大會影響滅菌效果,建議每袋500~1000個為宜。2)裝鍋時請勿靠近高壓鍋兩側的進汽口,離進汽口太近影響升溫。3)裝鍋時請勿堵塞前后門附近的排汽口,防止高壓時冷凝水不能及時排出而導致開鍋后濕包。4)裝鍋時盛裝丁基膠塞的無紡布袋不宜過于堆積,堆積過多將影響中間物品的滅菌效果,建議盛裝高壓鍋單層容量的50%~100%。
檢驗過程:將高壓滅菌后的丁基膠塞取一袋置于層流罩(局百環境)下,無菌取袋子中央的一個膠塞置于提前無菌過濾備用的10%血MEM溶液瓶中,蓋好瓶蓋上下顛倒搖勻3min~5min,再用5mL無菌注射器取樣,并分別接種硫乙醇酸鹽流體培養基2支、 胰酪大豆胨液體培養基1支和酪胨瓊脂培養基2支,每支接種0.2ml,分別在25℃(硫乙醇酸鹽流體培養基、 胰酪大豆胨液體培養基和酪胨瓊脂培養基各一支)和37℃(硫乙醇酸鹽流體培養基和酪胨瓊脂培養基各一支)條件下培養7天,每天觀察并記錄。檢驗結果:觀察7天,無菌檢驗培養基中均無菌落生長,無菌檢驗合格。
檢驗過程:用方法一中使用的10%血MEM溶液貼壁培養MDBK細胞,并37℃培養3天,觀察細胞是否染菌。檢驗結果:3天后細胞生長良好,顯微鏡鏡檢細胞輪廓清晰,視野干凈,未見雜菌。
在高壓滅菌丁基膠塞時選擇3個溫度可能最低的點分別放置生物指示劑(常用的生物指示劑嗜熱脂肪芽孢桿菌Bacillusstereathernophilus,其常規微生物耐熱參數值為121℃(1.5min~3.0min))。一同滅菌,滅菌結束后將滅菌后的生物指示劑及時取出并置于56℃培養箱中培養 48h,隨后取出培養后的生物指示劑, 觀察安瓿的內容物顏色,并與生物指示劑照片做比較觀察。檢驗結果:48h培養后的生物指示劑顏色呈紫紅色且澄清,說明該滅菌過程可有效殺滅孢子菌。
重復上述驗證,連續三次,結果均符合要求。
4 SHINVAXG1.DWT型脈動真空滅菌柜的非脈動滅菌和脈動滅菌模式的不同對比
4.1 升溫方式不同
非脈動滅菌模式下的程序升溫主要是通過改變滅菌程序參數里的置換時間來實現的,置換是在純蒸汽進入內室時通過重力將內室的冷空氣從排汽口逐漸置換出去,使內室溫度升高,盡可能減少溫度死角,置換時間的長短跟待滅菌物品的負載量有關,也跟待滅菌物品的導熱性能有關,要綜合考慮,根據負載量以及內室疏水溫度達標的時長(溫度達到 100℃~105℃,且疏水溫度不再波動)設定置換時間。
采用非脈動滅菌模式下的置換方式升溫較緩慢,主要適用于升溫較慢的液體培養基或用硫酸紙和牛皮紙包扎的桶瓶等用品用具的滅菌。
主要是通過脈動真空泵反復抽至真空實現的,真空泵運轉將設備內室氣體及冷凝水經抽空閥由真空泵抽出,抽真空后內室再注入純蒸汽,從而實現內室升溫的目的,徹底消除滅菌室內的冷點,保證了可靠的滅菌效果。一般情況,脈動上限為80kPa,脈動下限為-80kPa。抽空一次,排出量為80%;當抽空二次時,排出量為96%;當抽空三次時,排出量理論值可達99.2%,所以建議一次完整的滅菌程序一般脈動三次。
脈動式滅菌模式下的脈動式升溫速度較快,主要適用于可以快速升溫的物品,例如制藥行業分裝用丁基膠塞、無菌服、陶瓷泵等滅菌。
4.2 夾層與內室的排汽方式不同
非脈動滅菌模式下的液體程序,在滅菌過程結束后,慢排疏水閥打開,內室蒸汽經過慢排疏水閥慢速排出,使內室壓力緩慢下降,從而防止爆瓶和液體過度沸騰溢出,達到內室排汽的目的。
該模式下的滅菌階段結束后,程序轉入排汽階段。排汽氣動閥打開,開始排汽。當內室壓力下降到一定程度時,冷凝水閥打開,開始進水;真空泵開始運轉,使排汽速度加快。
5 使用脈動真空滅菌柜需要注意的其他事項
需要注意的其他事項如下。1)使用前需要檢查電器箱上方是否有液體滴漏,防止人員觸電。2)關鍋門時應將門輕輕推至與前封板靠近的位置,再按下關門按鈕,切勿用力過猛,防止撞壞行程開關。3)關門時要密切關注門升降情況,如有異常,立即取消操作(取消操作只需再次按壓同一按鈕),查看故障原因,并排除。4)脈動真空滅菌柜屬于特種設備,相關人員必須持證上崗。
6 結語
脈動真空滅菌柜在制藥行業扮演著非常重要的角色,如何規范、正確、高效地使用該設備非常重要,每個基層管理人員和專業操作人員必須熟練掌握。隨著GMP要求的不斷提高,設備也在不斷更新換代,這就要求設備使用人員要與時俱進,不斷學習和總結,提高自身的理論水平和專業技能。

