阻塞性睡眠呼吸暫停低通氣綜合征患者血清腫瘤壞死因子-α、白細胞介素-6水平的檢測及臨床意義
王越
(谷城縣人民醫院,谷城,441700)
阻塞性睡眠呼吸暫停低通氣綜合征(Obstructive Sleep Apnea-Hypopnea Syndrome,OSAHS)是臨床較為常見的睡眠呼吸疾病,臨床目前對其病因尚未有明確定論,上氣道組織黏液性水腫、肥胖等因素被認為與OSAHS發病有密切關聯,臨床表現主要有白天嗜睡,夜間睡眠出現反復上氣道阻塞,從而引起打鼾、睡眠中發生呼吸暫停等表現[1]。由于患者呼吸暫停引起夜間高碳酸和低氧癥反復發作,可導致冠心病、高血壓及糖尿病等心腦血管疾病,嚴重者出現夜間猝死,因此OSAHS有潛在的致死性,嚴重影響患者生命質量及生命健康。相關研究表明,患者體內的炎癥反應因子水平與血管病變有著重要的關聯性,而有效的臨床治療能夠改善患者體內炎性因子水平的異常狀態。本研究通過對病例進行對照比較,對OSAHS患者白細胞介素-6(IL-6)與血清腫瘤壞死因子-α(TNF-α)水平進行監測,從而探究TNF-α與IL-6水平于OSAHS患者病情程度及心腦血管疾病的相關性。現將結果報道如下。
1 資料與方法
1.1 一般資料 選取2017年3月至2019年7月谷城縣人民醫院收治的OSAHS患者90例作為研究對象,按照病情程度分為輕度、中度、重度各30例,并選擇同期收治的單純鼾癥患者30例作為研究對象,OSAHS患者中男65例,女25例;年齡27~48歲,平均年齡(39.45±14.36)歲;按照病情程度分為輕度、中度、重度各30例。單純鼾癥組中男20例,女10例;年齡26~46歲,平均年齡(38.59±12.69)歲。OSAHA中度、重度患者中,按照是否進行經鼻持續氣道正壓通氣(nCAPA)治療,分為觀察組(n=40)和對照組(n=20)。2組患者一般資料經比較,差異無統計學意義(P>0.05),具有可比性。
1.2 納入標準 1)患者經臨床診斷,病情符合OSAHS相關診斷標準,確診為OSAHS患者。2)患者對本研究知情并簽署研究知情同意書,自愿參與本研究。3)研究前未接受過OSAHS的相關針對性治療。
1.3 排除標準 1)研究近期(3個月內)有創傷史或手術史,應用過免疫抑制劑及激素、自由基清除劑等藥物者。2)合并感染性疾病、凝血功能疾病及其他血液系統疾病、神經肌肉障礙性疾病等患者[2]。
1.4 研究方法
1.4.1 多導睡眠監測 對受試者進行整晚7 h連續多導睡眠監測,監測項目包括:眼動、口鼻氣流、腦電圖、心電、鼾聲、胸腹運動、動脈血氧飽和度等。記錄指標包括:最低血氧飽和度(Min SpO2)、平均血氧飽和度(Mean SpO2)、夜間血氧飽和度<90%時長(tSpO2<90%)等。
1.4.2 血清標本采集與測定 于清晨睡眠監測結束覺醒后,受試者平臥10 min并采取靜脈血5 mL待檢。待標本凝固后常規離心處理,轉數設置為3 000 r/min,離心15 min。血清分離后取上清部分,置于-80 ℃的環境中保存。采血過程嚴格遵守無菌操作,標本無溶血現象。采用酶聯免疫吸附試驗(ELISA)法對血清中IL-6與TNF-α水平進行測定。
1.4.3 心腦血管疾病確定 根據患者提供的病史資料、體格檢查、常規心電圖、動態心電圖、動態血壓、心臟彩超等檢查結果為依據,患者符合高血壓、缺血性心臟病、心力衰竭、腦血管意外等疾病。
1.4.4 nCPAP治療 對40例中度及重度患者進行為期2個月的nCPAP治療,治療前對患者進行健康知識宣講,提升其治療配合性,以壓力滴定結果為依據進行治療壓力的確定,以能消除90%~95%以上的呼吸暫停的壓力為初始治療通氣壓力,后根據患者病情調整壓力,以保證夜間血氧飽和度在90%以上的最小壓力,且患者可耐受的程度為最終治療壓力。
1.5 觀察標準 對患者Min SpO2、Mean SpO2、tSpO2<90%、IL-6與TNF-α等指標進行監測與比較。
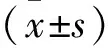
2 結果
2.1 不同病情程度的OSAHS患者各項生理學指標比較 MeanSpO2、MinSpO2、tSpO2<90%、IL-6、TNF-α等指標水平各組比較,差異有統計學意義(P<0.05)。其中重度OSAHS患者的IL-6、TNF-α水平最高,而單純鼾癥最低,中度及重度患者之間比較,差異無統計學意義(P>0.05)。單純性鼾癥患者MeanSpO2、MinSpO2水平最高,而重度OSAHS患者最低;心腦血管疾病發生率以重度患者最高,單純性鼾癥最低,二者比較,差異有統計學意義(P<0.05)。見表1。
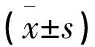
表1 不同病情程度的OSAHS患者各項生理學指標比較
2.2 中度及重度OSAHS患者治療前后各指標比較 治療前,觀察組與對照組的IL-6、TNF-α水平無明顯差異,治療后,觀察組患者兩項水平有顯著降低,而對照組患者兩項指標的水平較2月前無明顯變化,差異有統計學意義(P<0.05)。見表2。

表2 中度及重度OSAHS患者治療前后各指標比較
3 討論
OSAHS患者的低氧是間歇性的,這個過程與缺氧-再灌注損傷有相似性,也是OSAHS靶器官損傷的主要機制。有研究表示,OSAHS患者通常存在高TNF-α、高IL-6血癥,而TNF-α、IL-6是導致人體內炎癥反應的代表性炎癥介質,其在動脈粥樣硬化及代謝綜合征的發病中可能起著重要作用,與糖尿病、心腦血管病以及高脂血癥等疾病存在密切關聯[3]。本研究中發現,OSAHS患者血清中的TNF-α、IL-6水平隨著患者病情嚴重程度的加強而升高,與患者臨床癥狀嚴重程度呈正相關,提示OSAHS患者血清中炎癥介質水平的異常可能與其夜間反復多次發生的低氧血癥以及呼吸暫停有相關性;另外,本研究結果提示,患者體內TNF-α、IL-6水平越高、癥狀越嚴重,發生心腦血管疾病的概率也越高;因此采取合理有效的治療措施,或能改善患者體內炎癥介質的異常表現,從而預防和控制心腦血管疾病的發生。
本研究從OSAHS中度及重度患者中選取了40例進行治療,研究結果表示,接受相關治療的患者在治療后其TNF-α、IL-6水平明顯降低,而未接受治療的患者各項指標水平卻未見明顯差異,提示有效的治療能夠顯著改善患者體內TNF-α、IL-6水平的降低,從而減少患者發生心腦血管疾病的概率。
綜上所述,血清TNF-α、IL-6水平的監測對于OSAHS患者有重要意義,通過炎性因子水平的監測可對患者預后進行評估,從而采取有針對性的治療措施,降低其心腦血管疾病的發生。

