復合凝膠球對水中結晶紫的吸附特性
陸硯秋,周 俊,吳慧芳,吳艷霞
(南京工業大學城建學院,江蘇南京 211816)
中國是染料生產大國,各類染料在紡織、皮革、造紙、油墨等工業領域中被長期廣泛使用[1]。三苯甲烷類染料屬于多環芳烴化合物,目前已經發展成為繼偶氮、蒽醌染料之后使用量較多的合成染料[2]。結晶紫是常用的三苯甲烷類染料之一,分子結構復雜、穩定性高,排入水體后,可生化性低、色度高、難降解,嚴重威脅人體健康,具有潛在的環境危害性[3]。國內外主要利用物理、化學、生物法處理含結晶紫染料的廢水[4]。物理吸附法具有規模小、操作簡單、經濟效益高等優點,在深度處理低濃度染料廢水領域得到了較廣泛的應用[5]。
海藻酸鈉(SA)屬于天然高分子多糖類聚合物,可以與除汞、鎂以外的二價及以上金屬離子絡合形成海藻酸鹽水凝膠[6]。近年來,有研究者將碳材料、氧化物、有機物、礦物元素等固定在海藻酸鹽水凝膠的三維網狀結構內部制備復合凝膠球,對染料有良好的吸附作用[7]。殼聚糖(CTS)是一種天然堿性多糖,分子鏈上的羥基、氨基等活性基團可以通過靜電吸引、氫鍵等作用去除染料[8],但單獨使用殼聚糖時存在耐酸性差、易軟化流失等問題,在實際應用中受到一定限制。因此,可以將海藻酸鈉與殼聚糖結合,制備一種高效、環保、經濟的復合吸附劑。生物炭具有比表面積大、官能團豐富、穩定性高等優點[9],但直接用于吸附時易飛散,且難以回收再利用。本實驗以海藻酸鈉、玉米秸稈生物炭、殼聚糖為原料,制成海藻酸鈉/生物炭/殼聚糖復合凝膠球(SA/BC/CTS),以堿性三苯甲烷類染料結晶紫模擬的低質量濃度染料廢水作為研究對象進行靜態吸附實驗,并結合動力學方程與吸附等溫模型分析吸附劑結構與吸附性能之間的關系,以期為SA/BC/CTS 應用于三苯甲烷類染料廢水的處理研究提供參考依據。
1 實驗
1.1 材料
海藻酸鈉[(C6H7O6Na)n,化學純]、無水氯化鈣(CaCl2,分析純)、殼聚糖[(C6H11NO4)n,脫乙酰度80%~95%,生物試劑](國藥集團化學試劑有限公司),冰乙酸(CH3COOH,分析純,上海申博化工有限公司),結晶紫[C25H30ClN3,分析純,阿拉丁試劑(上海)有限公司],生物炭(將500 ℃恒溫熱解制備的玉米秸稈生物炭用去離子水煮沸3 次,去除粉塵和表面的殘留物,過濾后放入烘箱中100 ℃烘干至恒重,過120 目篩,避光干燥儲存),1%殼聚糖溶液(將1 g 殼聚糖溶解在100 mL 1%乙酸溶液中,攪拌至溶液澄清)。
1.2 儀器
T6 新世紀紫外-可見分光光度計(北京普析通用儀器有限責任公司),SHA-C 型恒溫振蕩器(常州智博瑞儀器制造有限公司),HH-6 數顯恒溫水浴鍋(常州國華電器有限公司),FA2104 型電子分析天平(常州市幸運電子設備有限公司),pH400 基礎型臺式pH計[安萊立思儀器科技(上海)有限公司],SU8010 日立掃描電子顯微鏡(上海西努光學科技有限公司),賽默飛iS5 傅里葉變換紅外光譜儀(天津博天勝達科技發展有限公司)。
1.3 復合凝膠球的制備
在100 mL 去離子水中加入2 g 海藻酸鈉與1 g 生物炭,在55 ℃水浴中加熱攪拌約30 min 至混合均勻,冷卻至室溫后,在10 cm 高度處用10 mL 注射器勻速滴入3%CaCl2溶液中,邊滴邊攪拌,防止凝膠球粘連,滴完后繼續攪拌30 min 使凝膠球硬化,放入4 ℃冰箱,靜置交聯4 h,濾出小球,用去離子水沖洗3 次,放入1%殼聚糖溶液中勻速攪拌10~15 min,濾出小球,用去離子水沖洗3 次,得到復合凝膠球SA/BC/CTS,密封放入4 ℃冰箱保存。
1.4 吸附實驗
將一定量SA/BC/CTS 加入50 mL 結晶紫染料溶液中,在30 ℃條件下于恒溫振蕩器中以150 r/min 振蕩吸附一定時間。將反應后的溶液過0.45 μm 濾膜,在最大吸收波長590 nm 處利用分光光度法測定吸光度,再利用標準工作曲線(y=0.239 4x-0.036 7,R2=0.999 7)計算溶液中結晶紫的質量濃度。按下式計算SA/BC/CTS 的吸附量和去除率:

式中:ρ0、ρe分別為初始、吸附平衡時染料的質量濃度,mg/L;V為吸附反應中溶液的體積,L;m為復合凝膠球的質量,g。
1.5 測試
SEM:對SA/BC/CTS 進行噴金處理后,再利用掃描電鏡進行觀察。
紅外光譜:將吸附結晶紫前后的SA/BC/CTS 真空干燥,研成粉末,過200 目篩,采用溴化鉀壓片制樣,利用紅外光譜儀測試,掃描范圍4 000~400 cm-1,掃描次數32,分辨率4 cm-1。
2 結果與討論
2.1 表征
2.1.1 SEM
由圖1 可看出,濕態SA/BC/CTS 的外觀呈黑色球狀,無粘連、拖尾現象,粒徑均勻,直徑為3.0~3.5 mm。

圖1 SA/BC/CTS 的外觀及掃描電鏡圖
SA/BC/CTS 表面包裹著由海藻酸鈉的羧基與殼聚糖的氨基通過靜電作用形成的聚電解質膜[10],所以從掃描電鏡圖中可以觀察到SA/BC/CTS 表面交錯分布著褶皺結構,增大其比表面積,有利于吸附。剖面圖中,生物炭均勻地分布在SA/BC/CTS 內部,具有骨架支撐作用,使內部呈現三維網絡結構,增加了活性位點,同時也增強了機械強度。
2.1.2 紅外光譜
由圖2可以看出,SA/BC/CTS含有豐富的官能團,3 386 cm-1處強而寬的吸收譜帶由羥基O—H 與亞氨基N—H 重疊而成,2 926 cm-1處的吸收峰對應C—H的振動,1 088 cm-1處為C—O 的伸縮振動峰,1 033 cm-1處為C—O—C 的伸縮振動峰。因為海藻酸鈉引入了多電子的共軛體系—COO-,所以在1 606、1 423 cm-1處出現羧酸根—COO-的反對稱伸縮振動峰和對稱伸縮振動峰。SA/BC/CTS 吸附結晶紫后,在2 926、1 088、1 033 cm-1等處的吸收峰與吸附前相比振動強度減弱,3 386 cm-1處的吸收峰偏移至3 357 cm-1處,1 606 cm-1處的吸收峰偏移至1 627 cm-1處,1 423 cm-1處的吸收峰偏移至1 400 cm-1處,表明O—H 與—COO-均參與了SA/BC/CTS 對結晶紫的吸附過程,證實整個過程存在化學吸附。
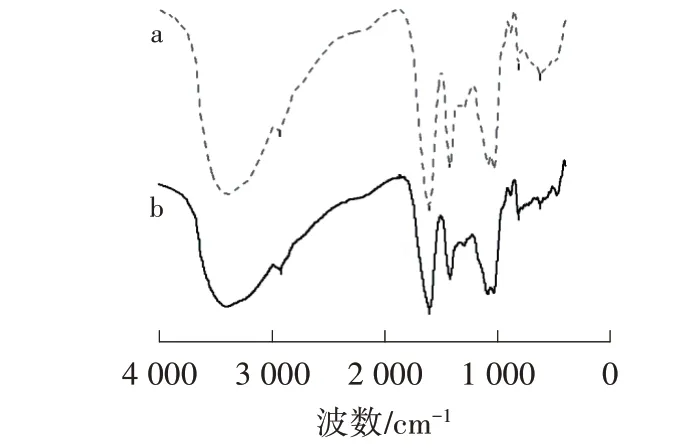
圖2 SA/BC/CTS 吸附前(a)后(b)的紅外光圖譜
2.2 復合凝膠球吸附結晶紫的影響因素
2.2.1 pH
由圖3 可以看出,當pH 為2 時,SA/BC/CTS 對結晶紫的去除率僅為42.55%。隨著pH 增加到5,結晶紫去除率的上升趨勢顯著,但是仍然不足90%。可能是由于當pH 較小時,溶于水呈陽離子狀態的結晶紫與溶液中的H+競爭SA/BC/CTS 上的活性吸附位點,去除率較低。當pH 大于6 時,去除率穩定在90%左右,可能是由于當溶液pH 較大時,SA/BC/CTS 分子鏈上的羧基解離程度提高,大量—COO-可以通過靜電吸引、離子鍵等作用與染料分子結合。因此,SA/BC/CTS適用于溶液pH 為6~10 的吸附體系,后續實驗中溶液pH 選擇6。
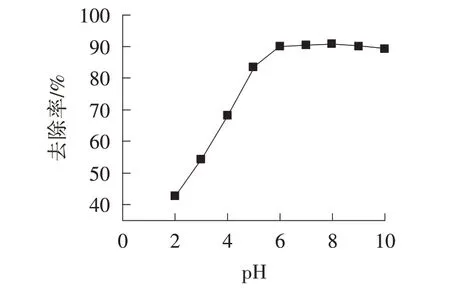
圖3 pH 對去除率的影響
2.2.2 SA/BC/CTS 質量濃度
由圖4 可看出,當SA/BC/CTS 質量濃度從2 g/L 增加至12 g/L 時,溶液中的染料分子獲得更多的活性吸附位點,結晶紫的去除率由78.22%增加到91.87%。當質量濃度超過6 g/L 后,因為溶液中的染料分子數量有限,過量的吸附劑不能被充分利用,大量活性位點處于不飽和狀態,去除率變化趨勢減緩。為了更加高效合理地利用資源,后續實驗中SA/BC/CTS 質量濃度選擇6 g/L。

圖4 SA/BC/CTS 質量濃度對去除率的影響
2.2.3 吸附時間
由圖5 可以看出,0~120 min 時,SA/BC/CTS 對結晶紫染料的去除率隨著時間的延長而提高,且上升趨勢明顯。
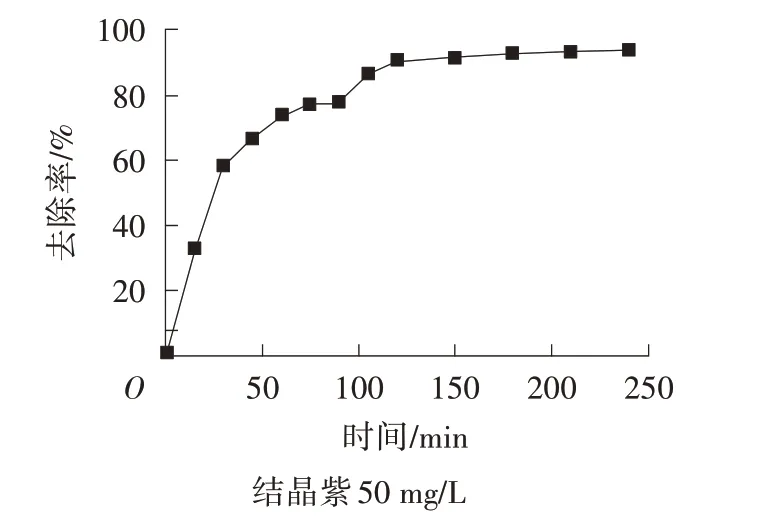
圖5 吸附時間對去除率的影響
120 min 時,SA/BC/CTS 對結晶紫染料的去除率達到90.5%,120 min 后,去除率上升趨勢減緩。吸附初期,SA/BC/CTS 表面可供結晶紫染料分子吸附的活性位點較多,在濃度梯度的作用下,染料分子迅速向SA/BC/CTS 表面擴散,與活性基團發生反應后占據吸附空位,所以去除率迅速上升。吸附后期,SA/BC/CTS表面大多數空位已經被占據,染料溶液的質量濃度降低,染料分子穿過固/液界面的推動力減小,去除率增長速度減緩,最終達到吸附動態平衡狀態[11]。因此吸附時間選擇120 min。
2.2.4 染料初始質量濃度
由圖6 可知,隨著結晶紫染料初始質量濃度從10 mg/L 增加至150 mg/L,SA/BC/CTS 對結晶紫的去除率由91.88%下降到85.51%。其原因可能是染料初始質量濃度越大,染料分子與復合凝膠球表面的吸附活性位點接觸的概率增加,但吸附位點數量有限,完全被占用后,去除率不再發生明顯變化[12]。當結晶紫染料初始質量濃度為10~70 mg/L 時,SA/BC/CTS 的吸附效果較好。因此,在實際應用中,SA/BC/CTS 主要適用于低質量濃度染料廢水的處理。
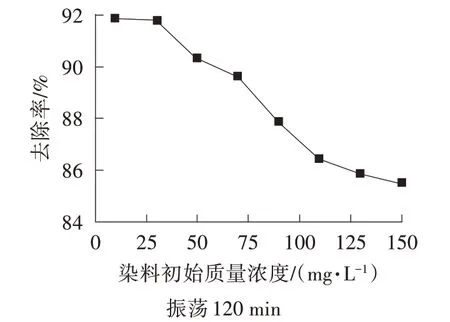
圖6 染料初始質量濃度對去除率的影響
2.3 吸附動力學
將50、100 mg/L 結晶紫溶液pH 調節至6,然后加入6 g/L SA/BC/CTS,在30 ℃下以150 r/min 恒溫振蕩,考察吸附時間對SA/BC/CTS 吸附結晶紫的影響。將實驗數據分別用準一級動力學模型以及準二級動力學模型(公式[13]如下)進行擬合,結果如圖7 所示,擬合參數見表1。
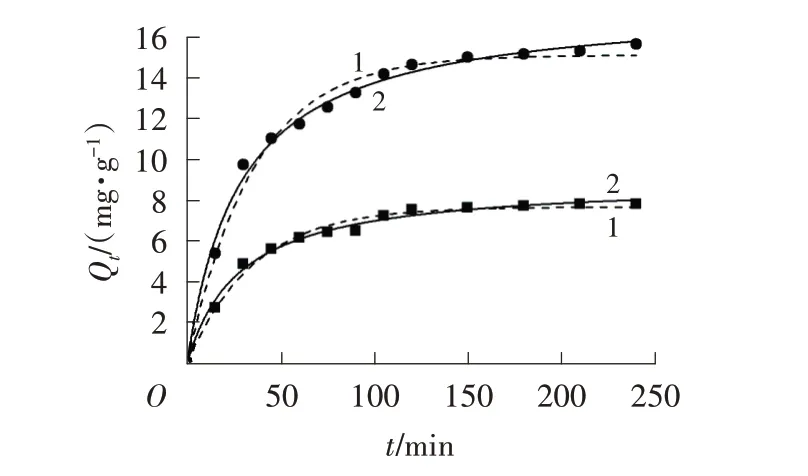
圖7 動力學模型非線性擬合圖
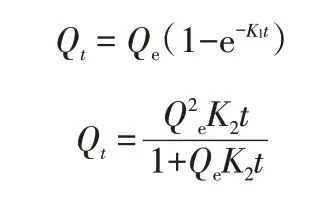
式中:Qt、Qe分別為t時刻、吸附平衡時的吸附量,mg/g;K1為準一級動力學反應速率常數,min-1;K2為準二級動力學反應速率常數,g/(mg·min)。
由表1 可知,準二級動力學模型的R2值均大于準一級動力學模型,可以判斷SA/BC/CTS 對結晶紫的吸附行為更符合準二級動力學模型。所以SA/BC/CTS吸附結晶紫的過程是以單分子層形式進行的化學吸附。
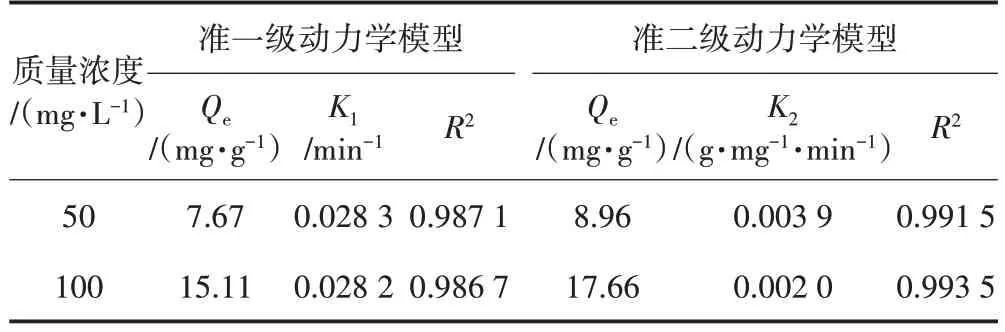
表1 吸附動力學參數
結合SA/BC/CTS 的掃描電鏡圖,考慮到在生物炭的支撐下,SA/BC/CTS 的孔隙率較高,有利于染料分子從SA/BC/CTS 外表面的孔隙擴散進入顆粒內表面,可能會對吸附速率產生影響[14],進一步采用顆粒內擴散方程進行擬合(公式[15]如下),結果如圖8 所示,擬合參數見表2。
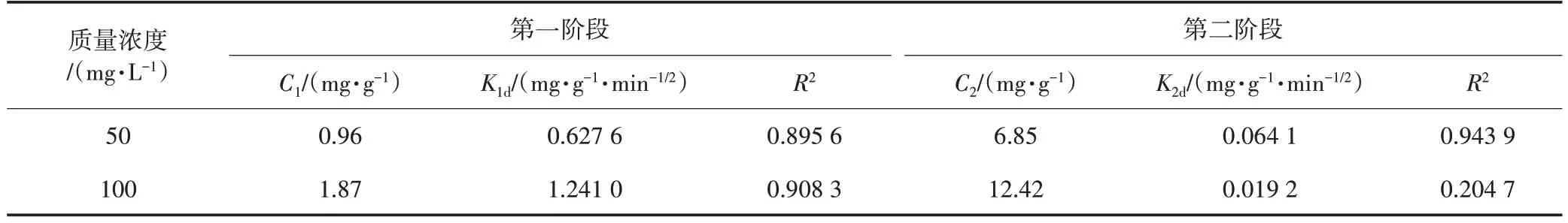
表2 顆粒內擴散動力學參數
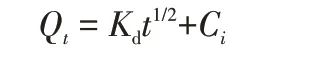
式中:Kd為顆粒內擴散速率常數,mg/(g·min1/2);Ci為與邊界層厚度相關的常數,mg/g。
SA/BC/CTS 對結晶紫的吸附過程可以分為2 個階段:第一階段是吸附反應初期,K1d值較高,吸附速率較快,染料分子從溶液中擴散到SA/BC/CTS 的外表面;第二階段K2d值較低,表明染料分子通過孔隙擴散到SA/BC/CTS 內表面的吸附位點。由圖8可以看出,Qt與t1/2呈現良好的線性關系,說明顆粒內擴散過程是SA/BC/CTS 吸附結晶紫染料的限速步驟,但是第二段擬合直線不通過原點,說明顆粒內擴散過程不是唯一的吸附速率控制步驟[16],吸附速率還會受其他吸附機制的影響。
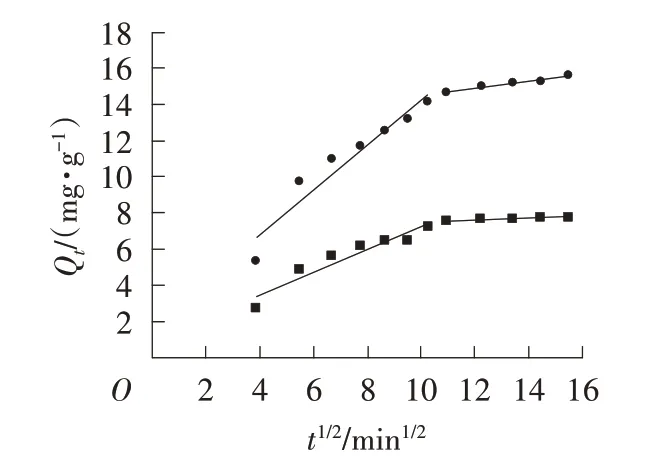
圖8 顆粒內擴散模型擬合圖
2.4 吸附等溫線
配制0~120 mg/L 結晶紫染料溶液,調節pH 至6,加入6 g/L SA/BC/CTS,在不同溫度下以150 r/min 恒溫振蕩,測定SA/BC/CTS 對結晶紫染料的吸附量。利用Langmuir 和Freundlich 2 種吸附等溫模型對實驗所得數據進行擬合(公式[17]如下),擬合結果如圖9 所示,相關參數見表3。
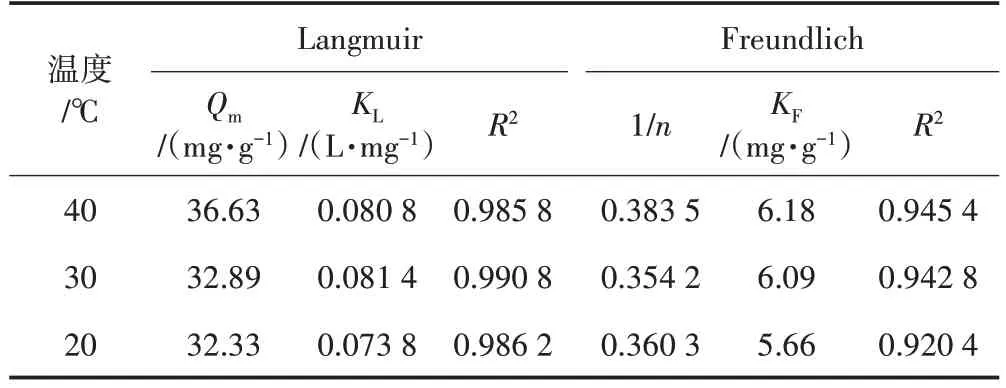
表3 吸附等溫線參數

圖9 吸附等溫線擬合曲線
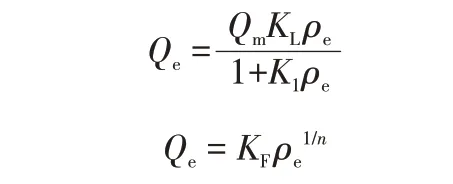
式中:ρe為吸附平衡時染料的質量濃度,mg/L;Qm為飽和吸附量,mg/g;KL為Langmuir 模型常數,L/mg;KF為Freundlich 模型常數,mg/g;n為非均質系數。
由表3中的R2可知,不同溫度下,SA/BC/CTS對結晶紫染料的等溫吸附數據與Freundlich 和Langmuir模型均有良好的相關性,但Langmuir 模型的擬合結果略優于Freundlich,說明SA/BC/CTS 對結晶紫染料的吸附過程同時存在單分子層吸附與多分子層吸附,以單分子層吸附為主。在20、30、40 ℃條件下,由Langmuir 模型計算的飽和吸附量依次為32.33、32.89、36.63 mg/g,與實際吸附所得的平衡吸附量30.00、30.76、34.08 mg/g 比較接近。根據Freundlich 理論,KF可以代表吸附劑的單位吸附能力,1/n可以代表吸附劑的吸附強度,吸附劑的吸附能力由吸附強度決定[18]。由表3 可知,KF隨著溫度升高逐漸減小,說明升高溫度有利于增強SA/BC/CTS 的吸附能力。1/n小于0.5,且n隨著溫度升高變化幅度較小,進一步證實SA/BC/CTS 對結晶紫的吸附較容易進行。
3 結論
(1)復合凝膠球SA/BC/CTS 作為一種新型生物質吸附劑具有多孔結構,表面粗糙,活性基團能與染料結合,同時克服生物炭粉末易飛散、難回收和海藻酸鈣水凝膠機械強度低、易分解等缺點,具有良好的固液分離性能,能夠高效處理含結晶紫染料的低質量濃度廢水。
(2)在SA/BC/CTS 對結晶紫染料的吸附實驗中,當溶液pH 為6~10 時,去除率受pH 影響較小;隨著SA/BC/CTS 質量濃度的增加,去除率上升;吸附體系在120 min 后逐漸接近吸附平衡狀態。在SA/BC/CTS用量為6 g/L、吸附時間為120 min、溶液pH 為6、溫度為30 ℃時,SA/BC/CTS 對結晶紫模擬染料廢水的去除率可以達到90.5%。SA/BC/CTS 對結晶紫的吸附過程符合準二級動力學模型和Langmuir 吸附模型,表明此過程以單分子層吸附為主,且化學吸附過程為吸附速率控制步驟。

