超聲輔助低共熔溶劑提取紅豆杉葉總黃酮工藝的優化
江石平,朱婉萍
(浙江省中醫藥研究院,浙江 杭州 310007)
低共熔溶劑是一種新型溶劑,它是由某些固體有機分子與特定的離子型化合物按照一定比例混合,在室溫下呈液體狀態的低共熔混合物[1],具有低熔點、低成本、低毒性、易制備、能再生、可生物降解等優點[2]。現代研究表明,低共熔溶劑能顯著提高多酚、黃酮、多糖等成分的提取率[3-4],是提取中藥活性成分的理想溶劑。
南方紅豆杉Taxuschinensisvar.mairei是國內特有的紅豆杉科紅豆杉屬植物[5],其葉中成分主要為紫杉萜、黃酮、多糖、生物堿、揮發油等[6],其中黃酮具有抗癌、抗肝臟毒性、抗菌、抗氧化等多種藥理作用[7]。目前,中藥中黃酮類成分的提取溶劑主要是水和有機溶劑[8],但均存在能耗高、制備周期長、提取率低、不夠環保等缺點,故尋找綠色溶劑具有重要意義。本實驗采用超聲輔助提取技術,研究不同低共熔溶劑對總黃酮提取率的影響,并利用響應面對工藝進行優化,以期為該成分開發利用提供參考依據。
1 材料
紫外-可見光分光光度計(型號UV-1800,日本島津公司);電子分析天平(型號Sartorius BS224S,德國賽多利斯公司);超聲清洗器(型號KQ5200DE,昆山市超聲儀器有限公司);磁力攪拌器(型號90-2,常州越新儀器制造有限公司)。
氯化膽堿[阿拉丁試劑(上海)有限公司,批號B1920039];1,4-丁二醇(批號B1807141)、丙三醇(批號170315)、1,3-丁二醇(批號D1726006)、乙二醇(批號20170425)(西隴科學股份有限公司);硝酸鋁(美國Mackin公司,批號C10373927);亞硝酸鈉(批號20140107)、氫氧化鈉(批號20121114)(國藥集團化學試劑有限公司)。蘆丁對照品(中國食品藥品檢定研究院,批號100080-201409)。紅豆杉葉購于寧波泰康紅豆杉生物科技有限公司,經浙江省中醫藥研究院藥用資源研究中心浦錦寶研究員鑒定為南方紅豆杉Taxuschinensisvar.mairei枝葉。超純水為自制。
2 方法與結果
2.1 低共熔溶劑制備 按照1∶1∶1摩爾比精密稱取氯化膽堿-(1,4-丁二醇)-水、氯化膽堿-丙三醇-水、氯化膽堿-乙二醇-水、氯化膽堿-(1,3-丁二醇)-水適量,置于燒杯中,在85 ℃下磁力攪拌器充分攪拌至產生均勻剔透的液體為止,冷卻至室溫,即得。
2.2 線性關系考察 參考文獻[8]報道,精密稱取蘆丁對照品5 mg,置于25 mL量瓶中,65%乙醇定容至刻度,超聲溶解,配制0.2 mg/mL母液,分別精密吸取5、4、3、2、1、0 mL至10 mL量瓶中,65%乙醇定容至5 mL,搖勻,加入5%亞硝酸鈉溶液0.3 mL,搖勻,放置6 min,加入10%硝酸鋁溶液0.3 mL,搖勻,放置6 min,加入4%氫氧化鈉溶液4 mL,65%乙醇定容,搖勻,放置15 min。采用紫外-可見光分光光度計測定蘆丁在200~800 nm波長處的吸光度,發現該成分在508 nm處有最大吸收。以蘆丁質量濃度為橫坐標(X),吸光度為縱坐標(A)進行回歸,得到方程為A=11.958X+0.019(R2=0.999 3),在0.019~0.096 mg/mL范圍內呈良好的線性關系。
2.3 供試品溶液制備 取紅豆杉葉末約0.1 g,精密稱定,加入一定體積不同體積分數(0、12.5%、25%、75%、100%)的低共熔溶劑水溶液,在一定溫度下超聲提取一段時間,0.45 μm微孔濾膜過濾,即得供試品溶液,精密量取0.2 mL,置于10 mL量瓶中,65%乙醇定容5 mL,搖勻,加入5%亞硝酸鈉溶液0.3 mL,搖勻,放置6 min,加入10%硝酸鋁溶液0.3 mL,搖勻,放置6 min,加入4%氫氧化鈉溶液4 mL,再以65%乙醇定容,搖勻,放置15 min,測定吸光度,計算總黃酮提取率,公式為提取率=[(C×V/0.2×N)/M]×100%,其中C為總黃酮質量濃度,V為樣品溶液體積,N為稀釋倍數(10倍),M為樣品質量。
2.4 單因素試驗
2.4.1 低共熔溶劑種類 考察氯化膽堿-(1,4-丁二醇)-水、氯化膽堿-丙三醇-水、氯化膽堿-乙二醇-水、氯化膽堿-(1,3-丁二醇)-水對總黃酮提取率的影響,結果見圖1。由此可知,4種低共熔溶劑的提取率均高于65%乙醇提取,以氯化膽堿-乙二醇-水更明顯,故選擇其作為提取溶劑。

注:DES-1為氯化膽堿-乙二醇-水,DES-2為氯化膽堿-丙三醇-水,DES-3為氯化膽堿-(1,4-丁二醇)-水,DES-4為氯化膽堿-(1,3-丁二醇)-水。圖1 低共熔溶劑種類對總黃酮提取率的影響
2.4.2 低共熔溶劑體積分數 考察0、12.5%、25%、75%、100%對總黃酮提取率的影響,結果見圖2。由此可知,在75%時總黃酮提取率最高,故選擇其作為低共熔溶劑體積分數。

圖2 低共熔溶劑體積分數對總黃酮提取率的影響
2.4.3 液料比 考察10∶1、20∶1、30∶1、40∶1、50∶1對總黃酮提取率的影響,結果見圖3。由此可知,總黃酮提取率隨著液料比增加先顯著升高,后略有降低,在30∶1時最高,故選擇其作為液料比。

圖3 液料比對總黃酮提取率的影響
2.4.4 提取時間 考察30、40、50、60、70 min對總黃酮提取率的影響,結果見圖4。由此可知,提取60 min時提取率最高,故選擇其作為提取時間。
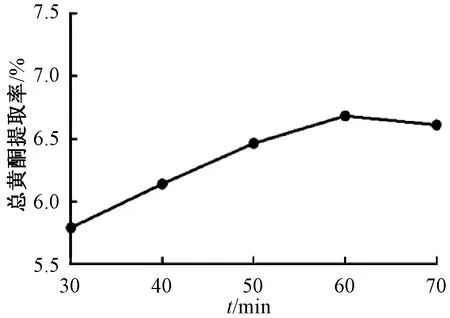
圖4 提取時間對總黃酮提取率的影響
2.4.5 提取溫度 考察30、40、50、60、70 ℃對總黃酮提取率的影響,結果見圖5。由此可知,提取率隨著提取溫度增加先升后降,在60 ℃時最高,故選擇其作為提取溫度。
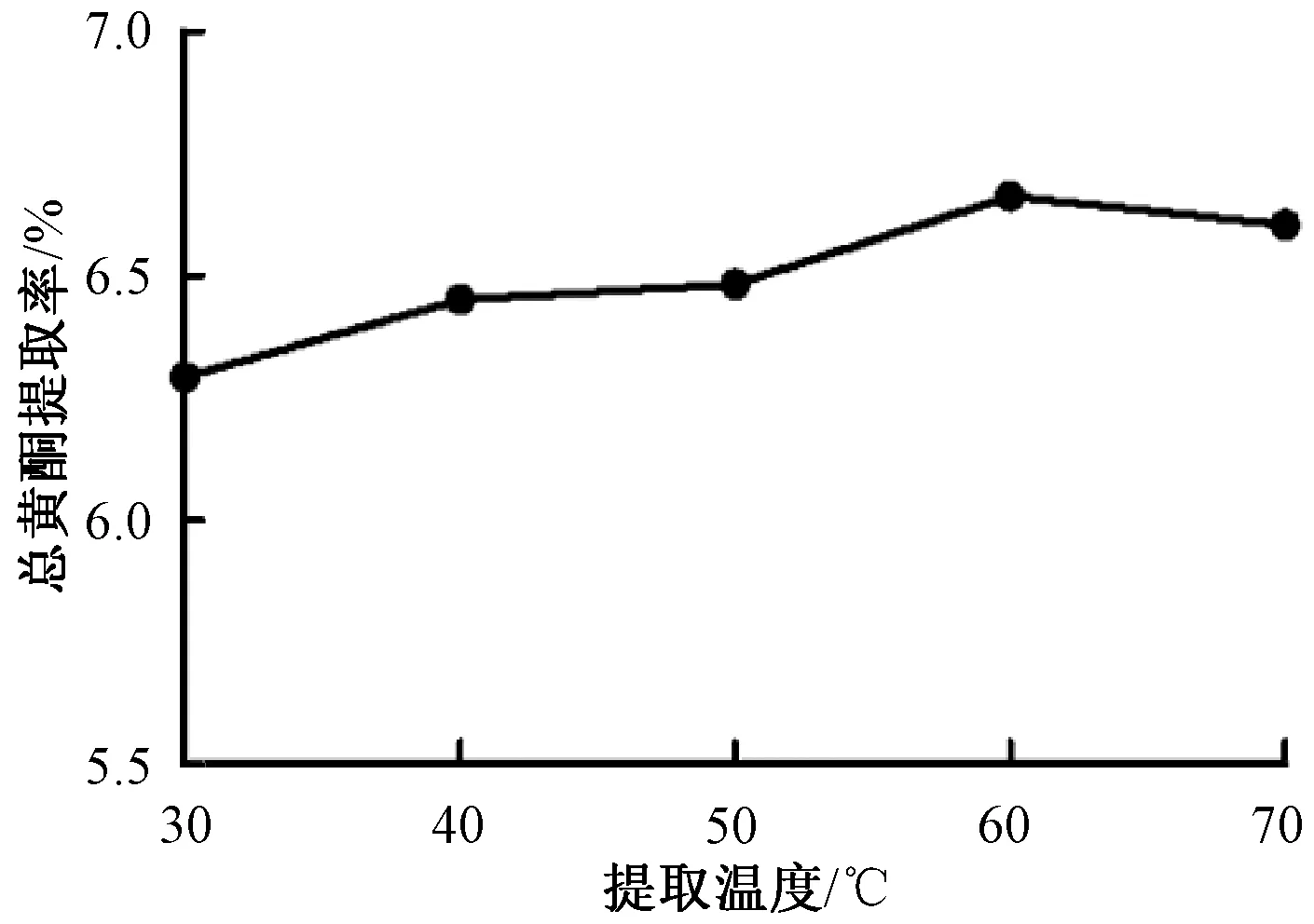
圖5 提取溫度對總黃酮提取率的影響
2.5 響應面試驗 依據單因素試驗結果,選擇對總黃酮提取率影響較大的低共熔溶劑體積分數(A)、液料比(B)、提取時間(C)作為影響因素,總黃酮提取率作為評價指標(Y),依據Box-Behnken設計原理進行3因素3水平試驗,共17組,因素水平見表1,結果見表2。

表1 因素水平
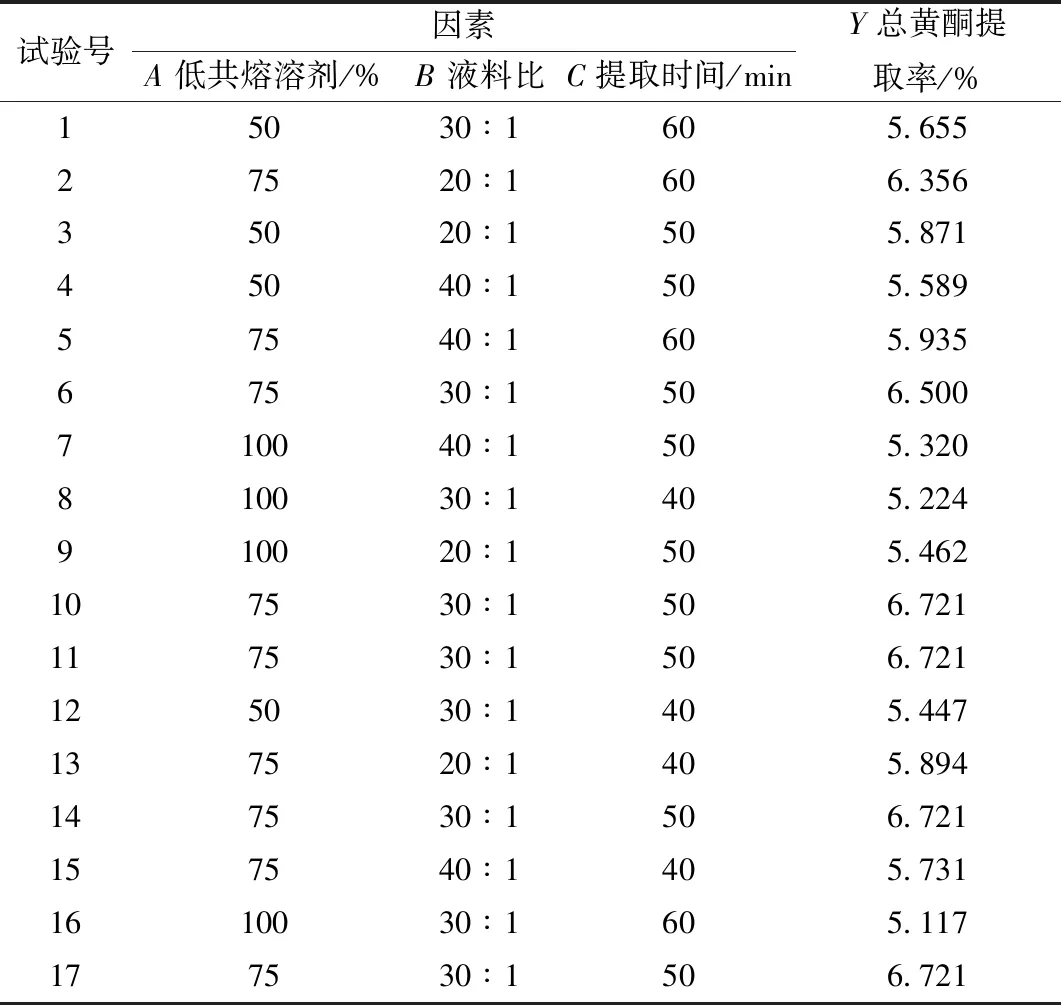
表2 試驗設計與結果
通過Design Expert 8.0.6軟件進行多元回歸擬合,得方程為Y=65.45-1.80A-1.26B+0.96C+0.35AB-0.79AC-0.64BC-8.01A2-1.83B2-3.83C2,方差分析見表3。由此可知,模型P<0.01,具有顯著性差異;失擬項P>0.05,表明模型失擬度不顯著,結果準確可靠;相關系數R2為0.980 8,表明可用該方程解釋98.08%的數據;因素A、B、C、A2、B2、C2對總黃酮提取率均有顯著影響(P<0.05,P<0.01),影響程度依次為A>B>C。
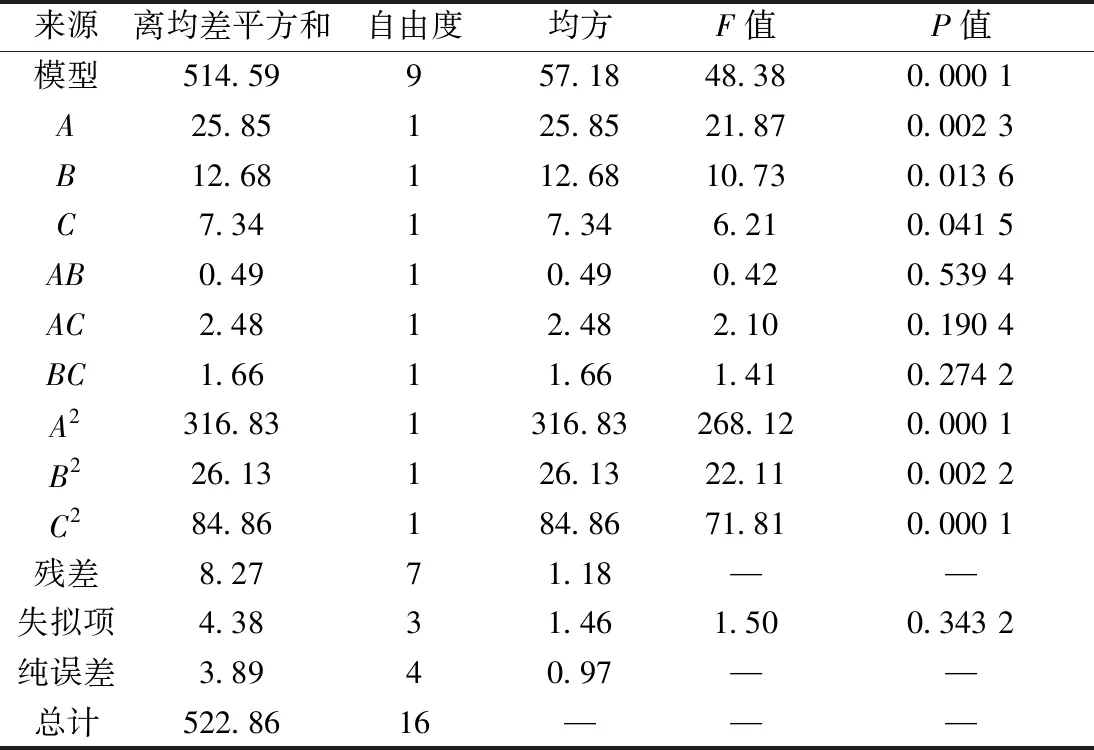
表3 方差分析
響應面分析[9]見圖6。由此可知,隨著液料比、低共熔溶劑體積分數增加,總黃酮提取率先升后降,低共熔溶劑體積分數的變化曲面比液料比陡峭,等高線沿前者方向的變化相對密集,表明它對響應值峰值的影響更大;低共熔溶劑體積分數的變化曲面比提取時間陡峭,表明前者對響應值峰值的影響大于后者;液料比、提取時間的變化曲面坡度相差不大,兩者交互作用不明顯。

圖6 各因素響應面圖
2.6 驗證試驗 根據Design Expert 8.0.6軟件,得到最優工藝為低共熔溶劑體積分數72.13%,液料比27.22∶1,提取時間51.37 min,總黃酮提取率為6.711%,為了后續實驗方便操作,將其修正為低共熔溶劑體積分數72%,液料比27∶1,提取時間51 min。在此優化工藝下進行3批驗證試驗,測得總黃酮平均提取率為6.703%,與預測值6.711%接近,表明該工藝穩定可靠。
3 討論
文獻[10]報道,提取紅豆杉總黃酮最佳提取溶劑為65%乙醇;本實驗發現,與65%乙醇提取比較,4種低共熔溶劑的提取率分別高出23.17%、16.34%、19.07%、17.76%,表明低共熔溶劑可顯著提高總黃酮提取率,其原因可能是它對植物細胞壁有較強的破壞作用[11],并且具有一定黏度,有利于紅豆杉葉粉末懸浮分散在溶劑中,增大接觸面積,從而更有利于黃酮流出。結果表明,低共熔溶劑種類不同,提取率升高程度有所差異,以丙二醇最明顯,推測可能是其本身溶解性、黏性、導電性等物理性質的差異所致。
另外,低共熔溶劑體積分數對總黃酮提取率也有顯著影響,其較高時溶液比較黏稠,不利于進入紅豆杉葉基質內部,導致提取率下降;當加入一定量水后,可顯著降低黏度,使其更好地滲入到基質內部,破壞細胞壁,促進黃酮流出,但含水量過高時會破壞醇羥基與氯化膽堿之間的氫鍵,減少低共熔溶劑與黃酮之間的相互作用[12],導致提取率下降。
綜上所述,本實驗在單因素試驗基礎上采用響應面法優化超聲輔助低共熔溶劑提取紅豆杉葉總黃酮工藝,發現該方法優于傳統有機溶劑提取工藝,可為該成分開發利用提供參考。

