遠程缺血預適應訓練對短暫性腦缺血發作患者血清Lp-PLA2 HIF-1α水平及終點事件的影響
馬俊保 梁家輝 楊六紅
平頂山市第二人民醫院,河南 平頂山 467000
短暫性腦缺血發作(transcient ischemic attacks,TIA)是老年常見的腦缺血性疾病,是由顱內血管病變導致的一種局灶性、反復性、短暫性、可逆性腦局部功能喪失疾病[1],具有發病率高、復發率高、病死率高等特點,影響患者的認知功能,是發生腦梗死的高危預警提示,同時也是導致死亡和致殘的主要原因之一[2-3]。TIA多發于50~70歲中老年群體,大多數患者伴常見的腦血管病危險因素(高血壓、血脂異常、糖尿病和心臟疾病等),起病迅速,患者突然出現身體一側麻木、無力、言語障礙、視力下降甚至視野缺損等癥狀,癥狀持續5~60 min,大多數癥狀和體征會在1 h 內消失,不遺留永久損害,多有反復發作的病史,每次發作情況相似[4-5]。TIA主要由顱內血管(頸動脈或椎基動脈)發生短暫性血液供應不足,局部病灶腦缺血引起的短暫腦神經或視網膜功能障礙,若不及時診治,可后續發展為腦梗死,產生大量自由基,危及患者生命[6-7]。而大動脈粥樣硬化是缺血性腦卒中的主要主要原因,研究表明動脈粥樣硬化形成的原因與內皮損傷、血管炎癥有關[8]。血清脂蛋白磷脂酶A2(Lp-PLA2)是一種與低密度脂蛋白代謝為促炎介質有關的酶,參與動脈粥樣硬化形成過程。有數據顯示,高水平的血清Lp-PLA2參與了腦梗死發病,可能是腦梗死重要的危險因素[9]。血清缺氧誘導因子-1α(HIF-1α)是一種在缺氧情況下的發揮活性的轉錄因子,廣泛參與細胞促凋亡或抗凋亡過程,有關報道顯示,高表達的HIF-1α可通過激活泡沫細胞形成、增加炎癥、血管形成等,在動脈粥樣硬化進展中具有重要作用。有學者推斷減低Lp-PLA2、HIF-1α水平,可減輕卒中后血腦屏障損傷。因此,早期給予有效的檢查監測和干預對防御并控制腦梗死有重要意義。遠程缺血 預 適 應(remote ischemic preconditioning,RIP)是指機體部分器官(如一側下肢)在受到短暫、可逆的缺血缺氧刺激后,通過誘導缺血器官以外的其他臟器(如心臟、肝臟、腎)對疾病發作時產生嚴重或致命的缺血缺氧產生保護作用[10],以減少其他器官在急性缺血中的損傷。本研究將遠程缺血預適應運用于短暫性腦缺血發作患者中,旨在分析其對短暫性腦缺血發作患者患者血清Lp-PLA2、HIF-1α水平及終點事件的影響。
1 資料與方法
1.1 一般資料選取平頂山市第二人民醫院于2020-01—2020-12收治的TIA患者116例,訓練組58例和對照組58例,2組一般資料比較差異無統計學意義(P>0.05),見表1。1.1.1 納入標準:①符合短暫性腦缺血發作診斷標準[11],起病突然,持續時間短,通常5~20 min,癥狀在24 h內恢復,常反復發作;②患者臨床癥狀均表現為早期癥狀患者;③未合并其他嚴重疾病;④患者無語言障礙;⑤無傳染性疾病;⑥為新發梗死灶;⑦患者或其家屬簽署知情合同;⑧年齡18~70歲,性別不限。
表1 2組一般資料比較 (±s)Table 1 Comparison of general information of two groups (±s)

表1 2組一般資料比較 (±s)Table 1 Comparison of general information of two groups (±s)
組別訓練組對照組t/χ2值P值n 類型年齡/歲65.50±9.60 65.90±9.10 0.213 0.831性別男30 32 0.138 0.034女58 58 28 26中頸動脈系統TIA 35 34椎基動脈系統TIA 23 24 0.035 0.849發作持續時間(h)22.47±5.38 23.85±6.87 1.204 0.230
1.1.2 排除標準:①腦梗死;②惡性腫瘤;③居住地較遠,不能按時參與訓練;④神經功能異常;⑤中途退出或家屬不同意參加;⑥嚴重肝、腎、肺功能不全者。
1.2 方法
1.2.1 對照組:采用常規治療方法,患者發病前后根據病情給予降糖、降壓、調脂、抗感染、吸氧、腦保護劑、神經營養藥物等常規治療。指導病人發作時臥床休息,枕頭高度調整到人體與床面呈20°,保證不影響頭部血液供應,仰頭或頭部轉動時應緩慢且轉動幅度不宜太大。囑咐外出或沐浴時應有家人陪伴,注意防止摔倒。護理人員嚴格監測患者體征,警惕缺血性腦卒中的發生。
1.2.2 訓練組:在對照組的基礎上干預遠程缺血預適應訓練,訓練者持平躺或臥姿,用遠程缺血預適應訓練儀(廠家:廣東潤池科技,粵械廣審第2019020144號;型號規格:YX01-D)對雙側上臂進行加壓至200~220 mmHg(1 mmHg=0.133 kPa)間歇缺血訓練,保持5 min,然后再放氣休息5 min,接著再加壓至200~220 mmHg 5 min,重復5 個循環,共45 min。具體加壓刻度設置,一般按照訓練者的實際血壓數加40 mmHg,如正常血壓為140 mmHg,則加壓到180 mmHg以達到遠隔缺血的效果。2次/d,間隔5 h,堅持1個月。
1.3 觀察指標
1.3.1 測量血清人血漿脂蛋白磷脂酶A2(Lp-PLA2)水平:所有患者在TIA發作與治療后第1、3、6 小時分別抽取肘靜脈血3~5 mL,血標本以3 000 r/min 離心10 min,分離血清后,置于—20 ℃冷柜保存待檢。采用酶聯免疫分析(ELISA)試劑盒雙抗體夾心法[14](廠家:上海西唐生物)統一測定血清Lp-PLA2水平,嚴格按照說明書步驟進行。
1.3.2 測量血清缺氧誘導因子-1α(HIF-1α)水平:在TIA發作與治療后第1、3、6小時分別抽取肘靜脈血3~5 mL,血標本以3 000 r/min離心10 min,分離血清后,置于—20 ℃冷柜保存待檢。采用ELISA試劑盒(廠家:上海西唐生物)雙抗體夾心法統一測定血清HIF-1α水平,嚴格按照說明書步驟進行。
1.3.3 血清α-顆粒膜蛋白(GMP)、溶血磷脂酸(LPA)水平:在TIA發作與治療后第6小時分別抽取肘靜脈血3~5 mL,血標本以3 000 r/min離心10 min,分離血清后,放入—20 ℃冷柜保存待檢。用ELISA試劑盒(廠家:上海西唐生物)監測血清GMP、LPA水平。
1.3.4 終點事件:對2 組患者進行為期6 個月的隨訪,記錄2 組隨訪期間腦梗死、急性心肌梗死和猝死的發生率。
1.4 統計學分析以SPSS 20.0 軟件進行數據統計,對一般資料采用兩獨立樣本率比較,計量資料以均數±標準差(±s)表示,行兩獨立樣本與組間比較采用t 檢驗,計數資料比較采用卡方檢驗,P<0.05 為差異有統計學意義。
2 結果
2.1 訓練前后2組血清Lp-PLA2水平比較接受遠程缺血預適應訓練治療前,2 組血清Lp-PLA2 水平對比差異無統計學意義(P>0.05);治療后訓練組血清Lp-PLA2 水平較治療前下降,差異有統計學意義(P<0.05);2 組治療后1、3、6 h 3 個時間段對比,訓練組血清Lp-PLA2水平均較對照組下降更快,差異有統計學意義(P<0.05)。見表2。
表2 訓練前后2組血清Lp-PLA2水平比較 (μg/L,±s)Table 2 Comparison of serum Lp-PLA2 before and after training (μg/L,±s)
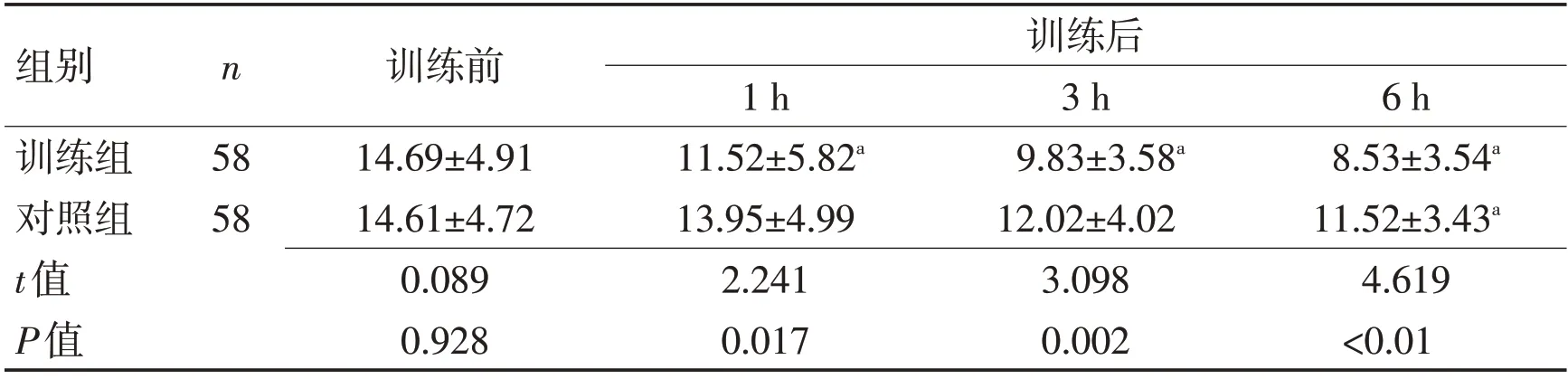
表2 訓練前后2組血清Lp-PLA2水平比較 (μg/L,±s)Table 2 Comparison of serum Lp-PLA2 before and after training (μg/L,±s)
注:與治療前比較,aP<0.01
組別訓練組對照組t值P值n 訓練后6 h 8.53±3.54a 11.52±3.43a 4.619<0.01 58 58訓練前14.69±4.91 14.61±4.72 0.089 0.928 1 h 11.52±5.82a 13.95±4.99 2.241 0.017 3 h 9.83±3.58a 12.02±4.02 3.098 0.002
2.2 訓練前后2 組血清HIF-1α水平比較接受遠程缺血預適應訓練治療前,2 組血清HIF-1α水平對比,差異無統計學意義(P>0.05);接受遠程缺血預適應訓練治療后,訓練組血清HIF-1α水平較治療前下降,差異有統計學意義(P<0.01);2組治療后1、3、6 h 3個時間段對比,訓練組血清HIF-1α水平均較對照組下降更快,差異有統計學意義(P<0.05)。見表3。
表3 訓練前后2組血清HIF-1α水平比較 (pg/mL,±s)Table 3 Comparison of serum HIF-1α level before and after training (pg/mL,±s)

表3 訓練前后2組血清HIF-1α水平比較 (pg/mL,±s)Table 3 Comparison of serum HIF-1α level before and after training (pg/mL,±s)
注:與治療前比較,aP<0.01
組別訓練組對照組t值P值n 訓練后訓練前363.87±99.68 362.85±98.72 0.055 0.955 58 58 1 h 301.82±89.82a 335.23±84.99 2.057 0.041 3 h 257.24±80.58a 294.23±76.02a 2.542 0.012 6 h 163.46±75.28a 206.35±73.43a 3.097 0.002
2.3 訓練前后2 組血清GMP、LPA 水平比較接受遠程缺血預適應訓練治療前,2組血清GMP、LPA水平對比,差異無統計學意義(P>0.05);接受遠程缺血預適應訓練治療后,訓練組較治療前血清GMP、LPA 水平下降,差異有統計學意義(P<0.01);2組治療后6 h血清對比,訓練組血清GMP、LPA 水平比對照組下降更快,差異有統計學意義(P<0.01)。見表4。
表4 訓練前后2組血清GMP、LPA水平比較 (μmol/L,±s)Table 4 Comparison of levels of serum GMP and LPA before and after training (μmol/L,±s)
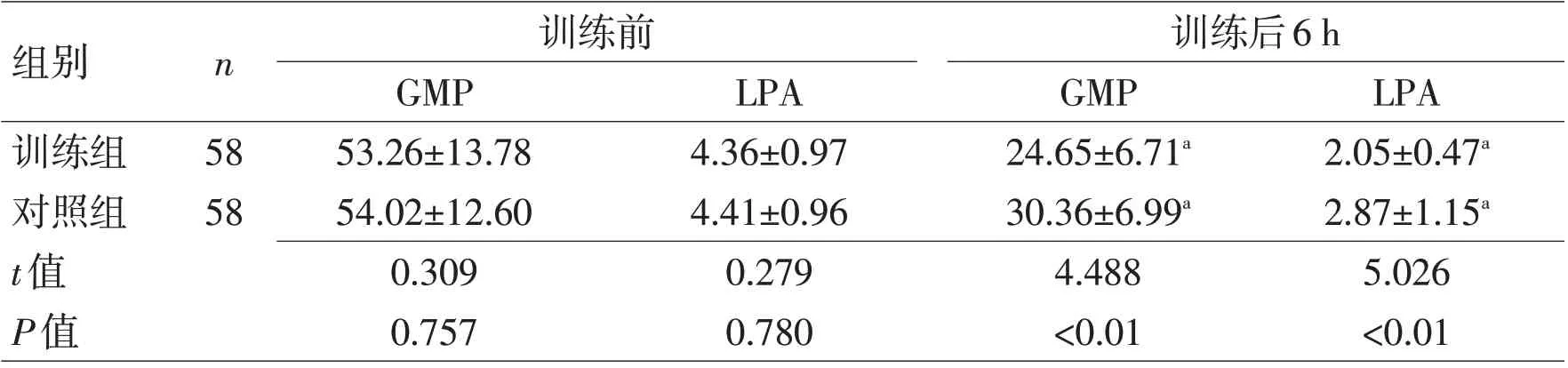
表4 訓練前后2組血清GMP、LPA水平比較 (μmol/L,±s)Table 4 Comparison of levels of serum GMP and LPA before and after training (μmol/L,±s)
注:與治療前比較,aP<0.01
組別訓練組對照組t值P值n LPA 2.05±0.47a 2.87±1.15a 5.026<0.01 58 58訓練前GMP 53.26±13.78 54.02±12.60 0.309 0.757 LPA 4.36±0.97 4.41±0.96 0.279 0.780訓練后6 h GMP 24.65±6.71a 30.36±6.99a 4.488<0.01
2.4 2組終點發生率比較接受遠程缺血預適應訓練治療后訓練組終點發生率顯著低于對照組,差異有統計學意義(P<0.05)。見表5。

表5 2組終點發生率比較 [n(%)]Table 5 Comparison of incidence of endpoint events between the two groups [n(%)]
3 討論
隨著生活條件的提高和生活方式的改變,腦血管疾病的發病率越來越高,目前已成為危害老年人群身體健康和生命安全的主要疾病[12]。數據顯示[13],每年約260 多萬人死于腦血管疾病,在腦血管疾病的患者已高居首位。TIA屬于高發的腦血管疾病之一,是由多種因素引起的頸動脈或椎基底動脈系統短暫缺血而導致的腦供血不足,其主要表現為反復發作的伴局灶癥狀的短暫的腦血液循環障礙[14]。以短暫性失語、癱瘓或感覺障礙為特點,神經系統局灶體征多在1 h 內恢復,癥狀和體征在24 h 內消失,60 歲以上老年人多見,男性多于女性,多在改變體位、過度活動或突然頸部轉動等情況下發病[15-16],且伴血管功能狀態及血流動力學改變,如得不到及時有效的控制,則易發展為腦梗死,給患者自身及家庭、社會帶來沉重的負擔,因此,在對TIA 的防治上應引起足夠的重視。
研究表明[17-19],有效的預防措施與鍛煉可明顯改善發作后的恢復情況。缺血預適應作為一種重要的內源性保護機制,相關信號轉導通路包括觸物質、介入物質及效應物質。目前國內外針對遠程缺血后適應與短暫性腦缺血發作方面的研究大多處于動物實驗階段[20],而這些實驗表明遠程缺血后適應治療可減輕大鼠腦水腫及缺血在灌注損傷,維持血-腦脊液屏障穩定性,對促進神經功能恢復具有幫助,這一研究提示遠程缺血預適應對治療腦血管疾病具有較高的價值。國內一項研究經顱多普勒(TCD)檢查評估遠程缺血后適應訓練對腦血流影響表明[24],遠程缺血預適應訓練可通過雙側患肢進行間歇缺血訓練,激發人體免疫系統應激機制,減輕缺血缺氧所致組織損害,以增加基底動脈的血流,從而改善腦灌注。雖然兩者研究對象不同,但提示遠程缺血預適應能改善腦血管患者缺血缺氧的耐受能力。而本研究中訓練組接受遠程缺血預適應訓練治療后心腦血管終點事件發生率明顯低于對照組(P<0.05),說明接受遠程缺血預適應訓練可使TIA患者終點事件發生率降低。考慮原因:患者在接受遠程缺血預適應訓練后,使患者肌體的部分器官受到短暫的缺血、缺氧刺激,誘導臟器產生保護機制,產生血管生長因子和腺苷等,增加毛細血管數量,促進吻合血管形成;降低組織代謝和能量需求,保護和修復損傷組織,從而減少血管內因血管痙攣、血小板聚集導致的纖維蛋白形成,降低并發癥(腦梗死、全性卒中、意識障礙、心臟猝死等)的發生概率,從而降低終點事件發生率[22-24]。
臨床研究顯示[25],遠程缺血預適應訓練可以通過調節自主神經活性改善心肌缺血和改善內皮細胞功能,并能通過激活NO合酶提高紅細胞的變形能力,對心臟起到重要的保護作用。且通過對受試驗者血漿進行分析[26],發現遠程缺血預適應訓練中能夠保護靜脈內皮細胞免受低氧誘導的細胞損傷,且提示這種保護作用可能與細胞內缺血誘導因子HIF-1α的變化有關。而HIF-1α是低氧誘導因子家族中的蛋白因子,參與了細胞促凋亡或抗凋亡過程,正常狀態下HIF-1α受泛素蛋白酶體系統的影響處于低水平,組織低氧時HIF-1α的降解會減少,促進蛋白表達顯著增加[27]。研究證實[28],接受遠程缺血預適應訓練可以調節HIF-1α、血管內皮因子及腺苷的表達,促進新血管的形成,從而保護和修復受損腦組織,提高缺血缺氧的耐受能力。Lp-PLA2 是磷脂酶超家族的成員之一,由炎性細胞分泌的一種磷脂酶可促使氧化磷脂水解,可水解血小板活化因子與其他致炎因子,也是新發現具有血管特異性的血清炎性標記物,可水解形成血管內皮的氧化低密度脂蛋白,并損傷血管內皮細胞形成動脈粥樣硬化斑塊,當斑塊發生脫落、破裂等,引起缺血性腦血管疾病的形成,因此,當TIA發生時,Lp-PLA2 水 平 會 異 常 升 高[29];GMP、LPA、Lp-PLA2 均是血小板活化標志物,GMP 是血小板和內皮細胞共同合成的一種黏附分子,能介導內皮小板與血小板、白細胞的黏附;LPA是一種的甘油磷脂,由凝血酶活化的血小板在血液凝集的早期產生,通過G蛋白偶聯受體影響可激活紅細胞的鈣通道,促進血栓的發展,導致血小板活化和聚集[30-32]。本研究發現,接受遠程缺血預適應訓練治療后,訓練組血清Lp-PLA2、HIF-1α水平均比對照組下降更快(P<0.05);血清GMP、LPA 水平比對照組下降更快(P<0.01)。說明接受遠程缺血預適應訓練可以使TIA 患者血清Lp-PLA2、HIF-1α、GMP、LPA水平降低,分析原因:患者在接受短暫、反復的缺血預適應訓練后,可調動機體的自身防御和修復功能,提高大腦及其他器官組織對缺血缺氧的預防和適應能力,激發人體免疫系統應急機制,釋放內源性保護物質(如緩激肽等低氧誘導因子)參與保護心肌細胞和促進能量代謝,使腦組織內氧氣量增加,降低血清HIF-1α水平;維持腦血管供血,減少血管內血小板聚集,從而降低血清GMP、LPA、Lp-PLA2含量,減輕氧化應激損傷及炎癥反應,減少人體由于缺血缺氧而造成的機體損傷[33-41]。
本研究通過觀察遠程缺血預適應訓練對TIA患者腦血清指標及終點事件的影響發現,予以訓練的患者血清Lp-PLA2、HIF-1 α、GMP、LPA水平降低,終點事件發生率減少,說明TIA 患者經此治療后腦部供血及供氧情況均得到明顯改善,且操作簡便、易于掌握,是一種有效的防治措施。

