基于時間分辨免疫熒光法的降鈣素原試劑盒臨床性能評價
李登紅(通信作者),陸建偉,王洪濤,蔡美玲,農麗松,黃光強
1 巴迪泰(廣西)生物科技有限公司 (廣西南寧 530031);2 廣西中醫(yī)藥大學第一附屬醫(yī)院檢驗科 (廣西南寧 530022)
新生兒因免疫系統(tǒng)發(fā)育尚不成熟,肺部易被感染,其中以新生兒肺炎較為多見,其易導致死亡,病死率約為5%~20%[1-2]。新生兒肺炎早期通常不易區(qū)分是由如細菌、病毒或衣原體等何種病原體感染所致,因此易導致抗生素藥物被廣泛濫用。目前,降鈣素原(procalcitonin,PCT)作為可靠、有效的炎癥標志物,在感染的早期診斷中表現出較高的臨床價值[3]。PCT 為沒有激素活性的降鈣素前肽物質,在人體內的半衰期較長,可達到25~30 h,穩(wěn)定性優(yōu)良[4]。
目前,臨床上測定PCT 的常見方法包括酶聯(lián)免疫熒光法、免疫熒光法、電化學發(fā)光法等[5],其中普通PCT 即時檢驗(point-of-care testing,POCT)產品的檢測靈敏度較低,大部分在0.1 ng/ml 以上,無法精確判斷感染程度,對于細菌性肺炎,部分患者的PCT 值會<0.1 ng/ml[6],普通PCT POCT 產品易判讀為假陰性,導致患者錯過最佳治療時機。超敏PCT(PCT plus)檢測試劑盒是巴迪泰(廣西)生物科技有限公司生產的一種能夠快速進行診斷的試劑盒,將層析技術和時間分辨免疫熒光技術進行融合,利用生物學抗體和抗原的特異性反應,最低可檢測到0.01 ng/ml 濃度,靈敏度得到較大提高,檢測時只需與配套的熒光免疫分析儀進行簡單的操作,12 min 即可得到結果,對于新生兒肺炎的診斷效果理想。為證明基于時間分辨免疫熒光法的PCT plus 檢測試劑盒的臨床性能,以法國生物梅里埃股份有限公司生產的PCT 測定試劑盒(酶聯(lián)免疫熒光法)作為對照,對PCT plus 檢測試劑盒開展性能方面的驗證,現報道如下。
1 資料與方法
1.1 一般資料
選取2020年10—12月廣西中醫(yī)藥大學第一附屬醫(yī)院的150例患者的血清樣本作為研究對象,其中男80例,女70例;年齡0~85歲;血清樣本來自輕、重度炎癥患者及健康人,為準確評估兩種方法的一致性,排除嚴重溶血樣本或有黃疸樣本或樣本量少的樣本。
1.2 方法
1.2.1 儀器與試劑
酶聯(lián)免疫熒光法:PCT 測定試劑盒(酶聯(lián)免疫熒光法)及自配校準品、質控品(法國生物梅里埃股份有限公司),mini-VIDAS 全自動熒光免疫分析儀(法國生物梅里埃股份有限公司)。
時間分辨免疫熒光法:PCT plus 檢測試劑盒(免疫熒光干式定量法)及自配校準品、質控品[巴迪泰(廣西)生物科技有限公司],A2000干式熒光免疫分析儀[巴迪泰(廣西)生物科技有限公司] 。
1.2.2 評價方法
(1)精密度評價:參考CLSI EP15-A2《用戶確認精密度和正確度的性能驗證指南-第二版》文件,采用PCT 測定試劑盒(酶聯(lián)免疫熒光法)和PCT plus 檢測試劑盒(時間分辨免疫熒光法)分別檢測2個濃度的質控血清(S1、S2)及自配質控品(Lv.1、Lv.2),4次/d,每次間隔4 h,連續(xù)測定5 d,計算總變異示數(coefficient of variation, CV)。(2)準確度評價:采用PCT 測定試劑盒(酶聯(lián)免疫熒光法)和PCT plus 檢測試劑盒(時間分辨免疫熒光法)分別檢測150例患者的血清樣本,其中檢測血清樣本濃度涵蓋試劑盒檢測范圍,使用t檢驗進行結果評價,計算酶聯(lián)免疫熒光法和時間分辨免疫熒光法檢驗值的偏差。(3)相關性評價:采用PCT測定試劑盒(酶聯(lián)免疫熒光法)和PCT plus檢測試劑盒(時間分辨免疫熒光法)分別檢測150例患者的血清樣本,其中檢測血清樣本濃度涵蓋試劑盒檢測范圍,使用一元線性回歸對結果進行擬合,計算一元線性方程和相關系數。(4)一致性評價:使用Bland-Altman 法、ROC 曲線分析及Kappa一致性檢驗進行一致性評價。
1.3 評價標準
(1)精密度:批內總CV<10%,表示精密度良好。(2)準確度:酶聯(lián)免疫熒光法和時間分辨免疫熒光法偏差<10%,表示準確度良好。(3)相關性:一次線性回歸方程,斜率為0.9~1.1,r>0.975,表示相關性良好。(4)一致性:Bland-Altman 散點分析超出±1.96 SD 范圍比例<5%,ROC 曲線下面積≥0.9、Kappa值≥0.75,表示一致性較好。
1.4 統(tǒng)計學處理
采用Origin8 SR4[v8.0951(B951)]和MedCalc(Version 18.2.1)軟件進行數據處理,計量資料以±s表示,采用t檢驗,相關性分析采用一元線性回歸分析法,一致性分析采用Bland-Altman 法和Pearson相關系數,采用Kappa檢驗。
2 結果
2.1 精密度
時間分辨免疫熒光法檢測PCT 的CV<10%,見表1。
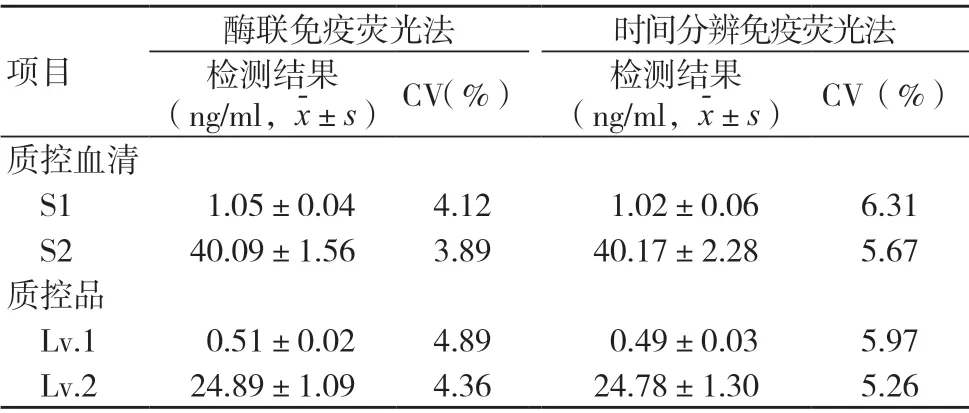
表1 酶聯(lián)免疫熒光法和時間分辨免疫熒光法檢測結果比較
2.2 準確度
使用t檢驗分析,在置信限P=0.05條件下,t臨界值為2.05,時間分辨免疫熒光法檢測結果均值為4.02 ng/ml,酶聯(lián)免疫熒光法檢測結果均值為3.87 ng/ml,兩種分析方法的偏差為3.88%。
2.3 相關性
酶聯(lián)免疫熒光法和時間分辨免疫熒光法檢測150例患者血清樣本的結果一元線性回歸方程為y=1.018x+0.0121,r=0.9911>0.975,P<0.01,在試劑盒檢測范圍內(0.01~50.0 ng/ml),兩種分析方法成線性,如圖1所示。

圖1 兩種分析方法檢測結果的線性相關圖
2.4 一致性
基于Bland-Altman 法,對150例患者血清樣本的檢測結果繪制散點圖,在試劑盒線性檢測范圍內,兩種分析方法的差值表現出均勻分布,如圖2所示,僅有4個點超出±1.96 SD 范圍,占比2.67%,證明兩種分析方法具有良好的一致性。

圖2 兩種分析方法的Bland-Altman 散點圖
在Cut Off值(0.5 ng/ml)下的ROC曲線下面積為0.990,P<0.01,靈敏度為95.29%,特異度為98.44%,如圖3所示;以Cut Off 值(0.5 ng/ml)作Kappa檢驗,Kappa值為0.891,可以認為兩種分析方法的診斷結果無顯著性差異。
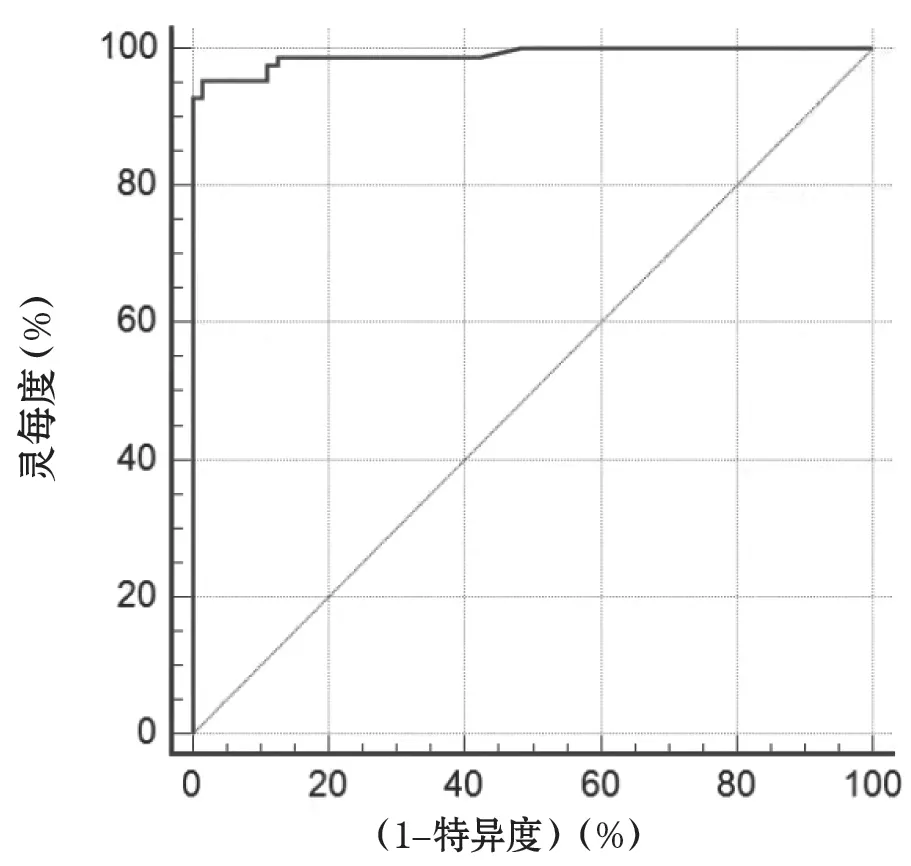
圖3 兩種方法檢測PCT 的ROC 曲線
3 討論
新生兒出生時由于抵抗力差,易被各種病菌感染,且臨床上早期出現感染表現比較隱蔽[7],部分患兒表現有咳嗽、咳痰、體溫升高等現象,但易被家長忽視,有研究顯示,在中國西部農村已確定死亡原因的423例新生兒中,約有34.5%死于肺炎[8]。PCT 作為敏感生物指標,與新生兒肺炎病情嚴重程度及病原菌感染類型有一定關系,可用于肺炎的早期診斷[9]。
目前,臨床上使用酶聯(lián)免疫熒光法測定PCT 的效果較好,如法國生物梅里埃股份有限公司的PCT 測定試劑盒,其精密度、靈敏度、特異度、準確度均得到廣泛認可,但最低檢測限只能達到0.05 mg/ml。PCT plus 檢測試劑盒使用時間分辨熒光免疫法[10],將探測物質、反應緩沖液和血樣混合,緩沖液中的PCT 抗體與血樣中的PCT 抗原結合形成抗體-抗原復合物;將混合樣本加入到反應板的加樣孔中,通過毛細血管作用在硝化纖維基質的檢測帶上擴散被檢測帶上的另一種PCT 抗體所捕獲;血樣中的PCT 抗原越多,檢測帶上形成的抗體-抗原-抗體復合物積聚也越多。熒光信號的強度反映了被捕獲的PCT 抗原數量,通過配套免疫熒光分析儀的判斷,能夠定量檢測出血液樣本中的PCT抗原濃度。為提高檢測試劑盒的靈敏度和特異度,采用親和素和熒光素放大系統(tǒng)[11],將熒光信號進行放大,提高了檢測靈敏度和特異度,使最低檢出限達到0.01 ng/ml,解決了普通POCT 產品靈敏度低的問題。
本研究結果顯示,時間分辨免疫熒光法擁有良好的精密度,檢測PCT 的CV<10%;時間分辨免疫熒光法和酶聯(lián)免疫熒光法之間存在一定的系統(tǒng)性偏差(3.88%),符合生產廠家的聲明;兩種分析方法擁有良好的相關性(斜率為1.018,r=0.9911>0.975,P<0.01);在Cut Off值(0.5 ng/ml)下的ROC 曲線下面積為0.990,P<0.01,靈敏度為95.29%,特異度為98.44%,Kappa值為0.891,說明兩種分析方法一致性較好。
綜上所述,時間分辨免疫熒光法檢測PCT 的結果良好,表現在檢測重復性良好,和酶聯(lián)免疫熒光法偏差小,相關性高,一致性強,用戶可結合實際實際情況選擇時間分辨免疫熒光法的PCT plus 檢測試劑盒。

