胸腔鏡下體外循環二尖瓣置換術vs傳統開胸手術治療風濕性心臟病效果及對患者炎性因子的影響
王豪杰,梁冰,井元虎,趙輝,施鞏寧,張沛(河南大學淮河醫院,河南 開封 475000)
上世紀80年代起,腔鏡外科逐漸興起,如今已經走向成熟階段,從腹腔鏡普通外科到腹腔鏡婦科再到胸腔鏡肺葉手術,是微創外科發展的趨勢所在[1-2]。手術是治療RHD II、III級患者的主要手段,胸腔鏡MVR與TT相比,創傷小、切口美觀、術后恢復快[3-4]。本文就對比TT與MVR在RHD患者中的圍手術期效果、炎癥因子及術后正常工作或生活時間等指標進行評價,現匯報如下。
1 資料及方法
1.1 一般資料 選取我院收治的82例RHD患者,均于2017年5月-2020年5月期間收治,采用奇數偶數分組法其分成兩組(觀察組、對照組),各41例;觀察組:男20例,女21例,年齡:36-69歲,平均年齡(49.45±3.89)歲;疾病類型:單純二尖瓣狹窄22例,二尖瓣狹窄伴關閉不全19例。對照組:男19例,女22例,年齡:37-70歲,平均年齡(49.52±3.91)歲;單純二尖瓣狹窄23例,二尖瓣狹窄伴關閉不全18例。兩組性別、年齡、疾病類型滿足可比性差異,P>0.05。
納入標準:①經影像學檢查確診;②符合《內科學》II、III級RHD診斷標準;③知情此研究;④經本院倫理委員會批準。排除標準:①入組前曾服免疫調節藥物;②合并惡性腫瘤者;③凝血功能障礙者。
1.2 方法 對照組:全麻后胸骨正中作一切口建立體外循環,心臟停搏后去除病變的二尖瓣,確保瓣周無漏后,將人工瓣置入二尖瓣環內,完成后,去除升主動脈阻斷鉗,心臟復跳,縫合切口,血流動力學穩定后停機[5-6]。觀察組實施胸腔鏡下體外循環MVR,體位、麻醉同對照組,于右側胸骨旁第3肋間作1個1.5cm左右的切口作為主操作孔,于右側腋前線第4肋間作1個1.5cm切口作為副操作孔,右側腋中線第5肋間作1個1-2cm切口作為腔鏡操作孔,股動靜脈插管建立體外循環,對轉機降溫,從副操作孔阻斷升主動脈及上下腔靜脈,并將高價鉀停跳液注入升主動脈根部,往心包腔注入生理鹽水,經主操作孔切開左心房,胸腔鏡檢查二尖瓣并切除病變部位,再經主操作孔對二尖瓣進行全間斷縫合,確定無瓣周漏后,縫合切口,并對心臟排氣,其余步驟同對照組[7]。
1.3 觀察指標 ①臨床圍手術期指標;②炎性因子水平,包括腫瘤壞死因子-α(TNF-α)、白介素-6(IL-6)血清C反應蛋白(CRP)。
1.4 統計學分析 采用統計學軟件STATA12.0完成,炎癥指標等(±s)表示,兩組比較t檢驗,后恢復工作時間采用log-rank檢驗,P<0.05為有統計差異。
2 結果
2.1 臨床指標 兩組體外循環轉流時間比較無統計學意義,P>0.05;其余指標比較均有統計學差異,P<0.05,見表1。
表1 兩組臨床指標對比表(±s)
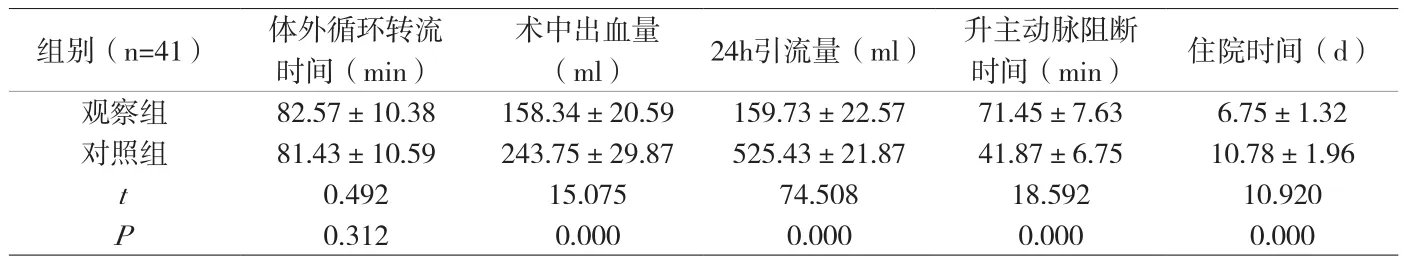
表1 兩組臨床指標對比表(±s)
組別(n=41) 體外循環轉流時間(min)術中出血量(ml) 24h引流量(ml) 升主動脈阻斷時間(min) 住院時間(d)觀察組 82.57±10.38 158.34±20.59 159.73±22.57 71.45±7.63 6.75±1.32對照組 81.43±10.59 243.75±29.87 525.43±21.87 41.87±6.75 10.78±1.96 t 0.492 15.075 74.508 18.592 10.920 P 0.312 0.000 0.000 0.000 0.000
2.2 炎性因子水平 術前,兩組炎性因子水平比較,P>0.05;術后,兩組炎性因子水平均有所升高,觀察組各水平均低于對照組(P<0.05),見表2。
表2 兩組炎性因子水平對比表(±s)
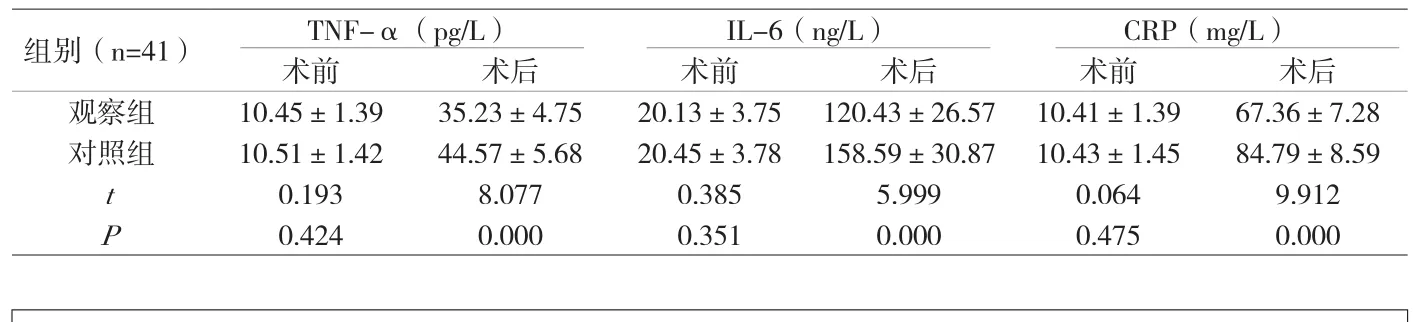
表2 兩組炎性因子水平對比表(±s)
組別(n=41) TNF-α(pg/L) IL-6(ng/L) CRP(mg/L)術前 術后 術前 術后 術前 術后觀察組 10.45±1.39 35.23±4.75 20.13±3.75 120.43±26.57 10.41±1.39 67.36±7.28對照組 10.51±1.42 44.57±5.68 20.45±3.78 158.59±30.87 10.43±1.45 84.79±8.59 t 0.193 8.077 0.385 5.999 0.064 9.912 P 0.424 0.000 0.351 0.000 0.475 0.000
2.3 術后恢復工作時間 觀察組術后恢復工作或正常生活中位時間為(6.23±1.20)周,而對照組為(8.11±1.60)周,兩組比較,觀察組顯著低于對照組(HR=1.68,95%CI:1.08-2.58,P<0.05),見圖1。
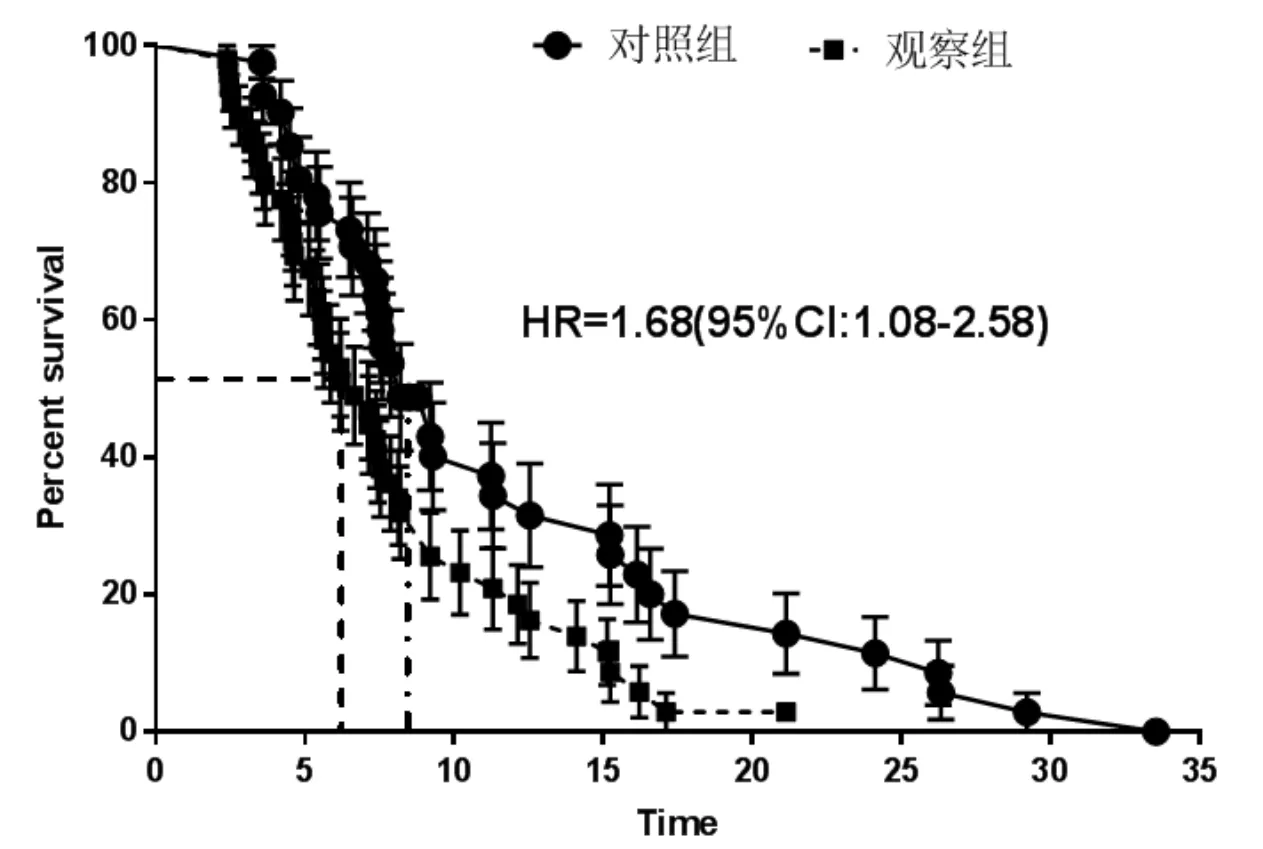
圖1 Kaplan-Meier曲線比較兩組患者術后恢復工作或正常生活時間
3 討論
風濕病心臟病是常見的心內科疾病之一,是風濕性活動引起的心臟瓣膜病變,瓣膜性心臟病是涉及心臟四個瓣膜中的一個或多個(心臟左側的主動脈瓣和二尖瓣以及心臟右側的肺動脈瓣和三尖瓣)的任何心血管疾病過程[8-9]。在解剖學上,瓣膜是心臟致密結締組織的一部分,負責調節流經心臟和大血管的血流。瓣膜功能障礙可導致心臟功能減退,受損瓣膜的治療通常涉及外科瓣膜修復(瓣膜成形術)或置換[10]。臨床上治療RHD以消除心肌炎癥,恢復心臟供血、供氧功能,而大部分患者心臟病為二尖瓣,通過人工置換二尖瓣,可減輕機體炎癥,恢復瓣膜及心臟功能[11]。臨床上常用的手術方式有胸腔鏡MVR和TT手術,MVR手術創傷小、視野清晰和術后恢復快等特點。但相較于TT手術,對醫療單位的手術團隊要求高、手術操作相對復雜、術中對于大出血的風險控制可能不如TT手術[12]。
觀察組胸腔鏡下體循環MVR操作復雜、困難,術中需頻繁的調整腔鏡鏡頭角度和位置,使體外循環時間延長,從而延長了升主動脈阻斷時間。觀察組其他圍手術期指標均低于或短于對照組,腔鏡下可在短時間內迅速經鼓動靜脈建立體外循環,手術迅速,術中腔鏡顯示清晰,縫合確切,術中止血更易,加之小切口無需縫合胸骨,明顯減少出血;術中轉機時間短,術后引流量少,因此,胸腔鏡下體外循環MVR安全、可靠。TNF-α具有啟動和觸發炎癥反應的作用[13],患者在進行體外循環后,TNF-α反應最早,而TNF-α又可促進IL-6的釋放,IL-6與體外循環后心功能不全有關[14]。本研究結果顯示,術后,兩組TNF-α、IL-6、CRP均上升,觀察組低于對照組,說明手術均可引起機體炎性反應,而胸腔鏡下體外循環MVR創傷小,可減少炎性因子釋放。同時研究還顯示,觀察組患者術后恢復工作或正常生活的時間明顯短于對照組,提示胸腔鏡微創治療,有利于患者術后康復,并快速回歸正常生活或工作學習。
綜上所述,在RHD的治療中,胸腔鏡MVR治療RHD創傷小,減輕機體炎性反應,加速患者術后康復。但研究納入樣本量較少,統計學效能不高,且受試者數據均來自同一個手術小組,可能存在患者選擇偏倚。

