精準醫學與乳腺癌外科的個體化治療
王 韌,楊 斌,趙宗盛,吳香萍,劉翔凌,祝長華
(景德鎮市第二人民醫院普外一科,江西 景德鎮 333000)
隨著乳腺癌發病率的持續升高,乳腺癌的臨床治療逐漸成為人們的關注重點[1-2]。伴隨著乳腺癌相關研究的不斷深入,乳腺癌的治療體系也逐漸變得越來越完善。目前,以精準醫學為基礎的個體化治療已成為臨床干預乳腺癌的重要方式,為探討其臨床價值,本研究選取40例乳腺癌患者進行分析研究。現報告如下。
1 資料與方法
1.1一般資料:選取我院2019年2月~2020年8月收治的40例乳腺癌患者為研究對象。依據入院時間分成對照組與干預組各20例。對照組年齡(46.2±14.2)年;病程(1.9±0.6)歲。干預組年齡(46.0±13.9)歲;病程(2.1±0.6)年。兩組一般資料差異無統計學意義(P>0.05)。本次研究經過本院醫學倫理委員會同意。
1.2方法:對照組接受常規外科治療。干預組實施精準外科治療:①精準術前評估:精準分期。給予乳腺癌患者核磁共振(MRI)檢查,根據檢查結果評估乳腺癌患者的腫瘤浸潤深度、腋窩淋巴結轉移狀況(依據環周切緣判定)以及血管侵犯狀況等,并根據上述信息,劃分乳腺癌分期。本組20例乳腺癌患者中,7例為T1期,8例為T2期,3例為T3期,另外2例患者為T4期;可切除性判斷:參照乳腺癌患者的MRI檢查結果,開展可切除性判斷。MRI檢查期間,重點觀察乳腺癌患者病灶周圍血管受侵狀況(是否有血管內皮環繞、血管內是否有漂浮狀成團癌細胞)。如經MRI檢查發現:乳腺癌患者伴局部腫瘤遠處轉移、腫瘤擴展、周圍鄰近器官受侵犯、胰腺及腹水周圍血管受累狀況,判定為不可切除。無上述狀況者,提示其具有可切除性。②精準基因檢測:多基因檢測,根據乳腺癌患者需要,開展21基因檢測、70基因檢測以及復發評分檢測等多基因檢測;分子分型:根據基因技術(或免疫組化檢測技術)確定乳腺癌患者的分子分型,包含Luminal A型、Luminal B型、Her-2過表達型以及三陰性型共4大類。③個體化治療:腫瘤切除術:依據乳腺癌患者的術前評估結果,制定個體化治療方案。經可切除性判斷證實為不可切除性者,避免實施腫瘤切除術治療;證實具有可切除性者,擬定腫瘤切除術方案;輔助放化療及靶向:參照乳腺癌患者的基因檢測結果,制定輔助放化療、靶向治療方案。21基因檢測:經21基因檢測后,低危、高危乳腺癌患者中,RS<18分者從化療中獲益較少,需避免為這類乳腺癌患者實施化療;RS≥31分者的化療獲益較高,實施化療。70基因檢測:經70基因檢測證實,符合低危標準者,提示其從化療中獲益較少,可免于化療;而符合高危標準者的化療獲益良好,擬實施化療。分子分型檢測:證實為Luminal A型者,擬定內分泌治療方案。但如Luminal A型乳腺癌患者的基因檢測結果提示符合高危標準,可在原內分泌治療方案基礎上加用輔助化療;Luminal B型乳腺癌患者,實施內分泌(芳香化酶抑制劑)加輔助化療方案;Her-2過表達型乳腺癌患者,實施輔助化療加靶向治療(對內分泌治療不敏感);三陰性型乳腺癌患者,因其化療敏感性較高,擬定化療方案(伴BRCA1基因突變者采用鉑類藥物實施化療)。

2 結果
2.1兩組患者療效比較:對照組乳腺癌患者總有效率(70.00%)低于干預組,差異有統計學意義(P<0.05)。見表1。
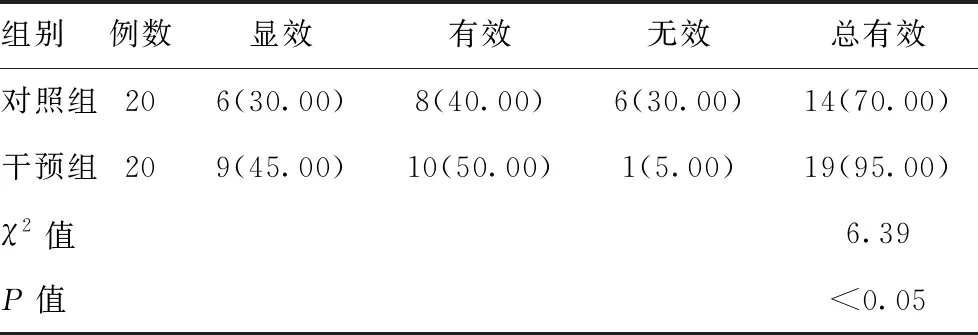
表1 兩組療效比較[例(%)]
2.2兩組患者生存質量比較:治療前,兩組乳腺癌患者生存質量KPS評分差異無統計學意義(P>0.05);治療后,對照組KPS評分(71.59±6.35)分,低于干預組(76.62±6.04),差異有統計學意義(P<0.05)。見表2。
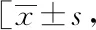
表2 兩組患者生存質量比較分]
2.3兩組并發癥發生率比較:對照組2例手術損傷,2例放射性損傷,3例伴不良反應,并發癥發生率為35.00%,高于干預組(10.00%),差異有統計學意義(P<0.05)。見表3。
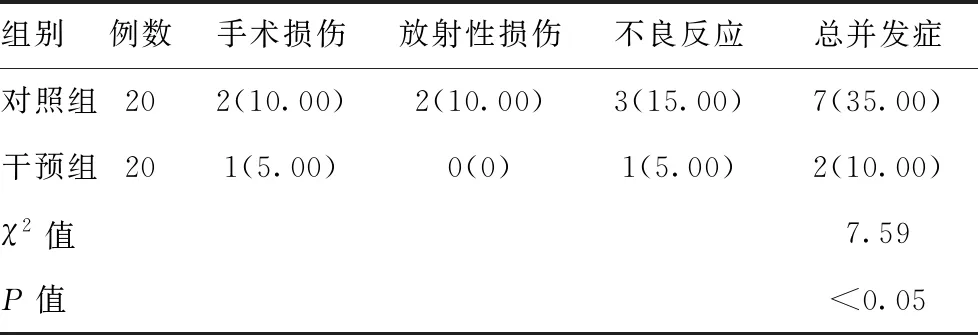
表3 并發癥發生率[例(%)]
3 討論
隨著我國乳腺癌患者規模的不斷擴大,如何改善乳腺癌的預后及生存狀況,逐漸成為乳腺癌臨床管理面臨的重點。依據既往經驗,乳腺癌治療的復雜性在于:①患者病情差異較大。目前,乳腺癌已經成為危害各年齡層女性群體健康的主要惡性腫瘤[3]。由于受到年齡、基礎健康狀況、生活習慣等因素的影響,各乳腺癌患者的病情差異較大。如采用統一化方案進行治療,容易出現顯效速度慢、病情控制效果不顯著等狀況。②復發風險高。乳腺癌的復發風險較高[4],在擬定治療方案期間,所選治療方法是否可抑制復發風險、是否做好乳腺癌患者的復發風險評估等,均可能影響乳腺癌患者的遠期預后狀況。③對不同治療方法敏感性、適應性各異。化療、手術、放療、靶向治療,均為臨床治療乳腺癌的常用方法。乳腺癌患者對各治療方法的適應性、敏感性水平各異。上述狀況對乳腺癌患者治療方案的制定工作提出了較高的要求。
精準醫學于2011年初由美國國家科學院所提出,該理論的核心為:通過對患者組學信息的評估,建立完善的疾病知識網絡,為患者制定個體化的治療方案[5]。基于精準醫學理論的個體化治療強調依據乳腺癌患者的分期、分型,準確制定治療決策(方案),以達到腫瘤病灶去除、損傷控制以及臟器保護間的最佳平衡[6]。在乳腺癌治療中,該方法主要經精準術前評估、基因檢測、個體化治療方案制定這一流程,改善乳腺癌患者的預后狀況[7]。
乳腺癌治療中,基于精準醫學的個體化治療的應用優勢在于:①療效顯著。對于乳腺癌患者,尤其是病程較長的腫瘤患者而言,所選治療方案能否抑制腫瘤細胞的增殖、轉移,直接影響其情緒狀態及生活質量。常規治療主要根據乳腺癌患者的病程、影像學檢查結果,選擇治療方法。該方法對乳腺癌患者病情的評估欠充分,且其所制定治療方案與乳腺癌患者病情的契合度欠佳。而在基于精準醫學的個體化治療中,該方法則可借助影像學技術,確定乳腺癌患者的分期及可切除性,并通過多基因檢測、復發風險評估、分子分型檢測,指導乳腺癌患者治療方案的制定。由于最終所確定個體化治療方案與乳腺癌患者的契合度較高,因此,患者的腫瘤增殖、生長狀況可得到良好抑制,該方法的抗腫瘤效果良好。本研究提示:干預組總有效率高于對照組,差異有統計學意義(P<0.05)。②安全性良好。雖然腫瘤切除術、放療、化療等方法對乳腺癌的抗腫瘤作用已經得到了明確證實,但經上述方法干預后,乳腺癌患者可能會面臨術后損傷、放射性損傷、化療不良反應等問題[8]。與常規治療相比,基于精準醫學的個體化治療更加強調抗腫瘤治療的療效、微創性及安全性。在這一模式下,醫師可根據乳腺癌患者的組學信息,制定具有微創性特征的手術方案,確定最佳輔助治療方法。如乳腺癌患者經分子分型檢測證實為Her-2過表達型后,可將其治療方案制定為靶向治療加輔助化療[9]。一方面,靶向治療的精準化特征,可有效抑制乳腺癌患者病情的持續發展;另一方面,靶向治療與化療形成的協同作用,則可強化該方案的抗腫瘤效果,進而確保Her-2過表達型患者病情的改善。本研究提示:干預組并發癥發生率低于對照組,差異有統計學意義(P<0.05)。③可改善生存質量。乳腺癌患者的生存質量普遍欠佳,原因在于:乳腺癌帶來的一系列癥狀,容易干擾患者的情緒穩定性及正常生活[10]。此外,乳腺癌患者對乳腺癌的錯誤認知、對治療方法作用的偏差認知等,也會造成其生存質量的進一步改變[11]。經常規治療后,病情控制良好乳腺癌患者的生存質量可得到一定改善,但當患者出現復發、放射性損傷等問題時,其生存質量的改善狀況將受到明顯影響。相比之下,實施基于精準醫學的個體化治療后,該方法的良好病灶去除作用、損傷控制作用以及臟器保護作用,可充分滿足乳腺癌患者對抗腫瘤效果及治療安全性的要求,并于較短時間內清除乳腺癌患者生存質量的一系列影響因素,使其生存質量逐漸接近于發病前狀態。本研究結果顯示:治療后,干預組生存質量(76.62±6.04)分,高于對照組,差異有統計學意義(P<0.05)。④優化患者獲益,提高患者滿意度。根據既往乳腺癌治療經驗,不同乳腺癌患者對化療、放療、外科手術等方法的獲益不同。常規治療以醫師的乳腺癌治療經驗為主導。經該方法治療后,雖然部分乳腺癌可從治療方案中獲益,但其與獲益最大化要求仍有一定差距。而推行基于精準醫學的個體化治療后,精確的影像學檢查結果、基因檢測結果,則可有效預測乳腺癌患者對化療、靶向治療等方法的獲益狀況,同時有針對性地選擇適宜獲益良好的抗腫瘤方法,幫助乳腺癌患者實現獲益個體化、最大化。這種治療方法在抗腫瘤獲益方面的優勢,可促進乳腺癌患者滿意度水平的提升。
綜上所述,宜于乳腺癌患者的臨床治療中,引入基于精準醫學的個體化治療,以借助該方法,保障乳腺癌患者的治療有效性及安全性,并促進其生存質量的改善。

