原發性肝細胞肝癌破裂出血手術治療的臨床特點、影響以及預后的相關因素分析
馬 欣 梅展展 王光霞
原發性肝癌為臨床常見惡性腫瘤,目前尚缺乏特效治療,導致病死率高、預后差[1]。原發性肝癌隨著病情進展,并發癥頻發,腫瘤破裂出血為常見并發癥之一,因肝臟具有較為豐富的血供,出血會引發休克,威脅患者生命安全[2-3]。原發性肝癌破裂出血臨床治療難度較大,在控制出血的同時,還需處理腫瘤,常用方法包括姑息性止血法、急診肝切除、經肝動脈栓塞化療(TACE)、保守治療等,不同治療方法所帶來的效果也不盡相同,為改善患者預后,全面了解影響肝癌破裂出血手術臨床特點及預后因素尤為重要[4-5]。鑒于此,本研究進一步探討原發性肝細胞肝癌破裂出血手術治療的臨床特點、影響以及預后的相關因素。現總結如下。
1 資料與方法
1.1 一般資料
回顧性分析2017年2月至2019年2月我院收治的90例原發性肝細胞肝癌破裂出血患者臨床資料,其中男性52例,女性38例;年齡40~81歲,平均年齡(55.34±6.12)歲;病灶直徑2~11 cm,平均直徑(6.51±1.64)cm;均未發生肝外轉移,并行手術治療,39例肝葉及局部切除,51例半肝切除。
1.2 入選標準
納入標準:①原發性肝細胞癌經病理證實;②患者突發腹痛,伴或不伴休克;③均滿足手術指征;④自愿簽署知情同意書。排除標準:①外傷導致的肝臟出血;②已發生遠處轉移;③心肝腎功能嚴重障礙;④伴有精神疾病或認知障礙。
1.3 方法
入選者均實施手術治療,由同一手術組進行手術,根據患者實際情況合理選擇術式,切緣應超過腫瘤邊緣2 cm以上,術后進行對癥干預。所有患者隨訪2年,統計2年生存率。根據患者生存情況分為預后良好組與預后不良組,統計兩組相關資料,包括性別(男、女)、年齡(>60歲、≤60歲)、腫瘤直徑(>5 cm、≤5 cm)、腫瘤數量(單發、多發)、手術方式(肝葉及局部切除、半肝切除)、手術時間(>3 h、≤3 h)、肝功能分級(Child A級、Child B級)、侵犯血管(是、否)、合并肝硬化(是、否)、術前甲胎蛋白(AFP,>400 μg/l、≤400 μg/l)、術后進行肝動脈栓塞化療(是、否),分析影響原發性肝細胞肝癌破裂出血手術治療預后的相關因素。
1.4 統計學分析
2 結果
2.1 隨訪結果
隨訪2年,90例原發性肝細胞肝癌破裂出血患者中,有30例預后不良,占33.33%(30/90),預后良好60例,占66.67%(60/90)。
2.2 單因素分析
后不良組腫瘤直徑>5 cm、手術時間>3 h、侵犯血管、合并肝硬化、術前AFP>400 μg/l、術后未行預防性TACE治療占比均高于預后良好組,差異有統計學意義(P<0.05);兩組性別、年齡、腫瘤數量、手術方式、肝功能分級等對比,差異無統計學意義(P>0.05),見表1。
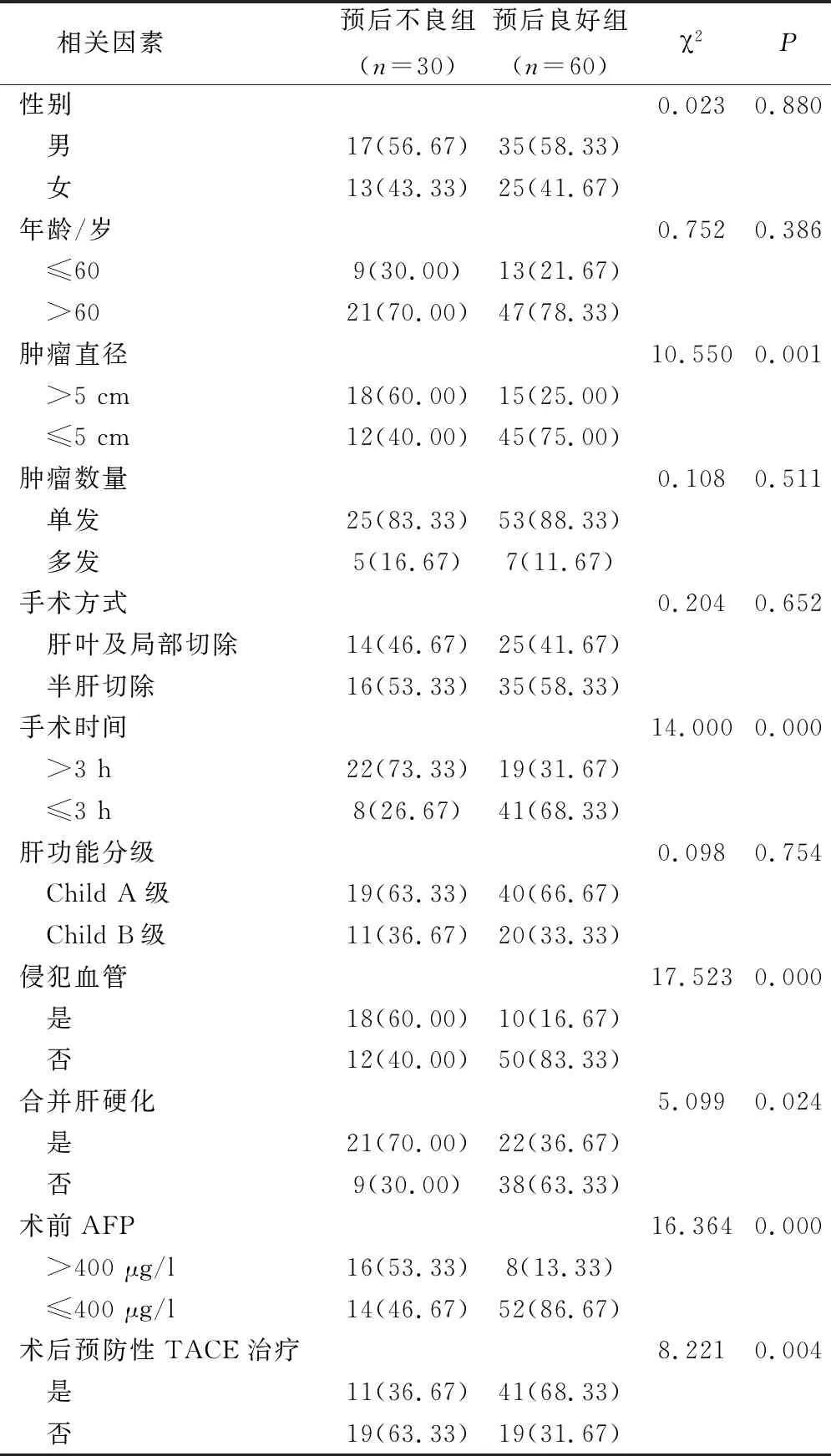
表1 原發性肝細胞肝癌破裂出血手術預后不良的單因素分析(例,%)
2.3 多因素分析
Logistic回歸分析:腫瘤直徑>5 cm、手術時間>3 h、侵犯血管、合并肝硬化、術前AFP>400 μg/L、術后未行預防性TACE治療是原發性肝細胞肝癌破裂出血手術預后不良的獨立危險因素(P<0.05且OR≥1)。見表2。
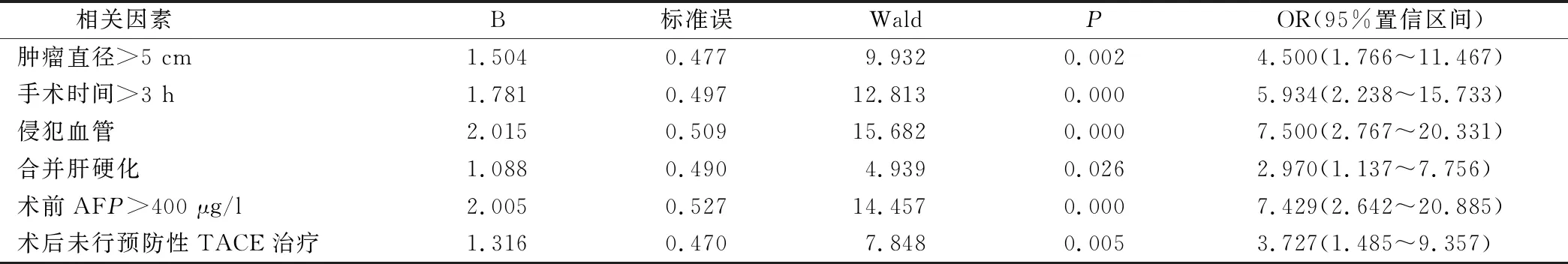
表2 原發性肝細胞肝癌破裂出血手術預后不良的多因素分析
3 討論
原發性肝細胞肝癌破裂出血為常見并發癥,具體發病機制至今尚未安全明確,可能與凝血障礙,腫瘤侵犯靜脈導致瘀血, 病灶快速生長以致中心壞死,加之病灶邊緣組織較為脆弱,當呼吸導致膈肌摩擦腫瘤或腹內壓突然增高均會引發腫瘤破裂[6]。肝臟血供極為豐富,一旦腫瘤破裂出血,患者易出現休克表現,威脅患者生命安全。目前臨床治療肝癌雖主張多學科綜合治療,但仍以外科手術效果最佳,尤其是治療并發破裂出血,手術能夠有效止血,獲得理想效果[7]。但臨床廣泛應用發現,手術治療原發性肝細胞肝癌破裂出血短時間止血效果理想,但長期隨訪發現其對提高生存率無明顯優勢,全面分析影響手術預后的危險因素至關重要[8]。
本研究結果顯示,隨訪2年,90例原發性肝細胞肝癌破裂出血患者中,有30例預后不良,占比為33.33%(30/90),預后不良組腫瘤直徑>5 cm、手術時間>3 h、侵犯血管、合并肝硬化、術前AFP>400 μg/l、術后未行預防性TACE治療占比均高于預后良好組;Logistic回歸分析:腫瘤直徑>5 cm、手術時間>3 h、侵犯血管、合并肝硬化、術前AFP>400 μg/l、術后未行預防性TACE治療是原發性肝細胞肝癌破裂出血手術預后不良的獨立危險因素。由此可原發性肝細胞肝癌破裂出血患者采用手術治療切實可行,術前準確評估、合理選擇術式、控制手術時間、加強術后治療能夠改善患者預后,提高生存率。分析其原因為,腫瘤直徑越大表示其生長速度越快,對肝臟侵襲程度深,所占肝臟體積大,血管浸潤風險更高,極易出現轉移,手術治療時所需切除的范圍較大,使得患者預后差[9]。同類型手術、同一手術組實施手術,手術時間長提示手術操作復雜,所需時間更長,且患者腹腔長時間暴露,會增加感染風險,導致機體免疫力低下,機體免疫無法抵抗殘留的癌細胞,復發風險高,導致預后不理想。血管侵犯分為微血管與大體血管侵犯,兩種血管侵犯均會增加復發與轉移風險,術中操作時需謹慎,避免擠壓瘤體[10]。當患者合并肝硬化時,會損傷患者肝功能,使得術中切除的體積受到限制,影響術后功能恢復,甚至導致術后肝功能不全,引發肝衰竭;另外肝硬化多合并凝血異常,術中出血風險增加,操作難度更大[11]。AFP為常見的糖蛋白,活動性肝病下其水平會出現升高,是臨床診斷原發性肝癌的重要指標,另外該指標水平與癌細胞數量、增生程度關系密切[12]。術后行預防性TACE治療可減少病灶播散,改善患者預后。
綜上所述,原發性肝細胞肝癌破裂出血手術治療優勢突出,能夠有效止血、切除病變組織,術前仔細評估,在確保耐受情況下手術可作為首選方法,但腫瘤直徑>5 cm、手術時間>3 h、侵犯血管、合并肝硬化、術前AFP>400 μg/l、術后未行預防性TACE治療可能會影響其預后,臨床需予以重視。

