隔日禁食結合濟饑辟谷方對NAFLD大鼠肝臟氧化應激及IRS 2的影響*
張 揚 駱建興 楊 芳 扈曉宇
成都中醫藥大學附屬醫院感染科 (四川 成都, 610072)
間歇性禁食也稱輕斷食,是一種正常飲食和禁食交替進行的飲食療法,包括時間限制禁食、隔日禁食和周期性禁食等。由于患者較易堅持,間歇性禁食在人群中流行較廣。作為全球性公共衛生問題,非酒精性脂肪性肝病(NAFLD)發生發展的病理機制復雜,其中氧化應激及胰島素抵抗(IR)發揮著關鍵作用。動物實驗和臨床研究已證實,隔日禁食可在短期內改善NAFLD及肝臟氧化應激[1-3]。先前研究表明,隔日禁食結合濟饑辟谷方能控制小鼠體質量增加和良性調節血糖、血脂[4],但兩者結合對NAFLD的影響尚未見報道。故本文研究隔日禁食結合濟饑辟谷方對NAFLD大鼠肝臟氧化應激及胰島素受體底物(IRS)2 mRNA的影響。
1 材料與方法
1.1 實驗動物、材料與儀器 清潔級雄性SD大鼠,5~6周齡,體質量(160±10)g,共44只,購自成都達碩實驗動物有限公司[生產許可證為SCXK(川)2015-030]。高脂飼料(含41.6 kcal%脂肪,TP26300)和低脂對照飼料(含12.5 kcal%脂肪,TP26312)由南通特洛菲飼料科技有限公司生產[生產許可證號:蘇飼證(2014)06092]。結合文獻[4],利用現代加工技術將濟饑辟谷方(黑豆、火麻仁、糯米等)制成干脆塊狀。BCD-236H型-70℃電冰箱(中國海爾集團有限公司),KDC-2046型低速冷凍離心機(科大創新股份有限公司),721型分光光度計(上海精密科學儀器有限公司),7170A型全自動生化分析儀(日本日立公司),轉輪式切片機(德國徠卡公司),TSJ-Ⅱ型全自動封閉式組織脫水機和PHY-Ⅲ型病理組織漂烘儀(常州市中威電子儀器有限公司),BMJ-Ⅲ型包埋機(常州郊區中威電子儀器廠),BA400Digital型數碼三目攝像顯微鏡(麥克奧迪實業集團有限公司),圖像分析軟件Image-Pro Plus 6.0(美國Media Cybernetics公司)。超氧化物歧化酶(SOD)、還原型谷胱甘肽(GSH)和丙二醛(MDA)測定試劑盒(南京建成生物工程研究所),4%多聚甲醛固定液(國藥集團化學試劑有限公司),PBS磷酸鹽緩沖液(北京中杉金橋生物技術有限公司),無水乙醇AR級(江蘇海興化工有限公司),二甲苯AR級(天津致遠化學試劑有限公司),中性樹膠(國藥集團化學試劑有限公司)等。
1.2 動物分組、干預及標本采集 44只健康雄性SD大鼠,經適應性飼養后,隨機分為兩組,正常對照組(n=12)采用低脂飼料喂養12周;高脂飼料組(n=32) 參照文獻[5]方法,采用高脂飼料喂養12周,構建NAFLD大鼠模型。12周后,每組各取2只處死,行病理檢測確定模型成功后,高脂飼料組隨機分為模型組、隔日禁食組、結合濟饑辟谷方組,每組10只,干預4周。隔日禁食采取第1天早9∶00投飼,第2天早9∶00撤回,如此往復。各組大鼠分籠飼養于(25±2)℃、明暗各12 h的動物實驗室內,自由飲水。于實驗第16周末,大鼠禁食12 h后,4%水合氯醛溶液腹腔注射麻醉,股動脈取血,取肝右葉相同部位(距離肝邊緣0.5cm處)組織若干,用于相關檢測。
1.3 觀察項目 ①血脂及肝功能測定:采集的血液在4℃下3 000 r/min離心10 min,取上層血清,用全自動生化分析法檢測總膽固醇(TC)、甘油三酯(TG)、丙氨酸氨基轉移酶(ALT)、天門冬氨酸氨基轉移酶(AST)等。②肝臟病理檢查:取肝組織置于4%多聚甲醛中固定,制備冰凍切片及石蠟切片,油紅O和TUNEL染色觀察肝細胞脂質沉積和凋亡情況,HE染色觀察肝組織形態學改變。③肝臟氧化應激指標測定:取肝組織加冷生理鹽水制成10%肝勻漿,離心,取上清液,采用試劑盒檢測SOD、GSH和MDA。④肝臟IRS2 mRNA表達:用TRIzol試劑提取肝組織總RNA,利用隨機六聚體引物反轉錄合成cDNA,使用LightCycler-FastStart DNA Master SYBR Green 1試劑盒進行實時RT-PCR。IRS-2引物序列(GenBankTMNM-003749):上游:5′-ACAACAACCACAGCGTGCGC-3′,下游:5′-GTAGAGGGCGATCAGGTACTTG-3′。β-actin引物序列(GenBankTMNM-001101):上游:5′-GCAAGAGAGGCATCCTCACC-3′,下游:5′-CGTAGATGGGCACAGTGTGG-3′。反應體積為20 μl,含有LightCycler-FastStart DNA Master SYBR Green 1,4 mmol/L MgCl2,0.5 μmol/L上游和下游PCR引物及2 μl cDNA。擴增反應如下進行:50℃ 2 min,95℃ 10 min,95℃ 15 s,60℃ 1 min,循環40次。儀器自動計算CT值。

2 結果
2.1 各組大鼠血脂及肝功能的比較 與正常對照組比較,模型組血清TC、TG、ALT、AST水平明顯升高(P<0.05);與模型組比較,隔日禁食組及結合濟饑辟谷方組均能顯著降低血清TC、TG、ALT、AST水平(P<0.05),并且結合療法的效果優于隔日禁食組。見表1。
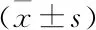
表1 各組大鼠血脂及肝功能情況比較
2.2 各組大鼠肝臟氧化應激及胰島素抵抗指標的比較 與正常對照組比較,模型組肝臟MDA含量升高、SOD和GSH活性降低、IRS 2 mRNA表達下降(P<0.05);與模型組比較,單純隔日禁食及結合濟饑辟谷方治療均能促進肝臟MDA含量、SOD和GSH活性、IRS 2 mRNA表達的恢復(P<0.05),并且二者結合的效果優于隔日禁食組。見表2。
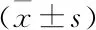
表2 各組大鼠肝組織氧化應激指標情況
2.3 各組大鼠肝臟油紅O染色的變化 正常對照組肝細胞排列整齊,間隙清晰,未見紅染脂滴。與正常對照組比較,模型組肝細胞明顯腫脹,脂質沉積,可見彌漫性的紅染脂滴及脂滴融合。與模型組比較,隔日禁食組及結合濟饑辟谷方組均能減少脂質沉積,其中二者結合的效果更佳。見圖1。

圖1 各組大鼠肝組織油紅O染色(400倍)
2.4 各組大鼠肝臟TUNEL染色的變化 正常對照組肝組織未見核呈棕褐色的凋亡細胞。與正常對照組比較,模型組肝組織內出現大量棕褐色凋亡細胞。與模型組比較,隔日禁食組及結合濟饑辟谷方組均能減少凋亡細胞,其中二者結合的效果更佳。見圖2。

圖2 各組大鼠肝組織TUNEL染色(400倍)
2.5 各組大鼠肝臟HE染色的變化 正常對照組肝細胞形態正常,結構完整,未見明顯脂肪變性及炎性細胞浸潤。與正常對照組比較,模型組肝細胞內出現大量大小不等的脂滴空泡,小葉中可見點狀壞死及炎性細胞浸潤,部分肝細胞腫脹,胞質疏松,甚至氣球樣變。與模型組比較,隔日禁食組及結合濟饑辟谷方組均能緩解肝臟脂質沉積、炎性細胞浸潤及肝細胞損傷(氣球樣變和點狀壞死),其中二者結合的效果更佳。見圖3。

圖3 各組大鼠肝組織HE染色(400倍)
3 討論
本研究發現,單純隔日禁食或隔日禁食結合濟饑辟谷方均可顯著提高NAFLD大鼠肝臟抗氧化物酶活性,減輕氧化應激,而改善肝臟脂質沉積及肝細胞損傷,且兩者結合組的效果更優。
NAFLD的發病機制尚未完全闡明,目前廣為接受的是“二次打擊”學說。第一次打擊是IR導致肝臟脂質沉積,第二次打擊主要是氧化應激致使肝臟的進一步損害[6]。線粒體是脂肪酸進行β-氧化和三羧酸循環、ATP合成及氧自由基(ROS)形成的主要場所。肝細胞內脂質超載促使過多的脂肪酸進入β-氧化途徑,進而增加ROS的產生,大量生成的ROS超過抗氧化系統清除能力時便發生氧化應激。蓄積的ROS與膜磷脂的不飽和脂肪酸反應形成脂質過氧化產物(LPO),后者又可加重線粒體損傷,增加肝細胞脂質沉積和ROS產生,如此惡性循環,最終導致肝細胞凋亡、肝臟炎性及纖維化[7,8]。本研究結果顯示,模型組肝臟脂質過氧化反應產物MDA含量升高,而抗氧化酶SOD、GSH活性降低。提示NAFLD大鼠脂質過氧化增加,抗氧化酶大量消耗,繼而引發肝細胞氧化應激損傷。因而提高肝細胞抗氧化能力使之適應脂質超負荷,對于緩解病情具有重要意義。
隔日禁食是間歇性禁食的主要形式之一。有研究認為,隔日禁食可以在不減少熱量攝入的情況下降低多種疾病的風險[9]。據報道,隔日禁食可提高年齡相關性淋巴瘤小鼠脾臟SOD、GSH活性,降低MDA含量,減少ROS產生而延長壽命[10]。它也能增加糖尿病大鼠腎臟SOD 活性,減少MDA 含量,而延緩糖尿病腎病的進展[11]。本研究結果表明,隔日禁食結合濟饑辟谷方可提高NAFLD大鼠肝組織抗氧化酶活性,減輕氧化應激損傷,并對胰島素信號通路中關鍵信號分子IRS 2 mRNA表達有調節作用。
既往證實,NAFLD常存在IR,伴有高血糖、高胰島素血癥及胰島素敏感性下降。肝臟是胰島素作用的靶器官,當存在高胰島素血癥時,肝糖輸出持續增加,加重高血糖、高胰島素血癥及IR[12]。有研究認為,肝臟IR是NAFLD進展的啟動環節,而肝臟局部氧化應激的產生可能是誘發肝臟IR的關鍵環節[13]。可以推測,隔日禁食結合濟饑辟谷方對NAFLD大鼠肝臟IR的改善作用可能與減輕氧化應激有關。
《服氣精義論·服藥論》言:“夫五臟通榮衛之氣,六腑資水谷之味。……又既絕谷,則腑味之不足。”又言:“谷不入半日,則氣衰;一日,則氣少。故須諸藥以代于谷,使氣味兼致臟腑而全也。”認為辟谷必須服餌。有研究對古代中醫文獻中服餌辟谷方劑的用藥規律進行分析,發現服餌辟谷組方選藥首重安全,盡量選擇無毒無害服用安全性高的藥物;總體上用藥平和,以甘味藥與平性藥為主,遵循甘緩平補之法;用藥多歸脾肺二經,著重調節辟谷期間體內氣的生化與運行[14]。濟饑辟谷方是一個代表性的服餌辟谷組方,由黑豆、火麻仁、糯米等高蛋白食物組成,可使患者“氣足不思食”。
綜上,隔日禁食結合濟饑辟谷方能減少NAFLD大鼠肝臟脂質沉積及肝細胞損傷,其發揮作用的機制與改善肝臟氧化應激和IR有關。二者結合既能提高個體對饑餓的耐受性,亦可提高治療效果,對NAFLD的治療提供新思路、新方法,值得深入探討。

