分側腎小球濾過率評估動脈粥樣硬化性單側腎動脈狹窄經皮腎動脈支架植入術效果分析
曾一梅,許建忠,陳 歆,初少莉,李明春
作者單位:201800 上海交通大學醫學院附屬瑞金醫院高血壓科
經皮腎動脈支架植入術(percutaneous transluminal renal angioplasty with stent,PTRAS)是治療動脈粥樣硬化所致腎動脈狹窄的主要方法,可改善腎小球濾過率(GFR)[1-3]。目前PTRAS 施行指征依據影像學狹窄程度,但影像學檢查不能反映狹窄側腎臟功能,而GFR 是評估腎動脈狹窄導致腎功能下降患者心血管疾病的重要預測指標,99mTc-EDTA 顯像劑檢測分側GFR 有助于腎功能不全早期發現缺血性腎病所造成的GFR 降低[4-6]。本研究旨在探討GFR 值評估動脈粥樣硬化所致單側腎動脈狹窄及其治療效果。
1 材料與方法
1.1 入院標準
選擇2014年7月至2019年7月在上海瑞金醫院接受PTRAS 治療的64 例動脈粥樣硬化所致腎動脈狹窄患者。入組標準:①血壓重度升高,難治性高血壓(至少三聯用藥血壓>140/90 mmHg)(1 mmHg=0.133 kPa);②術前腎動脈CTA 或MRA證實有重度腎動脈狹窄;③術前完善常規生化檢查及放射性核素腎動態顯像99mTc-乙二胺四乙酸(EDTA)檢測分側GFR;④簽署知情同意書。排除標準:①腎臟長度<7 cm;②GFR 值<10 mL/min;③雙側腎動脈狹窄或獨腎伴腎動脈狹窄;④大動脈炎或纖維肌性發育不良(FMD)引起的腎動脈狹窄;⑤嚴重肝腎功能不全或嚴重感染、心力衰竭;⑥腫瘤、自身免疫性疾病、慢性結締組織病;⑦其他手術禁忌證。
1.2 檢查方法
完善腎動脈CTA 增強掃描檢查,有CT 禁忌證者改用MR 檢查。采集清晨空腹肘靜脈血,采用AU5800 型自動生化分析儀(美國Beckman Coulter公司)測定血糖、血脂、肝腎功能及電解質。采用99mTc-EDTA 核素顯像劑檢測分側GFR。
1.3 手術方法
術前3 d 口服阿司匹林腸溶片(100 mg/d)、氯吡格雷(75 mg/d)。手術由同一組介入醫師施行,局部麻醉,6 F 或7 F 股動脈鞘管穿刺,術中應用5 000~7 000 U 肝素;造影導管證實腎動脈狹窄≥70%,依據血管狹窄病變長度和直徑選擇Sterling 球囊(美國Boston 科技公司),預擴張到達壓力后立即釋放球囊,植入合適的Express SD 球囊擴張式支架(美國Boston 科技公司)。術后口服阿司匹林腸溶片(100 mg/d)和氯吡格雷(75 mg/d)3 個月,然后改為口服阿司匹林或氯吡格雷12 個月。同時囑患者改善生活方式,予以強化他汀類藥物調脂抗動脈粥樣硬化治療,根據血壓、血糖情況調整降壓降糖藥物。
1.4 隨訪
術后隨訪12 個月,患者自行測量血壓3 次,記錄3 次收縮壓平均值;復查患者術后降壓藥調整情況,記錄降壓藥種類和劑量;復查血肌酐、分側GFR,腎臟疾病膳食改良(MDRD)公式計算GFR 估計值(eGFR)。
1.5 統計學分析
采用SPSS 19.0 軟件進行統計學分析。計量資料符合正態分布以±s 表示,組間比較用獨立樣本t檢驗或成對t檢驗,非正態分布以M(P25~P75)表示。P<0.05 為差異有統計學意義。
2 結果
64 例患者PTRAS 術均順利成功,其中1 例單側植入2 枚腎動脈支架。患者基本資料見表1。術后隨訪12 個月,患者收縮壓、舒張壓較術前顯著改善(P<0.001,P=0.003),降壓藥種類較術前差異無統計學意義(P>0.05);MDRD 公式計算顯示,eGFR 較術前無明顯改善(P>0.05),見表2。雙側腎臟GFR檢測結果顯示,術前患側GFR 與健側相比明顯下降(P=0.002),術后12 個月患側GFR 與健側差異無統計學意義(P>0.05),但患側GFR 較術前顯著改善(P=0.001),見表3。
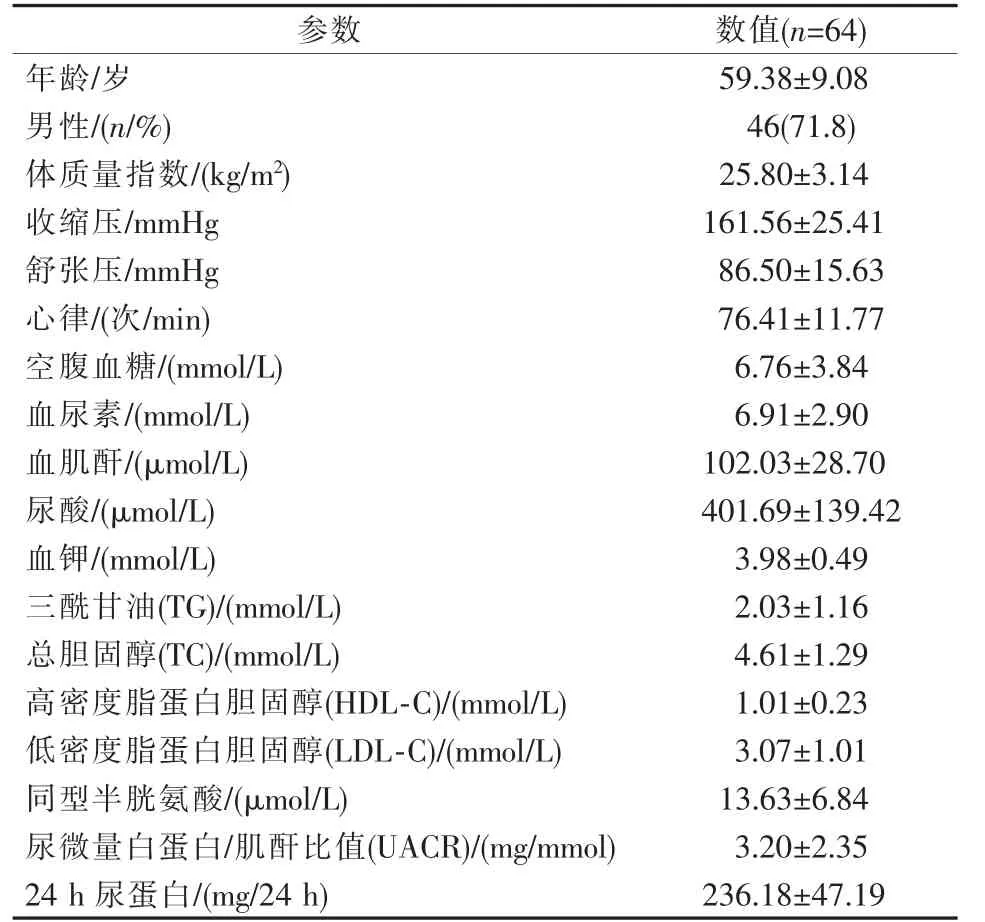
表1 患者基本資料
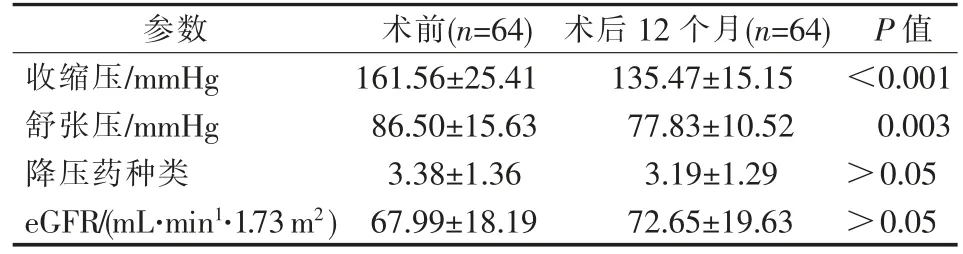
表2 術前與術后12 個月相關參數比較

表3 患側與健側GFR 比較
3 討論
腎動脈狹窄是繼發性高血壓原因之一,其激活腎素-血管緊張素-醛固酮系統(RAS),導致血管緊張素升高,引起血壓升高。動脈粥樣硬化是腎動脈狹窄常見原因。有研究顯示PTRAS 可改善腎動脈狹窄引起的血壓升高[7-10]。雖然PTRAS 治療是腎動脈成形術主要術式,但一些臨床研究通過血肌酐和eGFR 評估腎臟功能后認為,PTRAS 與藥物治療相比并不改善遠期生存率和腎臟功能[8]。本研究結果顯示,PTRAS 術后12 個月患者平均收縮壓和舒張壓與術前相比均明顯下降,術后平均收縮壓下降較舒張壓明顯,但降壓藥劑量無明顯改善。這與既往研究結果一致[7-9]。
PTRAS 治療的另一目的是防止慢性進行性腎衰竭,但術后能否改善腎功能目前尚存爭議,尤其是對于術前腎功能正常或僅有輕度腎功能障礙患者。有研究報道PTRAS 不能改善腎功能[2-3,7-8]。PTRAS 治療、藥物治療及外科治療對比研究顯示,PTRAS 在改善患者腎功能方面無明顯優勢,術后血清肌酐水平無明顯變化,根據肌酐計算eGFR 無明顯改善[3,8]。但腎動脈狹窄可引起患側腎臟缺血,導致GFR 下降,而非狹窄側腎臟因代償,超濾維持正常eGFR,隨后在血管重建和血壓控制下GFR 降低至正常值,以限制總eGFR 改善的可能性[4-5,11]。腎動脈狹窄等長期缺血會導致GFR 不可逆受損,甚至使腎臟萎縮。有研究報道顯示GFR 與腎動脈狹窄患者心血管事件有關[5]。PTRAS 可逆轉腎臟缺血,保護腎臟,但對健側腎臟GFR 無明顯改善。本研究通過直接檢測分側GFR 反映單側腎臟功能,更可直接反映腎臟缺血性損害,術后隨訪分側GFR 有助于更精準地評估PTRAS 對患側腎功能改善情況[12]。本研究顯示PTRAS 術前腎動脈狹窄患者患側GFR 較健側明顯下降,術后12 個月健側GFR 較術前差異無統計學意義,但患側GFR 較術前顯著改善。
綜上所述,PTRAS 可提高動脈粥樣硬化性腎動脈狹窄患者患側GFR,分側GFR 下降可作為行PTRAS 指征之一。分側GFR 可較好地預測血管重建效果。本研究為單中心小樣本研究,未設置對照組,有待多中心大樣本隨機對照研究進一步證實。

