局部應用不同劑量普伐他汀干預兔激素性股骨頭壞死的組織學觀察*
楊業靜 梁紅鎖 蔡 敏 農桔安 劉 雷 杜勇軍
廣西南寧市第二人民醫院關節外科 530031
研究表明,他汀類藥物局部應用于骨內具備骨誘導作用,可促進新骨形成[1-2]。骨形態發生蛋白2(Bone morphogenetic protein-2,BMP-2)因具有顯著的誘導骨與軟骨形成特性而被廣泛應用于骨科基礎與臨床研究,本課題組前期研究中發現普伐他汀局部應用干預兔激素性股骨頭壞死(Steroid-induced osteonecrosis of the femoral head,SONFH),可以促進壞死股骨頭BMP-2高表達,加速骨壞死修復[3-4]。理論上隨著局部用藥量的增加,藥物本身所產生的不良反應可能會增多。本實驗旨在觀察局部給予不同劑量普伐他汀干預SONFH的效果,探討其給藥的最佳劑量,以期為SONFH治療提供新的方法。報道如下。
1 材料與方法
1.1 實驗動物 成年健康新西蘭兔40只,雌雄不限,體質量2.5~3.0kg,由廣西醫科大學實驗動物中心提供,實驗動物使用許可證號:SYXK(桂)2014-0003。所有動物在同一室內分籠飼養,給予定量飼料喂養,自由飲水。室溫20~22℃,濕度40%~60%,維持室內自然光照及良好通風。
1.2 動物模型制備與分組 所有動物常規適應性喂養2周,再次稱重后制備SONFH模型,參照秦嶺等[5]的造模方法:以10μg/kg劑量經兔耳緣靜脈注射內毒素(Lippolysaccharide,美國Sigma公司)1次,24h后以20mg/kg劑量的甲強龍(Methylprednisolone,美國輝瑞公司)進行3次臀肌注射,每次間隔24h。造模6周后,采用隨機數字表法將動物分為A、B、C、D 4組,每組10只,各組間動物體質量及雌雄構成比無統計學意義(P>0.05)。所有動物在麻醉后進行股骨頭髓芯減壓術,其中A組于股骨頭髓芯減壓通道內植入含1mg普伐他汀(鈷60輻照滅菌,下同)的明膠海綿,B組植入含2mg普伐他汀的明膠海綿,C組植入含5mg普伐他汀的明膠海綿,D組植入含10mg普伐他汀的明膠海綿。髓芯減壓采用本課題組前期實驗方法[6]。
1.3 觀察指標 分別在股骨頭髓芯減壓術后第8、12周以空氣栓塞法每組各處死5只兔子,取其左側股骨頭標本進行病理學研究,對側行分子生物學相關研究(另文發表)。剔除股骨頭周圍軟組織,將兔股骨頭沿冠狀面正中縱行切開進行大體觀察,重點觀察兔股骨頭的外形、顏色、軟骨厚度等。隨后股骨頭標本以10%甲醛溶液固定后,5%硝酸浸泡脫鈣,梯度乙醇脫水,常規石蠟包埋后進行切片,厚度為5μm。脫蠟后進行HE染色,光鏡下觀察軟骨、軟骨下骨、骨髓腔內骨小梁結構及各種細胞成分如骨細胞、脂肪細胞等變化情況。每個標本光鏡下隨機選取5個高倍視野,每個視野計數20個骨細胞中的空骨陷窩數量,其平均值即為該股骨頭的空骨陷窩率(空骨陷窩數量/20×100%)。
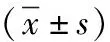
2 結果
2.1 大體觀察 A組:髓芯減壓術后第8周,股骨頭軟骨面顏色暗紅,骨皮質薄且松脆,易于切開,髓腔內可見大范圍骨壞死。術后第12周,股骨頭外形正常,骨皮質較前稍增厚,骨壞死面積稍減小。B組:術后第8周,股骨頭軟骨面顏色較暗,骨皮質薄且脆,髓腔內有較多壞死骨組織。術后第12周,股骨頭外觀正常,骨壞死面積較前減少。C組:術后第8周,股骨頭軟骨面顏色稍暗,骨皮質稍薄,質硬,有少量壞死骨組織。術后第12周,股骨頭外形正常,顏色正常,軟骨面光滑、完整。D組:術后第8周,股骨頭軟骨面顏色稍白,骨皮質略薄,骨質較硬,髓腔內可見有少量壞死組織。術后第12周,股骨頭外觀及軟骨面顏色正常。
2.2 光鏡觀察 A組:術后第8周,股骨頭內可見大量壞死骨組織,骨小梁稀疏、斷裂,有較多空骨陷窩,脂肪細胞堆積。術后第12周,股骨頭內有部分纖維組織及新生骨小梁形成,空骨陷窩較前稍減少(見圖1)。B組:術后第8周,股骨頭內有較多壞死骨組織,脂肪細胞數目增多,骨小梁纖細、紊亂,空骨陷窩數較多。術后第12周,股骨頭內有少量新生骨小梁形成,空骨陷窩數稍減少(見圖2)。C組:術后第8周,股骨頭內可見少量脂肪細胞,骨小梁相對致密,排列稍紊亂,空骨陷窩數較少。術后第12周,股骨頭內有廣泛新生骨小梁形成,空骨陷窩少(見圖3)。D組:術后第8周,股骨頭內骨小梁較排列較整齊、規則,脂肪細胞少,有少量空骨陷窩。術后第12周,股骨頭內可見骨小梁致密,脂肪細胞形態正常,空骨陷窩少(見圖4)。
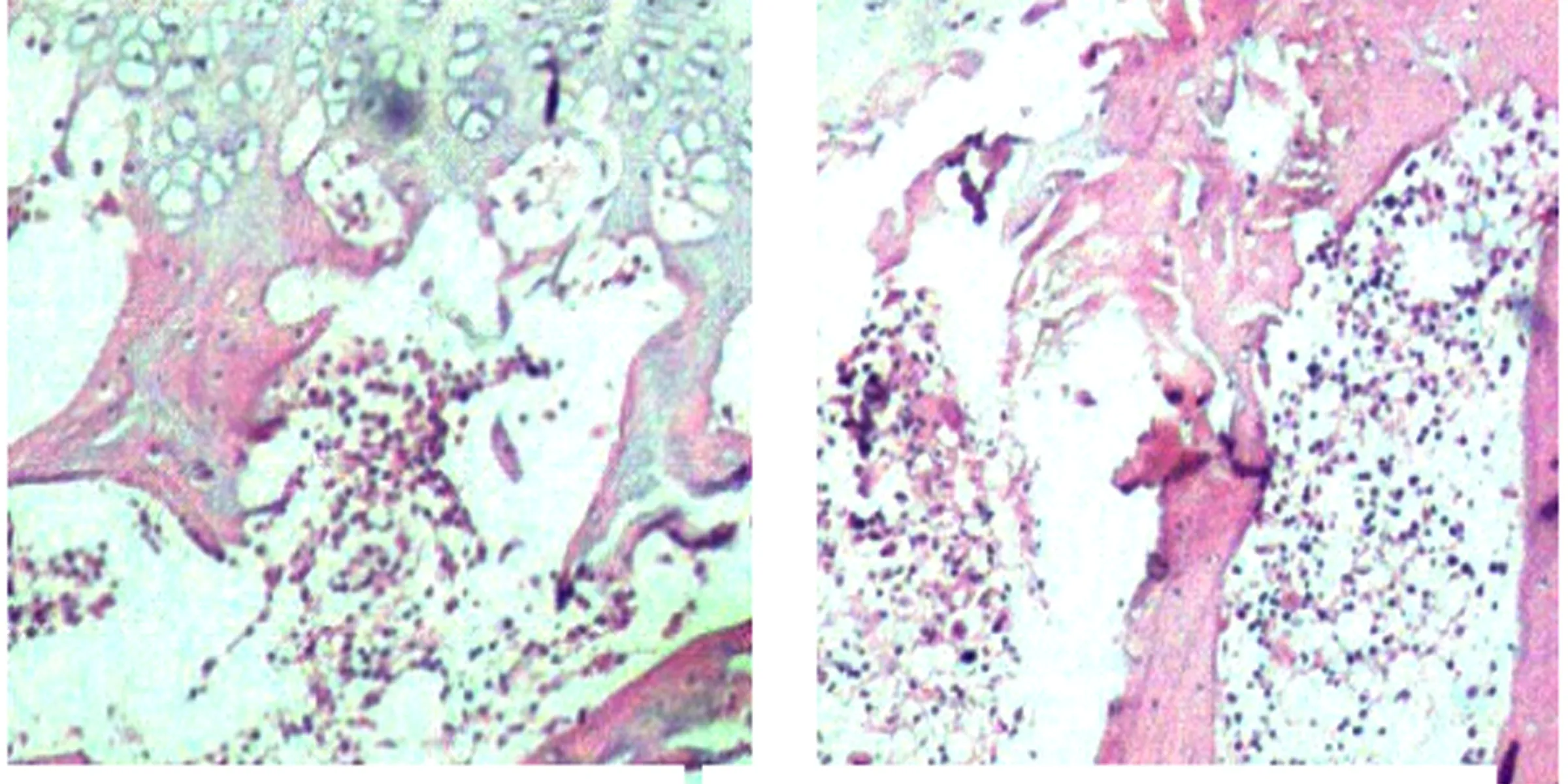
圖1 A組術后第12周HE染色(×200) 圖2 B組術后第12周HE染色(×200)

圖3 C組術后第12周HE染色(×200) 圖4 D組術后第12周HE染色(×200)
2.3 各組不同時間點空骨陷窩率比較 術后第8、12周,C、D兩組空骨陷窩率均低于A、B兩組(P<0.05),其中A、B兩組間空骨陷窩率比較,差異無統計學意義(P>0.05),C、D兩組間比較,差異亦無統計學意義(P>0.05),見表1。

表1 4組術后第8、12周空骨陷窩率
3 討論
因應用激素而導致的SONFH是一種骨科常見病,如未進行有效干預,約80%的患者在發病2~4年后出現股骨頭塌陷、變扁,導致髖關節疼痛和功能障礙。現有以保留股骨頭為主的各種方法如髓芯減壓、帶血管蒂的骨移植、血管束植入等,雖然取得了一定的療效,但其遠期效果欠理想。SONFH患者主要以青壯年為主,好發年齡為30~50歲,常累及雙髖,病情進展迅速,如未進行有效治療,大部分患者最終需接受人工全髖關節置換術。由于人工關節假體使用壽命有限,且假體植入后存在感染、松動及假體周圍骨折等并發癥,如發生上述情況還需進行人工髖關節翻修手術。如此不僅治療費用昂貴,同時還存在圍手術期失血量大、假體植入后因關節周圍骨量丟失穩定性差等潛在風險,給患者造成嚴重的手術創傷和沉重的經濟負擔。對于該類青壯年患者,如何在早期盡可能保留其自體股骨頭,推遲實施人工髖關節置換,甚或逆轉乃至治愈SONFH具有重要的現實意義。
SONFH的發病機制目前尚未完全明確。糖皮質激素在進行機體脂肪動員的同時,抑制組織細胞對血液中脂肪的利用,引發高脂血癥。同時激素還誘導骨髓干細胞向脂肪細胞轉化,加之股骨頭內特有的微循環系統,引起股骨頭血管內脂肪栓塞和微血栓形成,最終導致骨壞死[7]。因此,應用降脂藥物來干預早期SONFH是值得進行的有益探索。他汀類藥物為3-羥基-3-甲基戊二酰輔酶A(3-Hydroxy-3-mothylglutaryl coenzyme A,HMG-COA)還原酶抑制劑,是膽固醇合成的限速酶,已廣泛應用于臨床來防治高脂血癥、冠心病、腦梗死等心腦血管疾病。Nishida等[8]以匹伐他汀對兔早期SONFH進行干預,與激素模型組相比,匹伐他汀組股骨頭髓腔內脂肪細胞體積明顯減小,數量顯著減少,表明匹伐他汀可明顯改善SONFH預后。近年來,有研究表明他汀類藥物在降脂的同時,可促進新骨形成、增加骨密度[9-10]。他汀類藥物口服給藥能有效促進SONFH骨組織內相關成骨因子的表達,加速激素性壞死股骨頭修復[11-12]。
由于他汀類藥物口服后經過肝臟的首過效應,其作用于骨組織中濃度更低,如要達到其有效治療濃度,勢必加大給藥劑量,如此該副作用將進一步增加,導致臨床應用受限[13]。與系統給藥相比,局部給藥可明顯增加藥物在骨組織中濃度,使其更加直接、快捷地作用于病變部位,實際療效可能會更優。Papadimitriou等[1]制作兔股骨骨缺損模型后,在骨缺損局部植入辛伐他汀,發現其局部應用能明顯促進骨缺損修復。Ishihara等[14]以自體髂骨聯合負載辛伐他汀的明膠支架植入脊柱融合的大鼠模型中,與自體髂骨聯合明膠支架相比,前者脊柱融合率明顯提高,表明辛伐他汀局部應用能有效促進術區新骨形成。本研究將負載不同劑量普伐他汀的明膠海綿植入兔激素性壞死股骨頭內,觀察其干預骨壞死效果。結果表明,A、B兩低劑量組內僅有少量新骨形成,空骨陷窩數較多。C、D兩較高劑量組中,術后各時間點股骨頭內均有較多新生骨組織形成,且隨著時間延長,新骨形成逐步增加,與A、B兩組相比,空骨陷窩數明顯減少(P<0.05)。同期C、D兩組空骨陷窩率比較并無統計學差異(P>0.05),推測可能與局部用藥量增加而影響新生血管長入等因素有關,其具體機制還有待深入研究。
綜上所述,本實驗通過在兔激素性壞死股骨頭內局部應用普伐他汀,發現較高濃度的普伐他汀可有效促進新骨形成與骨壞死修復,5mg與10mg劑量效果相似。

