蒼耳子治療過敏性鼻炎的分子機制研究
王 康,孟 泳,王玉潔,季紹威,鄧澤坤
過敏性鼻炎(Allergic rhinitis)又稱變應性鼻炎,普遍認為其是以IgE 介導的I 型變態反應。臨床癥狀為陣發性噴嚏、清水樣涕、鼻塞、鼻癢等,嚴重影響患者的睡眠及生活質量。據流行病學顯示,全球約有10%~40%的人口患有此病[1]。在我國,過敏性鼻炎患病率達10%以上,近幾年呈上升趨勢[2]。長期的臨床觀察發現,過敏性鼻炎控制不當,易誘發支氣管哮喘。
蒼耳子為菊科植物,性味辛、苦、溫,具有散風寒、通鼻竅的功效,是治療鼻鼽的良藥,臨床應用廣泛。在對治療鼻部疾病的常用方劑統計發現[3],含有蒼耳子的方劑占比約80%。經動物實驗證實[4],含蒼耳子正丁醇的滴鼻劑和蒼耳油對變應性鼻炎有較好的治療作用,但其具體作用機制不明。網絡藥理學是中醫藥研究的新途徑,不但能揭示中藥對機體的網絡調控,也能為新藥的研發提供方向,節約成本[5]。為了更好地闡述蒼耳子治療疾病的分子機制,本研究將借助網絡藥理學對此進行探討。
1 材料和方法
1.1 數據庫及軟件 本研究所涉及的數據庫:中藥系統藥理學數據庫與分析平臺(traditional Chinese medicine systems pharmacology database and analysis platform,TCMSP)(https://tcmspw.com/tcmsp.php),有機小分子生物活性數據庫(PubChem)(https://pubchem.ncbi.nlm.nih.gov/),在線人類孟德爾遺傳數據庫(online mendelian inheritance in man, OMIM)(https://omim.org/),基因組注釋數據庫平臺(GeneCards)(https://www.genecards.org/),基因與疾病關聯數據庫(DisGeNET)(https://www.disgenet.org/),全球蛋白資源數據庫(Uniprot)(https://www.uniprot.org/),蛋白質相互作用關系網絡數據庫(String)(https://string?db.org/),蛋白質結構數據庫(prorein data bank,PDB)(https://www.rcsb.org/),生物信息學開源軟件平臺(Bioconductor)(http://www.bioconductor.org/)。軟件:R 語言(V4.1.1)(https://www.r?project.org/),Cytoscape(V3.7.0)(https://cytoscape.org/),PyMOL(V2.1.1)(https://pymol.org/),iGemdock(V2.1)(http://gemdock.life.nctu.edu.tw),AutoDock Tools(V1.5.6)(http://autodock.scripps.edu/)。
1.2 中藥蒼耳子化學成分收集及靶點預測 借助TCMSP 平臺查找蒼耳子的化學成分,以口服利用度(oral bioavailability,OB)≥30%以及藥物相似性(drug?likeness,DL)≥0.18 為條件進行篩選,獲取藥物的有效活性成分。繼續運用TCMSP 數據庫查找其有效活性成分的對應靶點,借助Uniprot 數據庫對蛋白靶點進行人類基因標注并規范化處理。
1.3 過敏性鼻炎靶點篩選 以“Allergic rhinitis”為關鍵詞,分別在疾病數據庫OMIM、GeneCards和Dis-GeNET進行檢索,對得到靶點進行匯總及去重處理。
1.4 “成分?靶點”網絡構建 借助Excel 2019 軟件對1.2和1.3得到的結果進行比對,找出中藥與疾病的共同蛋白靶點,并將其導入Cytoscape 軟件平臺,構建“成分?靶點”網絡。網絡中節點由中藥的活性成分和中藥治療疾病的靶點兩部分構成。兩者的相互關系以邊表示。
1.5 蛋白相互作用(PPI)網絡構建 將1.4 中找到的共同蛋白靶點導入在線數據庫String 中進行分析,種屬選擇Homo sapien,將得到的蛋白相互作用關系數據(combined score≥0.4)進行下載,將所得數據導入Cytoscape 軟件進行分析,按照度值大小選出藥物治療疾病的關鍵靶點。
1.6 GO 功能富集和KEGG 通路富集 運用R 語言將1.4 中找到的共同蛋白靶點進行基因本體論(gene ontology, GO)功能富集和(kyoto encyclopedia of genes and genomes,KEGG)通路富集分析,得到蒼耳子治療過敏性鼻炎的主要功能富集和作用通路。
1.7 小分子優化處理 對1.4 得到的主要活性成分通過PubChem 數據庫查找相應的3D 結構(或2D 結構)并下載“SDF”格式文件,用Pymol軟件進行格式轉換。將1.5所得到的治療過敏性鼻炎的關鍵靶點通過PDB 數據庫查找蛋白晶體結構,依據分辨率Resolution(A)、配體等條件進行篩選,選出最佳蛋白晶體結構并下載“PDB”格式文件。通過Pymol軟件對所得到的蛋白晶體結構進行除水、剔除雜質等優化處理。
1.8 分子對接 用AutoDock Tools 軟件對主要活性成分(配體)和優化后的蛋白晶體結構(受體)進行分子對接前數據處理。受體進行加氫、計算電荷、添加原子類型等結構處理并保存PDB 文件格式。配體進行root 判定及扭轉鍵選擇等操作處理并保存PDB 格式。利用iGemdock 軟件對受體配體進行匹配篩選,找出最佳受體與配體的匹配方式。將最佳匹配方式運用AutoDock Tools軟件進行分子對接。用Pymol軟件對對接結果進行優化展示。
2 結果
2.1 中藥化學成分收集及靶點預測 以OB≥30%、DL≥0.18 為條件在TCMSP 進行蒼耳子有效成分的查找與篩選,得到有效活性成分11 個,搜索到有對應靶點的有效活性成分7 個(無對應靶點的有效成分已剔除),表1。

表1 蒼耳子有效活性成分
2.2“成分?靶點數據庫”建立 通過查詢疾病數據庫OMIM、Gene Cards和DisGeNET,得到過敏性鼻炎疾病相關基因1 575個。通過與蒼耳子蛋白基因進行比對,得到蒼耳子治療過敏性鼻炎的潛在靶點15個,構建“蒼耳子?過敏性鼻炎疾病靶點”數據庫。
2.3 “成分?靶點”網絡構建 將“蒼耳子?過敏性鼻炎疾病靶點”數據庫導入Cytoscape軟件構建網絡圖(圖1)。該網絡圖共有22個節點和26條邊,圖中紫色長方形代表疾病,黃色橢圓形代表藥物,粉色八邊形代表潛在靶點,藍色六邊形代表有效成分。
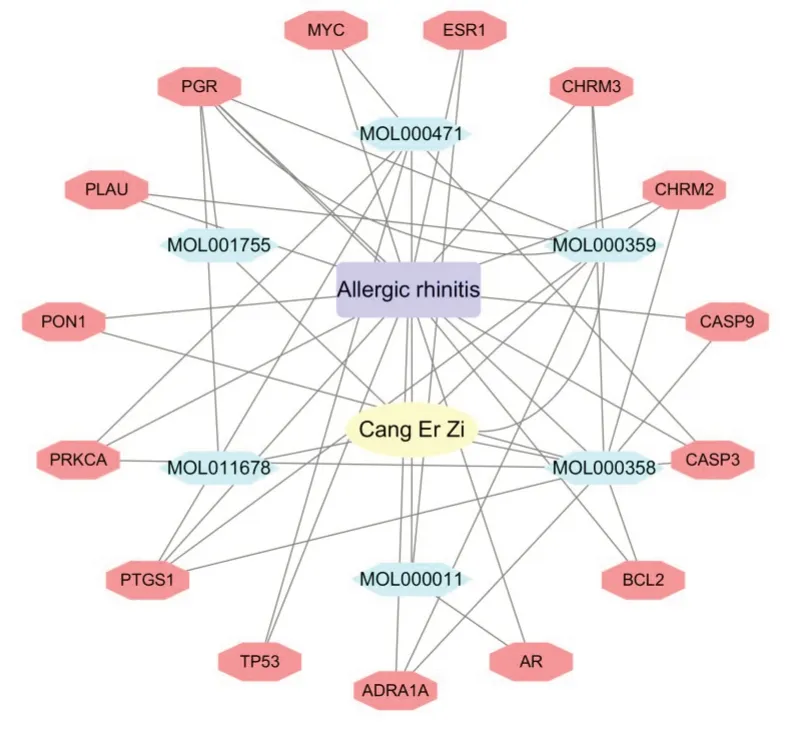
圖1 蒼耳子的有效成分?靶點相互作用網絡
經網絡拓撲學分析后,將蒼耳子的7 種有效成分按照度值大小排序,排名前4的有效成分為beta?sitosterol(β 谷甾醇)、stigmasterol(豆甾醇)、aloe?emodin(蘆薈大黃素)、(2R,3R)?3?(4?hydroxy?3?methoxy?phenyl)?5?methoxy?2?methylol?2,3?dihydropyrano(5,6?h)(1,4)benzodioxin?9?one(即 Cleomiscosin A,黃花菜木脂素A)。
2.4 蛋白相互作用(PPI)網絡構建 借助String 平臺對蒼耳子治療過敏性鼻炎的潛在靶點進行分析,獲得PPI網絡圖(剔除游離蛋白),圖2。
圖2 蒼耳子治療過敏性鼻炎的潛在靶點PPI網絡圖
對PPI 所得的數據按照度值進行可視化處理,圖3。度值越大表明與其他蛋白的相互作用越強,地位越關鍵。
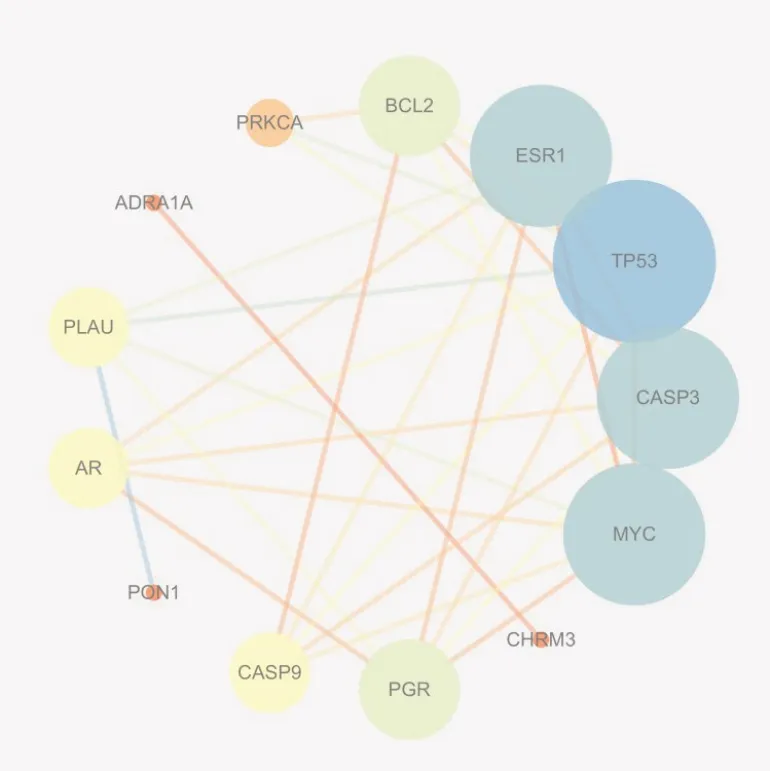
圖3 蛋白相互作用度值數可視化
從圖3 可知,度值較大的靶點蛋白分別是:細胞腫瘤抗原p53(tumor protein 53,TP53)、半胱氨酸蛋白酶?3(cysteine protease?3,CASP3)、雌激素受體(estrogen receptor,ESR1)、Myc 原癌基因蛋白(myc proto?oncogene protein,MYC)、細胞凋亡調節因子Bcl?2(apoptosis regulator bcl?2,BCL2)及孕酮受體(progesterone receptor,PGR)。
2.5 GO 功能富集分析 運用R 語言對蒼耳子治療過敏性鼻炎的潛在靶點進行GO 功能富集分析,篩選條件:pvalueCutoff=0.05。通過Goplot 對結果進行展示,圖4。

圖4 蒼耳子治療過敏性鼻炎的功能?靶點Goplot圖
由圖4 可知,靶點參與的生物過程主要有:參與神經膠質細胞凋亡過程(glial cell apoptotic process)、上皮管細胞的分支形態發生(branching morphogenesis of an epithelial tube)、上皮管細胞形態發生(epithelial tube morphogenesis)、分支上皮細胞的形態發生(morphogenesis of a branching epithelium)、分支結構細胞的形態發生(morphogenesis of a branching structure)、對紫外線的反應(response to UV)以及女性性特征的發育等。
2.6 KEGG通路富集分析結果
運用R 包(ClusterProfiler)對蒼耳子治療過敏性鼻炎的潛在靶點進行KEGG 通路富集分析,設定條件pvalueCutoff=0.05。在得到的結果中,選出顯著性差異最大的20條通路繪制條形圖,圖5。
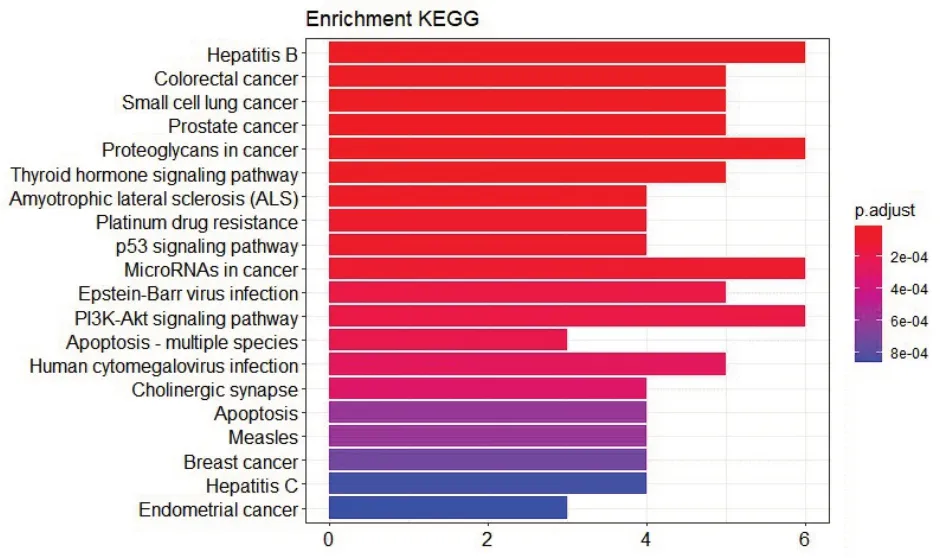
圖5 蒼耳子治療過敏性鼻炎的潛在靶點KEGG富集通路條形圖
由圖5可知,靶點參與的信號通路有:甲狀腺激素信號通路(Thyroid hormone signaling pathway)、p53信號通路(p53 signaling pathway)、PI3K?Akt信號通路(PI3K?Akt signaling pathway),和相關疾病通路如乙型肝炎(Hepatitis B)、結腸直腸癌(Colorectal cancer)、小細胞肺癌(Small cell lung cancer)、前列腺癌(Prostate cancer)、麻疹(Measles)等。
2.7 分子對接結果 借助AutoDock Tools 軟件對主要有效成分的小分子(配體)及關鍵蛋白靶點(受體)結構優化后,運用iGemdock 軟件對配體與受體進行對接匹配(表2)。配體與受體結合能越低,表示兩者發生作用的可能性就越大。由表2 可知MOL000011(即 Cleomiscosin A)與TP53、CASP3、ESR1、MYC及PGR均是最優對接形式。運用AutoDock Tools 軟件對Cleomiscosin A 的最優結合模式進行分子對接驗證(圖6)。
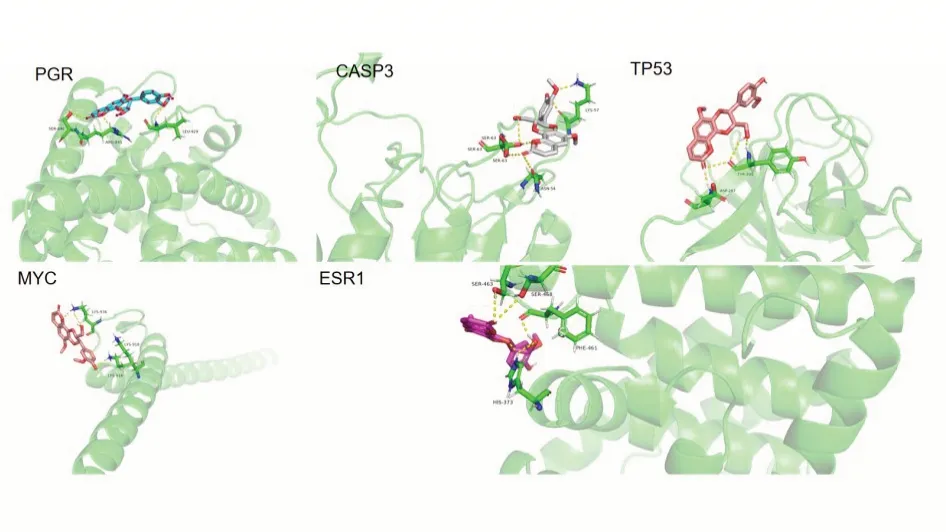
圖6 MOL000011與TP53、CASP3、ESR1、MYC及PGR蛋白的分子對接圖
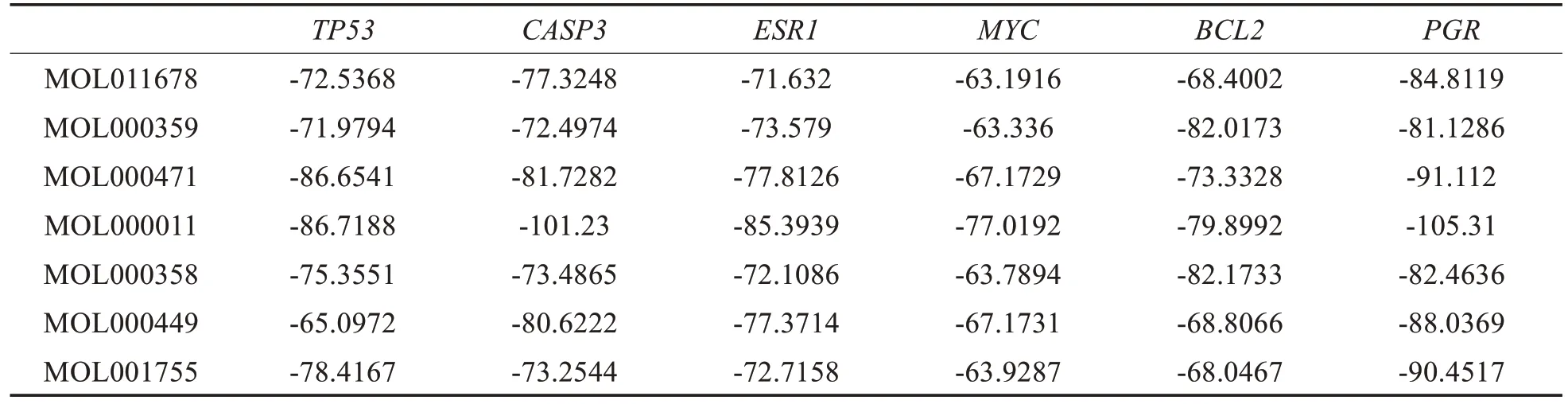
表2 主要有效成分與關鍵靶點的結合能
從圖 6 可知,Cleomiscosin A 與TP53、CASP3、ESR1、MYC、PGR5 個靶點蛋白的氨基酸殘基均形成了2個以上的氫鍵。
3 討論
過敏性鼻炎為呼吸系統的常見疾病,發作具有明顯的季節性。發作時,嚴重影響患者的正常工作與生活。隨著對過敏性鼻炎研究的深入,人們發現其發病與鼻黏膜上皮細胞及上皮源性細胞因子、II型固有淋巴細胞、輔助T 細胞免疫失衡、Breg 細胞、樹狀突細胞、肥大細胞、嗜酸性粒細胞相關,是由輔助T細胞、肥大細胞等炎性細胞與IL?4、IL?5等細胞因子共同相互作用的結果[6]。蒼耳子為傳統中醫治療鼻炎的常用藥物。現代藥理學研究指出[7],蒼耳子含有脂肪酸、木脂素類級酚酸類等多種化學成分,并具有抗炎鎮痛、抗菌、抗病毒等多種藥理作用。通過小鼠動物實驗研究發現[8],蒼耳子通過穩定肥大細胞膜,減少組胺等過敏介質的釋放,抑制肥大細胞依賴性速發型過敏反應。
本研究通過對數據庫的檢索及數據處理,明確了蒼耳子中 beta?sitosterol、Stigmasterol、aloe?emodin、Cleomiscosin A 是治療過敏性鼻炎的主要有效成分。經過模擬分子對接發現,Cleomiscosin A 與TP53、CASP3、ESR1、MYC及PGR都能較好的結合。文獻指出,Cleomiscosin A 為一種有機雜三環化合物,屬于天然香豆素內酯范疇,具有抗炎活性,可抑制TSLP 表達[9]。TSLP 被認為是最常見的炎癥性過敏性疾病,如哮喘、特應性皮炎及特應性鼻炎的主開關,在小鼠動物實驗中[10],當阻斷TSLP 信號表達時,變應原特異性血清IgE 水平、嗜酸性氣道組織炎癥及Th2細胞因子水平等顯著降低。Th2細胞因子水平與過敏性鼻炎的發生關系密切。當Th2 細胞因子活性增強時能誘導體內IgE 合成,促使前列腺素、白三烯及組織胺等遞質釋放,增加毛細血管通透性及腺體分泌,導致嗜酸性粒細胞水平升高,進而引起過敏性鼻炎的相關臨床癥狀[11]。beta?sitosterol 和Stigmasterol 均屬于植物甾醇類,具有抗炎、抗氧化及免疫調節的作用。研究發現[12-13],β?谷甾醇具有降低血清組胺和IgE 水平,減少肥大細胞的產生及下調TSLP 水平的作用。豆甾醇在治療IgE介導的過敏性疾病方面有巨大潛力。蘆薈大黃素為蒽醌類生物活性成分,能通過抑制T 細胞達到機體免疫調節的功能[14]。以上研究表明,蒼耳子通過多成分治療過敏性鼻炎。
通過GO 功能富集以及KEGG 通路富集得出,蒼耳子可能通過甲狀腺激素信號通路、p53 信號通路及PI3K?Akt 信號通路來達到調節上皮細胞及控制神經膠質細胞的凋亡,從而達到治療過敏性鼻炎的作用。研究發現[15],神經膠質細胞中的小膠質細胞能調節T細胞的增殖。T細胞和上皮細胞的異常是過敏性鼻炎誘發的因素[16-17]。
本研究借助網絡藥理學方法,展示了蒼耳子治療過敏性鼻炎的多成分、多靶點、多通路、多功能的作用特點,通過對T細胞和上皮細胞的調控來達到治療過敏性鼻炎的目的。經過分子對接展示蒼耳子發揮作用的可能過程,為后續實驗驗證提供理論指導。

