基于冠狀動脈CTA的FFRCT與斑塊特征對冠心病患者主要不良心臟事件的預測價值
孫欣杰 徐 怡 朱曉梅 葛穎倩 祝因蘇 薛秋蒼 施海彬
冠心病(coronary artery disease,CAD)是臨床最常見的心血管疾病,其患病率和死亡率仍處上升階段。冠狀動脈(冠脈)斑塊進展可致血管狹窄、斑塊破裂及心肌血流灌注異常,從而引發主要不良心臟事件(major adverse cardiac events,MACE)[1-2]。大量研究證實冠脈CT血管成像(computed tomography angiography,CTA)可以準確評估冠脈解剖狹窄率,但對于冠脈狹窄的功能學評估存在局限性。近年來,基于冠脈CTA數據并應用人工智能算法獲得其血流儲備分數(FFRCT)的技術已逐漸成熟。研究[3]表明,通過增加冠脈狹窄的相關功能學信息,使得FFRCT對CAD患者特異性心肌缺血的判斷具有比冠脈解剖狹窄率這一指標更高的診斷價值,且FFRCT被證明與有創性FFR有良好的相關性。此外,冠脈CTA可以顯示管壁上的斑塊并借助軟件對斑塊進行定量評估,還可以依據形態學特征識別易損斑塊[4]。但是,從冠脈CTA所獲得的斑塊特征和FFRCT對CAD患者MACE的預測潛力尚不明確。本研究旨在比較基于冠脈CTA的解剖狹窄程度、FFRCT、斑塊特征以及三者聯合對CAD患者MACE的預測價值。
方 法
1.臨床資料
回顧性分析2016年6月至2018年12月我院心臟外科收治的疑似CAD而行冠脈CTA及侵入性冠脈造影(ICA)檢查的患者資料。根據隨訪中MACE發生情況分為MACE陽性組與MACE陰性組。MACE定義為:①心源性死亡(致死性心肌梗死);②非致死性心肌梗死;③不穩定心絞痛致冠脈再血管化;④不穩定心絞痛致再住院治療。納入標準:①冠脈CTA顯示管腔狹窄率為30%~70%且與ICA結果相一致;②冠脈CTA與初次ICA檢查間隔時間≤3個月,且未行經皮冠脈介入治療(PCI);③病史資料完整,并獲得隨訪結果。排除標準:①既往有心肌梗死、PCI或冠脈旁路移植術(CABG)史(n=17);②患者年齡>80歲(n=4);③圖像質量不佳(n=13);④冠脈CTA顯示單支血管多處病變(狹窄率均大于50%)及多支血管(狹窄率均大于50%)多處病變,無法判定責任血管(n=10)。最終納入88例患者。
2.MACE相關責任病變
對于MACE陽性患者:①若僅單支冠脈狹窄率>50%,則認為該血管是MACE責任血管;②若多支血管狹窄率>50%,則再血管化治療血管為責任血管;③心電圖提示有異常或者超聲心動圖室壁運動異常節段相對應供血血管認為是MACE責任血管。
3.冠脈CTA檢查方法
使用第一代、第三代雙源CT(SOMATOM Definition,Force;Siemens,Germany)及256排CT(Revolution;GE Healthcare,USA)獲得冠脈CTA圖像。所有患者于檢查前5 min舌下含服硝酸甘油。先進行常規鈣化積分掃描。增強掃描的觸發采用Bolus Tracking技術,掃描范圍自氣管分叉下方1 cm至心尖部。碘對比劑以4.0~6.0 ml/s的流率注射,總量50~80 ml。第一代雙源CT掃描主參數:管電壓120 kV/100 kV,管電流自動調節,探測器準直為32 mm×0.6 mm,機架旋轉時間0.33 s;第三代雙源CT掃描主要參數:自動管電壓及管電流調節技術,探測器準直96 mm×0.6 mm,機架旋轉時間0.25 s;Revolution CT掃描主要參數:管電壓120 kV/100 kV,管電流自動調節,準直器寬度160 mm,機架旋轉時間0.28 s。圖像層厚0.75 mm或0.625 mm。所有冠脈CTA數據均傳至工作站(syngo.via VB10,Siemens)進行后處理。
4.圖像分析與后處理
4.1 FFRCT值測量
選取收縮期或舒張期圖像中質量較好的一期圖像,使用基于機器學習軟件(Siemens cFFR,3.1.2版)獲得冠脈的FFRCT值。該算法基于冠脈CTA血管解剖的幾何特征,采用降維模式計算流體力學參數,利用學習后的關系計算FFRCT值。對于冠脈樹內的任何一點,FFRCT是通過計算一個心動周期內的平均局部壓力與平均主動脈壓力之比而生成的,由此產生了彩色編碼的三維網格,允許獲得任意位置的FFRCT值。FFRCT值均在狹窄病變遠端2 cm處進行測量。如果一支血管多處病變,則FFRCT值測量以最遠端病變為準[5]。
4.2 冠脈解剖狹窄率測定和斑塊特征定量分析
對冠脈CTA檢測到的所有血管斑塊(長度≥2 mm者),在相應FFRCT測量后行冠脈解剖狹窄率測定和斑塊特征定量分析。當一支血管多處病變時,病變間距>2 mm時則視為串聯病變。冠脈解剖狹窄率測定:在曲面重建(CPR)圖像上,在最窄病變處的垂直斷面水平手動測得最小管腔直徑(MLD)和最小管腔面積(MLA),獲取管腔直徑狹窄率。斑塊特征定量分析:①使用Coronary Plaque Analysis 4.3.1半自動軟件測得斑塊長度、管腔體積、血管總體積、斑塊總體積、非鈣化斑塊體積(NCPV)、脂質斑塊體積、纖維斑塊體積、鈣化斑塊體積(CPV)、重塑指數(remodeling index,RI;定義為冠脈最狹窄處管腔面積與近端正常血管面積的比值。②通過計算獲取非鈣化斑塊體積百分比(定義為非鈣化斑塊體積占斑塊總體積的比值)、斑塊負荷(plaque burden,PB;定義為該支血管上斑塊總體積與血管總體積的比值)。
4.3 易損斑塊評估
評估指標/特征:①正性重構(positive remodeling,PR),定義為RI≥1.1;②低密度斑塊(LAP),定義為冠脈斑塊內任何一點CT值低于30 HU;③點狀鈣化(spot calcification,SC),是非鈣化斑塊內的鈣化斑塊長度<3 mm或鈣化斑塊組成小于血管周長的90°;④餐巾環征(napkin sign,NPS),是指低密度斑塊核心周圍環繞著高密度的邊緣區[4]。具備上述2個以上特征即判定為易損斑塊。
以上均由一位有2年冠脈CTA診斷經驗的影像科醫師在不知患者隨訪結果的條件下進行測量和評估,并由另一位有10年冠脈CTA工作經驗的影像科醫師對測量準確性進行評價。
5.隨訪
共計17例(19%)患者發生MACE事件。MACE至少包含以下任一項[6]:心源性死亡(1例),非致死性(非ST段抬高型)心肌梗死(1例),不穩定心絞痛再住院(4例,其中2例發作時心肌酶譜升高,2例入院時心電圖異常),不穩定心絞痛再血管化治療(11例,其中9例PCI,2例CABG)。隨訪截止日期為2020年1月31日。
6.統計學分析
使用SPSS 23.0軟件對數據進行統計學分析。以患者血管為計數單位,分析冠脈斑塊特征定量參數、斑塊易損性和FFRCT。連續性變量先進行正態性檢驗(K?S檢驗),呈正態分布者以均數±標準差(±s)表示,采用配對t檢驗;非正態分布的變量以中位數(下四分位數,上四分位數)表示,采用Mann?WhitneyU檢驗或Wilcoxon非參數檢驗。計數(定性)資料根據需要,通過卡方檢驗或Fisher精確檢驗進行比較。對單因素分析中有統計學意義的變量進行多因素邏輯回歸分析,并確定MACE相關的獨立危險因素。采用受試者操作特征(ROC)曲線評估上述參數(獨立危險因素)單個或聯合對MACE的預測價值。P<0.05認為具有統計學意義。
結 果
MACE陽性組17例患者共計17處責任血管(均為單支血管單處病變),MACE陰性組71例患者共計80支非責任血管。圖1為MACE陽性患者相關影像資料示例。
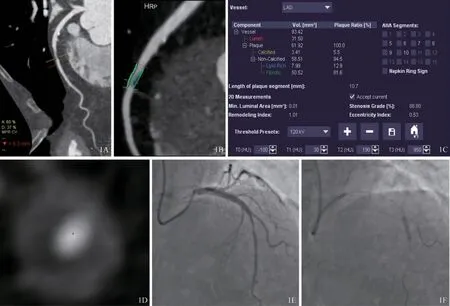
圖1 MACE陽性患者(女,64歲)影像資料
MACE陽性組和陰性組FFRCT及斑塊特征參數值比較見表1。共13項定量參數,其中FFRCT、管腔直徑狹窄率、最小管腔面積、斑塊長度、血管總體積、斑塊總體積、斑塊負荷、非鈣化斑塊體積、這8項定量參數在2組間存在差異,并具有統計學意義。4項易損性特征中,低密度斑塊發生率在2組中存在顯著性差異,MACE陽性患者中低密度斑塊發生率更高。
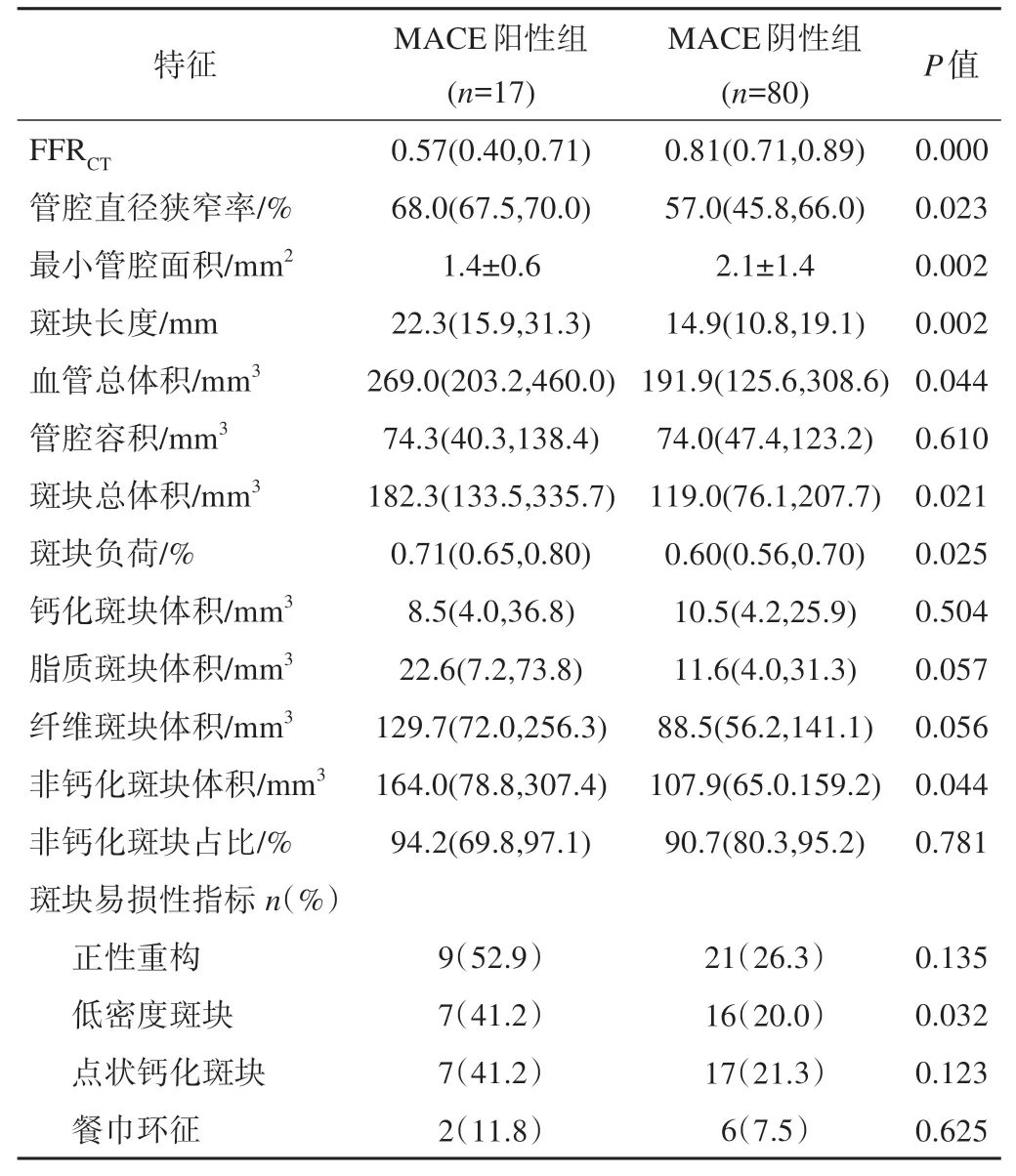
表1 FFRCT及冠脈斑塊特征單因素分析對MACE的預測價值比較
FFRCT及冠脈斑塊特征多因素回歸分析結果(表2)表明,FFRCT≤0.8(OR=9.643,P<0.001)、管腔直徑狹窄率>60.5%(OR=1.13,P=0.033)、低密度斑塊出現(OR=2.86,P=0.024)、斑塊負荷>0.67(OR=1.08,P=0.014)和斑塊長度>19.4 mm(OR=1.038,P=0.030)是MACE的獨立危險因子。其中,FFRCT≤0.8是最有力的預測因子(其識別MACE的最佳閾值最高)。
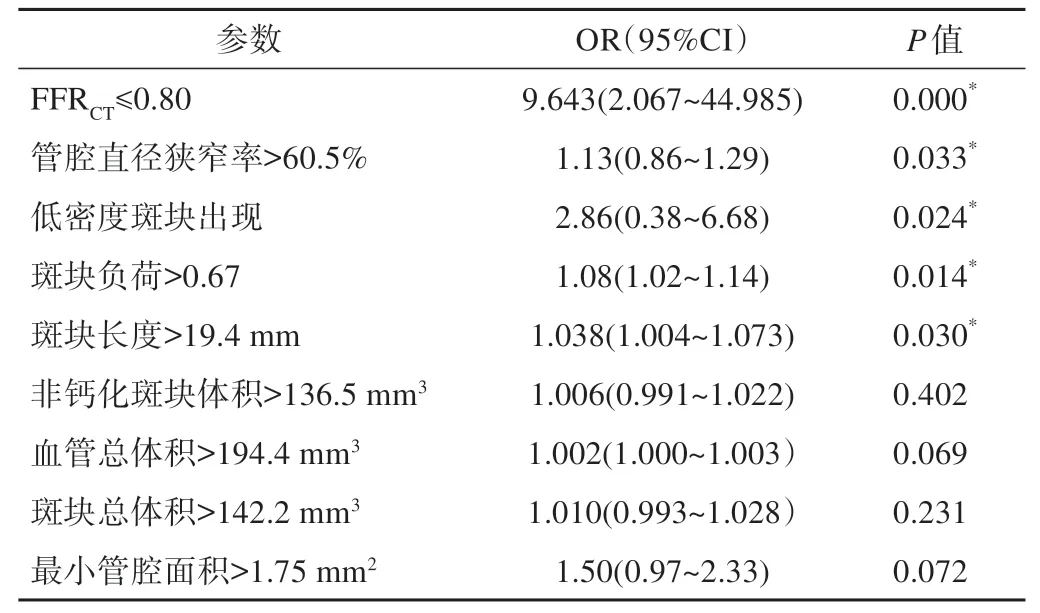
表2 FFRCT及冠脈斑塊特征多因素回歸分析結果
FFRCT及冠脈斑塊特征預測MACE的ROC曲線分析結果(圖2)顯示:當模型中只納入基于冠脈CTA的解剖狹窄程度(管腔直徑狹窄率>60.5%)單一指標時,其對MACE的預測價值最低,ROC曲線下面積(AUC)僅為0.664;添加FFRCT≤0.8指標后,模型預測價值得以提高(AUC增加至0.783);再添加斑塊特征(斑塊長度、斑塊負荷、低密度斑塊)指標后,模型預測價值進一步提高(AUC達0.821)。
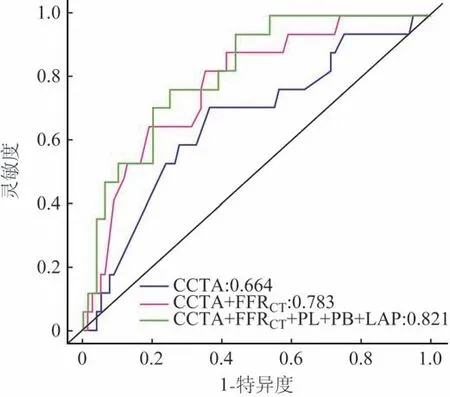
圖2 ROC曲線分析
討 論
本研究通過獲取基于冠脈CTA的冠脈解剖狹窄率(管腔直徑狹窄率)、FFRCT、斑塊特征參數,分析它們與CAD患者MACE發生的相關性,發現FFRCT≤0.8、冠脈解剖狹窄率>60.5%、斑塊負荷>0.67、斑塊長度>19.4 mm及低密度斑塊出現是MACE發生的獨立危險因素,其中FFRCT≤0.8是最有力的預測因子;聯合解剖狹窄率、FFRCT、斑塊特征比單獨解剖狹窄率對MACE具有更高的預測價值。
基于ICA的FFR是有效評估冠脈狹窄相關心肌血流灌注功能學異常的金標準,用FFR指導CAD治療后,患者MACE發生率顯著降低[7]。先前研究[3]已證明FFRCT與有創性FFR有良好的相關性。本研究中,我們發現FFRCT預測MACE的價值優于基于冠脈CTA的解剖狹窄程度(前者的OR為9.64,后者的OR為1.13);并且解剖狹窄程度在結合FFRCT≤0.80指標后,其預測價值得以提高(AUC由0.664增至0.783)。Duguay等[8]的研究觀察到FFRCT與基于ICA的解剖狹窄程度相比,對于非責任病變(狹窄率≥25%)的未來MACE預測更具有價值。Lu等[9]研究FFRCT對MACE的預后價值時也發現,FFRCT≤0.80的患者發生MACE的風險比FFRCT>0.80的患者高4.3倍。這些都說明了FFRCT≤0.80對MACE有預測價值,且比單獨解剖狹窄率有增益效應,與我們的研究結果一致。我們認為,這是由于FFRCT≤0.80表明狹窄病變處存在功能性缺血,無以滿足負荷下游心肌供血,心肌供氧和需氧失去平衡,心肌細胞無氧酵解代謝增加,因而進一步發展為MACE。
與以往研究相似,本研究也確定了眾多斑塊特征參數對MACE的預后價值。我們發現MACE陽性組斑塊總體積、血管總體積、非鈣化斑塊體積、斑塊長度、斑塊負荷以及低密度斑塊均顯著高于MACE陰性組,這與Tesche等[10]的研究結果一致。斑塊定量特征參數中,斑塊負荷具有最高預測價值(OR=1.08,P=0.014),斑塊負荷反映斑塊總體積占血管總體積的比例,當斑塊負荷增大時,斑塊內部更易發現脂質核心或發生斑塊內出血,導致斑塊脫落阻塞冠脈分支,進而引發MACE。易損斑塊特征中,MACE陽性組中低密度斑塊的發生率高于MACE陰性組(41.2%比20.0%)并具有預測價值(OR=2.86,P=0.024);并且在單因素分析中非鈣化斑塊體積也顯著高于對照組;上述這些特征都是斑塊內較多脂質存在的表現。研究[11]表明,富含脂質的斑塊內含大量可以釋放蛋白酶和組織因子的炎癥細胞,可加速斑塊纖維帽的溶解,激活平滑肌細胞,增加斑塊的不穩定性,從而最終導致MACE的發生。
本研究中冠脈解剖狹窄率范圍為30%~70%,其中發生MACE的血管解剖狹窄率均>50%。且在MACE陽性病例中有1支血管FFRCT>0.80。因此,我們聯合解剖狹窄率、FFRCT≤0.80及斑塊特征,發現它們聯合時對MACE的預測價值最高,這證明將解剖學、形態學及功能學信息結合可以為臨床提供更多信息,對CAD患者的治療方案及預后分析有重要意義。
本研究存在一定局限性:①本研究是屬于單中心回顧性研究,入選病例較少,且隨訪MACE事件類型分布不均。我們發現大部分MACE患者為不穩定心絞痛再血管化治療(11例),而急性冠脈綜合征(ACS)僅存在1例。因此,可以預見病變血流動力學意義(FFRCT)而非斑塊破裂(高危斑塊征象)是導致MACE的主導因素。②本研究缺乏有創性FFR作為金標準對照。③本研究冠脈CTA數據源自3臺不同機器,可能對測量值產生一定影響。④本研究MACE組患者均為單支血管單處病變,這可能導致研究結果存在偏移。本研究雖是小樣本研究,但最終也有較好的結果被論證。今后,我們會進一步增加MACE陽性患者存在單支血管多處病變及多支血管多處病變的研究,擴大樣本量,參與到前瞻性臨床研究中,來進一步證實這些因素對MACE事件的預測價值。
綜上,冠脈解剖狹窄率、FFRCT、冠脈斑塊特征對冠心病患者MACE的發生具有預測價值。當聯合解剖狹窄率、FFRCT、冠脈斑塊特征時,對MACE具有較高的預測效能。

